第1章 物质及其变化(氢氧化钠变质的探究)(课件 15张PPT)
文档属性
| 名称 | 第1章 物质及其变化(氢氧化钠变质的探究)(课件 15张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 4.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-10-16 00:00:00 | ||
图片预览






文档简介
(共15张PPT)
氢氧化钠变质的探究之旅
不能与OH-离子共存的有哪些离子?
H+(气体和水)、Ca2+、Ba2+、 Mg2+ 、 Al3+、 Mn2+、 Zn2+、Fe2+、 Fe3+、Cu2+、 Ag+
不能与CO32-离子共存的有哪些离子?
H+(水)、 NH4+ (气体)、 Mg2+ 、 Al3+、 Mn2+、 Zn2+、Fe2+、 Fe3+、 Cu2+、 Ag+
想一想:
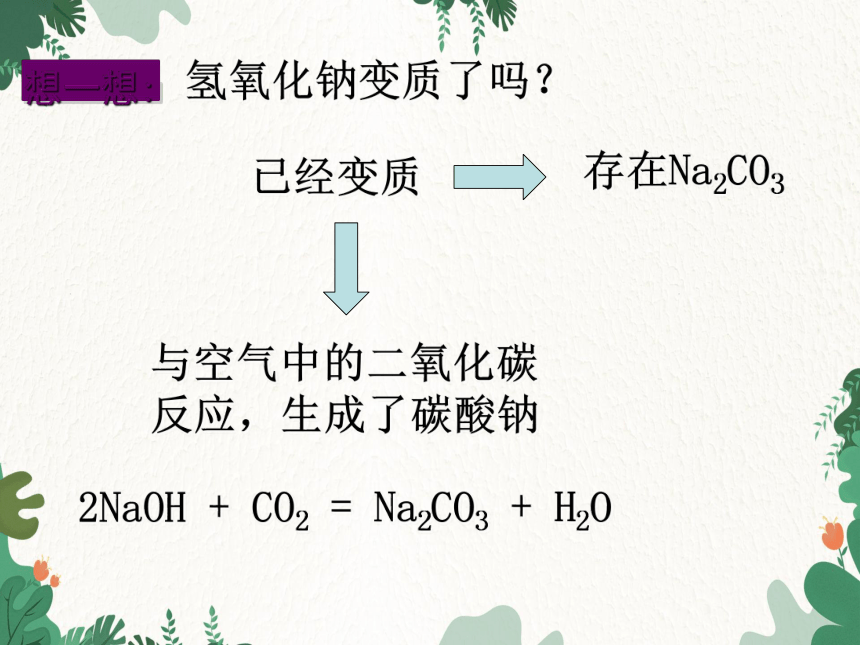
氢氧化钠变质了吗?
已经变质
与空气中的二氧化碳反应,生成了碳酸钠
2NaOH + CO2 = Na2CO3 + H2O
存在Na2CO3
如何验证一瓶NaOH溶液是否已经变质?请选择不同类别的试剂。书写化学方程式
1.酸 稀盐酸 稀硫酸
3.可溶盐 Ca(NO3)2溶液 BaCl2溶液
2.可溶碱 Ca(OH)2溶液 Ba(OH)2溶液
实验步骤 实验现象 实验结论
氢氧化钠溶液没有变质
氢氧化钠溶液已经变质
实验方案:
方法一:取少量待测液于试管中,向其中滴加足量的稀盐酸
方法二:取少量待测液于试管中,向其中滴加少量的Ca(NO3)2溶液
没有气泡产生
有气泡产生
没有产生白色沉淀
产生白色沉淀
盐酸先与NaOH反应,NaOH完全反应后,再与Na2CO3反应
氢氧化钠是否变质
本质:检验CO32-是否存在
方法:滴加某种试剂和Na2CO3 反应产生明显的实验现象
试剂的选择:能与Na2CO3反应而不能与
NaOH反应
氢氧化钠溶液变质的程度如何?
想一想:
全部变质
部分变质
只有Na2CO3
Na2CO3和NaOH
本质:检验OH-是否存在
OH-
CO32-
Na+
如何检验氢氧根离子的存在?(明显现象)
1、指示剂(酚酞)
2、CuCl2等
碳酸根离子会干扰氢氧根离子的检验,怎么办?
除去碳酸根离子后再检验OH- :
1、稀盐酸
×
2、Ca(OH)2
×
3、Ca(NO3)2
√
除去碳酸根离子的同时把待检验的氢氧根离子也除去了
除去碳酸根离子的同时生成了氢氧化钠
确定试剂
1、先滴加硝酸钙再滴加酚酞
↓
过量,确保完全除去碳酸根离子
↓
几滴
2、先滴加硝酸钙再滴加氯化铜
酚酞溶液
OH–
Na+
CO32-
过量CaCl2溶液
CaCO3
Na+
Na+
Cl-
Ca2+
Cl-
Cl-
Ca2+
Cl-
Na+
CO32-
CaCO3
Na+
Cl-
Ca2+
Cl-
Cl-
Ca2+
Cl-
碱性
中性
部分变质:Na2CO3和NaOH
全部变质:Na2CO3
红色
无色
酚酞溶液
可以选择CaCl2溶液和酚酞溶液。
实验方案
实验步骤 实验现象 实验结论
氢氧化钠溶液
全部变质
氢氧化钠溶液
部分变质
(1)取少量待测液于试管中,向其中滴加过量的
Ca(NO3)2溶液
(2)再向其中滴加无色酚酞试液
有白色沉淀生成
有白色沉淀生成
溶液没有明显变化
溶液变成红色
探究变质的氢氧化钠溶液变质的程度
实验方案
实验步骤 实验现象 实验结论
氢氧化钠溶液
全部变质
氢氧化钠溶液
部分变质
(1)取少量待测液于试管中,向其中滴加过量的
Ca(NO3)2溶液
(2)过滤向滤液中滴加CuCl2溶液
有白色沉淀生成
有白色沉淀生成
溶液没有明显变化
有蓝色沉淀生成
探究变质的氢氧化钠溶液变质的程度
先滴加几滴酚酞,再滴加过量硝酸钙溶液?
是否可行?
氢氧化钠变质的探究之旅
不能与OH-离子共存的有哪些离子?
H+(气体和水)、Ca2+、Ba2+、 Mg2+ 、 Al3+、 Mn2+、 Zn2+、Fe2+、 Fe3+、Cu2+、 Ag+
不能与CO32-离子共存的有哪些离子?
H+(水)、 NH4+ (气体)、 Mg2+ 、 Al3+、 Mn2+、 Zn2+、Fe2+、 Fe3+、 Cu2+、 Ag+
想一想:
氢氧化钠变质了吗?
已经变质
与空气中的二氧化碳反应,生成了碳酸钠
2NaOH + CO2 = Na2CO3 + H2O
存在Na2CO3
如何验证一瓶NaOH溶液是否已经变质?请选择不同类别的试剂。书写化学方程式
1.酸 稀盐酸 稀硫酸
3.可溶盐 Ca(NO3)2溶液 BaCl2溶液
2.可溶碱 Ca(OH)2溶液 Ba(OH)2溶液
实验步骤 实验现象 实验结论
氢氧化钠溶液没有变质
氢氧化钠溶液已经变质
实验方案:
方法一:取少量待测液于试管中,向其中滴加足量的稀盐酸
方法二:取少量待测液于试管中,向其中滴加少量的Ca(NO3)2溶液
没有气泡产生
有气泡产生
没有产生白色沉淀
产生白色沉淀
盐酸先与NaOH反应,NaOH完全反应后,再与Na2CO3反应
氢氧化钠是否变质
本质:检验CO32-是否存在
方法:滴加某种试剂和Na2CO3 反应产生明显的实验现象
试剂的选择:能与Na2CO3反应而不能与
NaOH反应
氢氧化钠溶液变质的程度如何?
想一想:
全部变质
部分变质
只有Na2CO3
Na2CO3和NaOH
本质:检验OH-是否存在
OH-
CO32-
Na+
如何检验氢氧根离子的存在?(明显现象)
1、指示剂(酚酞)
2、CuCl2等
碳酸根离子会干扰氢氧根离子的检验,怎么办?
除去碳酸根离子后再检验OH- :
1、稀盐酸
×
2、Ca(OH)2
×
3、Ca(NO3)2
√
除去碳酸根离子的同时把待检验的氢氧根离子也除去了
除去碳酸根离子的同时生成了氢氧化钠
确定试剂
1、先滴加硝酸钙再滴加酚酞
↓
过量,确保完全除去碳酸根离子
↓
几滴
2、先滴加硝酸钙再滴加氯化铜
酚酞溶液
OH–
Na+
CO32-
过量CaCl2溶液
CaCO3
Na+
Na+
Cl-
Ca2+
Cl-
Cl-
Ca2+
Cl-
Na+
CO32-
CaCO3
Na+
Cl-
Ca2+
Cl-
Cl-
Ca2+
Cl-
碱性
中性
部分变质:Na2CO3和NaOH
全部变质:Na2CO3
红色
无色
酚酞溶液
可以选择CaCl2溶液和酚酞溶液。
实验方案
实验步骤 实验现象 实验结论
氢氧化钠溶液
全部变质
氢氧化钠溶液
部分变质
(1)取少量待测液于试管中,向其中滴加过量的
Ca(NO3)2溶液
(2)再向其中滴加无色酚酞试液
有白色沉淀生成
有白色沉淀生成
溶液没有明显变化
溶液变成红色
探究变质的氢氧化钠溶液变质的程度
实验方案
实验步骤 实验现象 实验结论
氢氧化钠溶液
全部变质
氢氧化钠溶液
部分变质
(1)取少量待测液于试管中,向其中滴加过量的
Ca(NO3)2溶液
(2)过滤向滤液中滴加CuCl2溶液
有白色沉淀生成
有白色沉淀生成
溶液没有明显变化
有蓝色沉淀生成
探究变质的氢氧化钠溶液变质的程度
先滴加几滴酚酞,再滴加过量硝酸钙溶液?
是否可行?
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
