第12章《盐》同步训练2022-2023学年九年级化学京改版(2013)下册(有答案)
文档属性
| 名称 | 第12章《盐》同步训练2022-2023学年九年级化学京改版(2013)下册(有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 66.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-15 00:00:00 | ||
图片预览


文档简介
第12章《盐》同步训练
一、单选题
1.下列物质的化学式、俗称、名称表示同一种物质的是
A. 生石灰 氢氧化钙
B. 熟石灰 氧化钙
C. 烧碱 氢氧化钠
D. 石灰石 碳酸钙
2.同学们夏季郊游时,发现稻田里的水稻叶子发黄并倒下了一片,都认为应该向稻田中施用的复合肥是
A.NH4NO3 B.KNO3
C.Ca3(PO4)2 D.KCl
3.化肥碳酸氢铵具有以下性质:易溶于水,受潮时在常温下即能分解放出氨气,温度越高分解越快,遇碱性物质时也会放出氨气。该花费在运输、贮存和施用中做法错误的是
A.运输时注意密封 B.贮存时不能受潮或暴晒
C.与草木灰混合施用 D.施用后立即盖上
4.某pH=12的无色溶液中大量存在的离子有Na+、Ba2+、NO、X,则X可能是
A.Cu2+ B.Cl- C.H+ D.SO
5.下列物质不能与NaOH溶液反应的是
A.二氧化碳 B.硝酸
C.硫酸铜 D.氢氧化铁
6.下列物质间能够发生反应,但没有出现明显现象的是
A.将稀盐酸滴入盛石灰石的试管中
B.将CO2通入NaOH溶液中
C.将碳酸钠溶液滴入澄清石灰水中
D.将稀硫酸滴入NaCl溶液中
7.下列关于碳酸钙的说法错误的是
A.大理石的主要成分是碳酸钙
B.实验室常用碳酸钙与稀硫酸反应制取CO2
C.碳酸钙可用作补钙剂
D.石灰浆粉刷墙壁,“出汗”后变成碳酸钙
8.下列实验目的与所用试剂相符的是
A.证明NaOH溶液中含有Na2CO3――酚酞试剂
B.证明NaOH溶液中含有Na2CO3――澄清石灰水
C.除去NaOH溶液中的Na2CO3杂质――稀盐酸
D.除去NaOH溶液中的Na2CO3杂质――CaCl2溶液
9.硝酸铵(NH4NO3)是一种高效化肥,它属于
A.氮肥 B.磷肥 C.钾肥 D.复合肥
10.使用下列试剂能将氯化钠、碳酸钠、氯化钡三种溶液鉴别出来的是
A.稀硫酸 B.氯化钠溶液 C.铁片 D.氢氧化钠溶液
11.除去下列各组物质中的杂质(括号内为杂质),所选用的试剂(足量)及操作方法均正确的是( )
选项 物质 选用试剂 操作方法
A Fe2O3(Fe) 盐酸 浸泡、过滤、洗涤、烘干
B CO(CO2) NaOH溶液、浓硫酸 洗气、干燥
C CaO(CaCO3) 水 过滤、烘干
D NaCl(Na2CO3) Ca(NO3)2溶液 溶解、过滤、蒸发、结晶
A.A B.B C.C D.D
二、简答题
12.在硫酸铜溶液中滴加石灰水,可以看到_____________,发生反应的方程式为_______________农业上用此配成_________液对农作物有很好的杀虫作用。
13.人的胃液里含有适量盐酸。服用含MgCO3 的抗酸药可治疗胃酸过多症,有关反应的化学方程式为 ;该抗酸药说明书上标明的食用方法为“嚼食”,将药片嚼碎后服用的优点是 。
三、推断题
14.有一种白色固体可能含有:BaCl2、KCl、Na2CO3、Na2SO4和CuSO4中的一种或几种。对该固体进行如下实验。
①取样,加足量的水,充分搅拌,过滤。得到白色沉淀A和无色溶液B。
②在白色沉淀A中加入稀盐酸,沉淀全部溶解,放出能使石灰水变浑浊的无色气体。
③在无色溶液B中加入AgNO3溶液,得到白色沉淀,再加入稀硝酸,白色沉淀不溶解。请回答下列问题。
(1)原白色固体中一定不含有_____;一定含有_____。
(2)实验①得到的无色溶液B中一定含有的溶质是_____。
(3)实验①中反应的化学方程式为_____。
(4)原白色固体中可能含有_____。
15.A、B、C三种物质均含有人体中含量最多的金属元素,D可作气体肥料,它们的转化关系如图(部分物质和反应条件已略去),A的相对分子质量为56,A与水化合得B.则A→B的化学方程式为_____;C→A的化学反应类型属于_____;D→C的化学方程式为_____。
四、实验题
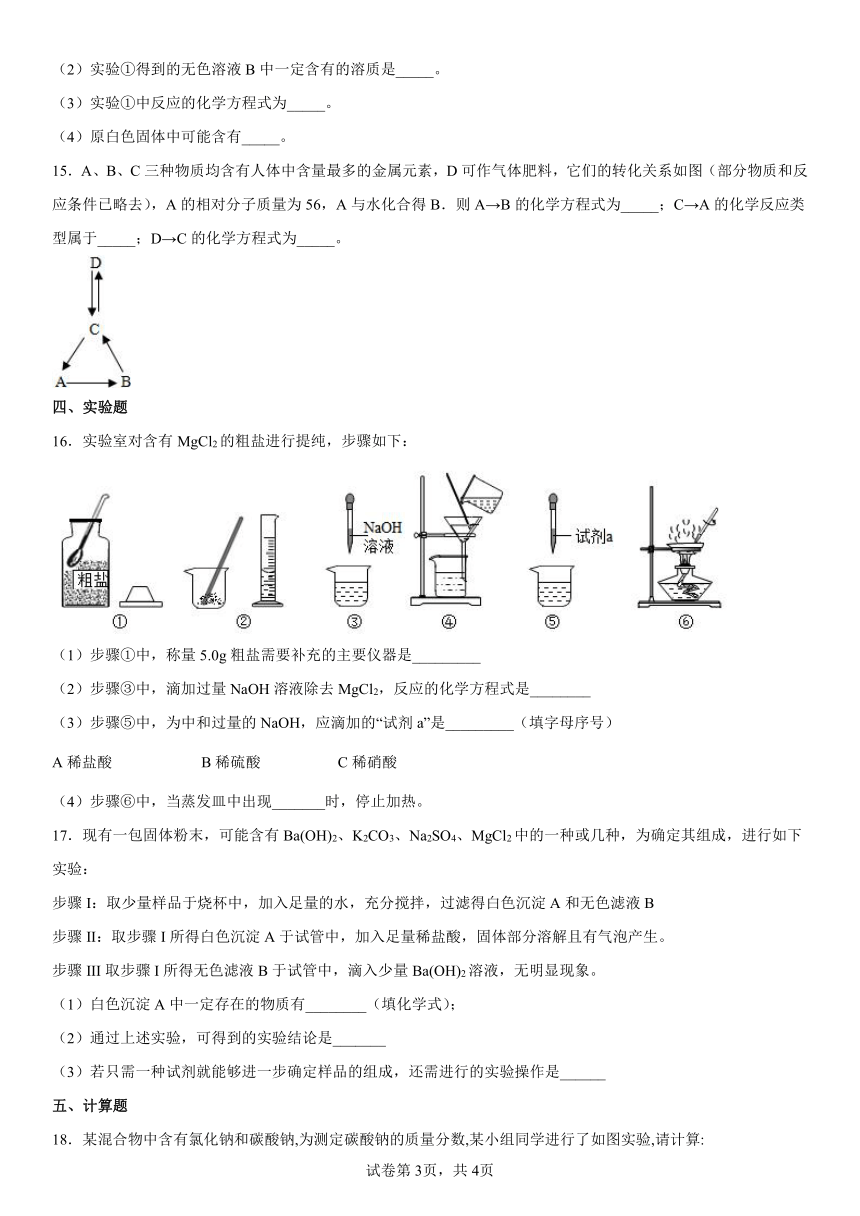
16.实验室对含有MgCl2的粗盐进行提纯,步骤如下:
(1)步骤①中,称量5.0g粗盐需要补充的主要仪器是_________
(2)步骤③中,滴加过量NaOH溶液除去MgCl2,反应的化学方程式是________
(3)步骤⑤中,为中和过量的NaOH,应滴加的“试剂a”是_________(填字母序号)
A稀盐酸 B稀硫酸 C稀硝酸
(4)步骤⑥中,当蒸发皿中出现_______时,停止加热。
17.现有一包固体粉末,可能含有Ba(OH)2、K2CO3、Na2SO4、MgCl2中的一种或几种,为确定其组成,进行如下实验:
步骤I:取少量样品于烧杯中,加入足量的水,充分搅拌,过滤得白色沉淀A和无色滤液B
步骤II:取步骤I所得白色沉淀A于试管中,加入足量稀盐酸,固体部分溶解且有气泡产生。
步骤III取步骤I所得无色滤液B于试管中,滴入少量Ba(OH)2溶液,无明显现象。
(1)白色沉淀A中一定存在的物质有________(填化学式);
(2)通过上述实验,可得到的实验结论是_______
(3)若只需一种试剂就能够进一步确定样品的组成,还需进行的实验操作是______
五、计算题
18.某混合物中含有氯化钠和碳酸钠,为测定碳酸钠的质量分数,某小组同学进行了如图实验,请计算:
(1)生成二氧化碳的总质量为 。
(2)样品中碳酸钠的质量分数(计算结果精确至0. 1%)。
19.碳酸钠和碳酸氢钠的混合物共20.0克加热到到质量不再减少,冷却后称量固体质量为16.9克。(已知碳酸氢钠加热分解得到碳酸钠和两种氧化物)
(1)碳酸氢钠俗称______,常用治疗胃酸过多;
(2)求原混合物中碳酸氢钠的质量?(请写出化学方程式和必要的过程)
20.为了测定某小苏打样品中碳酸氢钠的质量分数,小兰同学进行了如下实验:向盛有10g样品的烧杯中加入稀硫酸,恰好完全反应时,加入稀硫酸的质量为90g,反应后烧杯内物质的总质量为95.6g。(杂质不溶于水也不与酸发生反应)
(1)该反应生成二氧化碳的质量为______g。
(2)求该样品中碳酸氢钠的质量分数(写出计算过程)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.B
3.C
4.B
5.D
6.B
7.B
8.B
9.A
10.A
11.B
12. 蓝色沉淀生成 CuSO4+Ca(OH)2═Cu(OH)2↓+CaSO4 波尔多
13. MgCO3+2HCl=MgCl2+H2O+CO2↑ 增大接触面积利于吸收
14. CuSO4、Na2SO4 BaCl2、Na2CO3 NaCl Na2CO3+BaCl2=2NaCl+BaCO3↓ KCl
15. 分解反应
16. 托盘天平 A 较多固体
17. BaCO3、BaSO4 固体粉末一定含有Ba(OH)2、Na2SO4、K2CO3,可能含有MgCl2 向步骤Ⅱ的上层清液滴加足量的氢氧化钠溶液
18.4.4g、88.3%
19.(1)小苏打(2)碳酸氢钠加热分解得到碳酸钠和两种氧化物,根据质量守恒定律可知,碳酸氢钠加热分解生成碳酸钠、水和二氧化碳,设原混合物中碳酸氢钠的质量为x,
解得x=8.4g;
答:原混合物中碳酸氢钠的质量8.4g。
20.(1)4.4
(2)解:设参加反应的碳酸氢钠的质量为x。
该样品中碳酸氢钠的质量分数为
答:该样品中碳酸氢钠的质量分数为84%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列物质的化学式、俗称、名称表示同一种物质的是
A. 生石灰 氢氧化钙
B. 熟石灰 氧化钙
C. 烧碱 氢氧化钠
D. 石灰石 碳酸钙
2.同学们夏季郊游时,发现稻田里的水稻叶子发黄并倒下了一片,都认为应该向稻田中施用的复合肥是
A.NH4NO3 B.KNO3
C.Ca3(PO4)2 D.KCl
3.化肥碳酸氢铵具有以下性质:易溶于水,受潮时在常温下即能分解放出氨气,温度越高分解越快,遇碱性物质时也会放出氨气。该花费在运输、贮存和施用中做法错误的是
A.运输时注意密封 B.贮存时不能受潮或暴晒
C.与草木灰混合施用 D.施用后立即盖上
4.某pH=12的无色溶液中大量存在的离子有Na+、Ba2+、NO、X,则X可能是
A.Cu2+ B.Cl- C.H+ D.SO
5.下列物质不能与NaOH溶液反应的是
A.二氧化碳 B.硝酸
C.硫酸铜 D.氢氧化铁
6.下列物质间能够发生反应,但没有出现明显现象的是
A.将稀盐酸滴入盛石灰石的试管中
B.将CO2通入NaOH溶液中
C.将碳酸钠溶液滴入澄清石灰水中
D.将稀硫酸滴入NaCl溶液中
7.下列关于碳酸钙的说法错误的是
A.大理石的主要成分是碳酸钙
B.实验室常用碳酸钙与稀硫酸反应制取CO2
C.碳酸钙可用作补钙剂
D.石灰浆粉刷墙壁,“出汗”后变成碳酸钙
8.下列实验目的与所用试剂相符的是
A.证明NaOH溶液中含有Na2CO3――酚酞试剂
B.证明NaOH溶液中含有Na2CO3――澄清石灰水
C.除去NaOH溶液中的Na2CO3杂质――稀盐酸
D.除去NaOH溶液中的Na2CO3杂质――CaCl2溶液
9.硝酸铵(NH4NO3)是一种高效化肥,它属于
A.氮肥 B.磷肥 C.钾肥 D.复合肥
10.使用下列试剂能将氯化钠、碳酸钠、氯化钡三种溶液鉴别出来的是
A.稀硫酸 B.氯化钠溶液 C.铁片 D.氢氧化钠溶液
11.除去下列各组物质中的杂质(括号内为杂质),所选用的试剂(足量)及操作方法均正确的是( )
选项 物质 选用试剂 操作方法
A Fe2O3(Fe) 盐酸 浸泡、过滤、洗涤、烘干
B CO(CO2) NaOH溶液、浓硫酸 洗气、干燥
C CaO(CaCO3) 水 过滤、烘干
D NaCl(Na2CO3) Ca(NO3)2溶液 溶解、过滤、蒸发、结晶
A.A B.B C.C D.D
二、简答题
12.在硫酸铜溶液中滴加石灰水,可以看到_____________,发生反应的方程式为_______________农业上用此配成_________液对农作物有很好的杀虫作用。
13.人的胃液里含有适量盐酸。服用含MgCO3 的抗酸药可治疗胃酸过多症,有关反应的化学方程式为 ;该抗酸药说明书上标明的食用方法为“嚼食”,将药片嚼碎后服用的优点是 。
三、推断题
14.有一种白色固体可能含有:BaCl2、KCl、Na2CO3、Na2SO4和CuSO4中的一种或几种。对该固体进行如下实验。
①取样,加足量的水,充分搅拌,过滤。得到白色沉淀A和无色溶液B。
②在白色沉淀A中加入稀盐酸,沉淀全部溶解,放出能使石灰水变浑浊的无色气体。
③在无色溶液B中加入AgNO3溶液,得到白色沉淀,再加入稀硝酸,白色沉淀不溶解。请回答下列问题。
(1)原白色固体中一定不含有_____;一定含有_____。
(2)实验①得到的无色溶液B中一定含有的溶质是_____。
(3)实验①中反应的化学方程式为_____。
(4)原白色固体中可能含有_____。
15.A、B、C三种物质均含有人体中含量最多的金属元素,D可作气体肥料,它们的转化关系如图(部分物质和反应条件已略去),A的相对分子质量为56,A与水化合得B.则A→B的化学方程式为_____;C→A的化学反应类型属于_____;D→C的化学方程式为_____。
四、实验题
16.实验室对含有MgCl2的粗盐进行提纯,步骤如下:
(1)步骤①中,称量5.0g粗盐需要补充的主要仪器是_________
(2)步骤③中,滴加过量NaOH溶液除去MgCl2,反应的化学方程式是________
(3)步骤⑤中,为中和过量的NaOH,应滴加的“试剂a”是_________(填字母序号)
A稀盐酸 B稀硫酸 C稀硝酸
(4)步骤⑥中,当蒸发皿中出现_______时,停止加热。
17.现有一包固体粉末,可能含有Ba(OH)2、K2CO3、Na2SO4、MgCl2中的一种或几种,为确定其组成,进行如下实验:
步骤I:取少量样品于烧杯中,加入足量的水,充分搅拌,过滤得白色沉淀A和无色滤液B
步骤II:取步骤I所得白色沉淀A于试管中,加入足量稀盐酸,固体部分溶解且有气泡产生。
步骤III取步骤I所得无色滤液B于试管中,滴入少量Ba(OH)2溶液,无明显现象。
(1)白色沉淀A中一定存在的物质有________(填化学式);
(2)通过上述实验,可得到的实验结论是_______
(3)若只需一种试剂就能够进一步确定样品的组成,还需进行的实验操作是______
五、计算题
18.某混合物中含有氯化钠和碳酸钠,为测定碳酸钠的质量分数,某小组同学进行了如图实验,请计算:
(1)生成二氧化碳的总质量为 。
(2)样品中碳酸钠的质量分数(计算结果精确至0. 1%)。
19.碳酸钠和碳酸氢钠的混合物共20.0克加热到到质量不再减少,冷却后称量固体质量为16.9克。(已知碳酸氢钠加热分解得到碳酸钠和两种氧化物)
(1)碳酸氢钠俗称______,常用治疗胃酸过多;
(2)求原混合物中碳酸氢钠的质量?(请写出化学方程式和必要的过程)
20.为了测定某小苏打样品中碳酸氢钠的质量分数,小兰同学进行了如下实验:向盛有10g样品的烧杯中加入稀硫酸,恰好完全反应时,加入稀硫酸的质量为90g,反应后烧杯内物质的总质量为95.6g。(杂质不溶于水也不与酸发生反应)
(1)该反应生成二氧化碳的质量为______g。
(2)求该样品中碳酸氢钠的质量分数(写出计算过程)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.B
3.C
4.B
5.D
6.B
7.B
8.B
9.A
10.A
11.B
12. 蓝色沉淀生成 CuSO4+Ca(OH)2═Cu(OH)2↓+CaSO4 波尔多
13. MgCO3+2HCl=MgCl2+H2O+CO2↑ 增大接触面积利于吸收
14. CuSO4、Na2SO4 BaCl2、Na2CO3 NaCl Na2CO3+BaCl2=2NaCl+BaCO3↓ KCl
15. 分解反应
16. 托盘天平 A 较多固体
17. BaCO3、BaSO4 固体粉末一定含有Ba(OH)2、Na2SO4、K2CO3,可能含有MgCl2 向步骤Ⅱ的上层清液滴加足量的氢氧化钠溶液
18.4.4g、88.3%
19.(1)小苏打(2)碳酸氢钠加热分解得到碳酸钠和两种氧化物,根据质量守恒定律可知,碳酸氢钠加热分解生成碳酸钠、水和二氧化碳,设原混合物中碳酸氢钠的质量为x,
解得x=8.4g;
答:原混合物中碳酸氢钠的质量8.4g。
20.(1)4.4
(2)解:设参加反应的碳酸氢钠的质量为x。
该样品中碳酸氢钠的质量分数为
答:该样品中碳酸氢钠的质量分数为84%。
答案第1页,共2页
答案第1页,共2页
