第七单元常见的酸和碱同步练习题2022-2023学年九年级化学鲁教版下册(有答案)
文档属性
| 名称 | 第七单元常见的酸和碱同步练习题2022-2023学年九年级化学鲁教版下册(有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 120.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-15 00:00:00 | ||
图片预览



文档简介
第七单元常见的酸和碱同步练习题
一、单选题
1.下列物质的性质与用途,不相匹配的是( )
A.氧气可以支持燃烧 工业上可用作燃料
B.氮气的化学性质定稳 工业上可用作焊接保护气
C.白醋含有醋酸,显酸性 家庭中可用作除水垢
D.硫酸钡既不溶于水,也不与酸反应 医疗上可用于“钡餐”造影
2.下列物质属于盐的是
A.NaOH B.CaO C.Cu D.CaCO3
3.下表是几种作物适宜生长的pH范围:
作物 马铃薯 茶树 水稻 莲
pH 4.8~5.5 5.0~5.5 6.0~7.0 8.0~9.0
某地土壤呈碱性,则该地适宜种植的作物是( )A.马铃薯 B.茶树 C.水稻 D.莲
4.下列实验现象叙述正确的是( )
A.硫粉在空气中燃烧:产生明亮的蓝紫色火焰,放热,生成有刺激性气味的气体
B.氢气通入灼热的氧化铜:黑色固体变成紫红色,试管口有无色液滴生成
C.铁粉加入稀硫酸:银白色固体表面有气泡产生,固体减少,放热,溶液由无色变为浅绿色
D.水通电:两极均有气体生成,正极多,负极少,体积比约为1:2
5.因胃酸过多引起的胃病可用抗酸剂治疗。下列常用抗酸剂中,属于氧化物的是
A.MgO B.CaCO3 C.NaHCO3 D.Al(OH)3
6.如图所示是盐酸滴入氢氧化钠溶液中,有关粒子之间反应的示意图.下列说法错误的是( )
A.盐酸溶液中含有氢离子和氯离子
B.氢氧化钠溶液中含有钠离子和氢氧根离子
C.两种溶液混合时,氢离子与氢氧根离子结合生成了水分子
D.两种溶液混合时,钠离子与氯离子结合生成了氯化钠分子
7.等质量、等质量分数的稀硫酸和烧碱溶液混合后,滴入紫色石蕊溶液,溶液呈现的颜色是( )
A.红色 B.蓝色 C.无色 D.紫色
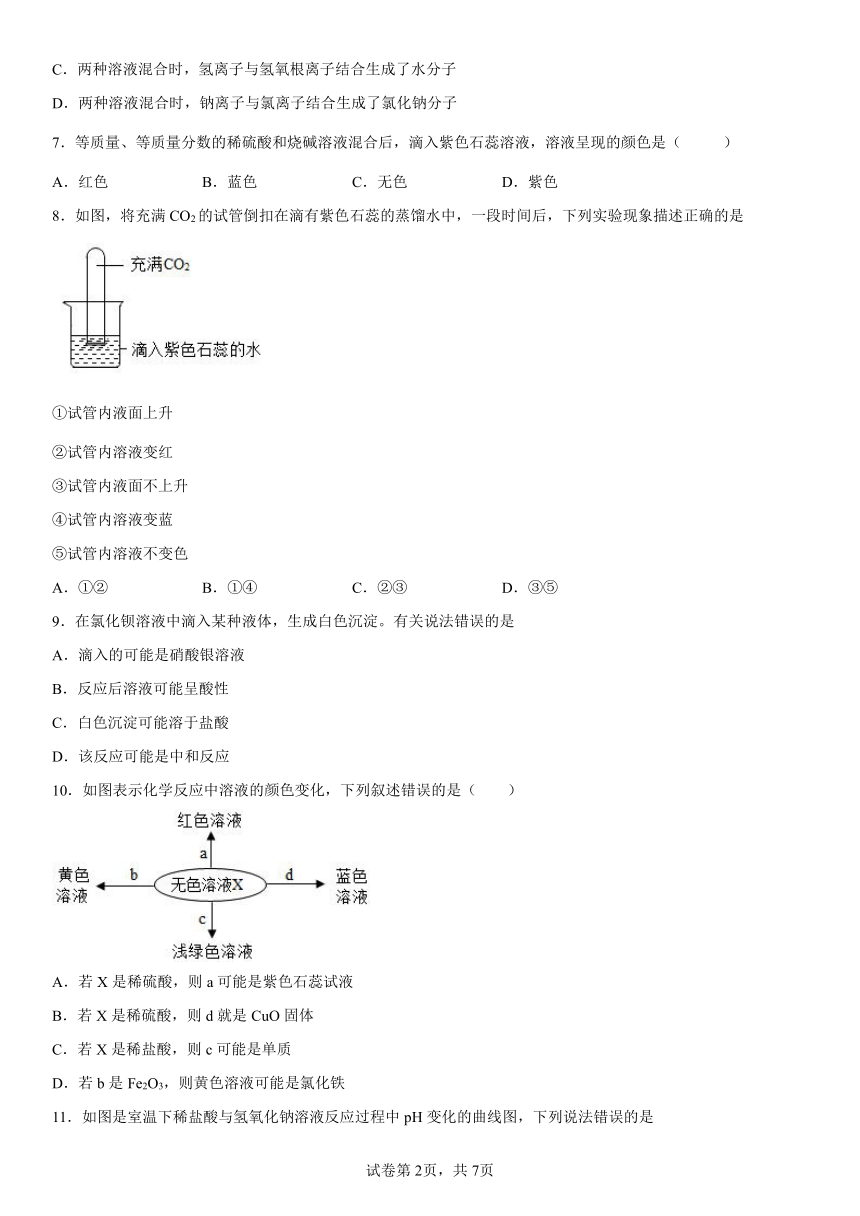
8.如图,将充满CO2的试管倒扣在滴有紫色石蕊的蒸馏水中,一段时间后,下列实验现象描述正确的是
①试管内液面上升
②试管内溶液变红
③试管内液面不上升
④试管内溶液变蓝
⑤试管内溶液不变色
A.①② B.①④ C.②③ D.③⑤
9.在氯化钡溶液中滴入某种液体,生成白色沉淀。有关说法错误的是
A.滴入的可能是硝酸银溶液
B.反应后溶液可能呈酸性
C.白色沉淀可能溶于盐酸
D.该反应可能是中和反应
10.如图表示化学反应中溶液的颜色变化,下列叙述错误的是( )
A.若X是稀硫酸,则a可能是紫色石蕊试液
B.若X是稀硫酸,则d就是CuO固体
C.若X是稀盐酸,则c可能是单质
D.若b是Fe2O3,则黄色溶液可能是氯化铁
11.如图是室温下稀盐酸与氢氧化钠溶液反应过程中pH变化的曲线图,下列说法错误的是
A.图中x是氢氧化钠溶液
B.a点溶液中含有两种溶质
C.b点表示两溶液恰好完全反应
D.滴加方式是将稀盐酸滴入到氢氧化钠溶液中
12.某化学小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法错误的是
A.该实验是将氢氧化钠溶液滴入稀盐酸中
B.a点所示溶液中,溶质只有NaCl
C.b点表示稀盐酸和氢氧化钠溶液恰好完全反应
D.向点c所示溶液中滴加紫色石蕊溶液,溶液变蓝色
二、简答题
13.(1)向盛有氢氧化钠溶液的烧杯中滴入几滴酚酞溶液,溶液变成_____色,pH_____(选填“>、=、<”)7,逐滴向烧杯中滴入稀盐酸,观察到的现象是_____,溶液的pH_____(选填“增大”或“减少”或“不变”);
(2)有一瓶溶液的pH是3.5,如果要使溶液的pH升高,可以通过加_____的方法。
14.“有一些花的颜色是红的、蓝的或紫的。这些花里含的色素叫“花青素”。花青素遇到酸就变红,遇到碱就变蓝…”小红在阅读此段文字后,做了如下家庭实验:将一朵紫色喇叭花泡在肥皂水里,喇叭花很快就变成了蓝色。她又将另一朵紫色喇叭花泡在家庭厨房里的某种调味品中,喇叭花变成了红色。请你根据以上实验现象回答:
(1)试确定肥皂水的值的范围。
(2)小红选用的调味品可能是什么?
(3)喇叭花汁液的性质与化学实验中常用的哪种指示剂的性质相似?
15.2003年重庆开县天然气发生井喷,喷出的气体中含有高浓度的硫化氢气体,该气体有毒,可燃烧产生二氧化硫和水,若当时及时点燃天然气,处理得当就不会造成大量人员伤亡。
⑴请写出硫化氢燃烧的化学方程式_____________________。
⑵反应前后各物质的化学计量数之和为___________。
⑶硫化氢的水溶液称为氢硫酸,能与NaOH溶液发生中和反应,反应的化学方程式是_______________。
三、推断题
16.A-E 为铁、稀硫酸、硫酸铜溶液、澄清石灰水、碳酸钠溶液中的一种,其中 E 是 蓝色溶液,B 为固体。它们之间的关系如图所示(“—”表示相连的物质能发生反应,所涉及 反应均为初中常见的化学反应),请回答下列问题:
(1)D 的化学式为__________________。
(2)E 与 C 反应的化学方程式_________________。
(3)图中属于复分解反应的有______个。
(4)如果 A、C、D、E 都不变,各物质间的关系不变,B 还可能 是________________。
A. Ag B .KOH C. BaCl2 D .Mg(OH)2 E .Fe2O3
17.有,,三种物质,已知为一种氯化物,为一种钠盐, 为一种碱.,,的溶液两两反应的实验现象如图所示,请根据有关实验现象回答.
(1)的化学式是 ______ ,的化学式是 ______ .
(2)与反应的化学方程式是 ______ .
(3)溶液与洁净的铁钉反应的化学方程式是 ______ .
四、实验题
18.硫酸是一种重要的化工原料,也是实验室中常用的化学试剂。下面是对硫酸的性质、用途等方面的探究,请回答有关问题。
(1)把50g质量分数为98%的浓硫酸稀释成10%的稀硫酸,需要水的质量是____________。
(2)浓硫酸稀释过程如右图所示,b中盛放的物质是__________。
(3)如下图所示将过量的稀硫酸分别加入A~E五只烧杯中。
①根据金属活动性顺序解释A烧杯中无明显现象的原因___________。
②反应结束后,B烧杯溶液中的溶质为___________(填化学式)。
③证明C中发生了化学反应的现象是__________。
④D中反应的化学方程式___________。
⑤根据E烧杯中的反应,写出硫酸的一种用途____________。
19.实验小组用pH传感器探究盐酸和氢氧化钠的反应。测定结果如图所示:
(1)盐酸和氢氧化钠反应的化学方程式为__________。
(2)向烧瓶中缓慢注入稀盐酸,能说明盐酸与氢氧化钠发生化学反应的现象是_______。
(3)d点时,烧瓶内溶液中的溶质有_________。
20.请根据如图回答问题:
(1)写出标有序号仪器的名称:①______;②______。
(2)实验室用高锰酸钾固体制取氧气的化学方程式为______;若要收集干燥的氧气,应选用装置______(填“A”、“B”或“C”)。
(3)装置D可以用来测量生成CO2的体积,其中在水面上放一层植物油的目的是______。
(4)收集CO2时,用燃着的木条来验满,是利用CO2______的化学性质。
(5)NH3是一种碱性气体,干燥时不能选用______作干燥剂(填“浓硫酸”或“生石灰”)。
五、计算题
21.化学实验小组的同学为研究某公共场所铁质护栏锈蚀的程度,将12.8g已生锈的铁片,放入一定浓度的稀盐酸中充分反应,测得产生气体的质量与稀盐酸的质量关系如图所示。(假设铁片只含有Fe2O3、Fe)
(1)生成氢气的质量为_______;
(2)所用稀盐酸中溶质的质量分数为_______?(写出计算过程)
22.现有溶质质量分数为20%的NaOH溶液20g,与-定质量的稀盐酸恰好完全反应。
计算:(1)NaOH溶液中溶质的质量为______g
(2)生成NaCl的质量_________。
23.造纸是我国古代四大发明之一,它有效地推动了人类文明的发展。
(1)回收农田产生的秸秆作为造纸原料,可以减少焚烧秸秆带来的______污染。秸秆的主要成分是纤维素[(C6H1005)n],纤维素中C、H、O三种元素的质量比为______(用最简整数比表示)。
(2)造纸会产生大量含NaOH的碱性废水,需经处理呈中性后排放。
①检测废水呈碱性的简单方法是_____。
②若某造纸厂废水中NaOH的质量分数为l.6%,现有废硫酸9.8 t(H2SO4的质量分数为20%),可以处理的废水质量是多少 (计算过程写在答题卡上)____________
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.D
3.D
4.B
5.A
6.D
7.B
8.A
9.D
10.B
11.A
12.B
13. 红 > 溶液由红色变成无色 减少 碱溶液如NaOH(或水、或其它合理答案)
14.(1)pH大于7
(2)食醋
(3)紫色石蕊试液
15. 2H2S + 3O2 2SO2+2H2O 9 H2S+2NaOH=Na2S+2H2O
16. H2SO4 Ca(OH)2+CuSO4=Cu(OH)2↓+CaSO4 3 BC
17.
18. 440g 浓硫酸 铜在金属活动性顺序中排在H后,不能与酸发生反应(或不能置换出酸中的氢) H2SO4和MgSO4 溶液红色褪去 除铁锈(或生产硫酸铁)
19. 溶液由红色逐渐变为无色,pH由大于7逐渐减小至小于7 NaCl、HCl
20.(1) 集气瓶 量筒
(2) A
(3)防止二氧化碳溶于水,且与水反应
(4)不燃烧,也不支持燃烧
(5)浓硫酸
21.(1)0.4g
(2)解:设所用稀盐酸中溶质的质量分数为x
答:所用稀盐酸中溶质的质量分数为14.6%。
22.(1)4 (2)5.85g
23. 烟尘 36∶5∶40 取样,滴入几滴无色酚酞溶液,若酚酞变红,则废水呈碱性(合理即可) 100t
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列物质的性质与用途,不相匹配的是( )
A.氧气可以支持燃烧 工业上可用作燃料
B.氮气的化学性质定稳 工业上可用作焊接保护气
C.白醋含有醋酸,显酸性 家庭中可用作除水垢
D.硫酸钡既不溶于水,也不与酸反应 医疗上可用于“钡餐”造影
2.下列物质属于盐的是
A.NaOH B.CaO C.Cu D.CaCO3
3.下表是几种作物适宜生长的pH范围:
作物 马铃薯 茶树 水稻 莲
pH 4.8~5.5 5.0~5.5 6.0~7.0 8.0~9.0
某地土壤呈碱性,则该地适宜种植的作物是( )A.马铃薯 B.茶树 C.水稻 D.莲
4.下列实验现象叙述正确的是( )
A.硫粉在空气中燃烧:产生明亮的蓝紫色火焰,放热,生成有刺激性气味的气体
B.氢气通入灼热的氧化铜:黑色固体变成紫红色,试管口有无色液滴生成
C.铁粉加入稀硫酸:银白色固体表面有气泡产生,固体减少,放热,溶液由无色变为浅绿色
D.水通电:两极均有气体生成,正极多,负极少,体积比约为1:2
5.因胃酸过多引起的胃病可用抗酸剂治疗。下列常用抗酸剂中,属于氧化物的是
A.MgO B.CaCO3 C.NaHCO3 D.Al(OH)3
6.如图所示是盐酸滴入氢氧化钠溶液中,有关粒子之间反应的示意图.下列说法错误的是( )
A.盐酸溶液中含有氢离子和氯离子
B.氢氧化钠溶液中含有钠离子和氢氧根离子
C.两种溶液混合时,氢离子与氢氧根离子结合生成了水分子
D.两种溶液混合时,钠离子与氯离子结合生成了氯化钠分子
7.等质量、等质量分数的稀硫酸和烧碱溶液混合后,滴入紫色石蕊溶液,溶液呈现的颜色是( )
A.红色 B.蓝色 C.无色 D.紫色
8.如图,将充满CO2的试管倒扣在滴有紫色石蕊的蒸馏水中,一段时间后,下列实验现象描述正确的是
①试管内液面上升
②试管内溶液变红
③试管内液面不上升
④试管内溶液变蓝
⑤试管内溶液不变色
A.①② B.①④ C.②③ D.③⑤
9.在氯化钡溶液中滴入某种液体,生成白色沉淀。有关说法错误的是
A.滴入的可能是硝酸银溶液
B.反应后溶液可能呈酸性
C.白色沉淀可能溶于盐酸
D.该反应可能是中和反应
10.如图表示化学反应中溶液的颜色变化,下列叙述错误的是( )
A.若X是稀硫酸,则a可能是紫色石蕊试液
B.若X是稀硫酸,则d就是CuO固体
C.若X是稀盐酸,则c可能是单质
D.若b是Fe2O3,则黄色溶液可能是氯化铁
11.如图是室温下稀盐酸与氢氧化钠溶液反应过程中pH变化的曲线图,下列说法错误的是
A.图中x是氢氧化钠溶液
B.a点溶液中含有两种溶质
C.b点表示两溶液恰好完全反应
D.滴加方式是将稀盐酸滴入到氢氧化钠溶液中
12.某化学小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法错误的是
A.该实验是将氢氧化钠溶液滴入稀盐酸中
B.a点所示溶液中,溶质只有NaCl
C.b点表示稀盐酸和氢氧化钠溶液恰好完全反应
D.向点c所示溶液中滴加紫色石蕊溶液,溶液变蓝色
二、简答题
13.(1)向盛有氢氧化钠溶液的烧杯中滴入几滴酚酞溶液,溶液变成_____色,pH_____(选填“>、=、<”)7,逐滴向烧杯中滴入稀盐酸,观察到的现象是_____,溶液的pH_____(选填“增大”或“减少”或“不变”);
(2)有一瓶溶液的pH是3.5,如果要使溶液的pH升高,可以通过加_____的方法。
14.“有一些花的颜色是红的、蓝的或紫的。这些花里含的色素叫“花青素”。花青素遇到酸就变红,遇到碱就变蓝…”小红在阅读此段文字后,做了如下家庭实验:将一朵紫色喇叭花泡在肥皂水里,喇叭花很快就变成了蓝色。她又将另一朵紫色喇叭花泡在家庭厨房里的某种调味品中,喇叭花变成了红色。请你根据以上实验现象回答:
(1)试确定肥皂水的值的范围。
(2)小红选用的调味品可能是什么?
(3)喇叭花汁液的性质与化学实验中常用的哪种指示剂的性质相似?
15.2003年重庆开县天然气发生井喷,喷出的气体中含有高浓度的硫化氢气体,该气体有毒,可燃烧产生二氧化硫和水,若当时及时点燃天然气,处理得当就不会造成大量人员伤亡。
⑴请写出硫化氢燃烧的化学方程式_____________________。
⑵反应前后各物质的化学计量数之和为___________。
⑶硫化氢的水溶液称为氢硫酸,能与NaOH溶液发生中和反应,反应的化学方程式是_______________。
三、推断题
16.A-E 为铁、稀硫酸、硫酸铜溶液、澄清石灰水、碳酸钠溶液中的一种,其中 E 是 蓝色溶液,B 为固体。它们之间的关系如图所示(“—”表示相连的物质能发生反应,所涉及 反应均为初中常见的化学反应),请回答下列问题:
(1)D 的化学式为__________________。
(2)E 与 C 反应的化学方程式_________________。
(3)图中属于复分解反应的有______个。
(4)如果 A、C、D、E 都不变,各物质间的关系不变,B 还可能 是________________。
A. Ag B .KOH C. BaCl2 D .Mg(OH)2 E .Fe2O3
17.有,,三种物质,已知为一种氯化物,为一种钠盐, 为一种碱.,,的溶液两两反应的实验现象如图所示,请根据有关实验现象回答.
(1)的化学式是 ______ ,的化学式是 ______ .
(2)与反应的化学方程式是 ______ .
(3)溶液与洁净的铁钉反应的化学方程式是 ______ .
四、实验题
18.硫酸是一种重要的化工原料,也是实验室中常用的化学试剂。下面是对硫酸的性质、用途等方面的探究,请回答有关问题。
(1)把50g质量分数为98%的浓硫酸稀释成10%的稀硫酸,需要水的质量是____________。
(2)浓硫酸稀释过程如右图所示,b中盛放的物质是__________。
(3)如下图所示将过量的稀硫酸分别加入A~E五只烧杯中。
①根据金属活动性顺序解释A烧杯中无明显现象的原因___________。
②反应结束后,B烧杯溶液中的溶质为___________(填化学式)。
③证明C中发生了化学反应的现象是__________。
④D中反应的化学方程式___________。
⑤根据E烧杯中的反应,写出硫酸的一种用途____________。
19.实验小组用pH传感器探究盐酸和氢氧化钠的反应。测定结果如图所示:
(1)盐酸和氢氧化钠反应的化学方程式为__________。
(2)向烧瓶中缓慢注入稀盐酸,能说明盐酸与氢氧化钠发生化学反应的现象是_______。
(3)d点时,烧瓶内溶液中的溶质有_________。
20.请根据如图回答问题:
(1)写出标有序号仪器的名称:①______;②______。
(2)实验室用高锰酸钾固体制取氧气的化学方程式为______;若要收集干燥的氧气,应选用装置______(填“A”、“B”或“C”)。
(3)装置D可以用来测量生成CO2的体积,其中在水面上放一层植物油的目的是______。
(4)收集CO2时,用燃着的木条来验满,是利用CO2______的化学性质。
(5)NH3是一种碱性气体,干燥时不能选用______作干燥剂(填“浓硫酸”或“生石灰”)。
五、计算题
21.化学实验小组的同学为研究某公共场所铁质护栏锈蚀的程度,将12.8g已生锈的铁片,放入一定浓度的稀盐酸中充分反应,测得产生气体的质量与稀盐酸的质量关系如图所示。(假设铁片只含有Fe2O3、Fe)
(1)生成氢气的质量为_______;
(2)所用稀盐酸中溶质的质量分数为_______?(写出计算过程)
22.现有溶质质量分数为20%的NaOH溶液20g,与-定质量的稀盐酸恰好完全反应。
计算:(1)NaOH溶液中溶质的质量为______g
(2)生成NaCl的质量_________。
23.造纸是我国古代四大发明之一,它有效地推动了人类文明的发展。
(1)回收农田产生的秸秆作为造纸原料,可以减少焚烧秸秆带来的______污染。秸秆的主要成分是纤维素[(C6H1005)n],纤维素中C、H、O三种元素的质量比为______(用最简整数比表示)。
(2)造纸会产生大量含NaOH的碱性废水,需经处理呈中性后排放。
①检测废水呈碱性的简单方法是_____。
②若某造纸厂废水中NaOH的质量分数为l.6%,现有废硫酸9.8 t(H2SO4的质量分数为20%),可以处理的废水质量是多少 (计算过程写在答题卡上)____________
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.D
3.D
4.B
5.A
6.D
7.B
8.A
9.D
10.B
11.A
12.B
13. 红 > 溶液由红色变成无色 减少 碱溶液如NaOH(或水、或其它合理答案)
14.(1)pH大于7
(2)食醋
(3)紫色石蕊试液
15. 2H2S + 3O2 2SO2+2H2O 9 H2S+2NaOH=Na2S+2H2O
16. H2SO4 Ca(OH)2+CuSO4=Cu(OH)2↓+CaSO4 3 BC
17.
18. 440g 浓硫酸 铜在金属活动性顺序中排在H后,不能与酸发生反应(或不能置换出酸中的氢) H2SO4和MgSO4 溶液红色褪去 除铁锈(或生产硫酸铁)
19. 溶液由红色逐渐变为无色,pH由大于7逐渐减小至小于7 NaCl、HCl
20.(1) 集气瓶 量筒
(2) A
(3)防止二氧化碳溶于水,且与水反应
(4)不燃烧,也不支持燃烧
(5)浓硫酸
21.(1)0.4g
(2)解:设所用稀盐酸中溶质的质量分数为x
答:所用稀盐酸中溶质的质量分数为14.6%。
22.(1)4 (2)5.85g
23. 烟尘 36∶5∶40 取样,滴入几滴无色酚酞溶液,若酚酞变红,则废水呈碱性(合理即可) 100t
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
