第四单元《盐化肥》练习—2022-2023学年九年级化学人教版(五四学制)全一册(有答案)
文档属性
| 名称 | 第四单元《盐化肥》练习—2022-2023学年九年级化学人教版(五四学制)全一册(有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 119.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-15 00:00:00 | ||
图片预览


文档简介
第四单元《盐 化肥》练习
一、单选题
1.只用水一种试剂不能将下列各组固体物质鉴别出来的是( )
A.CuSO4和MgSO4 B.CaCO3和CaCl2
C.NH4NO3和NaC1 D.K2SO4和Na2SO4
2.中国丝绸有几千年的历史传承。古代染坊常用某种“碱剂”来处理丝绸,该“碱剂”可使丝绸颜色洁白、质感柔软,其主要成分是一种盐,这种“碱剂”可能是
A.食醋 B.烧碱 C.草木灰 D.生石灰
3.将珍珠加入稀盐酸中,有气泡产生,生成的气体能使澄清石灰水变浑浊,则珍珠中含有下列离子中的( )
A.氯离子 B.硫酸根离子 C.碳酸根离子 D.氢氧根离子
4.下列有关常见酸、碱、盐的说法不正确的是( )
A.浓盐酸具有挥发性,浓硫酸具有吸水性
B.Na2CO3和CaCO3都是白色易溶于水的固体
C.NaCl是白色易溶于水的固体,溶解度受温度影响小
D.NaOH和Ca(OH)2露置在空气中容易变质
5.下列物质的名称或俗名,属同一种物质的是
A.生石灰 熟石灰 消石灰 B.冰 干冰 可燃冰
C.烧碱 苛性钠 火碱 D.石灰石 熟石灰 大理石
6.中华古代文化蕴含着丰富的化学知识,下列理解不合理的是
选项 文摘 理解
A 露从今夜白,月是故乡明 描述中有物理变化
B 暖暖远人村,依依墟里烟 描述中有化学变化
C 金(即铜)柔锡柔,合两柔则刚 合金的硬度比组成它的纯金属大
D 冬日灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣 其中的碱是指NaOH
A.A B.B C.C D.D
7.某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的 pH 随滴加液体体积变化的曲线如图所示。下列说法正确的是( )
A.图中a点所示溶液中,含有的溶质是NaCl和NaOH
B.由a点到b点的pH变化过程证明酸和碱发生了中和反应
C.向图中c点所示溶液中滴加无色酚酞,溶液不变色
D.该实验是将盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯中
8.盐酸先生闯迷宫(见图),请你帮他选择行进路线(不发生化学反应)。( )
A.A B.B C.C D.D
9.除去下列物质中的杂质,所选方法错误的是
A.除去CaO中的CaCO3:高温煅烧
B.除去氮气中含有的氧气:通过灼热的铜网
C.除去氧化铜中的木炭粉:隔绝空气充分灼烧
D.除去Ag粉中的Fe粉:加入过量的稀硫酸后过滤
10.下列图像能正确反映其对应变化关系的是
A.加热一定质量的高锰酸钾固体
B.向盛有少量硫酸溶液的烧杯中滴加一定质量的水
C.向盛有一定质量二氧化锰的烧杯中加入过氧化氢溶液
D.向盛有一定质量NaOH和Na2CO3混合溶液的烧杯中滴加稀盐酸
二、简答题
11.化学与生活密切相关,请回答下列问题:
(1)打开汽水瓶盖时,汽水为什么会自动喷出来?___________
(2)在书写具有保存价值的档案时,规定应使用碳素墨水,为什么?___________
(3)随意丢弃塑料制品会造成“白色污染”,请你谈一点减少“白色污染”的措施._____________
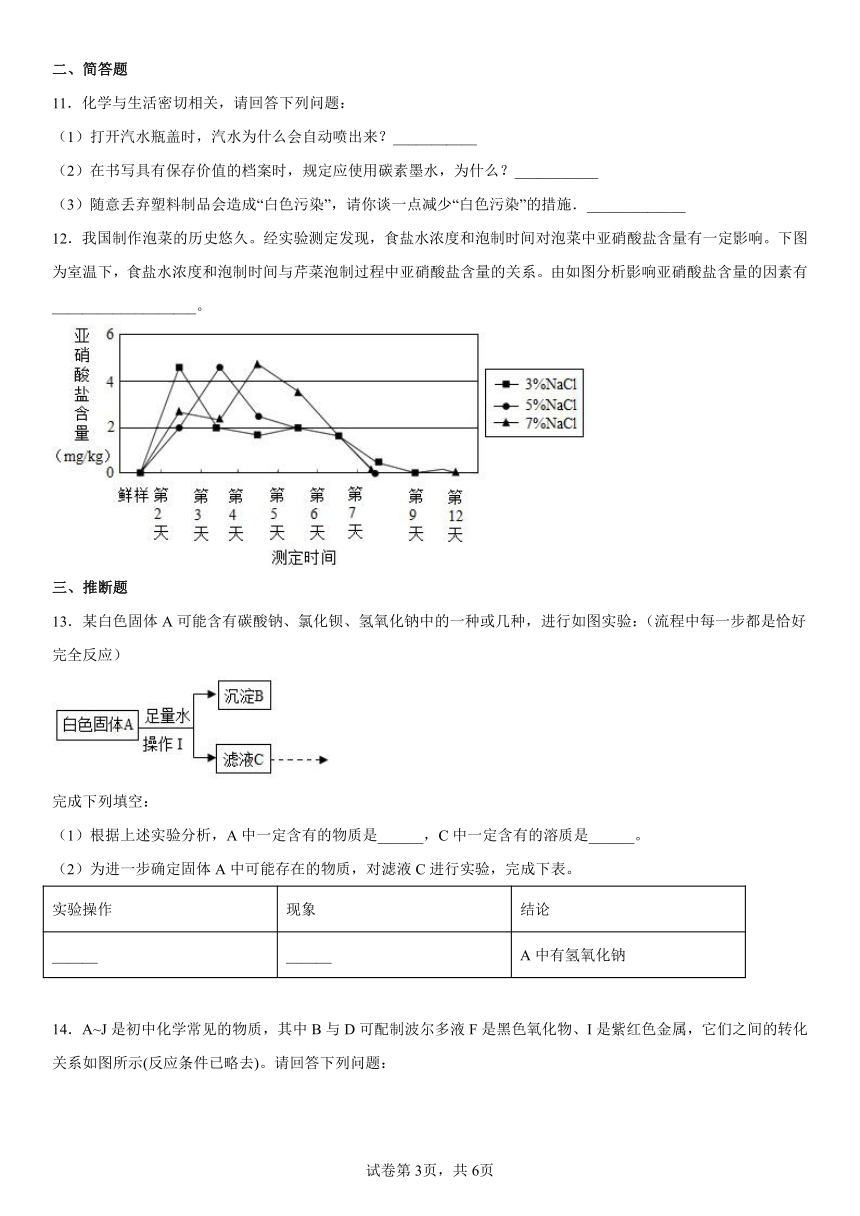
12.我国制作泡菜的历史悠久。经实验测定发现,食盐水浓度和泡制时间对泡菜中亚硝酸盐含量有一定影响。下图为室温下,食盐水浓度和泡制时间与芹菜泡制过程中亚硝酸盐含量的关系。由如图分析影响亚硝酸盐含量的因素有___________________。
三、推断题
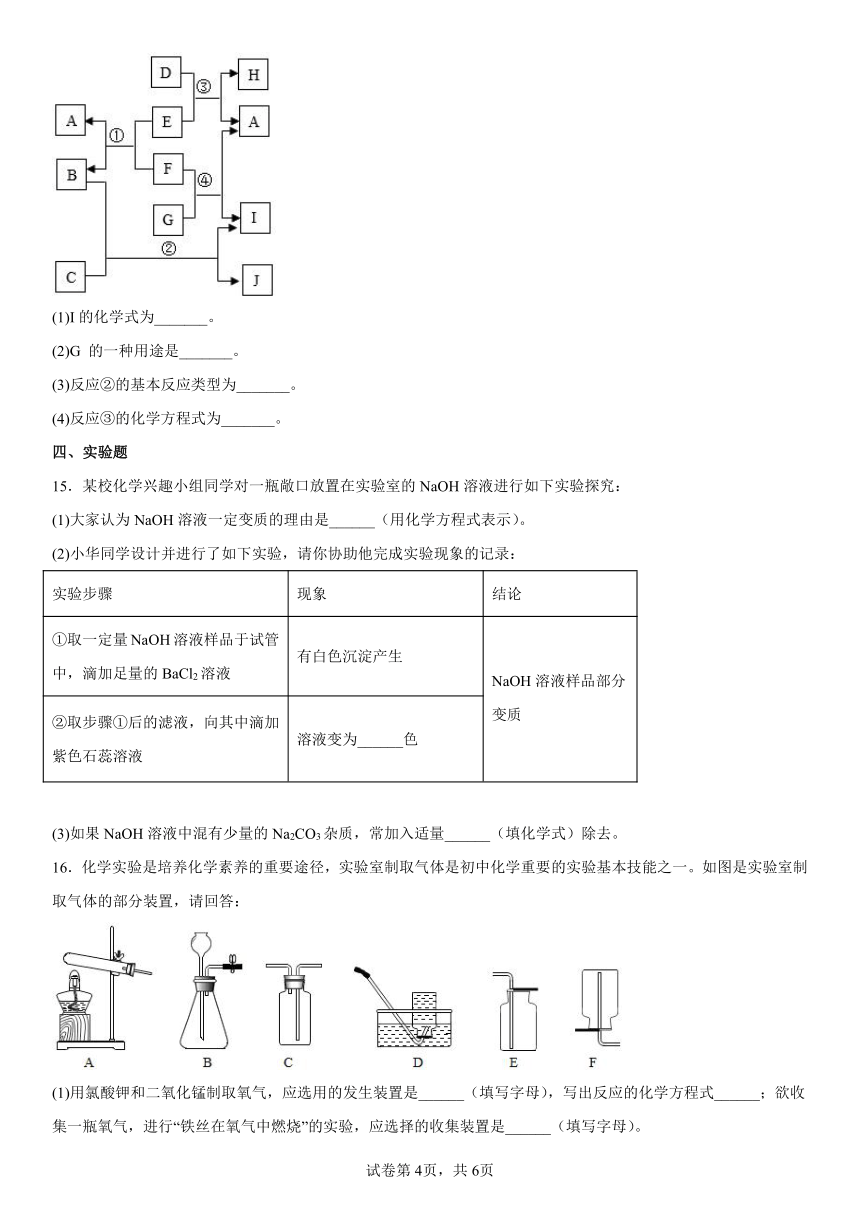
13.某白色固体A可能含有碳酸钠、氯化钡、氢氧化钠中的一种或几种,进行如图实验:(流程中每一步都是恰好完全反应)
完成下列填空:
(1)根据上述实验分析,A中一定含有的物质是______,C中一定含有的溶质是______。
(2)为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成下表。
实验操作 现象 结论
______ ______ A中有氢氧化钠
14.A~J是初中化学常见的物质,其中B与D可配制波尔多液F是黑色氧化物、I是紫红色金属,它们之间的转化关系如图所示(反应条件已略去)。请回答下列问题:
(1)I的化学式为_______。
(2)G 的一种用途是_______。
(3)反应②的基本反应类型为_______。
(4)反应③的化学方程式为_______。
四、实验题
15.某校化学兴趣小组同学对一瓶敞口放置在实验室的NaOH溶液进行如下实验探究:
(1)大家认为NaOH溶液一定变质的理由是______(用化学方程式表示)。
(2)小华同学设计并进行了如下实验,请你协助他完成实验现象的记录:
实验步骤 现象 结论
①取一定量NaOH溶液样品于试管中,滴加足量的BaCl2溶液 有白色沉淀产生 NaOH溶液样品部分变质
②取步骤①后的滤液,向其中滴加紫色石蕊溶液 溶液变为______色
(3)如果NaOH溶液中混有少量的Na2CO3杂质,常加入适量______(填化学式)除去。
16.化学实验是培养化学素养的重要途径,实验室制取气体是初中化学重要的实验基本技能之一。如图是实验室制取气体的部分装置,请回答:
(1)用氯酸钾和二氧化锰制取氧气,应选用的发生装置是______(填写字母),写出反应的化学方程式______;欲收集一瓶氧气,进行“铁丝在氧气中燃烧”的实验,应选择的收集装置是______(填写字母)。
(2)用大理石和稀盐酸制取二氧化碳气体,反应的化学方程式______。检验二氧化碳气体收集满的方法是______(填写序号)。
①将带火星木条伸入集气瓶中
②将少量石灰水倒入集气瓶中
③将燃着的木条放在集气瓶口
④将pH试纸放置在集气瓶口
上述实验结束一段时间后,同学们发现回收的大理石表面有一层白色固体物质,大家纷纷猜想它的成分。以下是同学们的实验过程,请你参与探究。
可供选择的试剂:回收的大理石、石蕊试液、酚酞试液、硝酸银溶液、稀硝酸、碳酸钠溶液、蒸馏水
实验操作 实验现象 实验结论
①将回收的大理石放入烧杯中,加入适量蒸馏水洗涤,过滤 白色固体物质溶解,得到澄清滤液 白色固体物质溶于水
②取滤液于试管中,滴加______溶液 有白色沉淀生成 滤液中有
③取滤液于试管中,滴加硝酸银溶液,再滴加稀硝酸 有白色沉淀生成 滤液中有______
结论:回收的大理石表面白色固体物质是没有洗涤的氯化钙
五、计算题
17.某化学小组进行硫酸铜溶液和氢氧化钠溶液相混合的实验实验过程及数据如下图所示:[反应原理为]。
计算氢氧化钠溶液中溶质的质量分数。
18.某中学化学课外实验兴趣小组欲测定一瓶混有氯化钠的苏打中碳酸钠的质量分数。从该瓶试剂中取出100克样品,放在锥形瓶中加水至全部溶解,再加入稀盐酸,实验相关数据如图。
(1)产生的二氧化碳气体是__________克;
(2)该瓶苏打中碳酸钠的质量分数是_________?(写出计算过程)
19.尿素是常用的一种化肥,其化学式为CO(NH2)2,根据其化学式进行计算:
(1)尿素的相对分子质量;
(2)尿素中氮元素的质量分数是多少?(结果保留1位小数)
(3)多少克碳酸氢铵(NH4HCO3)中所含的氮元素与60克尿素中所含的氮元素质量相等?(结果保留1位小数)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.C
3.C
4.B
5.C
6.D
7.B
8.B
9.C
10.D
11. 打开汽水瓶盖,压强变小,二氧化碳的溶解度减小 常温下,碳的化学性质不活泼 用布袋代替塑料袋等(合理即可)
12.食盐水浓度和泡制时间
13. Na2CO3、BaCl2(或填碳酸钠和氯化钡) NaC1(或填氯化钠) 取少量滤液C于试管中,滴加无色酚酞 滤液变为红色(答案不唯一,合理即可)
14. Cu 清洁燃料,或冶炼金属 置换反应 Ca(OH)2+H2SO4=CaSO4+2H2O
15.(1)2NaOH+CO2═Na2CO3+H2O
(2)蓝
(3)Ca(OH)2
16.(1) A 2KClO32KCl+3O2↑ D
(2) CaCO3+2HCl=CaCl2+H2O+CO2↑ ③ 碳酸钠 氯离子##Cl-
17.解:设参加反应的氢氧化钠质量为x。
x=4g
×100%=8%
答:氢氧化钠溶液中溶质的质量分数为8%。
18.(1)4.4(2)10.6%
19.(1)60(2)46.7%(3)158g
答案第1页,共2页
答案第1页,共2页
一、单选题
1.只用水一种试剂不能将下列各组固体物质鉴别出来的是( )
A.CuSO4和MgSO4 B.CaCO3和CaCl2
C.NH4NO3和NaC1 D.K2SO4和Na2SO4
2.中国丝绸有几千年的历史传承。古代染坊常用某种“碱剂”来处理丝绸,该“碱剂”可使丝绸颜色洁白、质感柔软,其主要成分是一种盐,这种“碱剂”可能是
A.食醋 B.烧碱 C.草木灰 D.生石灰
3.将珍珠加入稀盐酸中,有气泡产生,生成的气体能使澄清石灰水变浑浊,则珍珠中含有下列离子中的( )
A.氯离子 B.硫酸根离子 C.碳酸根离子 D.氢氧根离子
4.下列有关常见酸、碱、盐的说法不正确的是( )
A.浓盐酸具有挥发性,浓硫酸具有吸水性
B.Na2CO3和CaCO3都是白色易溶于水的固体
C.NaCl是白色易溶于水的固体,溶解度受温度影响小
D.NaOH和Ca(OH)2露置在空气中容易变质
5.下列物质的名称或俗名,属同一种物质的是
A.生石灰 熟石灰 消石灰 B.冰 干冰 可燃冰
C.烧碱 苛性钠 火碱 D.石灰石 熟石灰 大理石
6.中华古代文化蕴含着丰富的化学知识,下列理解不合理的是
选项 文摘 理解
A 露从今夜白,月是故乡明 描述中有物理变化
B 暖暖远人村,依依墟里烟 描述中有化学变化
C 金(即铜)柔锡柔,合两柔则刚 合金的硬度比组成它的纯金属大
D 冬日灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣 其中的碱是指NaOH
A.A B.B C.C D.D
7.某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的 pH 随滴加液体体积变化的曲线如图所示。下列说法正确的是( )
A.图中a点所示溶液中,含有的溶质是NaCl和NaOH
B.由a点到b点的pH变化过程证明酸和碱发生了中和反应
C.向图中c点所示溶液中滴加无色酚酞,溶液不变色
D.该实验是将盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯中
8.盐酸先生闯迷宫(见图),请你帮他选择行进路线(不发生化学反应)。( )
A.A B.B C.C D.D
9.除去下列物质中的杂质,所选方法错误的是
A.除去CaO中的CaCO3:高温煅烧
B.除去氮气中含有的氧气:通过灼热的铜网
C.除去氧化铜中的木炭粉:隔绝空气充分灼烧
D.除去Ag粉中的Fe粉:加入过量的稀硫酸后过滤
10.下列图像能正确反映其对应变化关系的是
A.加热一定质量的高锰酸钾固体
B.向盛有少量硫酸溶液的烧杯中滴加一定质量的水
C.向盛有一定质量二氧化锰的烧杯中加入过氧化氢溶液
D.向盛有一定质量NaOH和Na2CO3混合溶液的烧杯中滴加稀盐酸
二、简答题
11.化学与生活密切相关,请回答下列问题:
(1)打开汽水瓶盖时,汽水为什么会自动喷出来?___________
(2)在书写具有保存价值的档案时,规定应使用碳素墨水,为什么?___________
(3)随意丢弃塑料制品会造成“白色污染”,请你谈一点减少“白色污染”的措施._____________
12.我国制作泡菜的历史悠久。经实验测定发现,食盐水浓度和泡制时间对泡菜中亚硝酸盐含量有一定影响。下图为室温下,食盐水浓度和泡制时间与芹菜泡制过程中亚硝酸盐含量的关系。由如图分析影响亚硝酸盐含量的因素有___________________。
三、推断题
13.某白色固体A可能含有碳酸钠、氯化钡、氢氧化钠中的一种或几种,进行如图实验:(流程中每一步都是恰好完全反应)
完成下列填空:
(1)根据上述实验分析,A中一定含有的物质是______,C中一定含有的溶质是______。
(2)为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成下表。
实验操作 现象 结论
______ ______ A中有氢氧化钠
14.A~J是初中化学常见的物质,其中B与D可配制波尔多液F是黑色氧化物、I是紫红色金属,它们之间的转化关系如图所示(反应条件已略去)。请回答下列问题:
(1)I的化学式为_______。
(2)G 的一种用途是_______。
(3)反应②的基本反应类型为_______。
(4)反应③的化学方程式为_______。
四、实验题
15.某校化学兴趣小组同学对一瓶敞口放置在实验室的NaOH溶液进行如下实验探究:
(1)大家认为NaOH溶液一定变质的理由是______(用化学方程式表示)。
(2)小华同学设计并进行了如下实验,请你协助他完成实验现象的记录:
实验步骤 现象 结论
①取一定量NaOH溶液样品于试管中,滴加足量的BaCl2溶液 有白色沉淀产生 NaOH溶液样品部分变质
②取步骤①后的滤液,向其中滴加紫色石蕊溶液 溶液变为______色
(3)如果NaOH溶液中混有少量的Na2CO3杂质,常加入适量______(填化学式)除去。
16.化学实验是培养化学素养的重要途径,实验室制取气体是初中化学重要的实验基本技能之一。如图是实验室制取气体的部分装置,请回答:
(1)用氯酸钾和二氧化锰制取氧气,应选用的发生装置是______(填写字母),写出反应的化学方程式______;欲收集一瓶氧气,进行“铁丝在氧气中燃烧”的实验,应选择的收集装置是______(填写字母)。
(2)用大理石和稀盐酸制取二氧化碳气体,反应的化学方程式______。检验二氧化碳气体收集满的方法是______(填写序号)。
①将带火星木条伸入集气瓶中
②将少量石灰水倒入集气瓶中
③将燃着的木条放在集气瓶口
④将pH试纸放置在集气瓶口
上述实验结束一段时间后,同学们发现回收的大理石表面有一层白色固体物质,大家纷纷猜想它的成分。以下是同学们的实验过程,请你参与探究。
可供选择的试剂:回收的大理石、石蕊试液、酚酞试液、硝酸银溶液、稀硝酸、碳酸钠溶液、蒸馏水
实验操作 实验现象 实验结论
①将回收的大理石放入烧杯中,加入适量蒸馏水洗涤,过滤 白色固体物质溶解,得到澄清滤液 白色固体物质溶于水
②取滤液于试管中,滴加______溶液 有白色沉淀生成 滤液中有
③取滤液于试管中,滴加硝酸银溶液,再滴加稀硝酸 有白色沉淀生成 滤液中有______
结论:回收的大理石表面白色固体物质是没有洗涤的氯化钙
五、计算题
17.某化学小组进行硫酸铜溶液和氢氧化钠溶液相混合的实验实验过程及数据如下图所示:[反应原理为]。
计算氢氧化钠溶液中溶质的质量分数。
18.某中学化学课外实验兴趣小组欲测定一瓶混有氯化钠的苏打中碳酸钠的质量分数。从该瓶试剂中取出100克样品,放在锥形瓶中加水至全部溶解,再加入稀盐酸,实验相关数据如图。
(1)产生的二氧化碳气体是__________克;
(2)该瓶苏打中碳酸钠的质量分数是_________?(写出计算过程)
19.尿素是常用的一种化肥,其化学式为CO(NH2)2,根据其化学式进行计算:
(1)尿素的相对分子质量;
(2)尿素中氮元素的质量分数是多少?(结果保留1位小数)
(3)多少克碳酸氢铵(NH4HCO3)中所含的氮元素与60克尿素中所含的氮元素质量相等?(结果保留1位小数)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.C
3.C
4.B
5.C
6.D
7.B
8.B
9.C
10.D
11. 打开汽水瓶盖,压强变小,二氧化碳的溶解度减小 常温下,碳的化学性质不活泼 用布袋代替塑料袋等(合理即可)
12.食盐水浓度和泡制时间
13. Na2CO3、BaCl2(或填碳酸钠和氯化钡) NaC1(或填氯化钠) 取少量滤液C于试管中,滴加无色酚酞 滤液变为红色(答案不唯一,合理即可)
14. Cu 清洁燃料,或冶炼金属 置换反应 Ca(OH)2+H2SO4=CaSO4+2H2O
15.(1)2NaOH+CO2═Na2CO3+H2O
(2)蓝
(3)Ca(OH)2
16.(1) A 2KClO32KCl+3O2↑ D
(2) CaCO3+2HCl=CaCl2+H2O+CO2↑ ③ 碳酸钠 氯离子##Cl-
17.解:设参加反应的氢氧化钠质量为x。
x=4g
×100%=8%
答:氢氧化钠溶液中溶质的质量分数为8%。
18.(1)4.4(2)10.6%
19.(1)60(2)46.7%(3)158g
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
