人教版九年级化学 第八单元 金属和金属材料 复习课件(共24张PPT)
文档属性
| 名称 | 人教版九年级化学 第八单元 金属和金属材料 复习课件(共24张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-16 00:00:00 | ||
图片预览





文档简介
(共24张PPT)
单元复习
第八单元复习
目录
01
思维导图
03
重点突破
02
易错点透析
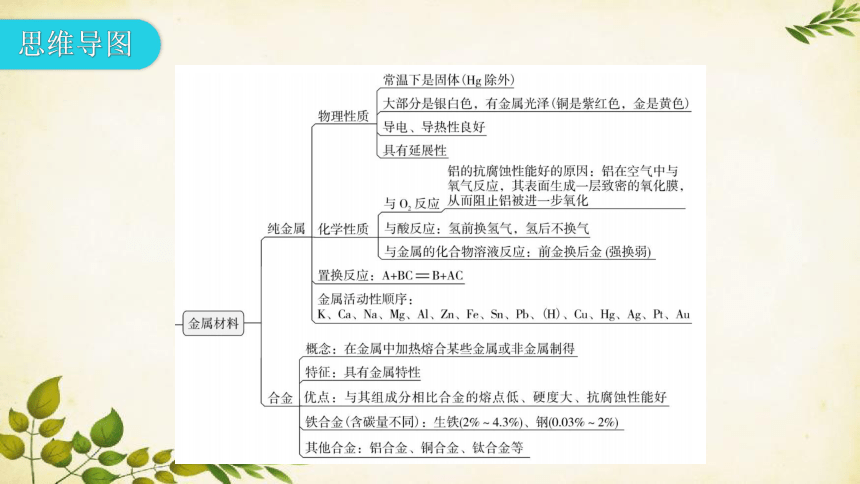
思维导图
易错点透析
易错点
不能正确应用金属活动性顺序
结合金属活动性顺序的应用推测实验方案的设计是否合理,然后做出选择即可。
【例】某同学为验证铁、铜、银三种金属的活动性顺序,他设计了以下四种实验方案,其中能达到目的是( )
A. 将Fe、Cu分别加入AgNO3溶液中
B. 将Fe、Cu、Ag分别加入稀盐酸中
C. 将Fe分别加入CuSO4、AgNO3溶液中
D. 将Fe、Ag分别加入CuSO4溶液中
易错提醒:这类题目不会采取“三取中”的方法。此方法是取中间金属的单质和两端金属的盐溶液反应或取中间金属的盐溶液与两端金属的单质反应。
正解:根据金属活动性顺序可知铁、铜、银的金属活动性顺序为铁>铜>银。根据两液夹一金,可选择试剂硫酸亚铁溶液、铜、硝酸银溶液;或根据两金夹一液,可选择试剂铁、硫酸铜溶液、银。
答案:D
学以致用
能验证Zn、Cu、Ag三种金属活动性顺序的一组试剂是( )
A. Zn、Cu、Ag、稀硫酸
B. Zn(NO3)2溶液、Ag、Cu(NO3)2溶液
C. Zn(NO3)2溶液、Cu、AgNO3溶液
D. Cu、Ag、Zn(NO3)2溶液
C
重点突破
重点1 化学方程式的书写
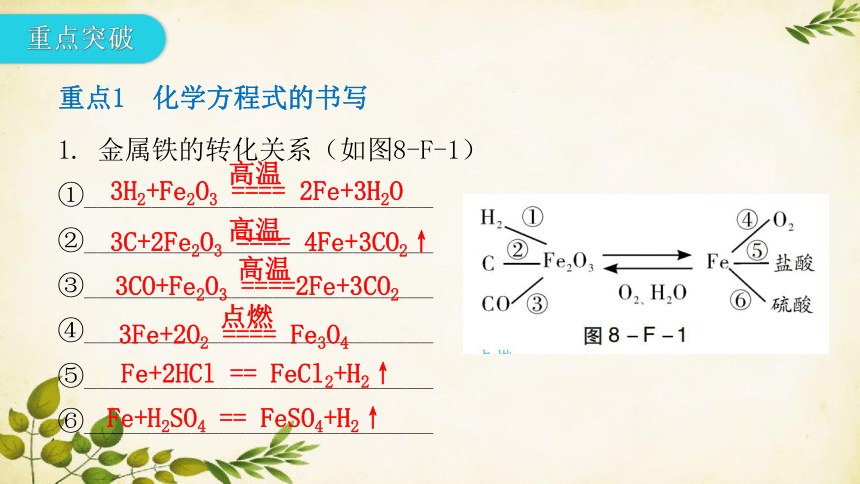
1. 金属铁的转化关系(如图8-F-1)
①__________________________
②__________________________
③__________________________
④__________________________
⑤__________________________
⑥__________________________
3H2+Fe2O3 ==== 2Fe+3H2O
高温
3C+2Fe2O3 ==== 4Fe+3CO2↑
高温
3CO+Fe2O3 ====2Fe+3CO2
高温
3Fe+2O2 ==== Fe3O4
点燃
Fe+2HCl == FeCl2+H2↑
Fe+H2SO4 == FeSO4+H2↑
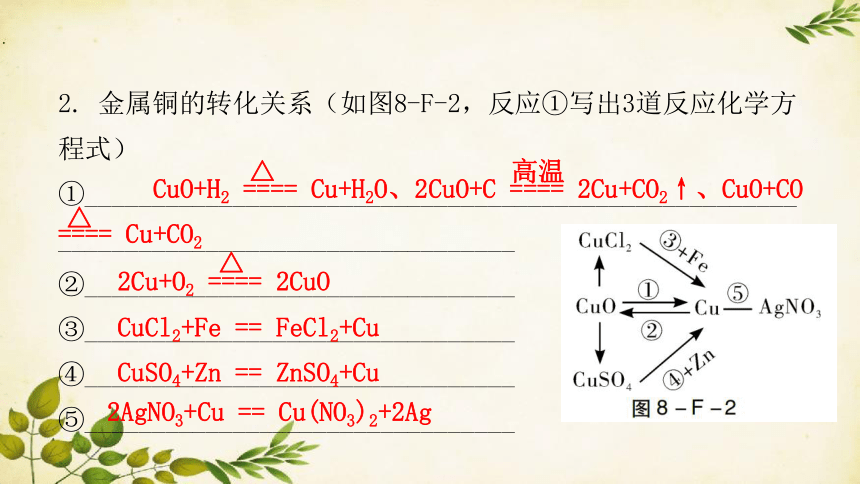
2. 金属铜的转化关系(如图8-F-2,反应①写出3道反应化学方程式)
①_____________________________________________________
__________________________________
②________________________________
③________________________________
④________________________________
⑤________________________________
CuO+H2 ==== Cu+H2O、2CuO+C ==== 2Cu+CO2↑、CuO+CO ==== Cu+CO2
△
高温
△
CuCl2+Fe == FeCl2+Cu
CuSO4+Zn == ZnSO4+Cu
2AgNO3+Cu == Cu(NO3)2+2Ag
2Cu+O2 ==== 2CuO
△
重点2 金属材料
3. (社会热点)狡猾的新冠病毒再次侵袭我国部分省市,随着气温下降新冠病毒的活性会有所增加,大家一定要少聚集、勤洗手、戴口罩!防疫不松懈!如图8-F-3所示为增强口罩的密封性,均放了鼻梁条,鼻梁条是铝合金做的,口罩核心材料为熔喷布。关于口罩的说法正确的是( )
A. 铝合金属于纯净物
B. 鼻梁条使用铝合金,利用其硬度大、抗腐
蚀性好的优点
C. 铝合金属于金属材料
D. 铝合金的熔点比金属铝高
C
4. 金属材料在现实生活中有极为重要的作用,下列金属材料的运用与金属所具有的性质不一致的是( )
A. 制造刀具——硬度大
B. 制造炊具——导热性
C. 制造集成电路板——硬度大
D. 制造装化工原料的容器——耐腐蚀
C
重点3 金属的化学性质
5. 常温下向一定质量的稀盐酸中逐渐加入镁条,充分反应(忽略挥发)。图8-F-4中的图像正确的是( )
A. ①② B. ②③ C. ①④ D. ②④
C
6. 某种手机电路板主要含有Fe、Cu、Ag(银)、Ni(镍)等金属及非金属材料,如图8-F-5所示是某工厂回收金属铜的工艺流程图。
(1)电路板不直接焚烧而采取热风处理的主要目的是_____________________________________________________。
(2)操作①的名称是__________。
防止金属和氧气反应生成金属氧化物
过滤
(3)写出滤液③与铁粉反应的化学方程式:_______________________________。
(4)Fe、Cu、Ag、Ni在溶液中的金属活动性顺序由强到弱依次为_______________________________。
(5)写出⑤得到纯铜的一种方法:_______________________________________________________。
Fe+CuSO4 == FeSO4+Cu
Fe>Ni>Cu>Ag
在滤渣中加入适量的稀硫酸,过滤、洗涤、干燥
重点4 金属的活动性顺序
7. 有X、Y、Z三种金属,X在常温下就能与氧气反应,Y、Z在常温下几乎不与氧气反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Z表面有银析出,而Y没有变化。根据以上实验事实,判断X、Y、Z三种金属的活动性由强弱的顺序正确的是( )
A. X、Y、Z B. X、Z、Y
C. Y、Z、X D. Z、Y、X
B
8. 除去下列物质中的杂质,所选方法错误的是( )
D
选项 物质 杂质 除杂方法
A Cu Fe 加入过量稀硫酸,过滤
B FeCl2溶液 CuCl2 加入过量铁粉,过滤
C N2 O2 通过灼热的铜网
D CO2 CO 点燃
重点5 金属防腐
9. (创新实验)如图8-F-6所示是某化学小组设计的铁制品锈蚀的实验装置。下列相关叙述中正确的是( )
①铁锈的主要成分是Fe2O3 ②一段时间后,塑料瓶可能会变瘪 ③一段时间后,水面处铁丝锈蚀最严重 ④一段时间后,铁丝会由下向上出现锈蚀现象
A. ②③④ B. ①②④
C. ①②③ D. ①③④
C
10. (实验情境)学习了铁在空气中生锈的条件后,小明和小红对铜在空气中生锈的条件产生了浓厚的兴趣,他们进行了如下探究过程。
【查阅资料】铜锈是绿色的,俗称铜绿,主要成分是碱式碳酸铜[Cu2(OH)2CO3],铜绿加热能分解生成三种常见的氧化物。
【提出猜想】小红猜测铜生锈与空气中的下列物质有关:①CO2;②O2;③N2;④H2O。
小明认为铜生锈与氮气一定无关,依据是___________________。
【实验探究】小明设计了如图8-F-7所示的实验,几天后观察到,A试管中的铜片在水面附近有绿色物质,B、C、D试管中铜片均无明显现象。请帮助分析实验过程并回答下列问题。
(1)根据上述实验得出,铜生锈与空气中相关物质有________________________________(填物质名称)。
铜绿中不含有氮元素
氧气、二氧化碳、水蒸气
(2)对比实验_______(填字母)说明铜生锈与氧气一定有关。
【实验反思】 通过学习,他们认为铁和铜在空气中更易生锈的是_____ ;理由是_______________________________________。
AB
铁
铁比铜更活泼;空气中二氧化碳的含量较低
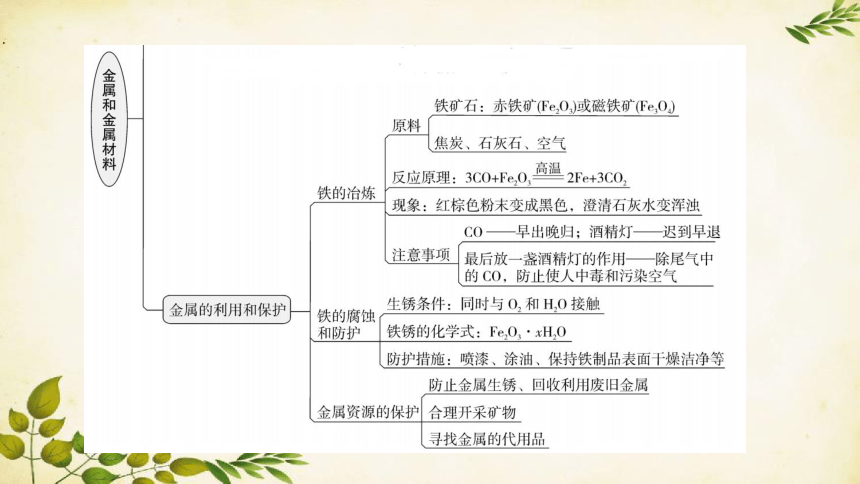
重点6 铁的冶炼
11. 利用如图8-F-8所示实验装置模拟工业炼铁。下列说法错误的是( )
A. 实验时应先通CO一段时间
再点燃酒精灯
B. b处可用澄清石灰水检验生成的CO2
C. 充分加热,a处固体由红棕色变为黑色
D. 可用水吸收尾气中的CO
D
12. 小瑾同学为测定生铁中铁的质量分数,先后进行了四次实验,实验数据记录如下表。
根据她的实验数据,回答下列问题。
(1)第__________次生铁完全反应。
(2)计算生铁中铁的质量分数。(写出计算过程)
实验次序 第一次 第二次 第三次 第四次
生铁的质量/g 10 10 10 10
稀硫酸的质量/g 25 50 75 100
生成氢气的质量/g 0.10 0.20 0.30 0.35
四
谢 谢
单元复习
第八单元复习
目录
01
思维导图
03
重点突破
02
易错点透析
思维导图
易错点透析
易错点
不能正确应用金属活动性顺序
结合金属活动性顺序的应用推测实验方案的设计是否合理,然后做出选择即可。
【例】某同学为验证铁、铜、银三种金属的活动性顺序,他设计了以下四种实验方案,其中能达到目的是( )
A. 将Fe、Cu分别加入AgNO3溶液中
B. 将Fe、Cu、Ag分别加入稀盐酸中
C. 将Fe分别加入CuSO4、AgNO3溶液中
D. 将Fe、Ag分别加入CuSO4溶液中
易错提醒:这类题目不会采取“三取中”的方法。此方法是取中间金属的单质和两端金属的盐溶液反应或取中间金属的盐溶液与两端金属的单质反应。
正解:根据金属活动性顺序可知铁、铜、银的金属活动性顺序为铁>铜>银。根据两液夹一金,可选择试剂硫酸亚铁溶液、铜、硝酸银溶液;或根据两金夹一液,可选择试剂铁、硫酸铜溶液、银。
答案:D
学以致用
能验证Zn、Cu、Ag三种金属活动性顺序的一组试剂是( )
A. Zn、Cu、Ag、稀硫酸
B. Zn(NO3)2溶液、Ag、Cu(NO3)2溶液
C. Zn(NO3)2溶液、Cu、AgNO3溶液
D. Cu、Ag、Zn(NO3)2溶液
C
重点突破
重点1 化学方程式的书写
1. 金属铁的转化关系(如图8-F-1)
①__________________________
②__________________________
③__________________________
④__________________________
⑤__________________________
⑥__________________________
3H2+Fe2O3 ==== 2Fe+3H2O
高温
3C+2Fe2O3 ==== 4Fe+3CO2↑
高温
3CO+Fe2O3 ====2Fe+3CO2
高温
3Fe+2O2 ==== Fe3O4
点燃
Fe+2HCl == FeCl2+H2↑
Fe+H2SO4 == FeSO4+H2↑
2. 金属铜的转化关系(如图8-F-2,反应①写出3道反应化学方程式)
①_____________________________________________________
__________________________________
②________________________________
③________________________________
④________________________________
⑤________________________________
CuO+H2 ==== Cu+H2O、2CuO+C ==== 2Cu+CO2↑、CuO+CO ==== Cu+CO2
△
高温
△
CuCl2+Fe == FeCl2+Cu
CuSO4+Zn == ZnSO4+Cu
2AgNO3+Cu == Cu(NO3)2+2Ag
2Cu+O2 ==== 2CuO
△
重点2 金属材料
3. (社会热点)狡猾的新冠病毒再次侵袭我国部分省市,随着气温下降新冠病毒的活性会有所增加,大家一定要少聚集、勤洗手、戴口罩!防疫不松懈!如图8-F-3所示为增强口罩的密封性,均放了鼻梁条,鼻梁条是铝合金做的,口罩核心材料为熔喷布。关于口罩的说法正确的是( )
A. 铝合金属于纯净物
B. 鼻梁条使用铝合金,利用其硬度大、抗腐
蚀性好的优点
C. 铝合金属于金属材料
D. 铝合金的熔点比金属铝高
C
4. 金属材料在现实生活中有极为重要的作用,下列金属材料的运用与金属所具有的性质不一致的是( )
A. 制造刀具——硬度大
B. 制造炊具——导热性
C. 制造集成电路板——硬度大
D. 制造装化工原料的容器——耐腐蚀
C
重点3 金属的化学性质
5. 常温下向一定质量的稀盐酸中逐渐加入镁条,充分反应(忽略挥发)。图8-F-4中的图像正确的是( )
A. ①② B. ②③ C. ①④ D. ②④
C
6. 某种手机电路板主要含有Fe、Cu、Ag(银)、Ni(镍)等金属及非金属材料,如图8-F-5所示是某工厂回收金属铜的工艺流程图。
(1)电路板不直接焚烧而采取热风处理的主要目的是_____________________________________________________。
(2)操作①的名称是__________。
防止金属和氧气反应生成金属氧化物
过滤
(3)写出滤液③与铁粉反应的化学方程式:_______________________________。
(4)Fe、Cu、Ag、Ni在溶液中的金属活动性顺序由强到弱依次为_______________________________。
(5)写出⑤得到纯铜的一种方法:_______________________________________________________。
Fe+CuSO4 == FeSO4+Cu
Fe>Ni>Cu>Ag
在滤渣中加入适量的稀硫酸,过滤、洗涤、干燥
重点4 金属的活动性顺序
7. 有X、Y、Z三种金属,X在常温下就能与氧气反应,Y、Z在常温下几乎不与氧气反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Z表面有银析出,而Y没有变化。根据以上实验事实,判断X、Y、Z三种金属的活动性由强弱的顺序正确的是( )
A. X、Y、Z B. X、Z、Y
C. Y、Z、X D. Z、Y、X
B
8. 除去下列物质中的杂质,所选方法错误的是( )
D
选项 物质 杂质 除杂方法
A Cu Fe 加入过量稀硫酸,过滤
B FeCl2溶液 CuCl2 加入过量铁粉,过滤
C N2 O2 通过灼热的铜网
D CO2 CO 点燃
重点5 金属防腐
9. (创新实验)如图8-F-6所示是某化学小组设计的铁制品锈蚀的实验装置。下列相关叙述中正确的是( )
①铁锈的主要成分是Fe2O3 ②一段时间后,塑料瓶可能会变瘪 ③一段时间后,水面处铁丝锈蚀最严重 ④一段时间后,铁丝会由下向上出现锈蚀现象
A. ②③④ B. ①②④
C. ①②③ D. ①③④
C
10. (实验情境)学习了铁在空气中生锈的条件后,小明和小红对铜在空气中生锈的条件产生了浓厚的兴趣,他们进行了如下探究过程。
【查阅资料】铜锈是绿色的,俗称铜绿,主要成分是碱式碳酸铜[Cu2(OH)2CO3],铜绿加热能分解生成三种常见的氧化物。
【提出猜想】小红猜测铜生锈与空气中的下列物质有关:①CO2;②O2;③N2;④H2O。
小明认为铜生锈与氮气一定无关,依据是___________________。
【实验探究】小明设计了如图8-F-7所示的实验,几天后观察到,A试管中的铜片在水面附近有绿色物质,B、C、D试管中铜片均无明显现象。请帮助分析实验过程并回答下列问题。
(1)根据上述实验得出,铜生锈与空气中相关物质有________________________________(填物质名称)。
铜绿中不含有氮元素
氧气、二氧化碳、水蒸气
(2)对比实验_______(填字母)说明铜生锈与氧气一定有关。
【实验反思】 通过学习,他们认为铁和铜在空气中更易生锈的是_____ ;理由是_______________________________________。
AB
铁
铁比铜更活泼;空气中二氧化碳的含量较低
重点6 铁的冶炼
11. 利用如图8-F-8所示实验装置模拟工业炼铁。下列说法错误的是( )
A. 实验时应先通CO一段时间
再点燃酒精灯
B. b处可用澄清石灰水检验生成的CO2
C. 充分加热,a处固体由红棕色变为黑色
D. 可用水吸收尾气中的CO
D
12. 小瑾同学为测定生铁中铁的质量分数,先后进行了四次实验,实验数据记录如下表。
根据她的实验数据,回答下列问题。
(1)第__________次生铁完全反应。
(2)计算生铁中铁的质量分数。(写出计算过程)
实验次序 第一次 第二次 第三次 第四次
生铁的质量/g 10 10 10 10
稀硫酸的质量/g 25 50 75 100
生成氢气的质量/g 0.10 0.20 0.30 0.35
四
谢 谢
同课章节目录
