第2章 第1节 课题2 钠的几种化合物(共27张ppt)
文档属性
| 名称 | 第2章 第1节 课题2 钠的几种化合物(共27张ppt) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-16 00:00:00 | ||
图片预览






文档简介
(共27张PPT)
第二章
海水中的重要元素——
钠和氯
第一节 钠及其化合物
课题2 钠的几种化合物
内容索引
学习目标
活动方案
课堂反馈
1. 认识氧化钠和过氧化钠的性质。
2. 认识碳酸钠和碳酸氢钠的性质。
3. 能利用焰色试验鉴别物质。
1. 氧化钠属于碱性氧化物,根据碱性氧化物的通性,写出氧化钠能发生反应的化学方程式(不同类型的物质各举一例)。
【答案】 与酸反应:Na2O+2HCl===2NaCl+H2O
与酸性氧化物反应:Na2O+CO2===Na2CO3
活动一:认识钠的两种氧化物的化学性质
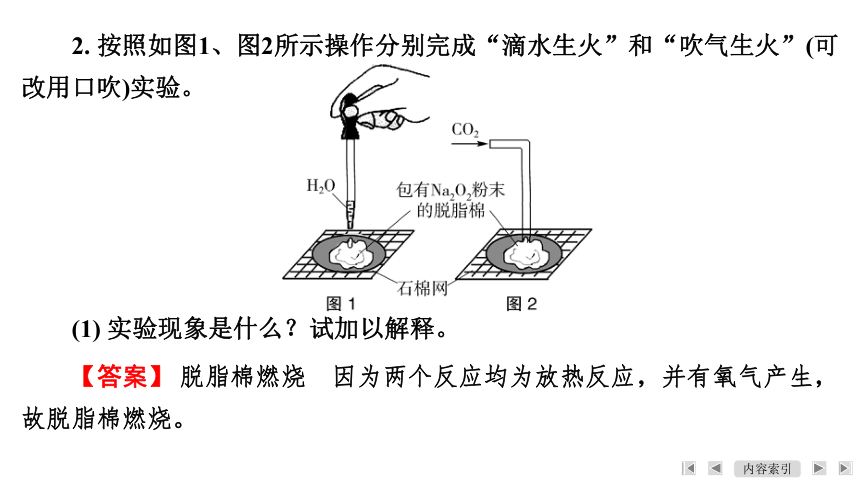
2. 按照如图1、图2所示操作分别完成“滴水生火”和“吹气生火”(可改用口吹)实验。
(1) 实验现象是什么?试加以解释。
【答案】 脱脂棉燃烧 因为两个反应均为放热反应,并有氧气产生,故脱脂棉燃烧。
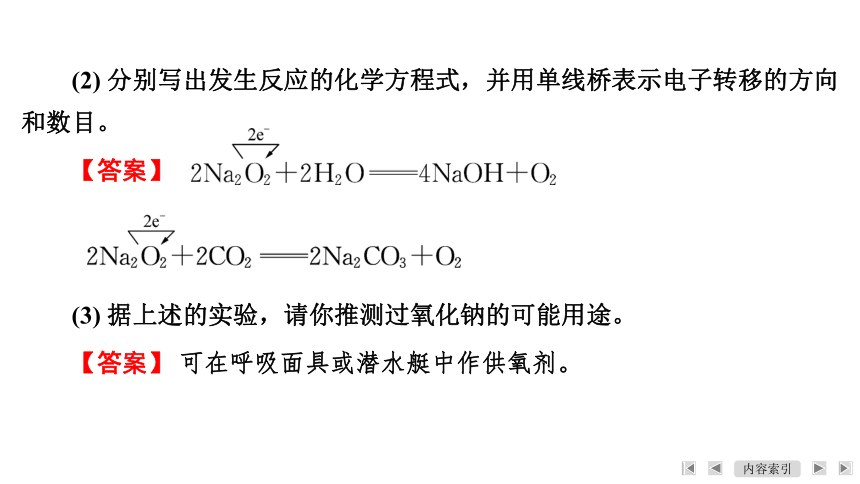
(2) 分别写出发生反应的化学方程式,并用单线桥表示电子转移的方向和数目。
【答案】
(3) 据上述的实验,请你推测过氧化钠的可能用途。
【答案】 可在呼吸面具或潜水艇中作供氧剂。
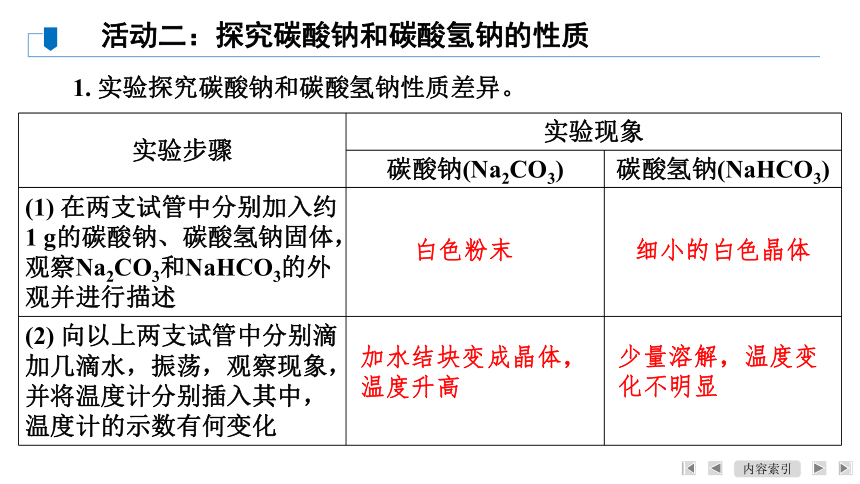
1. 实验探究碳酸钠和碳酸氢钠性质差异。
活动二:探究碳酸钠和碳酸氢钠的性质
实验步骤 实验现象
碳酸钠(Na2CO3) 碳酸氢钠(NaHCO3)
(1) 在两支试管中分别加入约1 g的碳酸钠、碳酸氢钠固体,观察Na2CO3和NaHCO3的外观并进行描述
(2) 向以上两支试管中分别滴加几滴水,振荡,观察现象,并将温度计分别插入其中,温度计的示数有何变化
白色粉末
细小的白色晶体
加水结块变成晶体,
温度升高
少量溶解,温度变
化不明显
实验步骤 实验现象
碳酸钠(Na2CO3) 碳酸氢钠(NaHCO3)
(3) 继续向两支试管内加入5 mL水,用力振荡,有何现象
(4) 继续向两支试管内滴加1~2滴酚酞溶液,有何现象
结论 溶解性
其他
固体完全溶解
不能完全溶解
溶液变为红色
溶液变为浅红色
碳酸钠在水中的溶解性强于碳酸氢钠
碳酸钠加水先变成含结晶水的碳酸钠晶体;
碳酸钠水溶液的碱性比碳酸氢钠强
2. 实验探究碳酸钠和碳酸氢钠的化学性质。
按下列步骤进行实验探究,并完成实验报告。
(1) 热稳定性:按右图所示装置,完成实验。
(2) 与酸反应:向分别盛有碳酸钠、碳酸氢钠固体的具脚试管(形如量筒,无刻度)中滴加几滴洗涤剂,再同时加入等体积、等浓度的盐酸(可用两支相同的玻璃管同时吸取)。
(3) 与盐反应:用试管分别取少量碳酸钠和碳酸氢钠溶液,滴加氯化钙稀溶液。
(3) 与盐反应:用试管分别取少量碳酸钠和碳酸氢钠溶液,滴加氯化钙稀溶液。
试管1中澄清石灰
水变浑浊,试管2
中无明显现象
不反应
碳酸氢钠固体与盐酸反应产生气体的速度比碳酸钠快
盛放碳酸钠溶液的
试管中产生白色沉
淀,另一支试管中
无明显现象
不反应
(4) 在前面《物质的转化》的学习中,我们曾构建了CO2、H2CO3和Na2CO3的转化图:
①请思考NaHCO3在图中应在哪个位置,请根据NaHCO3的位置推理NaHCO3的性质。
【答案】 NaHCO3属于酸式盐,介于H2CO3与Na2CO3之间 可推测其性质:既可以与酸反应,也能与碱反应。
②根据你的推理分析,能用澄清石灰水鉴别Na2CO3和NaHCO3溶液吗?并结合实验验证。
【答案】 不可以用澄清石灰水鉴别,均产生沉淀,反应现象相同。
1. 阅读教材内容,思考如何鉴别碳酸钠溶液和碳酸钾溶液?
【答案】 通过焰色试验。
2. 通过实验鉴别碳酸钠溶液和碳酸钾溶液,并回答下列问题。
(1) 碳酸钠溶液和碳酸钾溶液的焰色分别是什么颜色?
【答案】 黄色 浅紫色(透过蓝色的钴玻璃观察)
活动三:了解焰色试验及其应用
(2) 为什么用铂丝或铁丝等蘸取试剂做焰色试验,而不采用铜丝?为什么用盐酸洗涤铂丝而不用硫酸洗涤铂丝?
【答案】 铂、铁等金属灼烧时不会产生焰色,而铜丝会产生绿色火焰。因为盐酸的沸点比硫酸的沸点低,灼烧时容易挥发。
(3) 为什么观察K+ 焰色时要透过蓝色钴玻璃观察?
【答案】 Na+的黄色容易掩盖K+的浅紫色,必须用蓝色的钴玻璃滤去黄光。
2
4
5
1
3
6
1. 钠在自然界中存在的主要形式是( )
A. 单质 B. 氧化物
C. 氢氧化物 D. 盐
D
2
4
5
1
3
6
2. 某物质灼烧时,焰色为黄色。下列判断正确的是( )
A. 该物质一定是钠的化合物
B. 该物质一定是钠盐
C. 该物质一定是金属钠
D. 一定含有钠元素,不确定是否含有钾元素
D
2
4
5
1
3
6
3. 下列有关钠的叙述正确的是( )
A. 实验室可将金属钠存放在煤油中
B. 金属钠长期暴露在空气中会转化为氢氧化钠
C. 金属钠在空气中的燃烧产物为氧化钠
D. 金属钠发生火灾时,可用大量水进行扑灭
A
2
4
5
1
3
6
4. 下列关于Na2CO3、NaHCO3的说法正确的是( )
A. 受热时,Na2CO3较NaHCO3更不稳定,更容易分解产生CO2
B. 等质量的Na2CO3、NaHCO3与足量盐酸反应,前者产生的CO2更多
C. 常温下Na2CO3、NaHCO3的饱和溶液,前者碱性更强
D. 向Na2CO3、NaHCO3溶液中分别滴加澄清石灰水,前者产生白色沉淀,后者无沉淀
C
2
4
5
1
3
6
5. 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可作供氧剂。
(1) 装置A中盛放有大理石。写出A中发生反应的离子方程式:________________________________________________。
2
4
5
1
3
6
(2) 装置B、装置D中依次盛有饱和NaHCO3溶液、NaOH溶液,其目的分别是_______________________________________________。
(3) 装置C中发生反应的化学方程式为____________________________ _________、_____________________________________。
(4) 装置F中收集的气体为________。
O2
2
4
5
1
3
6
6. 下图表示A~E五种物质的转化关系。若将它们灼烧,火焰都呈黄色;其中A能跟水剧烈反应,D常用于潜水艇中作为氧气的来源。
(1) 试推断A~E各物质(写化学式):
A ____、B ______、C ________、D _________、E ____________。
(2) 以上三个反应中,属于氧化还原反应的是_______(填序号),其中氧化剂是__________,还原剂是________。
Na
Na2O
NaOH
Na2O2
Na2CO3
②
Na2O2
Na2O2
2
4
5
1
3
6
(3) 如果D中混有少量的B,若想得到纯净的D,应该采取的措施是_____________,反应的化学方程式为______________________________。
(4) C溶液中混有少量的E,写出除去E的离子方程式:______________ ____________________。
在空气中加热
谢谢观看
Thank you for watching
第二章
海水中的重要元素——
钠和氯
第一节 钠及其化合物
课题2 钠的几种化合物
内容索引
学习目标
活动方案
课堂反馈
1. 认识氧化钠和过氧化钠的性质。
2. 认识碳酸钠和碳酸氢钠的性质。
3. 能利用焰色试验鉴别物质。
1. 氧化钠属于碱性氧化物,根据碱性氧化物的通性,写出氧化钠能发生反应的化学方程式(不同类型的物质各举一例)。
【答案】 与酸反应:Na2O+2HCl===2NaCl+H2O
与酸性氧化物反应:Na2O+CO2===Na2CO3
活动一:认识钠的两种氧化物的化学性质
2. 按照如图1、图2所示操作分别完成“滴水生火”和“吹气生火”(可改用口吹)实验。
(1) 实验现象是什么?试加以解释。
【答案】 脱脂棉燃烧 因为两个反应均为放热反应,并有氧气产生,故脱脂棉燃烧。
(2) 分别写出发生反应的化学方程式,并用单线桥表示电子转移的方向和数目。
【答案】
(3) 据上述的实验,请你推测过氧化钠的可能用途。
【答案】 可在呼吸面具或潜水艇中作供氧剂。
1. 实验探究碳酸钠和碳酸氢钠性质差异。
活动二:探究碳酸钠和碳酸氢钠的性质
实验步骤 实验现象
碳酸钠(Na2CO3) 碳酸氢钠(NaHCO3)
(1) 在两支试管中分别加入约1 g的碳酸钠、碳酸氢钠固体,观察Na2CO3和NaHCO3的外观并进行描述
(2) 向以上两支试管中分别滴加几滴水,振荡,观察现象,并将温度计分别插入其中,温度计的示数有何变化
白色粉末
细小的白色晶体
加水结块变成晶体,
温度升高
少量溶解,温度变
化不明显
实验步骤 实验现象
碳酸钠(Na2CO3) 碳酸氢钠(NaHCO3)
(3) 继续向两支试管内加入5 mL水,用力振荡,有何现象
(4) 继续向两支试管内滴加1~2滴酚酞溶液,有何现象
结论 溶解性
其他
固体完全溶解
不能完全溶解
溶液变为红色
溶液变为浅红色
碳酸钠在水中的溶解性强于碳酸氢钠
碳酸钠加水先变成含结晶水的碳酸钠晶体;
碳酸钠水溶液的碱性比碳酸氢钠强
2. 实验探究碳酸钠和碳酸氢钠的化学性质。
按下列步骤进行实验探究,并完成实验报告。
(1) 热稳定性:按右图所示装置,完成实验。
(2) 与酸反应:向分别盛有碳酸钠、碳酸氢钠固体的具脚试管(形如量筒,无刻度)中滴加几滴洗涤剂,再同时加入等体积、等浓度的盐酸(可用两支相同的玻璃管同时吸取)。
(3) 与盐反应:用试管分别取少量碳酸钠和碳酸氢钠溶液,滴加氯化钙稀溶液。
(3) 与盐反应:用试管分别取少量碳酸钠和碳酸氢钠溶液,滴加氯化钙稀溶液。
试管1中澄清石灰
水变浑浊,试管2
中无明显现象
不反应
碳酸氢钠固体与盐酸反应产生气体的速度比碳酸钠快
盛放碳酸钠溶液的
试管中产生白色沉
淀,另一支试管中
无明显现象
不反应
(4) 在前面《物质的转化》的学习中,我们曾构建了CO2、H2CO3和Na2CO3的转化图:
①请思考NaHCO3在图中应在哪个位置,请根据NaHCO3的位置推理NaHCO3的性质。
【答案】 NaHCO3属于酸式盐,介于H2CO3与Na2CO3之间 可推测其性质:既可以与酸反应,也能与碱反应。
②根据你的推理分析,能用澄清石灰水鉴别Na2CO3和NaHCO3溶液吗?并结合实验验证。
【答案】 不可以用澄清石灰水鉴别,均产生沉淀,反应现象相同。
1. 阅读教材内容,思考如何鉴别碳酸钠溶液和碳酸钾溶液?
【答案】 通过焰色试验。
2. 通过实验鉴别碳酸钠溶液和碳酸钾溶液,并回答下列问题。
(1) 碳酸钠溶液和碳酸钾溶液的焰色分别是什么颜色?
【答案】 黄色 浅紫色(透过蓝色的钴玻璃观察)
活动三:了解焰色试验及其应用
(2) 为什么用铂丝或铁丝等蘸取试剂做焰色试验,而不采用铜丝?为什么用盐酸洗涤铂丝而不用硫酸洗涤铂丝?
【答案】 铂、铁等金属灼烧时不会产生焰色,而铜丝会产生绿色火焰。因为盐酸的沸点比硫酸的沸点低,灼烧时容易挥发。
(3) 为什么观察K+ 焰色时要透过蓝色钴玻璃观察?
【答案】 Na+的黄色容易掩盖K+的浅紫色,必须用蓝色的钴玻璃滤去黄光。
2
4
5
1
3
6
1. 钠在自然界中存在的主要形式是( )
A. 单质 B. 氧化物
C. 氢氧化物 D. 盐
D
2
4
5
1
3
6
2. 某物质灼烧时,焰色为黄色。下列判断正确的是( )
A. 该物质一定是钠的化合物
B. 该物质一定是钠盐
C. 该物质一定是金属钠
D. 一定含有钠元素,不确定是否含有钾元素
D
2
4
5
1
3
6
3. 下列有关钠的叙述正确的是( )
A. 实验室可将金属钠存放在煤油中
B. 金属钠长期暴露在空气中会转化为氢氧化钠
C. 金属钠在空气中的燃烧产物为氧化钠
D. 金属钠发生火灾时,可用大量水进行扑灭
A
2
4
5
1
3
6
4. 下列关于Na2CO3、NaHCO3的说法正确的是( )
A. 受热时,Na2CO3较NaHCO3更不稳定,更容易分解产生CO2
B. 等质量的Na2CO3、NaHCO3与足量盐酸反应,前者产生的CO2更多
C. 常温下Na2CO3、NaHCO3的饱和溶液,前者碱性更强
D. 向Na2CO3、NaHCO3溶液中分别滴加澄清石灰水,前者产生白色沉淀,后者无沉淀
C
2
4
5
1
3
6
5. 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可作供氧剂。
(1) 装置A中盛放有大理石。写出A中发生反应的离子方程式:________________________________________________。
2
4
5
1
3
6
(2) 装置B、装置D中依次盛有饱和NaHCO3溶液、NaOH溶液,其目的分别是_______________________________________________。
(3) 装置C中发生反应的化学方程式为____________________________ _________、_____________________________________。
(4) 装置F中收集的气体为________。
O2
2
4
5
1
3
6
6. 下图表示A~E五种物质的转化关系。若将它们灼烧,火焰都呈黄色;其中A能跟水剧烈反应,D常用于潜水艇中作为氧气的来源。
(1) 试推断A~E各物质(写化学式):
A ____、B ______、C ________、D _________、E ____________。
(2) 以上三个反应中,属于氧化还原反应的是_______(填序号),其中氧化剂是__________,还原剂是________。
Na
Na2O
NaOH
Na2O2
Na2CO3
②
Na2O2
Na2O2
2
4
5
1
3
6
(3) 如果D中混有少量的B,若想得到纯净的D,应该采取的措施是_____________,反应的化学方程式为______________________________。
(4) C溶液中混有少量的E,写出除去E的离子方程式:______________ ____________________。
在空气中加热
谢谢观看
Thank you for watching
