人教版九年级化学 第九单元课题3 课时1 溶质的质量分数溶液的稀释或浓缩 课件(共19张PPT)
文档属性
| 名称 | 人教版九年级化学 第九单元课题3 课时1 溶质的质量分数溶液的稀释或浓缩 课件(共19张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 422.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-18 00:00:00 | ||
图片预览






文档简介
(共19张PPT)
第九单元 溶液
课题3 溶液的浓度
课时1 溶质的质量分数 溶液的稀释或浓缩
目录
01
课程要求
03
知识点精讲
04
课堂检测
02
课前预习
认识溶质质量分数的含义;能进行溶质质量分数的简单计算。
课程要求
写出下列物质的化学式。
课前预习
氧化铁
Fe2O3
硫酸
H2SO4
氯化钠
NaCl
硫酸铜
CuSO4
氯化亚铁
FeCl2
硝酸银
AgNO3
知识点精讲
知识点1
溶质的质量分数
1. 观察课本P42“实验9-7”,填写下表。
物质 溶液颜色 溶剂质量/g 溶质质量/g 溶液质量/g 溶质的质量分数
(1)20 mL水+0.1 g无水硫酸铜 ____________ ____________ ____________ ____________ ____________
(2)20 mL水+0.5 g无水硫酸铜 ____________ ____________ ____________ ____________ ____________
(3)20 mL水+2 g无水硫酸铜 ____________ ____________ ____________ ____________ ____________
淡蓝
20
0.1
20.1
0.50%
浅蓝
20
0.5
20.5
2.44%
蓝
20
2
22
9.09%
越大
浓
大
浓
溶液质量
溶质质量
溶质质量
溶剂质量
溶质质量
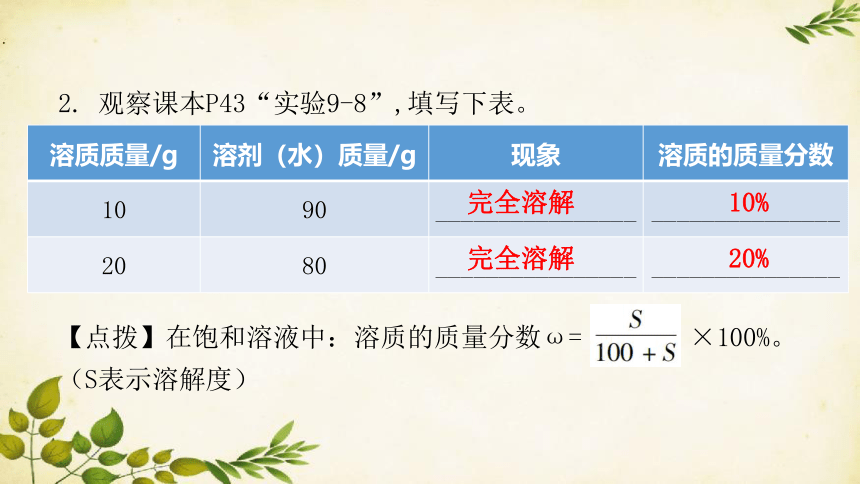
2. 观察课本P43“实验9-8”,填写下表。
溶质质量/g 溶剂(水)质量/g 现象 溶质的质量分数
10 90 ________________ _______________
20 80 ________________ _______________
完全溶解
10%
完全溶解
20%
【点拨】在饱和溶液中:溶质的质量分数ω= ×100%。(S表示溶解度)
课堂练习
1. 已知20 ℃时NaCl的溶解度是36 g,20 ℃时向100 g 水中加入50 g NaCl,充分溶解后,所得溶液中溶质的质量分数为( )
A. 36% B. 50% C. 33.3% D. 26.5%
2. 现配制50 g质量分数为10%的氢氧化钠溶液,需称量氢氧化钠的质量为( )
A. 10 g B. 5 g C. 0.5 g D. 15 g
D
B
思路点拨 根据溶质的质量分数的计算公式以及变式公式进行计算,同时注意,当向某种浓度的溶液中加入一定量的溶质或溶剂时,其溶液的量也会发生相应的改变。
知识点2
溶液的稀释或浓缩
3. 计算原理:稀释前________的质量=稀释后________的质量。
4. 方法:①____________;②___________________________。
5. 计算公式:_____________________×浓溶液中溶质的质量分数=稀溶液的质量×____________________________________。
6. 溶液稀释时需要加水的质量=____________的质量-____________的质量。
溶质
溶质
加入溶剂
加入低浓度溶液
浓溶液的质量
稀溶液中溶质的质量分数
稀溶液
浓溶液
课堂练习
3. 配制1 000 mL质量分数为10%氢氧化钠溶液(密度为1.1 g/cm3),需要氢氧化钠和水的质量各是多少?
解:1 000 mL=1 000 cm3
需要氢氧化钠的质量为1 000 cm3×1.1 g/cm3×10%=110 g
需要水的质量为1 000 cm3×1.1 g/cm3-110 g=990 g
答:需要氢氧化钠和水的质量分别为110 g和990 g。
思路点拨 在进行溶液的稀释(或浓缩)的计算时要注意,在稀释(或浓缩)前后,溶质的总质量不变。
课堂检测
1. 下列关于“10%的硝酸钾溶液”含义的说法中,错误的是( )
A.100 g水中溶解了10 g硝酸钾
B.100 g硝酸钾溶液中有10 g硝酸钾
C.将10 g硝酸钾溶于90 g水中所得的溶液
D.将硝酸钾与水按1∶9的质量比配制的溶液
A
2. (化学生活)无土栽培所用的某种营养液中,含硝酸钾的质量分数为7%,欲配制该营养液300 kg,需要硝酸钾的质量是( )
A.7 kg B.21 kg
C.70 kg D.140 kg
B
3. 25 ℃时,探究某固体物质的溶解性,实验记录如下表。下列实验结论正确的是( )
A. 实验①所得溶液质量分数为10%
B. 实验②说明25 ℃时该物质的溶解度是20 g
C. 实验③、④所得溶液溶质质量分数相同
D. 实验④所得溶液中含溶质20 g
C
编号 ① ② ③ ④
水的质量/g 50 50 50 50
加入固体质量/g 5 10 15 20
现象 固体完全溶解 固体完全溶解 剩余少量固体 剩余较多固体
4. 为了做好疫情防控,公共场所可用0.5%的过氧乙酸(C2H4O3)溶液来消毒,请回答下列问题。
(1)过氧乙酸中碳、氢、氧三种元素的原子个数比为__________________。
(2)现要配制溶质质量分数为0.5%的过氧乙酸溶液2 000 g,需要过氧乙酸的质量是____________。
5. 用4 g酚酞与酒精配制溶质质量分数为4%的酚酞溶液,需要酒精的质量是___________g,这些酒精的体积为___________mL(酒精的密度为0.8 g/mL)。
2∶4∶3
10 g
96
120
6. 图9-3-1是A、B两种物质的溶解度曲线。t2 ℃时,100 g水中溶解50 g A刚好饱和,那么50 g水中溶解____________g B也刚好饱和,此时溶液的溶质质量分数是____________(精确到0.1%)。
25
33.3%
7. 现有80 g质量分数为10%的硝酸钠溶液,试回答下列问题。(写出计算过程)
(1)若向上述溶液中加入20 g硝酸钠,则完全溶解后所得溶液中溶质质量分数为多少?
(2)若使上述溶液中溶质质量分数变为5%,则应加多少水?
谢 谢
第九单元 溶液
课题3 溶液的浓度
课时1 溶质的质量分数 溶液的稀释或浓缩
目录
01
课程要求
03
知识点精讲
04
课堂检测
02
课前预习
认识溶质质量分数的含义;能进行溶质质量分数的简单计算。
课程要求
写出下列物质的化学式。
课前预习
氧化铁
Fe2O3
硫酸
H2SO4
氯化钠
NaCl
硫酸铜
CuSO4
氯化亚铁
FeCl2
硝酸银
AgNO3
知识点精讲
知识点1
溶质的质量分数
1. 观察课本P42“实验9-7”,填写下表。
物质 溶液颜色 溶剂质量/g 溶质质量/g 溶液质量/g 溶质的质量分数
(1)20 mL水+0.1 g无水硫酸铜 ____________ ____________ ____________ ____________ ____________
(2)20 mL水+0.5 g无水硫酸铜 ____________ ____________ ____________ ____________ ____________
(3)20 mL水+2 g无水硫酸铜 ____________ ____________ ____________ ____________ ____________
淡蓝
20
0.1
20.1
0.50%
浅蓝
20
0.5
20.5
2.44%
蓝
20
2
22
9.09%
越大
浓
大
浓
溶液质量
溶质质量
溶质质量
溶剂质量
溶质质量
2. 观察课本P43“实验9-8”,填写下表。
溶质质量/g 溶剂(水)质量/g 现象 溶质的质量分数
10 90 ________________ _______________
20 80 ________________ _______________
完全溶解
10%
完全溶解
20%
【点拨】在饱和溶液中:溶质的质量分数ω= ×100%。(S表示溶解度)
课堂练习
1. 已知20 ℃时NaCl的溶解度是36 g,20 ℃时向100 g 水中加入50 g NaCl,充分溶解后,所得溶液中溶质的质量分数为( )
A. 36% B. 50% C. 33.3% D. 26.5%
2. 现配制50 g质量分数为10%的氢氧化钠溶液,需称量氢氧化钠的质量为( )
A. 10 g B. 5 g C. 0.5 g D. 15 g
D
B
思路点拨 根据溶质的质量分数的计算公式以及变式公式进行计算,同时注意,当向某种浓度的溶液中加入一定量的溶质或溶剂时,其溶液的量也会发生相应的改变。
知识点2
溶液的稀释或浓缩
3. 计算原理:稀释前________的质量=稀释后________的质量。
4. 方法:①____________;②___________________________。
5. 计算公式:_____________________×浓溶液中溶质的质量分数=稀溶液的质量×____________________________________。
6. 溶液稀释时需要加水的质量=____________的质量-____________的质量。
溶质
溶质
加入溶剂
加入低浓度溶液
浓溶液的质量
稀溶液中溶质的质量分数
稀溶液
浓溶液
课堂练习
3. 配制1 000 mL质量分数为10%氢氧化钠溶液(密度为1.1 g/cm3),需要氢氧化钠和水的质量各是多少?
解:1 000 mL=1 000 cm3
需要氢氧化钠的质量为1 000 cm3×1.1 g/cm3×10%=110 g
需要水的质量为1 000 cm3×1.1 g/cm3-110 g=990 g
答:需要氢氧化钠和水的质量分别为110 g和990 g。
思路点拨 在进行溶液的稀释(或浓缩)的计算时要注意,在稀释(或浓缩)前后,溶质的总质量不变。
课堂检测
1. 下列关于“10%的硝酸钾溶液”含义的说法中,错误的是( )
A.100 g水中溶解了10 g硝酸钾
B.100 g硝酸钾溶液中有10 g硝酸钾
C.将10 g硝酸钾溶于90 g水中所得的溶液
D.将硝酸钾与水按1∶9的质量比配制的溶液
A
2. (化学生活)无土栽培所用的某种营养液中,含硝酸钾的质量分数为7%,欲配制该营养液300 kg,需要硝酸钾的质量是( )
A.7 kg B.21 kg
C.70 kg D.140 kg
B
3. 25 ℃时,探究某固体物质的溶解性,实验记录如下表。下列实验结论正确的是( )
A. 实验①所得溶液质量分数为10%
B. 实验②说明25 ℃时该物质的溶解度是20 g
C. 实验③、④所得溶液溶质质量分数相同
D. 实验④所得溶液中含溶质20 g
C
编号 ① ② ③ ④
水的质量/g 50 50 50 50
加入固体质量/g 5 10 15 20
现象 固体完全溶解 固体完全溶解 剩余少量固体 剩余较多固体
4. 为了做好疫情防控,公共场所可用0.5%的过氧乙酸(C2H4O3)溶液来消毒,请回答下列问题。
(1)过氧乙酸中碳、氢、氧三种元素的原子个数比为__________________。
(2)现要配制溶质质量分数为0.5%的过氧乙酸溶液2 000 g,需要过氧乙酸的质量是____________。
5. 用4 g酚酞与酒精配制溶质质量分数为4%的酚酞溶液,需要酒精的质量是___________g,这些酒精的体积为___________mL(酒精的密度为0.8 g/mL)。
2∶4∶3
10 g
96
120
6. 图9-3-1是A、B两种物质的溶解度曲线。t2 ℃时,100 g水中溶解50 g A刚好饱和,那么50 g水中溶解____________g B也刚好饱和,此时溶液的溶质质量分数是____________(精确到0.1%)。
25
33.3%
7. 现有80 g质量分数为10%的硝酸钠溶液,试回答下列问题。(写出计算过程)
(1)若向上述溶液中加入20 g硝酸钠,则完全溶解后所得溶液中溶质质量分数为多少?
(2)若使上述溶液中溶质质量分数变为5%,则应加多少水?
谢 谢
同课章节目录
