(2018-2022)五年高考化学真题分类汇编 专题11 化学工艺流程(学生版+解析版)
文档属性
| 名称 | (2018-2022)五年高考化学真题分类汇编 专题11 化学工艺流程(学生版+解析版) |

|
|
| 格式 | |||
| 文件大小 | 9.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-19 00:00:00 | ||
图片预览



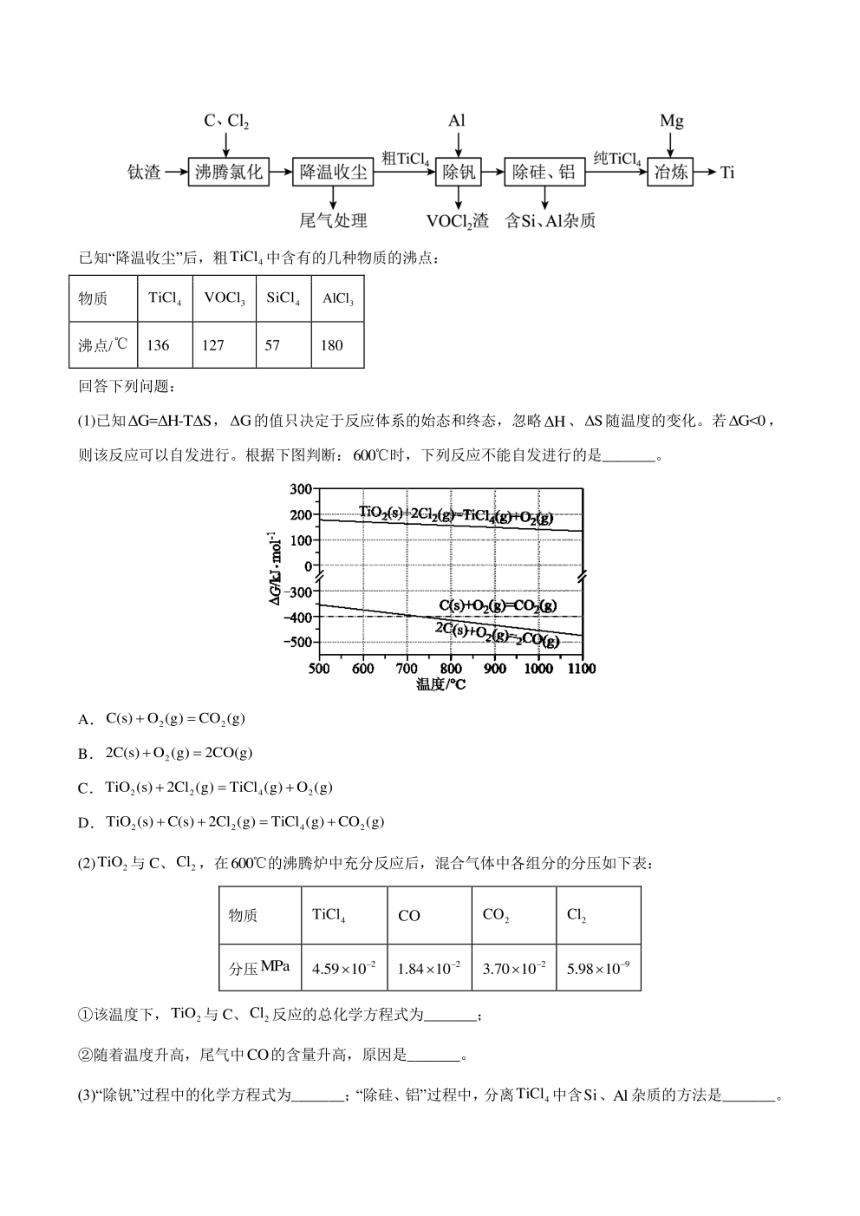
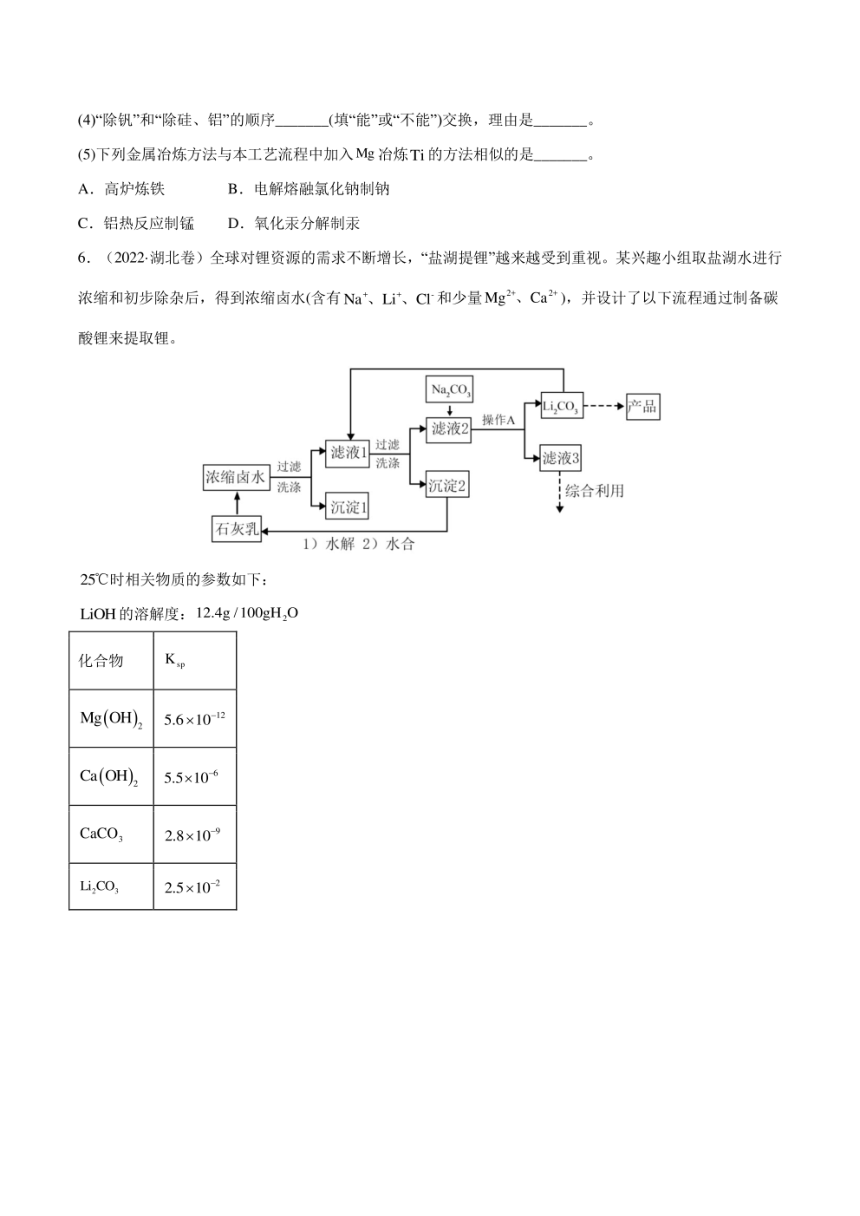
文档简介
专题11
化学工艺流程
【2022年】
1.(2022全国甲卷)硫酸锌(ZSO,)是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。硫
酸锌可由菱锌矿制备。菱锌矿的主要成分为ZnCO,,杂质为SiO,以及Ca、Mg、Fe、Cu等的化合物。其制
备流程如下:
菱锌矿
H-SO
X
KMnO
Zn粉
HF
焙烧
浸取
调H-5滤液①氧化滤液②转化滤液③脱钙镁
滤液④
+ZnS04·7H20
过滤
过滤
过滤
过滤
滤渣①
滤渣②
滤渣③
滤渣④
本题中所涉及离子的氯氧化物溶度积常数如下表:
离子
Fe3
Zn2
Cu2
Fe2+
Mg
4.0×1038
6.7×107
2.2×10-20
8.0×10-6
1.8×101
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为」
(2)为了提高锌的浸取效果,可采取的措施有
(3)加入物质X调溶液pH=5,最适宜使用的X是
(填标号)。
A.NH·H,OB.Ca(OH2
C.NaOH
滤渣①的主要成分是
(4)向80~90℃的滤液①中分批加入适量KMnO,溶液充分反应后过滤,滤渣②中有MnO2,该步反应的离子
方程式为
(5)滤液②中加入锌粉的目的是
d
(6)滤渣④与浓H,SO,反应可以释放HF并循环利用,同时得到的副产物是
0
2.(2022全国乙卷)废旧铅蓄电池的铅膏中主要含有PbSO,、PbO2、PbO和Pb。还有少量Ba、Fe、A1
的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅的回收。
NazCO3 HAc,H2O2 NaOH
铅膏一一脱硫一一酸浸一沉铅·Pb0
滤液滤渣滤液
一些难溶电解质的溶度积常数如下表:
难溶电解质
PbSO
PbCO.
BaSO
BaCO
长e
2.5×10-8
7.4×1014
1.1×10-10
2.6×109
一定条件下,一些金属氢氧化物沉淀时的H如下表:
金属氢氧化物
Fe(OH),
Fe(OH)2
Al(OH)
Pb(OH)2
开始沉淀的pH
2.3
6.8
3.5
7.2
完全沉淀的pH
3.2
8.3
4.6
9.1
回答下列问题:
(1)在“脱硫”中PbSO,转化反应的离子方程式为」
用沉淀溶解平衡原理解释选择Na,CO,的原因
_o
(2)在“脱硫”中,加入Na,CO,不能使铅膏中BaSO,完全转化,原因是,
(3)在“酸浸”中,除加入醋酸(HAc),还要加入H,O2。
(i)能被H,O,氧化的离子是一:
(i)HO2促进了金属Pb在醋酸中转化为Pb(Ac)2,,其化学方程式为
(ii)H,O2也能使PbO,转化为Pb(Ac)2,H,O2的作用是
(4)“酸浸”后溶液的pH约为4.9,滤渣的主要成分是
(⑤)“沉铅”的滤液中,金属离子有
0
3.(2022浙江卷)化合物X由三种元素组成,某实验小组按如下流程进行相关实验:
紫红色固体
固体混合物盐酸
0.960g
白色沉淀
X
足量NH
A
1.165g
1.965g△
无色溶液0.015mol
尾气
B
H2S04
无色溶液
足量
白色沉淀
BaCl2溶液
2.330g
化合物X在空气中加热到800℃,不发生反应。
请回答:
(1)组成X的三种元素为一;X的化学式为
(2)溶液C的溶质组成为
(用化学式表示)。
(3)①写出由X到A的化学方程式
化学工艺流程
【2022年】
1.(2022全国甲卷)硫酸锌(ZSO,)是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。硫
酸锌可由菱锌矿制备。菱锌矿的主要成分为ZnCO,,杂质为SiO,以及Ca、Mg、Fe、Cu等的化合物。其制
备流程如下:
菱锌矿
H-SO
X
KMnO
Zn粉
HF
焙烧
浸取
调H-5滤液①氧化滤液②转化滤液③脱钙镁
滤液④
+ZnS04·7H20
过滤
过滤
过滤
过滤
滤渣①
滤渣②
滤渣③
滤渣④
本题中所涉及离子的氯氧化物溶度积常数如下表:
离子
Fe3
Zn2
Cu2
Fe2+
Mg
4.0×1038
6.7×107
2.2×10-20
8.0×10-6
1.8×101
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为」
(2)为了提高锌的浸取效果,可采取的措施有
(3)加入物质X调溶液pH=5,最适宜使用的X是
(填标号)。
A.NH·H,OB.Ca(OH2
C.NaOH
滤渣①的主要成分是
(4)向80~90℃的滤液①中分批加入适量KMnO,溶液充分反应后过滤,滤渣②中有MnO2,该步反应的离子
方程式为
(5)滤液②中加入锌粉的目的是
d
(6)滤渣④与浓H,SO,反应可以释放HF并循环利用,同时得到的副产物是
0
2.(2022全国乙卷)废旧铅蓄电池的铅膏中主要含有PbSO,、PbO2、PbO和Pb。还有少量Ba、Fe、A1
的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅的回收。
NazCO3 HAc,H2O2 NaOH
铅膏一一脱硫一一酸浸一沉铅·Pb0
滤液滤渣滤液
一些难溶电解质的溶度积常数如下表:
难溶电解质
PbSO
PbCO.
BaSO
BaCO
长e
2.5×10-8
7.4×1014
1.1×10-10
2.6×109
一定条件下,一些金属氢氧化物沉淀时的H如下表:
金属氢氧化物
Fe(OH),
Fe(OH)2
Al(OH)
Pb(OH)2
开始沉淀的pH
2.3
6.8
3.5
7.2
完全沉淀的pH
3.2
8.3
4.6
9.1
回答下列问题:
(1)在“脱硫”中PbSO,转化反应的离子方程式为」
用沉淀溶解平衡原理解释选择Na,CO,的原因
_o
(2)在“脱硫”中,加入Na,CO,不能使铅膏中BaSO,完全转化,原因是,
(3)在“酸浸”中,除加入醋酸(HAc),还要加入H,O2。
(i)能被H,O,氧化的离子是一:
(i)HO2促进了金属Pb在醋酸中转化为Pb(Ac)2,,其化学方程式为
(ii)H,O2也能使PbO,转化为Pb(Ac)2,H,O2的作用是
(4)“酸浸”后溶液的pH约为4.9,滤渣的主要成分是
(⑤)“沉铅”的滤液中,金属离子有
0
3.(2022浙江卷)化合物X由三种元素组成,某实验小组按如下流程进行相关实验:
紫红色固体
固体混合物盐酸
0.960g
白色沉淀
X
足量NH
A
1.165g
1.965g△
无色溶液0.015mol
尾气
B
H2S04
无色溶液
足量
白色沉淀
BaCl2溶液
2.330g
化合物X在空气中加热到800℃,不发生反应。
请回答:
(1)组成X的三种元素为一;X的化学式为
(2)溶液C的溶质组成为
(用化学式表示)。
(3)①写出由X到A的化学方程式
同课章节目录
