构成物质的微粒(第一课时)
图片预览







文档简介
课件44张PPT。第6章 物质的构成万物---无论生物还是非生物,都是由分子,原子或者离子等微粒构成的第一节:构 成 物 质 的 微 粒3.将方形蔗糖碾碎后,用放大镜观察,你看到了什么? 5.实验探究2、我们能否把这块蔗糖变小呢?4、将碾碎的蔗糖溶入水中,用放大镜观察糖水,你还能看到蔗糖吗?1.观察一块蔗糖二、分子和原子思考 原来这些小颗粒在水中可以被分成更小的微粒,即使用显微镜也看不到,我们把这些微粒叫做 。1、蔗糖是否消失了?
怎样证明呢?
2、既然蔗糖还在水里,为什么看不到了呢?没有,水变甜了分子1、分子的定义保持物质化学性质的最小微粒,这种微粒被称为分子.
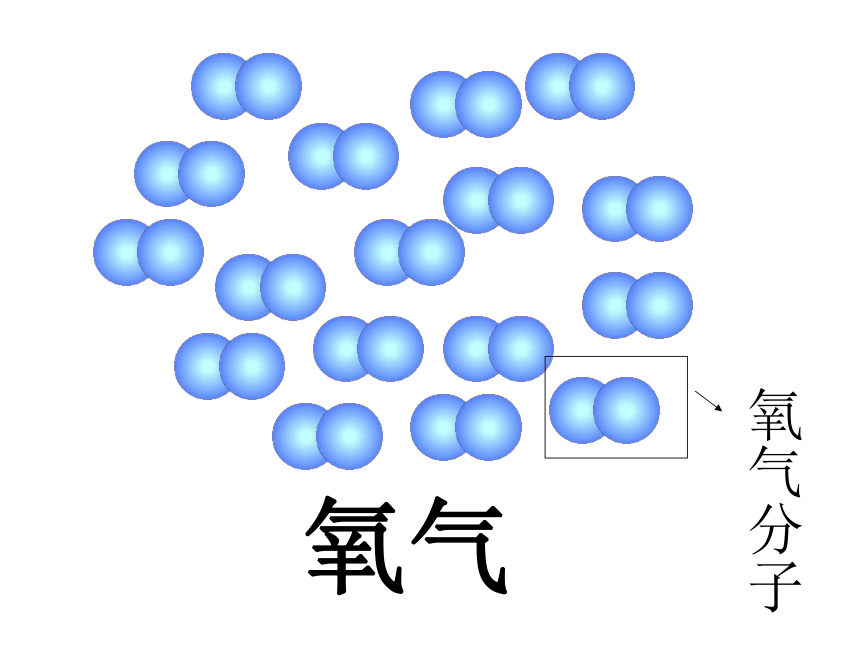
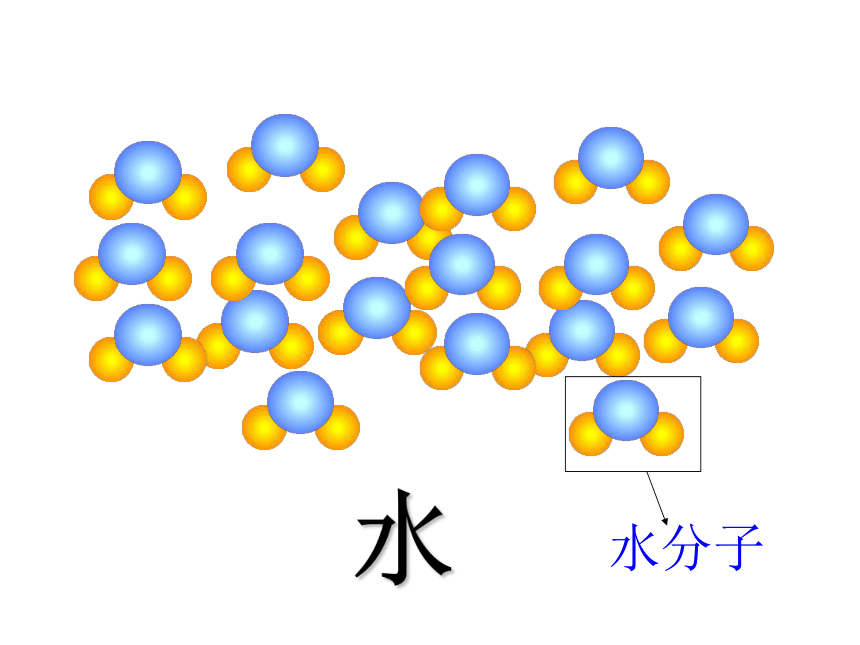
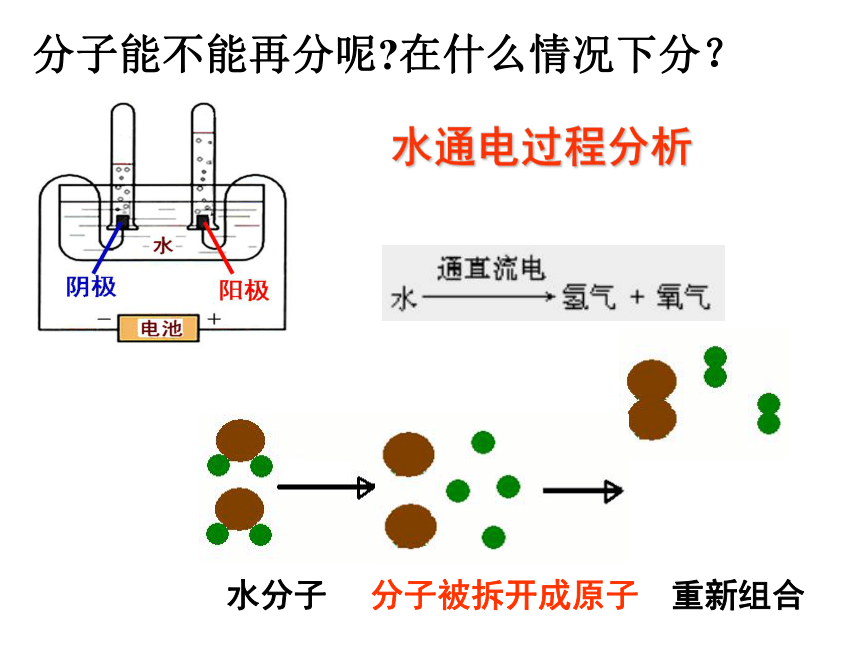
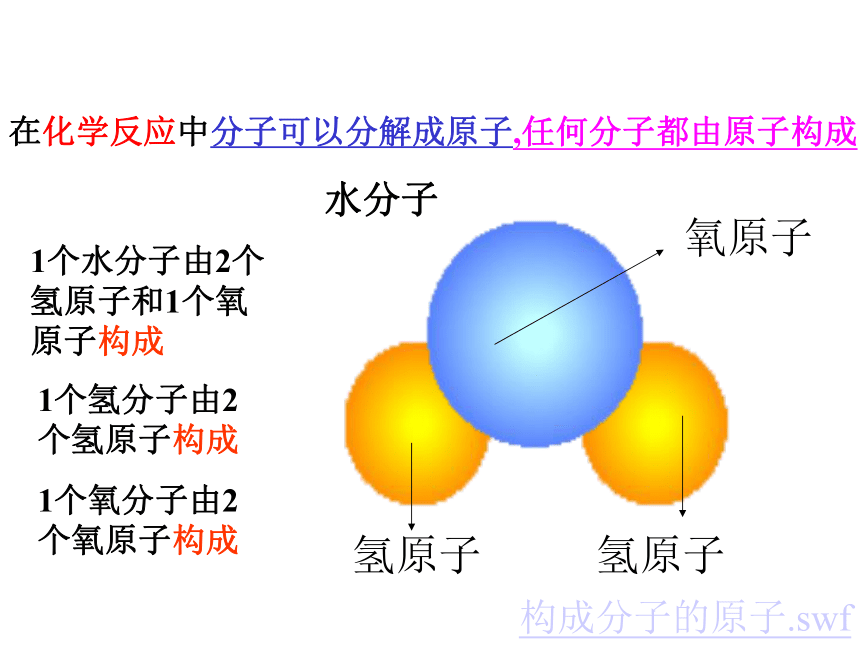
自然界中有许多的物质是由分子构成的尝试与归纳水分子氧气分子酒精分子分子是构成物质的一种的微粒氧气水水通电过程分析微粒变化示意图: 水分子分子被拆开成原子重新组合分子能不能再分呢?在什么情况下分?水分子构成分子的原子.swf在化学反应中分子可以分解成原子,任何分子都由原子构成1个水分子由2个氢原子和1个氧原子构成1个氢分子由2个氢原子构成
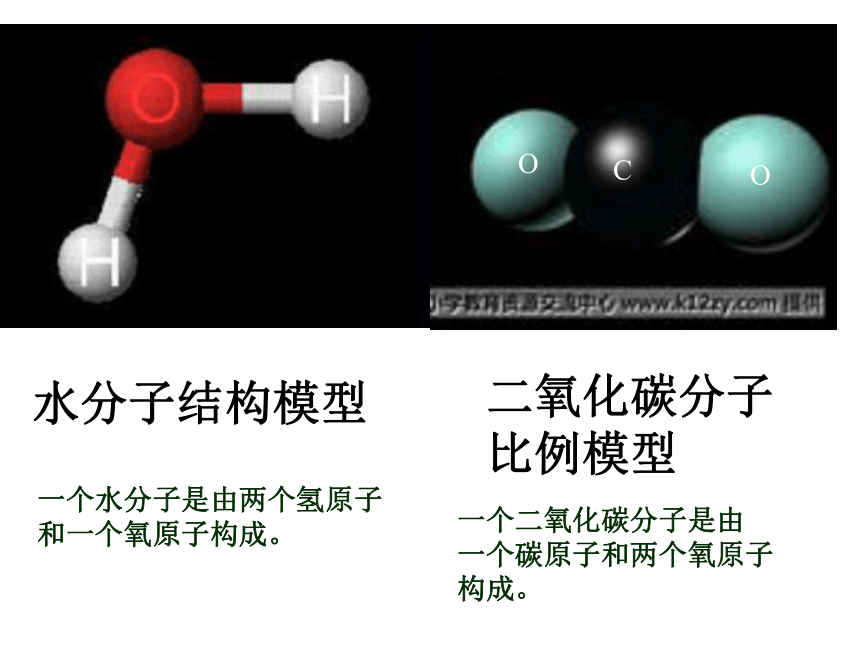
1个氧分子由2个氧原子构成水分子结构模型二氧化碳分子比例模型COO一个水分子是由两个氢原子
和一个氧原子构成。一个二氧化碳分子是由
一个碳原子和两个氧原子
构成。 二氧化硫分子
比例模型甲烷分子
比例模型一个二氧化硫分子是由一个
硫原子和两个氧原子构成。一个甲烷分子是由一个碳原子
和四个氢原子构成。分子的构成有的复杂,有的简单,例如一个蔗糖分子由12个碳原子,22个氢原子和11个氧原子构成,而很多的有机物例如核酸,蛋白质等是由很多个不同的原子 构成的。蛋白质分子图金,银,铜,铁等金属中不存在分子,分别由无数个金原子,银原子,铜原子等直接构成的。金属构成图2、分子的构成与大小1、一滴水的分子个数:
1000 000 000 000 000 000 000个水分子构成,
1ml水需要约20滴水组成。2、如果把水分子放大到乒乓球那么大,那么乒乓球就要放大到地球那么大。 数的启示?3、铅笔留下的黑色的笔迹是碳原子的堆积,一个句号竟有1018个碳原子。启示:1、分子和原子体积都很小一个氢原子质量:1.674×10-27千克一个碳原子质量:1.993×10-26千克一个氧原子质量:2.657×10-26千克一个氢分子质量:3.348×10-27千克一个二氧化碳分子质量:7.307×10-26千克(可以放大几百万倍)分子照片分子很小,即使用放大1500倍的光学显微镜,也不能直接观察,1982年IBM公司两位科学家发明了扫描隧道显微镜(STM),STM的发明被公认为20世纪80年代的重要发明之一,获得了1986年诺贝尔物理奖1.道尔顿原子模型
(1803年)实心球模型阅读:原子——分子论道尔顿原子模型一切物质都是由最小的不能再分的粒子——原子构成。
原子模型:原子是坚实的、不可再分的实心球。
同种原子的大小、形状、质量和性质完全相同,不同种原子则不相同。近代科学原子论 英国化学家道尔顿
(J.Dalton , 1766~1844)一切物质都是由最小的不能再分的粒子——原子构成。
原子模型:原子是坚实的、不可再分的实心球。
英国化学道尔顿
(J.Dalton , 1766~1844)错误。现代观点:有些物质由分子构成,有些物质由原子构成,有些物质由离子构成。错误。现代观点:原子还可以分成原子核和电子,原子核又由质子和中子构成。道尔顿原子论的局限性1811年,意大利化学家阿伏伽德罗提出分子假说,1860年提升为分子学说。从此,两种学说构成了一个完整的原子——分子论。汤姆生原子模型原子并不是构成物质的最小微粒 ——汤姆生发现了电子(1897年)英国物理学家汤姆生
(J.J.Thomson ,1856~1940) 电子是种带负电、有一定质
量的微粒,普遍存在于各种原子
之中。
汤姆生认为电子就像西瓜子
一样镶嵌在原子中问题:原子还能分吗?阅读 卢瑟福和他的助手做了著名α粒子散射实验英国科学家卢瑟福
(E.Rutherford,1871~1937)卢瑟福原子模型1-3α粒子轰击原子.swf想 一 想
1. 你看到了什么现象?
2. 是什么原因造成了这些现象? a. 极大多数的 α粒子通过金箔并按原方向行进。 b.约有万分之一的α粒子改变了方向 c.个别的α粒子竟被反射回来a.说明原子内部十分空旷且电子质量很小 b.这些α粒子碰到了障碍物,而且障碍物
占据的体积很小 c.发生偏转和被反射回来的α粒子可能碰到
质量大的多的粒子(原子核)原子是由居于原子中心的带正电的原子核和核外带负电的电子构成。原子核的质量几乎等于原子的全部质量,电子在原子核外空间绕核做高速运动。就像行星环绕太阳运转一样。根据实验,卢瑟福在1911年提出: 原子有核模型(又称行星原子模型) 玻尔原子模型(1913年):电子在原子核外空间的一定轨道上绕核做高速的圆周运动。 卢瑟福根据α粒子散射实验提出了原子有核模型.
认为原子是由带正电荷的原子核核带负电荷的核外电子构成的.
原子核位于中心,如果把原子比作一个乒乓球,那么原子核只有大头针的针尖那么小,核外电子受原子核吸引,并在原子核周围空旷的空间做高速运动.
实验证明,原子核由带正电荷的质子和不带电的中子构成.
原子核中的质子数和与核外电子数是相等的,因此,整个原子不带电荷实验证明,质子和中子是由更小的微粒“夸克”构成。
有关夸克的结构和性质仍有探索和研究中……原子的结构核模型1、原子是由带正电荷的原子核和
带负电的核外电子构成2、原子核很小、位于原子中心3、核外电子受原子核的吸引,
绕核作高速运动碳原子.swf原子原子核核外电子(负电性)(正电性)质子(带正电)中子(不带电)★原子核内质子数不一定等于中子数。普通氢原子的原子核内无中子。★原子中:质子数(正) =核电荷数(正)=电子数(负) ,原子呈电中性。原子结构(电中性)一杯水的微观层次分析你知道吗?
原子失去或得到电子后,将变成什么微粒?
构成物质的微粒除了原子和分子之外还有别的吗?四、离子食盐的主要成分—氯化钠,既不是原子构成的,也不是分子构成的,而是由大量的钠离子和大量的氯离子相互吸引,聚集在一起形成的一定的条件下,原子可以失去或者得到电子,成为带电荷的离子.例如氯原子和钠原子接近时,氯原子就会从钠原子中夺取一个电子成为带一个负电荷的氯离子,而钠原子失去一个电子成为带一个正电荷的钠离子钠原子钠离子(带正电)氯原子氯离子(带负电)钠离子和氯离子相互作用,构成氯化钠晶体离子的形成如:氯化钠不是由原子或分子构成,而是由大量的___和____相互作用,聚集在一起形成的。钠离子氯离子归纳:物质由分子、原子和离子等微粒构成。离子(ion)有些原子在发生化学反应相互结合时,会有电子的得失。
原子失去电子后成为_______;原子得到电子后成为_______。阴、阳离子由于静电作用结合在一起构成物质。阳离子阴离子分子
原子
离子分
解构
成得
失
电
子构成O2、N2、H2
直接构成金属,如Fe、Cu等构成NaCl、MgO等物质构成物质的微粒H2O、CO2等物质
稀有气体,如:氖气,氦气金刚石、硅等?比较这三种微粒?保持物质化学性质的最小微粒,任何分子由原子组成,金属中不存在分子任何分子由原子构成,原子由原子核和核外电子构成,化学反应中原子不可分原子(或分子)得失电子后形成离子,离子带电(分子原子电中性)水分子、二氧化碳分子金属由原子直接构成氯化钠1、都可以构成物质
2、? 1. 分子的体积和质量都非常小,是构成物质的一种微粒。
2. 物质可以由分子,原子,离子构成
3. 原子由带正电荷的原子核和带负电荷的核外电子构成
课堂小结原子物
质分子构成原子构成:离子构成:原子核 核外电子质子中子注意:1:质子数=核电荷数=核外电子数2:分子和原子的根本区别:分子 在化学变化中再分, 而原子不能分子由原子构成(水,氧气)(金属)(盐类物质)阳离子阴离子1、下列由原子直接构成的物质有( )
A、水 B、二氧化碳
C、铁 D以上都不是
2一杯水是由___________构成,________ 是由___________________ 构成。
一个水分子是由_____________________构成。
3、原子由______和_________构成。许多水分子水分子氧原子和氢原子
一个氧原子和二个氢原子原子核核外电子练一练C4、二氧化碳由________组成,水由____________组成,一个氧气分子由_____________ 构成。碳、氢氢、氧两个氧原子4.“O2”表示氧气,还可以表示( )
①氧元素②一个氧分子③2个氧元素④氧气是由氧元素组成的⑤每个氧分子是由2个氧原子构成⑥2个氧原子
①②③ B ②④⑤ C ④⑤⑥ D ①④⑥B
怎样证明呢?
2、既然蔗糖还在水里,为什么看不到了呢?没有,水变甜了分子1、分子的定义保持物质化学性质的最小微粒,这种微粒被称为分子.
自然界中有许多的物质是由分子构成的尝试与归纳水分子氧气分子酒精分子分子是构成物质的一种的微粒氧气水水通电过程分析微粒变化示意图: 水分子分子被拆开成原子重新组合分子能不能再分呢?在什么情况下分?水分子构成分子的原子.swf在化学反应中分子可以分解成原子,任何分子都由原子构成1个水分子由2个氢原子和1个氧原子构成1个氢分子由2个氢原子构成
1个氧分子由2个氧原子构成水分子结构模型二氧化碳分子比例模型COO一个水分子是由两个氢原子
和一个氧原子构成。一个二氧化碳分子是由
一个碳原子和两个氧原子
构成。 二氧化硫分子
比例模型甲烷分子
比例模型一个二氧化硫分子是由一个
硫原子和两个氧原子构成。一个甲烷分子是由一个碳原子
和四个氢原子构成。分子的构成有的复杂,有的简单,例如一个蔗糖分子由12个碳原子,22个氢原子和11个氧原子构成,而很多的有机物例如核酸,蛋白质等是由很多个不同的原子 构成的。蛋白质分子图金,银,铜,铁等金属中不存在分子,分别由无数个金原子,银原子,铜原子等直接构成的。金属构成图2、分子的构成与大小1、一滴水的分子个数:
1000 000 000 000 000 000 000个水分子构成,
1ml水需要约20滴水组成。2、如果把水分子放大到乒乓球那么大,那么乒乓球就要放大到地球那么大。 数的启示?3、铅笔留下的黑色的笔迹是碳原子的堆积,一个句号竟有1018个碳原子。启示:1、分子和原子体积都很小一个氢原子质量:1.674×10-27千克一个碳原子质量:1.993×10-26千克一个氧原子质量:2.657×10-26千克一个氢分子质量:3.348×10-27千克一个二氧化碳分子质量:7.307×10-26千克(可以放大几百万倍)分子照片分子很小,即使用放大1500倍的光学显微镜,也不能直接观察,1982年IBM公司两位科学家发明了扫描隧道显微镜(STM),STM的发明被公认为20世纪80年代的重要发明之一,获得了1986年诺贝尔物理奖1.道尔顿原子模型
(1803年)实心球模型阅读:原子——分子论道尔顿原子模型一切物质都是由最小的不能再分的粒子——原子构成。
原子模型:原子是坚实的、不可再分的实心球。
同种原子的大小、形状、质量和性质完全相同,不同种原子则不相同。近代科学原子论 英国化学家道尔顿
(J.Dalton , 1766~1844)一切物质都是由最小的不能再分的粒子——原子构成。
原子模型:原子是坚实的、不可再分的实心球。
英国化学道尔顿
(J.Dalton , 1766~1844)错误。现代观点:有些物质由分子构成,有些物质由原子构成,有些物质由离子构成。错误。现代观点:原子还可以分成原子核和电子,原子核又由质子和中子构成。道尔顿原子论的局限性1811年,意大利化学家阿伏伽德罗提出分子假说,1860年提升为分子学说。从此,两种学说构成了一个完整的原子——分子论。汤姆生原子模型原子并不是构成物质的最小微粒 ——汤姆生发现了电子(1897年)英国物理学家汤姆生
(J.J.Thomson ,1856~1940) 电子是种带负电、有一定质
量的微粒,普遍存在于各种原子
之中。
汤姆生认为电子就像西瓜子
一样镶嵌在原子中问题:原子还能分吗?阅读 卢瑟福和他的助手做了著名α粒子散射实验英国科学家卢瑟福
(E.Rutherford,1871~1937)卢瑟福原子模型1-3α粒子轰击原子.swf想 一 想
1. 你看到了什么现象?
2. 是什么原因造成了这些现象? a. 极大多数的 α粒子通过金箔并按原方向行进。 b.约有万分之一的α粒子改变了方向 c.个别的α粒子竟被反射回来a.说明原子内部十分空旷且电子质量很小 b.这些α粒子碰到了障碍物,而且障碍物
占据的体积很小 c.发生偏转和被反射回来的α粒子可能碰到
质量大的多的粒子(原子核)原子是由居于原子中心的带正电的原子核和核外带负电的电子构成。原子核的质量几乎等于原子的全部质量,电子在原子核外空间绕核做高速运动。就像行星环绕太阳运转一样。根据实验,卢瑟福在1911年提出: 原子有核模型(又称行星原子模型) 玻尔原子模型(1913年):电子在原子核外空间的一定轨道上绕核做高速的圆周运动。 卢瑟福根据α粒子散射实验提出了原子有核模型.
认为原子是由带正电荷的原子核核带负电荷的核外电子构成的.
原子核位于中心,如果把原子比作一个乒乓球,那么原子核只有大头针的针尖那么小,核外电子受原子核吸引,并在原子核周围空旷的空间做高速运动.
实验证明,原子核由带正电荷的质子和不带电的中子构成.
原子核中的质子数和与核外电子数是相等的,因此,整个原子不带电荷实验证明,质子和中子是由更小的微粒“夸克”构成。
有关夸克的结构和性质仍有探索和研究中……原子的结构核模型1、原子是由带正电荷的原子核和
带负电的核外电子构成2、原子核很小、位于原子中心3、核外电子受原子核的吸引,
绕核作高速运动碳原子.swf原子原子核核外电子(负电性)(正电性)质子(带正电)中子(不带电)★原子核内质子数不一定等于中子数。普通氢原子的原子核内无中子。★原子中:质子数(正) =核电荷数(正)=电子数(负) ,原子呈电中性。原子结构(电中性)一杯水的微观层次分析你知道吗?
原子失去或得到电子后,将变成什么微粒?
构成物质的微粒除了原子和分子之外还有别的吗?四、离子食盐的主要成分—氯化钠,既不是原子构成的,也不是分子构成的,而是由大量的钠离子和大量的氯离子相互吸引,聚集在一起形成的一定的条件下,原子可以失去或者得到电子,成为带电荷的离子.例如氯原子和钠原子接近时,氯原子就会从钠原子中夺取一个电子成为带一个负电荷的氯离子,而钠原子失去一个电子成为带一个正电荷的钠离子钠原子钠离子(带正电)氯原子氯离子(带负电)钠离子和氯离子相互作用,构成氯化钠晶体离子的形成如:氯化钠不是由原子或分子构成,而是由大量的___和____相互作用,聚集在一起形成的。钠离子氯离子归纳:物质由分子、原子和离子等微粒构成。离子(ion)有些原子在发生化学反应相互结合时,会有电子的得失。
原子失去电子后成为_______;原子得到电子后成为_______。阴、阳离子由于静电作用结合在一起构成物质。阳离子阴离子分子
原子
离子分
解构
成得
失
电
子构成O2、N2、H2
直接构成金属,如Fe、Cu等构成NaCl、MgO等物质构成物质的微粒H2O、CO2等物质
稀有气体,如:氖气,氦气金刚石、硅等?比较这三种微粒?保持物质化学性质的最小微粒,任何分子由原子组成,金属中不存在分子任何分子由原子构成,原子由原子核和核外电子构成,化学反应中原子不可分原子(或分子)得失电子后形成离子,离子带电(分子原子电中性)水分子、二氧化碳分子金属由原子直接构成氯化钠1、都可以构成物质
2、? 1. 分子的体积和质量都非常小,是构成物质的一种微粒。
2. 物质可以由分子,原子,离子构成
3. 原子由带正电荷的原子核和带负电荷的核外电子构成
课堂小结原子物
质分子构成原子构成:离子构成:原子核 核外电子质子中子注意:1:质子数=核电荷数=核外电子数2:分子和原子的根本区别:分子 在化学变化中再分, 而原子不能分子由原子构成(水,氧气)(金属)(盐类物质)阳离子阴离子1、下列由原子直接构成的物质有( )
A、水 B、二氧化碳
C、铁 D以上都不是
2一杯水是由___________构成,________ 是由___________________ 构成。
一个水分子是由_____________________构成。
3、原子由______和_________构成。许多水分子水分子氧原子和氢原子
一个氧原子和二个氢原子原子核核外电子练一练C4、二氧化碳由________组成,水由____________组成,一个氧气分子由_____________ 构成。碳、氢氢、氧两个氧原子4.“O2”表示氧气,还可以表示( )
①氧元素②一个氧分子③2个氧元素④氧气是由氧元素组成的⑤每个氧分子是由2个氧原子构成⑥2个氧原子
①②③ B ②④⑤ C ④⑤⑥ D ①④⑥B
同课章节目录
- 第1章 运动和力
- 1 机械运动
- 2 力
- 3 几种常见的力
- 4 运动和力
- 5 二力平衡的条件
- 第2章 压力 压强
- 1 压强
- 2 液体内部的压强
- 3 大气压强
- 4 流体的压强与流速的关系
- 第3章 浮力
- 1 密度
- 2 浮力
- 3 阿基米德原理
- 4 物体浮沉条件及其应用
- 第4章 植物的物质和能量的转化
- 1 绿色开花植物的营养器官
- 2 水在植物体中的代谢
- 3 无机盐在植物体内的代谢
- 4 植物的光合作用和呼吸作用
- 第5章 人体的物质和能量的转化
- 1 食物的消化和吸收
- 2 人体的呼吸
- 3 人体内的物质运输
- 4 人体的排泄
- 5 人体生命活动过程中物质和能量的转化
- 第6章 物质的构成
- 1 构成物质的微粒
- 2 元素
- 3 物质的分类
- 4 化学式
- 5 固态物质
