人教版九年级化学上册第三单元 构成物质的奥秘 单元测试卷(含答案解析版)
文档属性
| 名称 | 人教版九年级化学上册第三单元 构成物质的奥秘 单元测试卷(含答案解析版) |  | |
| 格式 | doc | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-24 10:13:26 | ||
图片预览


文档简介
人教版九年级化学上册第三单元 构成物质的奥秘 单元测试卷
一、选择题(14分)
1.一定条件下,3000L氮气可压入20L的钢瓶中。对此现象微观解释正确的是
A.氮气分子的形状发生了改变 B.氮气分的的质量变小了
C.氮气分子的数目减少 D.氮气分子间的间隔变小了
2.如图是溴元素的有关信息,下列有关说法不正确的是
A.溴元素在化合物中通常显+7价 B.溴的原子序数是35
C.溴属于非金属元素 D.溴元素位于元素周期表的第四周期
3.如图所示是三种粒子的结构示意图。下列说法正确的是
A.①表示阴离子 B.②③的化学性质相似
C.②③属于同种元素 D.②在化学变化中易失去电子
4.测量体温时,水银温度计内的汞柱会上升。用微粒的观点解释该现象正确的是
A.原子间间隔变大 B.原子数目增多 C.原子体积变大 D.原子质量变大
5.对以下原子结构示意图的分析得出的认识或判断,其中错误的是
A.在化合物中,①可显﹣2价,⑤可显+2价
B.③为相对稳定结构,通常很难发生化学变化
C.①②为非金属元素的原子,④⑤为金属元素的原子
D.上述粒子在发生化学反应时,其质子数、电子数均发生改变
6.元素周期表是学习化学的重要工具。如图是元素周期表的一部分,下列说法正确的是
A.铁的相对原子质量为55.85g B.锰元素为非金属元素
C.铬原子的原子核内有52个质子 D.铬原子核外电子数为24
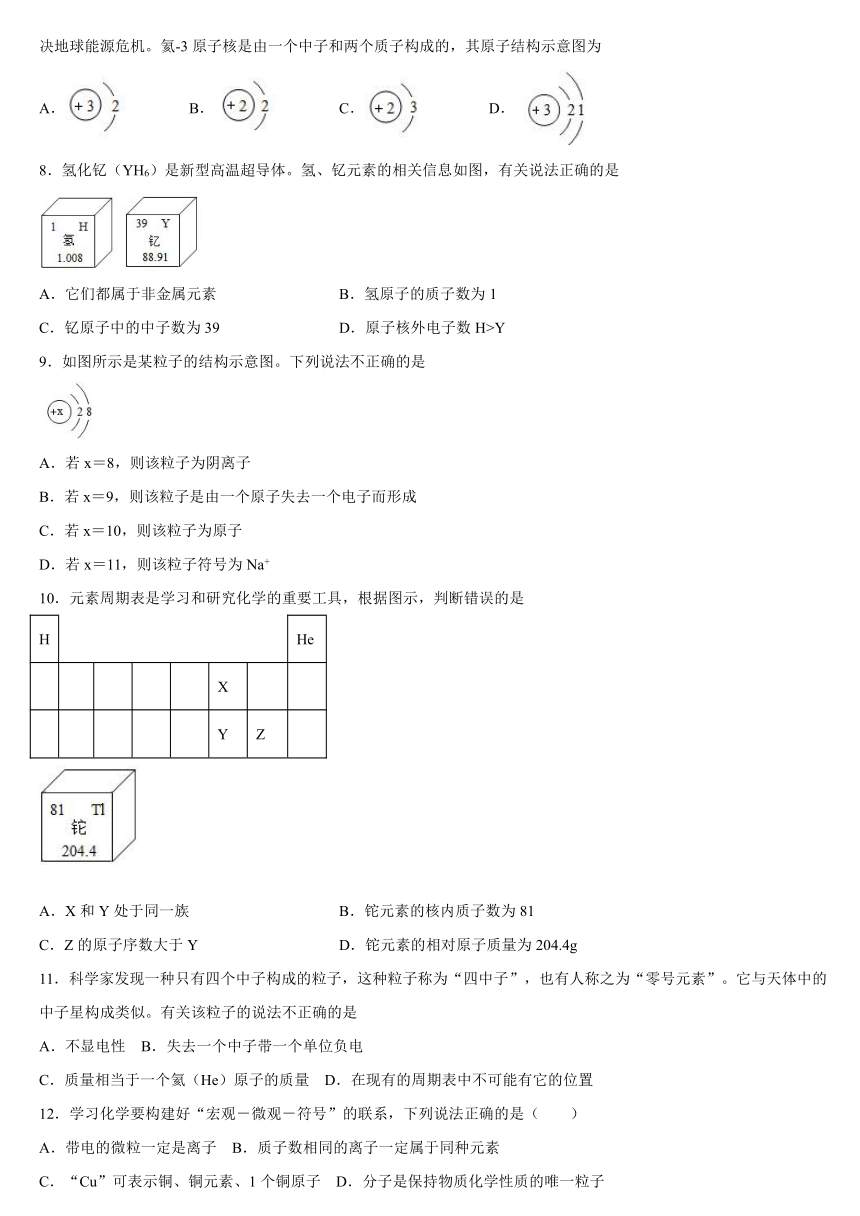
7.我国圆满完成了“嫦娥五号”探月工程,并采回月球土壤样品。月球土壤中含有较丰富的核聚变原料——氦-3,有望解决地球能源危机。氦-3原子核是由一个中子和两个质子构成的,其原子结构示意图为
A. B. C. D.
8.氢化钇(YH6)是新型高温超导体。氢、钇元素的相关信息如图,有关说法正确的是
A.它们都属于非金属元素 B.氢原子的质子数为1
C.钇原子中的中子数为39 D.原子核外电子数H>Y
9.如图所示是某粒子的结构示意图。下列说法不正确的是
A.若x=8,则该粒子为阴离子
B.若x=9,则该粒子是由一个原子失去一个电子而形成
C.若x=10,则该粒子为原子
D.若x=11,则该粒子符号为Na+
10.元素周期表是学习和研究化学的重要工具,根据图示,判断错误的是
H He
X
Y Z
A.X和Y处于同一族 B.铊元素的核内质子数为81
C.Z的原子序数大于Y D.铊元素的相对原子质量为204.4g
11.科学家发现一种只有四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。它与天体中的中子星构成类似。有关该粒子的说法不正确的是
A.不显电性 B.失去一个中子带一个单位负电
C.质量相当于一个氦(He)原子的质量 D.在现有的周期表中不可能有它的位置
12.学习化学要构建好“宏观-微观-符号”的联系,下列说法正确的是( )
A.带电的微粒一定是离子 B.质子数相同的离子一定属于同种元素
C.“Cu”可表示铜、铜元素、1个铜原子 D.分子是保持物质化学性质的唯一粒子
13.对Fe、Fe2+、Fe3+三种微粒,下列判断正确的是
①核电荷数相同②核外电子数相同③电子层结构完全相同④质量几乎相等⑤等质量的微粒所含的质子数相同
A.①②③④⑤ B.①③⑤ C.①④⑤ D.②③④
14.某元素原子A的质子数为z,已知B3﹣和A2+具有相同的核外电子数,则B元素的质子数为
A.z﹣2+3 B.z﹣2﹣3 C.z+2+3 D.z+2﹣3
二、填空题(16分)
15.写出下列元素的符号
(1)地壳中含量最多的元素______;
(2)空气中含量最多的元素______;
(3)相对原子质量最小的元素______;
(4)地壳中含量最多的金属元素______。
16.结合下图回答有关问题:
(1)氢氧化钠是由钠元素、______三种元素组成的;
(2)由图 A 可知,钠元素原子核电荷数是______;
(3)在图 B、C、D 中,钠离子结构示意图是______。
17.请用微观粒子的相关知识解释如下现象。
(1)走到天颐路正道小磨香油厂附近闻到油香___________。
(2)用水银温度计测量体温,发现水银柱升高___________。
18.在宏观、微观、符号之间建立联系,是化学学科独有的思维方式。请根据下图提供的信息,回答相关问题:
(1)A图表示一种原子,其中X的值是___________。
(2)化学性质相似的原子是___________(填字母序号)。
(3)D粒子的名称是___________。
19.有下列六种粒子的结构示意图:
(1)上述粒子共表示___________种元素。
(2)上述六种粒子中,化学性质相似的两种原子是___________(填写序号)。
20.已知一个碳12原子的质量为1.993×10﹣26kg,一个钬原子的质量是2.740×10﹣25kg,则钬的相对原子质量为___________;相同质量的钠、镁、铝含原子数目最多的是__________(钠、镁、铝的相对原子质量分别是23、24、27).
三、简答题(10分)
21.化学实验体现学生的科学素养。学习化学要不断地对实验进行思考、改进,在实验中理解化学反应的本质。如图是某同学探究浓氨水的性质改进实验。通过此实验,你能得出什么结论?(写出一条即可)
22.下面是分子的部分性质,请举出实例来说明分子的这些性质。
(1)分子在不断地运动__________;
(2)分子之间有间隔___________;
(3)温度越高,分子运动速率越快____________。
23.根据如图回答下列问题:
上下两个集气瓶中分别盛有空气和红棕色的二氧化氮气体,当抽出玻璃片后,过一会儿,可观察到什么现象________?你能用分子的观察解释这一现象吗________?
24.小明通过以下实验探究分子的某些性质,实验装置如下:
(1)对比描述B、C的实验现象_____;
(2)由此可以得到的实验结论是_____。
(3)保持水的化学性质的最小粒子是_____。
四、综合应用题(10分)
25.人教版九年级化学上册教材图3-12部分原子的结构示意图如下:
请回答:
(1)氧元素属于非金属元素,其原因是____________;
(2)同一周期(横行)的原子结构示意图具有共同的特点是____________(任写一点)。
(3)表中可由原子直接构成的气态物质有________(作写一种);12号和17号元素组成的化合物的化学式为___________,其中构成该物质的阳离子的符号是________。
(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素的原子具有相似化学性质的是 _________(填标号)。
a. He和Na b. Be和Mg c. Al和Si d. F和Cl
(5)一般地说,电子层数相同的原子,原子的半径随原子序数的递增而减小(稀有气体除外);最外层电子数相同的原子,原子的半径随电子层数的增加而增大。
请比较:氮原子半径________(填“>”或“<”,后同)磷原子半径;钠原子半径________铝原子半径。
【参考答案】
1.D 2.A 3.C 4.A 5.D 6.D 7.B 8.B 9.B 10.D 11.B 12.C 13.C 14.B
15.
(1)O
(2)N
(3)H
(4)Al
16.(1)氢元素和氧元素(2)11(3)C
17.分子是不断运动的 温度升高,汞原子间隔变大
18.9 AC 氯离子
19.五 EF
20.170 钠
21.分子在不断运动(或氨水显碱性,浓氨水易挥发)
22.走到花店门口能闻到花香等 压瘪的乒乓球放入热水中重新鼓起来等 湿衣服晒在太阳下比在阴凉处干得快等(答案合理即可给分)
23.上面的集气瓶中也充满了红棕色的气体 分子在不停的运动
24.C中液体比B中液体先变红 分子在运动,温度越高分子运动越快 水分子
25.氧原子最外层电子数大于4 各原子的电子层数相同 氦气(或氖气、氩气)(或其化学式) MgCl2 Mg2+ bd <
一、选择题(14分)
1.一定条件下,3000L氮气可压入20L的钢瓶中。对此现象微观解释正确的是
A.氮气分子的形状发生了改变 B.氮气分的的质量变小了
C.氮气分子的数目减少 D.氮气分子间的间隔变小了
2.如图是溴元素的有关信息,下列有关说法不正确的是
A.溴元素在化合物中通常显+7价 B.溴的原子序数是35
C.溴属于非金属元素 D.溴元素位于元素周期表的第四周期
3.如图所示是三种粒子的结构示意图。下列说法正确的是
A.①表示阴离子 B.②③的化学性质相似
C.②③属于同种元素 D.②在化学变化中易失去电子
4.测量体温时,水银温度计内的汞柱会上升。用微粒的观点解释该现象正确的是
A.原子间间隔变大 B.原子数目增多 C.原子体积变大 D.原子质量变大
5.对以下原子结构示意图的分析得出的认识或判断,其中错误的是
A.在化合物中,①可显﹣2价,⑤可显+2价
B.③为相对稳定结构,通常很难发生化学变化
C.①②为非金属元素的原子,④⑤为金属元素的原子
D.上述粒子在发生化学反应时,其质子数、电子数均发生改变
6.元素周期表是学习化学的重要工具。如图是元素周期表的一部分,下列说法正确的是
A.铁的相对原子质量为55.85g B.锰元素为非金属元素
C.铬原子的原子核内有52个质子 D.铬原子核外电子数为24
7.我国圆满完成了“嫦娥五号”探月工程,并采回月球土壤样品。月球土壤中含有较丰富的核聚变原料——氦-3,有望解决地球能源危机。氦-3原子核是由一个中子和两个质子构成的,其原子结构示意图为
A. B. C. D.
8.氢化钇(YH6)是新型高温超导体。氢、钇元素的相关信息如图,有关说法正确的是
A.它们都属于非金属元素 B.氢原子的质子数为1
C.钇原子中的中子数为39 D.原子核外电子数H>Y
9.如图所示是某粒子的结构示意图。下列说法不正确的是
A.若x=8,则该粒子为阴离子
B.若x=9,则该粒子是由一个原子失去一个电子而形成
C.若x=10,则该粒子为原子
D.若x=11,则该粒子符号为Na+
10.元素周期表是学习和研究化学的重要工具,根据图示,判断错误的是
H He
X
Y Z
A.X和Y处于同一族 B.铊元素的核内质子数为81
C.Z的原子序数大于Y D.铊元素的相对原子质量为204.4g
11.科学家发现一种只有四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。它与天体中的中子星构成类似。有关该粒子的说法不正确的是
A.不显电性 B.失去一个中子带一个单位负电
C.质量相当于一个氦(He)原子的质量 D.在现有的周期表中不可能有它的位置
12.学习化学要构建好“宏观-微观-符号”的联系,下列说法正确的是( )
A.带电的微粒一定是离子 B.质子数相同的离子一定属于同种元素
C.“Cu”可表示铜、铜元素、1个铜原子 D.分子是保持物质化学性质的唯一粒子
13.对Fe、Fe2+、Fe3+三种微粒,下列判断正确的是
①核电荷数相同②核外电子数相同③电子层结构完全相同④质量几乎相等⑤等质量的微粒所含的质子数相同
A.①②③④⑤ B.①③⑤ C.①④⑤ D.②③④
14.某元素原子A的质子数为z,已知B3﹣和A2+具有相同的核外电子数,则B元素的质子数为
A.z﹣2+3 B.z﹣2﹣3 C.z+2+3 D.z+2﹣3
二、填空题(16分)
15.写出下列元素的符号
(1)地壳中含量最多的元素______;
(2)空气中含量最多的元素______;
(3)相对原子质量最小的元素______;
(4)地壳中含量最多的金属元素______。
16.结合下图回答有关问题:
(1)氢氧化钠是由钠元素、______三种元素组成的;
(2)由图 A 可知,钠元素原子核电荷数是______;
(3)在图 B、C、D 中,钠离子结构示意图是______。
17.请用微观粒子的相关知识解释如下现象。
(1)走到天颐路正道小磨香油厂附近闻到油香___________。
(2)用水银温度计测量体温,发现水银柱升高___________。
18.在宏观、微观、符号之间建立联系,是化学学科独有的思维方式。请根据下图提供的信息,回答相关问题:
(1)A图表示一种原子,其中X的值是___________。
(2)化学性质相似的原子是___________(填字母序号)。
(3)D粒子的名称是___________。
19.有下列六种粒子的结构示意图:
(1)上述粒子共表示___________种元素。
(2)上述六种粒子中,化学性质相似的两种原子是___________(填写序号)。
20.已知一个碳12原子的质量为1.993×10﹣26kg,一个钬原子的质量是2.740×10﹣25kg,则钬的相对原子质量为___________;相同质量的钠、镁、铝含原子数目最多的是__________(钠、镁、铝的相对原子质量分别是23、24、27).
三、简答题(10分)
21.化学实验体现学生的科学素养。学习化学要不断地对实验进行思考、改进,在实验中理解化学反应的本质。如图是某同学探究浓氨水的性质改进实验。通过此实验,你能得出什么结论?(写出一条即可)
22.下面是分子的部分性质,请举出实例来说明分子的这些性质。
(1)分子在不断地运动__________;
(2)分子之间有间隔___________;
(3)温度越高,分子运动速率越快____________。
23.根据如图回答下列问题:
上下两个集气瓶中分别盛有空气和红棕色的二氧化氮气体,当抽出玻璃片后,过一会儿,可观察到什么现象________?你能用分子的观察解释这一现象吗________?
24.小明通过以下实验探究分子的某些性质,实验装置如下:
(1)对比描述B、C的实验现象_____;
(2)由此可以得到的实验结论是_____。
(3)保持水的化学性质的最小粒子是_____。
四、综合应用题(10分)
25.人教版九年级化学上册教材图3-12部分原子的结构示意图如下:
请回答:
(1)氧元素属于非金属元素,其原因是____________;
(2)同一周期(横行)的原子结构示意图具有共同的特点是____________(任写一点)。
(3)表中可由原子直接构成的气态物质有________(作写一种);12号和17号元素组成的化合物的化学式为___________,其中构成该物质的阳离子的符号是________。
(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素的原子具有相似化学性质的是 _________(填标号)。
a. He和Na b. Be和Mg c. Al和Si d. F和Cl
(5)一般地说,电子层数相同的原子,原子的半径随原子序数的递增而减小(稀有气体除外);最外层电子数相同的原子,原子的半径随电子层数的增加而增大。
请比较:氮原子半径________(填“>”或“<”,后同)磷原子半径;钠原子半径________铝原子半径。
【参考答案】
1.D 2.A 3.C 4.A 5.D 6.D 7.B 8.B 9.B 10.D 11.B 12.C 13.C 14.B
15.
(1)O
(2)N
(3)H
(4)Al
16.(1)氢元素和氧元素(2)11(3)C
17.分子是不断运动的 温度升高,汞原子间隔变大
18.9 AC 氯离子
19.五 EF
20.170 钠
21.分子在不断运动(或氨水显碱性,浓氨水易挥发)
22.走到花店门口能闻到花香等 压瘪的乒乓球放入热水中重新鼓起来等 湿衣服晒在太阳下比在阴凉处干得快等(答案合理即可给分)
23.上面的集气瓶中也充满了红棕色的气体 分子在不停的运动
24.C中液体比B中液体先变红 分子在运动,温度越高分子运动越快 水分子
25.氧原子最外层电子数大于4 各原子的电子层数相同 氦气(或氖气、氩气)(或其化学式) MgCl2 Mg2+ bd <
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
