人教版化学九年级上册 第三单元 物质构成的奥秘 复习课课件(共55张PPT)
文档属性
| 名称 | 人教版化学九年级上册 第三单元 物质构成的奥秘 复习课课件(共55张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-24 00:00:00 | ||
图片预览







文档简介
(共55张PPT)
第三单元
物质构成的奥秘复习
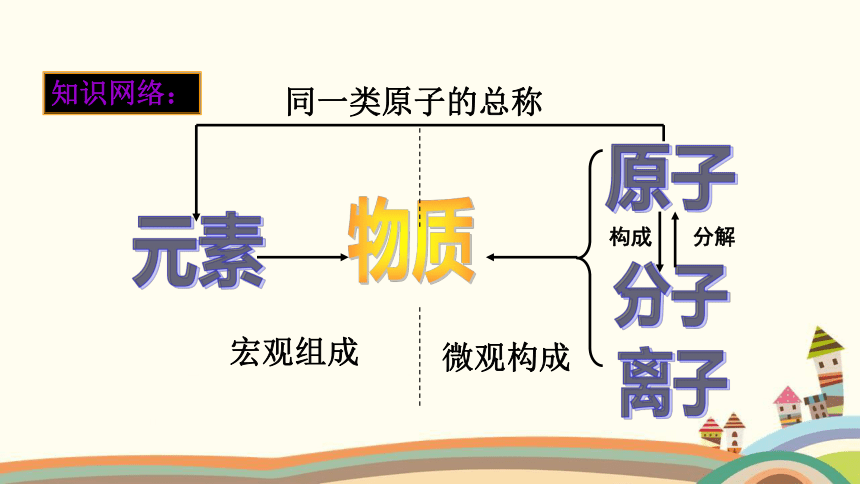
物质
分子
原子
离子
微观构成
元素
宏观组成
同一类原子的总称
知识网络:
构成
分解
微粒名称 定义 微粒特征 实例
构成物质的基本微粒 (微观)
分子
原子
离子
分子是保持物质化
学性质的最小微粒
原子是化学变化
中的最小微粒
带电的原子(或
原子团)叫离子
很小、运动、有空隙
很小、运动、有间隔
二氧化碳
水、氧气
铁、氖气、金刚石
氯化钠、
氧化镁
很小、运动、有空隙
基本概念_识记
元素:是具有相同核电荷数(即核内质子数)的一类原子的总称。(宏观)
元素的种类由原子中的质子数决定
离子
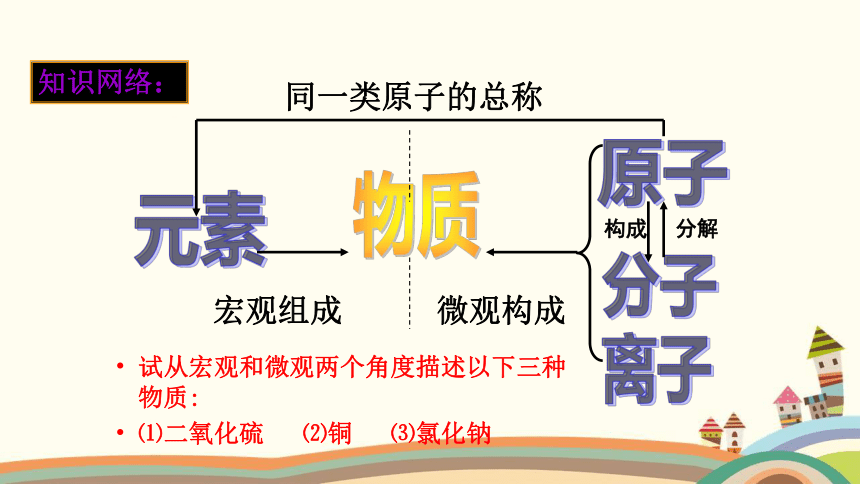
知识网络:
物质
分子
原子
微观构成
元素
宏观组成
同一类原子的总称
构成
分解
试从宏观和微观两个角度描述以下三种物质:
⑴二氧化硫 ⑵铜 ⑶氯化钠
1. 科学研究证明,物质是由元素组成的,由微粒构成的。请用元素或具体的微粒名称填空:
(1)汞由 组成;汞由 构成。
(2)氧气由 组成;氧气由许多
构成。
(3)水由 组成;水由许多 构成;一个水分子是由 和 构成。
(4)氯化钠由 组成,由 构成。
典型题
分子和原子之间有什么区别和联系呢
联系:分子是由原子构成的,在化学变化中,分子可以划分为原子。
区别:在化学变化中,分子可分,原子不可分。
化学变化的实质(微观):分子划分为原子,原子重新组合,构成新的分子。
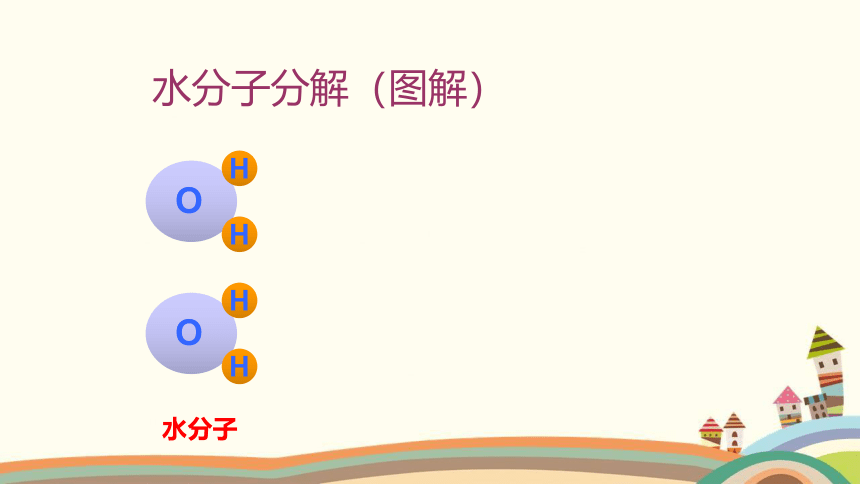
水分子分解(图解)
O
H
H
O
H
H
水分子
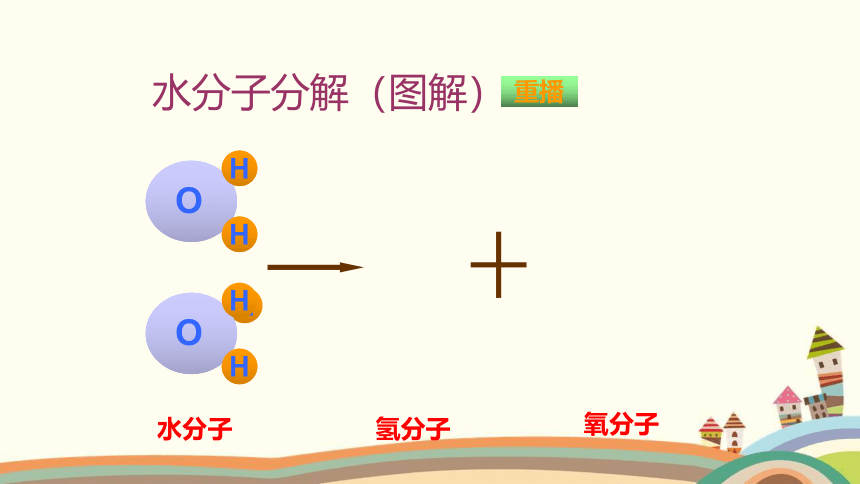
水分子分解(图解)
O
H
H
O
H
H
O
H
H
O
H
H
水分子
氢分子
氧分子
重播
试用分子、原子的知识解释:
双氧水在二氧化锰催化作用下生成水和氧气。
2.生活中的下列现象中,是分子发生变化生成其他分子的是 ( )
A.红磷燃烧 B.花香四溢 C.水分蒸发 D.热胀冷缩
3.在电解水这一变化中,没有变化的微粒是 ( )
A.水分子 B.水原子
C.氢、氧原子 D .以上都不是
典型题
A
C
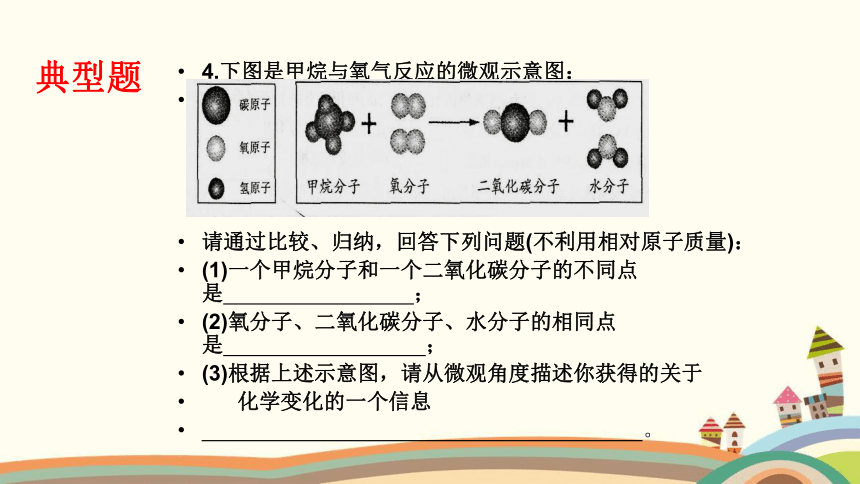
4.下图是甲烷与氧气反应的微观示意图:
请通过比较、归纳,回答下列问题(不利用相对原子质量):
(1)一个甲烷分子和一个二氧化碳分子的不同点是 ;
(2)氧分子、二氧化碳分子、水分子的相同点是 ;
(3)根据上述示意图,请从微观角度描述你获得的关于
化学变化的一个信息
。
典型题
原子
原子核
核外电子(-)
质子(+)
中子(不带电)
原子序数 = 核电荷数 = 质子数 = 核外电子数
原 子 的 质 量 主 要 集 中 在 原 子 核 上
5.在同一原子中一定相同的是 ( )
A.中子数和电子数 B.中子数和质子数
C.质子数和电子数 D.核电荷数和中子数
6.某些花岗岩石材中含有放射性的元素氡。氡原子的质子数为86,中子数为136,则氡原子的核外电子数为 ( )
A.50 B.86 C.136 D.222
典型题
C
B
1.国际上统一规定,以一种碳原子质量的1/12 (约1.66× 10-27 kg)作为标准,其它原子的质量跟它比较所得的值,就是这种原子的相对原子质量
相对原子质量
某原子的相对原子质量
=
该原子一个原子的实际质量
一种碳原子的质量 ×1 /12
=
质子数 + 中子数
3.相对原子质量
2.计算式:
4.相对原子质量的单位为1
5.相对原子质量与原子的实际质量成正比关系
1.观察下表:
原子种类 质子数 中子数 核外电子数 相对原子质量
氢(H) 1 0 1 1
氮(N) 7 7 7 14
氧(O) 8 8 8 16
铁(Fe) 26 30 26 56
铀(U) 92 143 92 235
通过此表,可以总结出的规律有:
(1) ;(2) ;
(3) ;(4) 。
典型题
2.1991年我国著名化学家张青莲教授与另一位化学家合作测定了铟(In)元素的相对原子质量新值。铟元素的核电荷数为49,相对原子质量为115。则铟的中子数为( )
A.115 B.49 C.66 D.164 2.
3.已知一个含有6个质子和6个中子的碳原子质量为Ag。若某原子的一个原子的实际质量为Bg,则该原子的质量为( )
A.12B/A B.B/12A
C.AB/12 D.12/AB
A
C
4.已知一个铁的相对原子质量为A,一个标准碳原子质量为bkg,则铁原子的质量为 。
练兵场
议一议:
在化学发展史上,道尔顿提出的近代原子学说对化学的发展起着十分重要的作用,因而拥有“原子之父”的美誉。在他的学说中有下述三个主要论点:①原子是不能再分的粒子;②质子数相同的原子的各种性质和质量都相同;③原子是微小的实心球体。从现代的观点看,你认为这三点中不确切的是哪几点,并说明理由。
原子结构示意图
电子层
电子层上
电子数
核电荷数
原子核
元素种类 最外层电子数 元素的化学性质
稀有气体
8个(He为2个)
比较稳定
元素的种类 最外层电子数 元素的化学性质
金 属
一般少于4个
易失电子
元素种类 最外层电子数 元素的化学性质
非金属
一般大于或等于4个
易得电子
原 子
离 子
元素的化学性质由最外层电子数决定
离子的形成:
阳离子( + )
原子
阴离子( - )
得电子
失电子
请结合此图讨论:由原子变成离子哪些一定改变,哪些可能改变,哪些一定不变。
原子与离子的区别与联系
原子是不稳定结构而离子是稳定结构
1、概念上:
2、电性上:
3、结构上:
区别
联系:
原子是化学变化中的最小微粒而离子是带电的原子或原子团
原子不带电而离子带电
原子
失电子
得电子
阳离子
失电子
得电子
阴离子
原子中: 核电荷数 质子数 核外电子数
阳离子: 核电荷数 质子数 核外电子数
阴离子: 核电荷数 质子数 核外电子数
=
=
=
=
>
<
1.下图是元素周期表中硫元素及其原子结构示意图,下列做法错误的是( )
A.硫的相对原子质量为16
B.硫属于非金属元素
C.硫原子在化学反应中容易得到电子
D.硫原子核内有16个质子
典型题
A
2.怎么看原子结构图和离子结构图
下面A、B、C、D四幅图,你知道那幅图是原子结构图,那幅是离子结构图吗?
属于原子的是 ,依据是 。
属于离子的是 ,依据是 ;
其中属于阳离子的是 ,因为: 。
其中属于阴离子的是 ,因为: 。
A、C
B、D
质子数=电子数
质子数≠电子数
D
B
质子数>电子数
质子数<电子数
3.根据下列原子或离子结构示意图填空。
(1)电子层排布相同的是 。
(2)属于同种元素的是 。
(3)属于金属元素的是 。
(4)属于稀有气体元素的是 。
(5)属于阴离子的是 ,
其离子符号是 。
B、C
A、B
D
C
B
F-
化学元素
元
素
元素:
现在已发现的元素有100多种,大部分为金属元素
元素符号:
拉丁文(第一字母大写,第二字母小写)
元素符号的含义:
一种元素;这种元素的一个原子
元素是同具有相同核电荷数的同一类原子的总称
元素的存在:
地壳中:
氧、硅、铝、铁、钙
人体中:
氧;碳、氢、氮
太阳上:
氢;氦
空气中:
氮、氧
元素与
人体健康
缺钙:骨质疏松 ;缺铁钴:贫血 ;
缺锌:智力低下 ;缺碘:甲亢 。
海水中:
氧、氢
元素分类:
金属元素:铁、镁、铝、钠、钾、铜、锰、锌、银、钡、汞、金等
非金属元素:氧、氢、氮、氯、碳、硫、磷、硅、碘等
稀有气体元素:氦、氖、氩等
在空格中填写适当的元素符号。
地壳中含量最多的非金属元素是 ,其次是 ;地壳中含量最多的金属元素是 ,其次是 ;地球大气里含量最多的元素是 ;人体里含量最多的元素是 ;海洋里含量最多的元素是 ;太阳中含量最多的元素是 ;地核中含量最多的元素是 ;人体缺少 元素,容易得贫血症;小儿体内缺少 元素,容易得佝偻病;缺 会导致儿童发育迟缓,智力低下;人体缺 元素会引起龋齿,但它含量过高,又会使牙齿釉质受损。
O
Si
Al
Fe
N
O
O
Fe
Fe
Ca
Zn
F
H
元素分布
练习:
1.氧化镁和氧气中都存在着______元素。
2.一种元素与另一种元素的本区别是( )
A.原子量 B.中子数
C.质子数 D.电子数
3.二氧化硫、氧化汞、氧气中都含有( )
A.氧气 B.氧原子
C.氧分子 D.氧元素
4.某药品说明书中标明:本品每克含碘150mg、镁65mg、锌1.5mg、铜2mg、锰1mg,这里所标的各成分是指 ( )
A.分子 B.原子 C.元素 D.无法确定
C
D
C
5.元素周期表是学习和研究化学的重要工具,它的内容非常丰富。你认为从元素周期表中不能直接获得的信息是( )
A.元素在自然界中的分布
B.元素性质的变化规律
C.元素符号
D.元素的原子序数
6.下列各组物质按单质、化合物、混合物顺序排列的是( )
A.氧气、水、白酒
B.天然气、煤、石油
C.水银、烧碱、纯碱
D.干冰、C60、酒精
物质
按物质
种类分
按元素
种类分
混合物
(不同种物质组成)
纯净物
(同种物质组成)
单质
(同种元素组成)
化合物
(不同种元素组成)
按性质分
金属(如Fe、Cu等)
非金属(如C、O2等)
稀有气体(如He、Ne等)
按组成和
性质分
氧化物(如H2O等)
其他
(如空气、海水、澄清石灰水、石灰石等)
物质分类
链接主页四
2.有下列两组物质,每组中均有一种与其他物质所属类别不同,氢在下面的横线上填写出这种物质的名称:
(1)食醋、牛奶、加碘盐、蔗糖
(2)氧化镁、水、碳酸钙、五氧化二磷
(1) (2)
1.家庭日常生活中经常用到的下列物质中,属于纯净物的是( )
A.餐饮用的可口可乐 B.调味用的加碘食盐
C.炒菜用的铁过 D.降温用的冰水共存物
D
蔗糖
碳酸钙
4.一瓶气体经化验只由一种元素组成,则该气体是( )
A.一种单质 B.一种化合物
C.一种纯净物
D.可能是一种单质,也可能是几种单质组成的
混合物
D
3.下列各组物质中,前者是单质,后者是氧化物的是( )
A.石灰石 冰 B.金刚石 干冰
C.液氧 氯酸钾 D.水银 碘酒
B
构成六种物质的微粒如图所示
(大圆表示氧原子,小圆表示氢原子)
2.C和D表示的物质有什么区别
它们是同种物质吗
1.哪些密闭容器中表示混合物
8.有六种物质能按下列顺序排列:①CO ②H2O ③NH3 ④X ⑤C2H4 ⑥P2O5 。根据它们的组成和排列的规律,X可能是 。请解释你选择该答案的原因: 。
A.NaNO3 B.CH4 C.Fe2O3 D.PCl5
化学式 化合价
判断
书写
化合价与化学式的关系
(1)知式标价:
例1:标出下列物质中各元素的化合价
氯化锌 金属锌 氢氧化钠
ZnCl2
+2 -1
Zn
0
NaOH
+1 -2 +1
(2)知式求价:
例2: 试确定氯酸钾中氯元素的化合价
解:设氯元素的化合价为X
先写出氯酸钾的化学式:KClO3 ,
已知钾的化合价为+1,氧为-2
由正负化合价的代数和为零得
(+1)+X+(-2)×3=0
X=+5
氮元素的“全家福”
NO
NO2
N2
HNO3
N2O
N2O3
NH3
1.
2.
3.
4.
5.
6.
7.
列队:按氮元素化合价从低到高排列
2.成语“饮鸩止渴”原指喝毒酒解渴,用于比喻采取极有害的方法解决眼前困难,不顾严重后果。“鸩”是指放了砒霜的毒酒。砒霜是三氧化二砷(As2O3)的俗称,有剧毒。As2O3中As的化合价为( )
A.-3 B.-2 C.+2 D.+3
3.LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠,已知P的化合价为+5价,则LiFePO4中Fe的化合价为 ( )
A.+1 B.+2 C.+3 D.+4
化学用语
元素符号的书写及其意义
离子符号的书写及其意义
化学式及其意义
原子(离子)结构示意图
表示粒个数
表示元素的正负化合价
一个离子所带的正负电荷值
一个分子中所含原子的个数
+
(-)
m
α
n
+
(-)
b
R
辨析下列粒子各自不同的含义
氢元素
一个氢原子
H
一个水分子
水这种物质
一个水分子由两个氢原子和一个氧原子构成
H2O
2H
两个氢原子
2H2O
两个水分子
H+
一个氢离子
H2O
-2
在水中氧元素显-2价
水由氢元素和氧元素组成
1.参照上面例子请写出下列粒子的含义:
(1)3个铁原子 .(2)一个镁离子 .(3)2个水分子 .
(4)氧化铁中铁元素显+3价 .(5)4个硫酸根 .
H2
氢气这种物质
一个氢分子
一个氢分子由两个氢原子构成
3Fe
Mg2+
2H2O
Fe2O3
+3
4SO4
2-
2.有符号①2O ②N2 ③2Cl2 ④H3PO4 ⑤2Fe3+
⑥SO42-,其中数字“2”表示的含义不同。则
“2”用来表示原子个数的是 (填序号同);
“2”用来表示离子个数的是 ;
“2”用来表示分子个数的是 ;
“2”用来表示分子构成的是 ;
“2”用来表示元素化合价的是 ;
“2”用来表示离子所带电荷的是 ;
①
⑤
③
②
-2
④
⑥
将下列符号的意义及符号中数字“2”
的意义填入表中:
符号 符号的意义 符号中”2”的意义
O2-
2O
O2
H2O
2HCl
练兵场
1.对于Fe、Fe2+、Fe3+三种微粒的判断,正确的是( )
①核电荷数相同
②核外电子数相等
③电子层结构完全相同
④质量几乎相等
⑤等质量的三种微粒所含的质子数相等
A.①④⑤ B.①③⑤
C.②③④ D.①②③④⑤
A
3.下列符号既能表示一种元素又能表示一个原子,还能表示一种单质的是 ( )
A.O2 B.Mg C.H D.N
2.下列符号中,既能表示宏观含义,也能表示微观含义的是( )
A.2H2O B. 5O C. S D. Fe 2+
B
C
4.保持氢气化学性质的最小微粒是( )
A.H2 B.H C.H+ D.H2O
A
1.用微粒的观点解释:
⑴2500L液化气能压缩在40L钢瓶中,说明
⑵丁香花开的季节可以闻到浓郁的香气,说明
⑶一滴水水中含有1.7×1021个水分子,说明
微粒间有空隙
微粒不断运动
微粒体积小
2.下列现象中不能用分子运动论解释的是( )
A.把两块表面平滑干净的铅压紧,就不容易将
它们拉开
B.在室内,同样表面积的热水比冷水蒸发得快
C.氧化汞受热分解生成汞和氧气
D.医院里充满了酒精味和药味
C
3.用原子和分子的观点解释:水通电生成氢气和氧气以及水蒸发形成水蒸气这两个变化的实质。
水是由水分子构成。水通电时,水分子分解成氢原子和氧原子,每两个氢原子结合成一个氢分子,每两个氧原子结合成一个氧分子,许多氢分子构成氢气,许多氧分子构成氧气。
水蒸发时,水分子本身没有变,只是水分子间的空隙变大,所以水变成水蒸气。
4.把充满红棕色NO2气体和无色H2的集气瓶中间的玻璃片抽走,使两瓶口密合在一起(不要振荡),可观察到左边的两瓶气体的颜色很快趋于一致(两瓶气体不反应),右边两瓶气体需要很长时间才能达到同样的效果。
NO2
NO2
H2
H2
观察、对比实验现象,你能得出的结论有:
(1)
(2)
NO2的密度比H2大
分子在不断运动
(或分子间有空隙)
如图:用盛放在烧杯中的水和酒精及一个细口瓶、一个细口容器,设计实验证明:分子间有空隙?
用哪个容器证明更好?为什么?
哪种倒法效果更好?为什么?
水入酒精
酒精入水
谢 谢!
第三单元
物质构成的奥秘复习
物质
分子
原子
离子
微观构成
元素
宏观组成
同一类原子的总称
知识网络:
构成
分解
微粒名称 定义 微粒特征 实例
构成物质的基本微粒 (微观)
分子
原子
离子
分子是保持物质化
学性质的最小微粒
原子是化学变化
中的最小微粒
带电的原子(或
原子团)叫离子
很小、运动、有空隙
很小、运动、有间隔
二氧化碳
水、氧气
铁、氖气、金刚石
氯化钠、
氧化镁
很小、运动、有空隙
基本概念_识记
元素:是具有相同核电荷数(即核内质子数)的一类原子的总称。(宏观)
元素的种类由原子中的质子数决定
离子
知识网络:
物质
分子
原子
微观构成
元素
宏观组成
同一类原子的总称
构成
分解
试从宏观和微观两个角度描述以下三种物质:
⑴二氧化硫 ⑵铜 ⑶氯化钠
1. 科学研究证明,物质是由元素组成的,由微粒构成的。请用元素或具体的微粒名称填空:
(1)汞由 组成;汞由 构成。
(2)氧气由 组成;氧气由许多
构成。
(3)水由 组成;水由许多 构成;一个水分子是由 和 构成。
(4)氯化钠由 组成,由 构成。
典型题
分子和原子之间有什么区别和联系呢
联系:分子是由原子构成的,在化学变化中,分子可以划分为原子。
区别:在化学变化中,分子可分,原子不可分。
化学变化的实质(微观):分子划分为原子,原子重新组合,构成新的分子。
水分子分解(图解)
O
H
H
O
H
H
水分子
水分子分解(图解)
O
H
H
O
H
H
O
H
H
O
H
H
水分子
氢分子
氧分子
重播
试用分子、原子的知识解释:
双氧水在二氧化锰催化作用下生成水和氧气。
2.生活中的下列现象中,是分子发生变化生成其他分子的是 ( )
A.红磷燃烧 B.花香四溢 C.水分蒸发 D.热胀冷缩
3.在电解水这一变化中,没有变化的微粒是 ( )
A.水分子 B.水原子
C.氢、氧原子 D .以上都不是
典型题
A
C
4.下图是甲烷与氧气反应的微观示意图:
请通过比较、归纳,回答下列问题(不利用相对原子质量):
(1)一个甲烷分子和一个二氧化碳分子的不同点是 ;
(2)氧分子、二氧化碳分子、水分子的相同点是 ;
(3)根据上述示意图,请从微观角度描述你获得的关于
化学变化的一个信息
。
典型题
原子
原子核
核外电子(-)
质子(+)
中子(不带电)
原子序数 = 核电荷数 = 质子数 = 核外电子数
原 子 的 质 量 主 要 集 中 在 原 子 核 上
5.在同一原子中一定相同的是 ( )
A.中子数和电子数 B.中子数和质子数
C.质子数和电子数 D.核电荷数和中子数
6.某些花岗岩石材中含有放射性的元素氡。氡原子的质子数为86,中子数为136,则氡原子的核外电子数为 ( )
A.50 B.86 C.136 D.222
典型题
C
B
1.国际上统一规定,以一种碳原子质量的1/12 (约1.66× 10-27 kg)作为标准,其它原子的质量跟它比较所得的值,就是这种原子的相对原子质量
相对原子质量
某原子的相对原子质量
=
该原子一个原子的实际质量
一种碳原子的质量 ×1 /12
=
质子数 + 中子数
3.相对原子质量
2.计算式:
4.相对原子质量的单位为1
5.相对原子质量与原子的实际质量成正比关系
1.观察下表:
原子种类 质子数 中子数 核外电子数 相对原子质量
氢(H) 1 0 1 1
氮(N) 7 7 7 14
氧(O) 8 8 8 16
铁(Fe) 26 30 26 56
铀(U) 92 143 92 235
通过此表,可以总结出的规律有:
(1) ;(2) ;
(3) ;(4) 。
典型题
2.1991年我国著名化学家张青莲教授与另一位化学家合作测定了铟(In)元素的相对原子质量新值。铟元素的核电荷数为49,相对原子质量为115。则铟的中子数为( )
A.115 B.49 C.66 D.164 2.
3.已知一个含有6个质子和6个中子的碳原子质量为Ag。若某原子的一个原子的实际质量为Bg,则该原子的质量为( )
A.12B/A B.B/12A
C.AB/12 D.12/AB
A
C
4.已知一个铁的相对原子质量为A,一个标准碳原子质量为bkg,则铁原子的质量为 。
练兵场
议一议:
在化学发展史上,道尔顿提出的近代原子学说对化学的发展起着十分重要的作用,因而拥有“原子之父”的美誉。在他的学说中有下述三个主要论点:①原子是不能再分的粒子;②质子数相同的原子的各种性质和质量都相同;③原子是微小的实心球体。从现代的观点看,你认为这三点中不确切的是哪几点,并说明理由。
原子结构示意图
电子层
电子层上
电子数
核电荷数
原子核
元素种类 最外层电子数 元素的化学性质
稀有气体
8个(He为2个)
比较稳定
元素的种类 最外层电子数 元素的化学性质
金 属
一般少于4个
易失电子
元素种类 最外层电子数 元素的化学性质
非金属
一般大于或等于4个
易得电子
原 子
离 子
元素的化学性质由最外层电子数决定
离子的形成:
阳离子( + )
原子
阴离子( - )
得电子
失电子
请结合此图讨论:由原子变成离子哪些一定改变,哪些可能改变,哪些一定不变。
原子与离子的区别与联系
原子是不稳定结构而离子是稳定结构
1、概念上:
2、电性上:
3、结构上:
区别
联系:
原子是化学变化中的最小微粒而离子是带电的原子或原子团
原子不带电而离子带电
原子
失电子
得电子
阳离子
失电子
得电子
阴离子
原子中: 核电荷数 质子数 核外电子数
阳离子: 核电荷数 质子数 核外电子数
阴离子: 核电荷数 质子数 核外电子数
=
=
=
=
>
<
1.下图是元素周期表中硫元素及其原子结构示意图,下列做法错误的是( )
A.硫的相对原子质量为16
B.硫属于非金属元素
C.硫原子在化学反应中容易得到电子
D.硫原子核内有16个质子
典型题
A
2.怎么看原子结构图和离子结构图
下面A、B、C、D四幅图,你知道那幅图是原子结构图,那幅是离子结构图吗?
属于原子的是 ,依据是 。
属于离子的是 ,依据是 ;
其中属于阳离子的是 ,因为: 。
其中属于阴离子的是 ,因为: 。
A、C
B、D
质子数=电子数
质子数≠电子数
D
B
质子数>电子数
质子数<电子数
3.根据下列原子或离子结构示意图填空。
(1)电子层排布相同的是 。
(2)属于同种元素的是 。
(3)属于金属元素的是 。
(4)属于稀有气体元素的是 。
(5)属于阴离子的是 ,
其离子符号是 。
B、C
A、B
D
C
B
F-
化学元素
元
素
元素:
现在已发现的元素有100多种,大部分为金属元素
元素符号:
拉丁文(第一字母大写,第二字母小写)
元素符号的含义:
一种元素;这种元素的一个原子
元素是同具有相同核电荷数的同一类原子的总称
元素的存在:
地壳中:
氧、硅、铝、铁、钙
人体中:
氧;碳、氢、氮
太阳上:
氢;氦
空气中:
氮、氧
元素与
人体健康
缺钙:骨质疏松 ;缺铁钴:贫血 ;
缺锌:智力低下 ;缺碘:甲亢 。
海水中:
氧、氢
元素分类:
金属元素:铁、镁、铝、钠、钾、铜、锰、锌、银、钡、汞、金等
非金属元素:氧、氢、氮、氯、碳、硫、磷、硅、碘等
稀有气体元素:氦、氖、氩等
在空格中填写适当的元素符号。
地壳中含量最多的非金属元素是 ,其次是 ;地壳中含量最多的金属元素是 ,其次是 ;地球大气里含量最多的元素是 ;人体里含量最多的元素是 ;海洋里含量最多的元素是 ;太阳中含量最多的元素是 ;地核中含量最多的元素是 ;人体缺少 元素,容易得贫血症;小儿体内缺少 元素,容易得佝偻病;缺 会导致儿童发育迟缓,智力低下;人体缺 元素会引起龋齿,但它含量过高,又会使牙齿釉质受损。
O
Si
Al
Fe
N
O
O
Fe
Fe
Ca
Zn
F
H
元素分布
练习:
1.氧化镁和氧气中都存在着______元素。
2.一种元素与另一种元素的本区别是( )
A.原子量 B.中子数
C.质子数 D.电子数
3.二氧化硫、氧化汞、氧气中都含有( )
A.氧气 B.氧原子
C.氧分子 D.氧元素
4.某药品说明书中标明:本品每克含碘150mg、镁65mg、锌1.5mg、铜2mg、锰1mg,这里所标的各成分是指 ( )
A.分子 B.原子 C.元素 D.无法确定
C
D
C
5.元素周期表是学习和研究化学的重要工具,它的内容非常丰富。你认为从元素周期表中不能直接获得的信息是( )
A.元素在自然界中的分布
B.元素性质的变化规律
C.元素符号
D.元素的原子序数
6.下列各组物质按单质、化合物、混合物顺序排列的是( )
A.氧气、水、白酒
B.天然气、煤、石油
C.水银、烧碱、纯碱
D.干冰、C60、酒精
物质
按物质
种类分
按元素
种类分
混合物
(不同种物质组成)
纯净物
(同种物质组成)
单质
(同种元素组成)
化合物
(不同种元素组成)
按性质分
金属(如Fe、Cu等)
非金属(如C、O2等)
稀有气体(如He、Ne等)
按组成和
性质分
氧化物(如H2O等)
其他
(如空气、海水、澄清石灰水、石灰石等)
物质分类
链接主页四
2.有下列两组物质,每组中均有一种与其他物质所属类别不同,氢在下面的横线上填写出这种物质的名称:
(1)食醋、牛奶、加碘盐、蔗糖
(2)氧化镁、水、碳酸钙、五氧化二磷
(1) (2)
1.家庭日常生活中经常用到的下列物质中,属于纯净物的是( )
A.餐饮用的可口可乐 B.调味用的加碘食盐
C.炒菜用的铁过 D.降温用的冰水共存物
D
蔗糖
碳酸钙
4.一瓶气体经化验只由一种元素组成,则该气体是( )
A.一种单质 B.一种化合物
C.一种纯净物
D.可能是一种单质,也可能是几种单质组成的
混合物
D
3.下列各组物质中,前者是单质,后者是氧化物的是( )
A.石灰石 冰 B.金刚石 干冰
C.液氧 氯酸钾 D.水银 碘酒
B
构成六种物质的微粒如图所示
(大圆表示氧原子,小圆表示氢原子)
2.C和D表示的物质有什么区别
它们是同种物质吗
1.哪些密闭容器中表示混合物
8.有六种物质能按下列顺序排列:①CO ②H2O ③NH3 ④X ⑤C2H4 ⑥P2O5 。根据它们的组成和排列的规律,X可能是 。请解释你选择该答案的原因: 。
A.NaNO3 B.CH4 C.Fe2O3 D.PCl5
化学式 化合价
判断
书写
化合价与化学式的关系
(1)知式标价:
例1:标出下列物质中各元素的化合价
氯化锌 金属锌 氢氧化钠
ZnCl2
+2 -1
Zn
0
NaOH
+1 -2 +1
(2)知式求价:
例2: 试确定氯酸钾中氯元素的化合价
解:设氯元素的化合价为X
先写出氯酸钾的化学式:KClO3 ,
已知钾的化合价为+1,氧为-2
由正负化合价的代数和为零得
(+1)+X+(-2)×3=0
X=+5
氮元素的“全家福”
NO
NO2
N2
HNO3
N2O
N2O3
NH3
1.
2.
3.
4.
5.
6.
7.
列队:按氮元素化合价从低到高排列
2.成语“饮鸩止渴”原指喝毒酒解渴,用于比喻采取极有害的方法解决眼前困难,不顾严重后果。“鸩”是指放了砒霜的毒酒。砒霜是三氧化二砷(As2O3)的俗称,有剧毒。As2O3中As的化合价为( )
A.-3 B.-2 C.+2 D.+3
3.LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠,已知P的化合价为+5价,则LiFePO4中Fe的化合价为 ( )
A.+1 B.+2 C.+3 D.+4
化学用语
元素符号的书写及其意义
离子符号的书写及其意义
化学式及其意义
原子(离子)结构示意图
表示粒个数
表示元素的正负化合价
一个离子所带的正负电荷值
一个分子中所含原子的个数
+
(-)
m
α
n
+
(-)
b
R
辨析下列粒子各自不同的含义
氢元素
一个氢原子
H
一个水分子
水这种物质
一个水分子由两个氢原子和一个氧原子构成
H2O
2H
两个氢原子
2H2O
两个水分子
H+
一个氢离子
H2O
-2
在水中氧元素显-2价
水由氢元素和氧元素组成
1.参照上面例子请写出下列粒子的含义:
(1)3个铁原子 .(2)一个镁离子 .(3)2个水分子 .
(4)氧化铁中铁元素显+3价 .(5)4个硫酸根 .
H2
氢气这种物质
一个氢分子
一个氢分子由两个氢原子构成
3Fe
Mg2+
2H2O
Fe2O3
+3
4SO4
2-
2.有符号①2O ②N2 ③2Cl2 ④H3PO4 ⑤2Fe3+
⑥SO42-,其中数字“2”表示的含义不同。则
“2”用来表示原子个数的是 (填序号同);
“2”用来表示离子个数的是 ;
“2”用来表示分子个数的是 ;
“2”用来表示分子构成的是 ;
“2”用来表示元素化合价的是 ;
“2”用来表示离子所带电荷的是 ;
①
⑤
③
②
-2
④
⑥
将下列符号的意义及符号中数字“2”
的意义填入表中:
符号 符号的意义 符号中”2”的意义
O2-
2O
O2
H2O
2HCl
练兵场
1.对于Fe、Fe2+、Fe3+三种微粒的判断,正确的是( )
①核电荷数相同
②核外电子数相等
③电子层结构完全相同
④质量几乎相等
⑤等质量的三种微粒所含的质子数相等
A.①④⑤ B.①③⑤
C.②③④ D.①②③④⑤
A
3.下列符号既能表示一种元素又能表示一个原子,还能表示一种单质的是 ( )
A.O2 B.Mg C.H D.N
2.下列符号中,既能表示宏观含义,也能表示微观含义的是( )
A.2H2O B. 5O C. S D. Fe 2+
B
C
4.保持氢气化学性质的最小微粒是( )
A.H2 B.H C.H+ D.H2O
A
1.用微粒的观点解释:
⑴2500L液化气能压缩在40L钢瓶中,说明
⑵丁香花开的季节可以闻到浓郁的香气,说明
⑶一滴水水中含有1.7×1021个水分子,说明
微粒间有空隙
微粒不断运动
微粒体积小
2.下列现象中不能用分子运动论解释的是( )
A.把两块表面平滑干净的铅压紧,就不容易将
它们拉开
B.在室内,同样表面积的热水比冷水蒸发得快
C.氧化汞受热分解生成汞和氧气
D.医院里充满了酒精味和药味
C
3.用原子和分子的观点解释:水通电生成氢气和氧气以及水蒸发形成水蒸气这两个变化的实质。
水是由水分子构成。水通电时,水分子分解成氢原子和氧原子,每两个氢原子结合成一个氢分子,每两个氧原子结合成一个氧分子,许多氢分子构成氢气,许多氧分子构成氧气。
水蒸发时,水分子本身没有变,只是水分子间的空隙变大,所以水变成水蒸气。
4.把充满红棕色NO2气体和无色H2的集气瓶中间的玻璃片抽走,使两瓶口密合在一起(不要振荡),可观察到左边的两瓶气体的颜色很快趋于一致(两瓶气体不反应),右边两瓶气体需要很长时间才能达到同样的效果。
NO2
NO2
H2
H2
观察、对比实验现象,你能得出的结论有:
(1)
(2)
NO2的密度比H2大
分子在不断运动
(或分子间有空隙)
如图:用盛放在烧杯中的水和酒精及一个细口瓶、一个细口容器,设计实验证明:分子间有空隙?
用哪个容器证明更好?为什么?
哪种倒法效果更好?为什么?
水入酒精
酒精入水
谢 谢!
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
