高中化学人教版(2019)必修第二册7.3.2.乙酸的性质(共36张ppt)
文档属性
| 名称 | 高中化学人教版(2019)必修第二册7.3.2.乙酸的性质(共36张ppt) |
|
|
| 格式 | zip | ||
| 文件大小 | 3.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-25 00:00:00 | ||
图片预览









文档简介
(共36张PPT)
猜一猜?
调味品
醒酒
有机物
酸
美容
食醋
醋的来历?
传说古代山西省有个酿酒高手叫杜康。他儿子黑塔跟父亲也学会了酿酒技术。后来,从山西迁到镇江。黑塔觉得酿酒后把酒糟扔掉可惜,就把酒糟浸泡在水缸里。到了第二十一日的酉时,一开缸,一股浓郁的香气扑鼻而来。黑塔忍不住尝了一口,酸酸的,味道很美。烧菜时放了一些,味道特别鲜美,便贮藏着作为“调味酱”。这“调味酱”就是今天的醋。
酉
一
日
廿
用醋蒸汽熏蒸居室能杀菌和消毒,防止感冒和传染病;
煮排骨或烧鱼时加点醋,食物更鲜美;
鱼骨梗喉,吞食几口醋,可使鱼骨酥软顺利咽下;
醋还有降血压、防止动脉硬化和治疗冠心病的效果。
日常生活离不开醋???
食醋的用途,举不胜举,那么食醋中是什么物质在起作用呢?它有着怎样的结构和性质呢?
第三节
生活中两种常见的有机物
第2课时 乙酸
高一化学人教版必修2 第三章有机化合物
学科教学(化学) 吴向娟
你有进过厨房吗?你知道厨房中的醋是什么味吗?
通过已有经验,阅读课本总结乙酸的物理性质。
一、乙酸的物理性质
颜色、状态
气 味
沸 点
熔 点
溶解性
无色液体
有强烈刺激性气味(可消毒)
16.6℃ (无水乙酸又称为冰醋酸)
易溶于水、乙醇等溶剂
117.9℃ (易挥发)
乙酸俗称醋酸,纯净的乙酸又称冰醋酸;食醋中含乙酸3%~ 5%
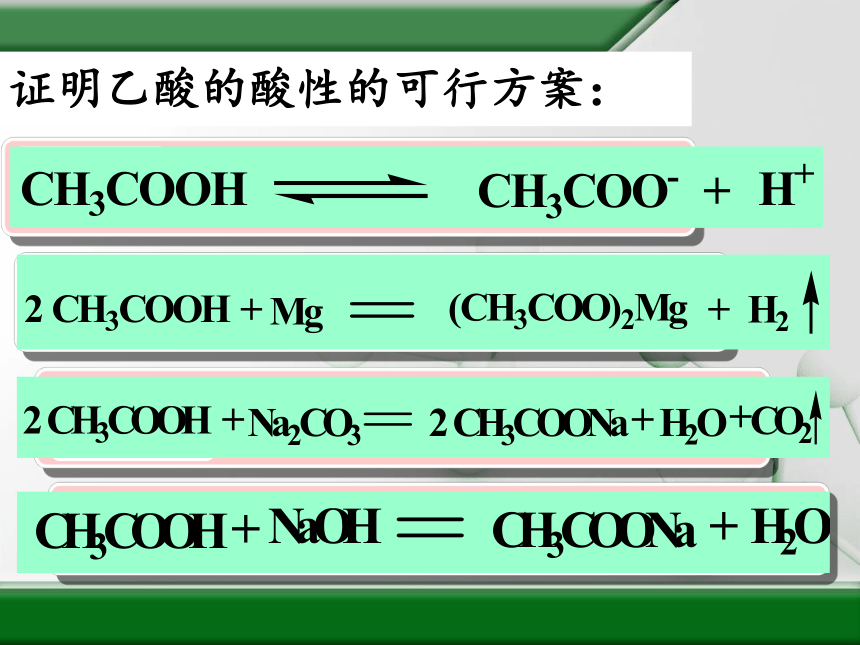
二、乙酸的分子结构
请看乙酸的比例模型和球棍模型,写出乙酸的分子式、结构式、结构简式,指出乙酸的官能团。
球棍模型
比例模型
分子式:
结构式:
结构简式 :
甲基
二、乙酸的分子结构
C2H4O2
或 CH3COOH
羧基
羧基(官能团):
—C—OH(或—COOH)
O
【思考与交流】
日常生活中,常用醋除去水垢(成分:Mg(OH)2和CaCO3), 说明乙酸具有什么性质?
酸的通性:
A、使紫色石蕊试液变红色
B、与活泼金属生成H2
C、与碱生成盐和水
D、与碱性氧化物生成盐和水
E、与某些盐反应生成新酸和新盐
活动·探究
根据下列药品设计实验方案证明乙酸具有酸性.
药品:镁粉、NaOH溶液、Na2CO3粉末、
乙酸溶液、酚酞、石蕊
证明乙酸的酸性的可行方案:
方案一: 往乙酸溶液中加石蕊
方案二:将镁条插入乙酸溶液
方案三: 往Na2CO3粉未中加入乙酸溶液
方案四: 向滴有酚酞的NaOH溶液中滴加乙酸溶液
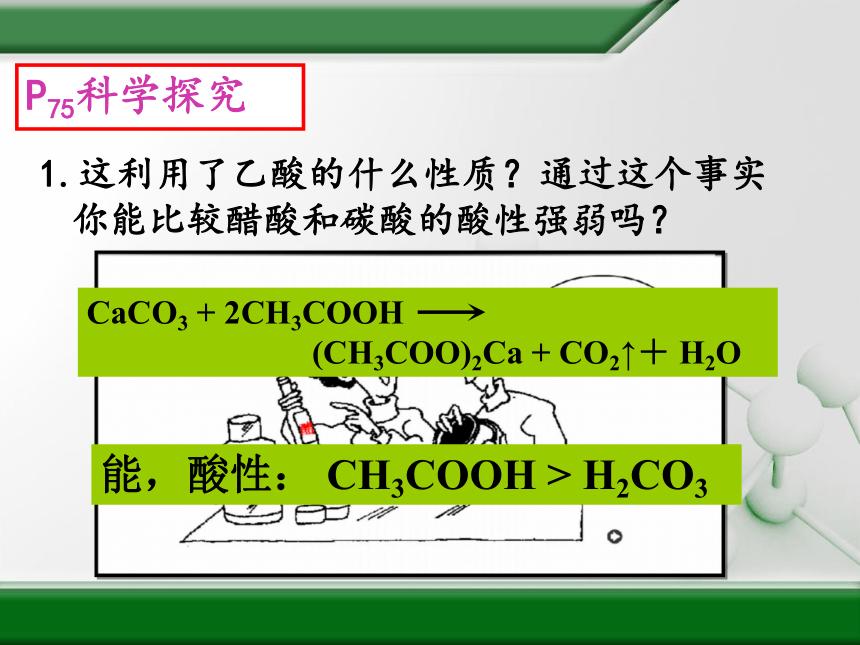
P75科学探究
1.这利用了乙酸的什么性质?通过这个事实你能比较醋酸和碳酸的酸性强弱吗?
CaCO3 + 2CH3COOH
(CH3COO)2Ca + CO2↑+ H2O
能,酸性: CH3COOH > H2CO3
2.如何设计实验比较酸性强弱:CH3COOH、H2CO3
实验方案:
1.向一试管中加入碳酸钠粉末。
2.向试管中加入醋酸,观察现象。
现象:有大量气泡产生
结论:酸性 CH3COOH>H2CO3
三、乙酸的化学性质
1.弱酸性:
CH3COOH
CH3COO-+H+
使紫色石蕊溶液变红,酚酞不变色
Mg + 2CH3COOH (CH3COO)2Mg + H2↑
NaOH+ CH3COOH CH3COONa + H2O
Na2CO3 + 2CH3COOH
2CH3COONa + CO2↑+ H2O
漫画
漫画
漫画
2.乙酸的酯化反应
三、乙酸的化学性质
碎瓷片
3mL乙醇
2mL浓硫酸
2mL乙酸
饱和的Na2CO3溶液
现象: 1、碳酸钠液面上有无色透明油状液体 ;
2、可闻到香味.
视频
实验室制备乙酸乙酯应注意那些问题?
1.试剂的加入顺序?
先加入乙醇,然后边震荡试管边慢慢加入浓硫酸,最后加入乙酸
2.导管末端为什么不能插入饱和Na2CO3溶液中?
防止加热不均,使溶液倒吸
3.浓硫酸的作用是什么?
催化剂(提高化学反应速率)和吸水剂(提高乙醇、乙酸的转化率)
4.试管倾斜加热的目的是什么
增大受热面积、有利于酯逸出
5.长导管的作用是什么?
冷凝回流和导气
6.碎瓷片的作用是什么?
防止暴沸
7.饱和Na2CO3溶液的作用是什么?
A、中和乙酸,吸收乙醇,便于闻到乙酸乙酯的味道
B、降低酯的溶解度,增大溶液的密度,便于分层
8.酯的分离方法是什么?
酯难溶于水或饱和无机盐溶液,比水的密小,用分液漏斗分液取上层即可。
酯化反应
CH3COOH + HOCH2CH3 CH3COOCH2CH3 + H2O
浓H2SO4
△
乙酸 乙醇 乙酸乙酯
酯化反应的概念:
酸和醇反应生成酯和水的反应。
可逆反应
探究:乙酸和乙醇是如何反应生成酯和水的呢?
反应类型:
取代反应
回看漫画
探究酯化反应可能的脱水方式
可能一
可能二
同位素示踪法:
----研究有机反应机理常用的方法
微观演示:
微观演示:
酯化反应的断键方式:
酸脱羟基、醇脱氢。
课堂练习
写出乙酸与甲醇、甲酸与乙醇反应的化学方程式:
甲酸乙酯
乙酸甲酯
酯化反应的实质:酸脱羟基、醇脱氢。
为什么呢?
“酒是陈的香”
厨师烧鱼时常加醋并加点酒,这样鱼的味道就变得无腥、香醇,特别鲜美。
为什么呢?
生活小帮手无“醋” 不在
食醋可以洗饰品
上的铁锈铜锈
擦鞋加几滴醋更加光亮
生活小帮手无“醋” 不在
洗毛衣加几滴
醋会焕然一新
用醋漱口可防感冒
乙酸是重要的化工原料
乙酸可以生产农药
乙酸可以生产涂料
喷漆溶剂
香料
医药
农药
染料
乙酸
有机化工原料
醋酸纤维
合成纤维
四、乙酸的用途
课堂练习:
1.下列物质中,能与醋酸发生反应的是( )
①乙醇 ②金属铝 ③甲烷④碳酸钙 ⑤氢氧化钠
⑥ 氧化镁
A.①③④⑤⑥ B.②③④⑤
C. ①②④⑤⑥ D.全部
C
课堂练习:
2.下列关于乙酸性质的叙述中,错误的是 ( )
A.乙酸的酸性比碳酸强,所以它可以跟碳酸盐溶液
反应,生成CO2气体
B.乙酸能跟钠反应放出H2且比乙醇与钠的反应剧烈
C.乙酸与乙醇的反应是中和反应
D.乙酸在温度低于16.6℃时,就凝结成冰状晶体
C
课堂练习:
3.用乙酸和含有18O的乙醇发生酯化反应,关于
18O的存在正确的是( )
A. CH3CH218OOCCH3
B. H218O
C. CH3CH2O18OCCH3
D. 以上都不对
A
O
CH3—C—O—H
酸性
酯化
官能团
结构决定性质
官能团的结构
决定
物质的化学性质
课堂小结:
1、写出 HCOOH 与 CH3CH2CH2OH 在浓硫酸
催化下的酯化反应方程式。
2、课本课后习题及练习册相应练习。
课后作业:
猜一猜?
调味品
醒酒
有机物
酸
美容
食醋
醋的来历?
传说古代山西省有个酿酒高手叫杜康。他儿子黑塔跟父亲也学会了酿酒技术。后来,从山西迁到镇江。黑塔觉得酿酒后把酒糟扔掉可惜,就把酒糟浸泡在水缸里。到了第二十一日的酉时,一开缸,一股浓郁的香气扑鼻而来。黑塔忍不住尝了一口,酸酸的,味道很美。烧菜时放了一些,味道特别鲜美,便贮藏着作为“调味酱”。这“调味酱”就是今天的醋。
酉
一
日
廿
用醋蒸汽熏蒸居室能杀菌和消毒,防止感冒和传染病;
煮排骨或烧鱼时加点醋,食物更鲜美;
鱼骨梗喉,吞食几口醋,可使鱼骨酥软顺利咽下;
醋还有降血压、防止动脉硬化和治疗冠心病的效果。
日常生活离不开醋???
食醋的用途,举不胜举,那么食醋中是什么物质在起作用呢?它有着怎样的结构和性质呢?
第三节
生活中两种常见的有机物
第2课时 乙酸
高一化学人教版必修2 第三章有机化合物
学科教学(化学) 吴向娟
你有进过厨房吗?你知道厨房中的醋是什么味吗?
通过已有经验,阅读课本总结乙酸的物理性质。
一、乙酸的物理性质
颜色、状态
气 味
沸 点
熔 点
溶解性
无色液体
有强烈刺激性气味(可消毒)
16.6℃ (无水乙酸又称为冰醋酸)
易溶于水、乙醇等溶剂
117.9℃ (易挥发)
乙酸俗称醋酸,纯净的乙酸又称冰醋酸;食醋中含乙酸3%~ 5%
二、乙酸的分子结构
请看乙酸的比例模型和球棍模型,写出乙酸的分子式、结构式、结构简式,指出乙酸的官能团。
球棍模型
比例模型
分子式:
结构式:
结构简式 :
甲基
二、乙酸的分子结构
C2H4O2
或 CH3COOH
羧基
羧基(官能团):
—C—OH(或—COOH)
O
【思考与交流】
日常生活中,常用醋除去水垢(成分:Mg(OH)2和CaCO3), 说明乙酸具有什么性质?
酸的通性:
A、使紫色石蕊试液变红色
B、与活泼金属生成H2
C、与碱生成盐和水
D、与碱性氧化物生成盐和水
E、与某些盐反应生成新酸和新盐
活动·探究
根据下列药品设计实验方案证明乙酸具有酸性.
药品:镁粉、NaOH溶液、Na2CO3粉末、
乙酸溶液、酚酞、石蕊
证明乙酸的酸性的可行方案:
方案一: 往乙酸溶液中加石蕊
方案二:将镁条插入乙酸溶液
方案三: 往Na2CO3粉未中加入乙酸溶液
方案四: 向滴有酚酞的NaOH溶液中滴加乙酸溶液
P75科学探究
1.这利用了乙酸的什么性质?通过这个事实你能比较醋酸和碳酸的酸性强弱吗?
CaCO3 + 2CH3COOH
(CH3COO)2Ca + CO2↑+ H2O
能,酸性: CH3COOH > H2CO3
2.如何设计实验比较酸性强弱:CH3COOH、H2CO3
实验方案:
1.向一试管中加入碳酸钠粉末。
2.向试管中加入醋酸,观察现象。
现象:有大量气泡产生
结论:酸性 CH3COOH>H2CO3
三、乙酸的化学性质
1.弱酸性:
CH3COOH
CH3COO-+H+
使紫色石蕊溶液变红,酚酞不变色
Mg + 2CH3COOH (CH3COO)2Mg + H2↑
NaOH+ CH3COOH CH3COONa + H2O
Na2CO3 + 2CH3COOH
2CH3COONa + CO2↑+ H2O
漫画
漫画
漫画
2.乙酸的酯化反应
三、乙酸的化学性质
碎瓷片
3mL乙醇
2mL浓硫酸
2mL乙酸
饱和的Na2CO3溶液
现象: 1、碳酸钠液面上有无色透明油状液体 ;
2、可闻到香味.
视频
实验室制备乙酸乙酯应注意那些问题?
1.试剂的加入顺序?
先加入乙醇,然后边震荡试管边慢慢加入浓硫酸,最后加入乙酸
2.导管末端为什么不能插入饱和Na2CO3溶液中?
防止加热不均,使溶液倒吸
3.浓硫酸的作用是什么?
催化剂(提高化学反应速率)和吸水剂(提高乙醇、乙酸的转化率)
4.试管倾斜加热的目的是什么
增大受热面积、有利于酯逸出
5.长导管的作用是什么?
冷凝回流和导气
6.碎瓷片的作用是什么?
防止暴沸
7.饱和Na2CO3溶液的作用是什么?
A、中和乙酸,吸收乙醇,便于闻到乙酸乙酯的味道
B、降低酯的溶解度,增大溶液的密度,便于分层
8.酯的分离方法是什么?
酯难溶于水或饱和无机盐溶液,比水的密小,用分液漏斗分液取上层即可。
酯化反应
CH3COOH + HOCH2CH3 CH3COOCH2CH3 + H2O
浓H2SO4
△
乙酸 乙醇 乙酸乙酯
酯化反应的概念:
酸和醇反应生成酯和水的反应。
可逆反应
探究:乙酸和乙醇是如何反应生成酯和水的呢?
反应类型:
取代反应
回看漫画
探究酯化反应可能的脱水方式
可能一
可能二
同位素示踪法:
----研究有机反应机理常用的方法
微观演示:
微观演示:
酯化反应的断键方式:
酸脱羟基、醇脱氢。
课堂练习
写出乙酸与甲醇、甲酸与乙醇反应的化学方程式:
甲酸乙酯
乙酸甲酯
酯化反应的实质:酸脱羟基、醇脱氢。
为什么呢?
“酒是陈的香”
厨师烧鱼时常加醋并加点酒,这样鱼的味道就变得无腥、香醇,特别鲜美。
为什么呢?
生活小帮手无“醋” 不在
食醋可以洗饰品
上的铁锈铜锈
擦鞋加几滴醋更加光亮
生活小帮手无“醋” 不在
洗毛衣加几滴
醋会焕然一新
用醋漱口可防感冒
乙酸是重要的化工原料
乙酸可以生产农药
乙酸可以生产涂料
喷漆溶剂
香料
医药
农药
染料
乙酸
有机化工原料
醋酸纤维
合成纤维
四、乙酸的用途
课堂练习:
1.下列物质中,能与醋酸发生反应的是( )
①乙醇 ②金属铝 ③甲烷④碳酸钙 ⑤氢氧化钠
⑥ 氧化镁
A.①③④⑤⑥ B.②③④⑤
C. ①②④⑤⑥ D.全部
C
课堂练习:
2.下列关于乙酸性质的叙述中,错误的是 ( )
A.乙酸的酸性比碳酸强,所以它可以跟碳酸盐溶液
反应,生成CO2气体
B.乙酸能跟钠反应放出H2且比乙醇与钠的反应剧烈
C.乙酸与乙醇的反应是中和反应
D.乙酸在温度低于16.6℃时,就凝结成冰状晶体
C
课堂练习:
3.用乙酸和含有18O的乙醇发生酯化反应,关于
18O的存在正确的是( )
A. CH3CH218OOCCH3
B. H218O
C. CH3CH2O18OCCH3
D. 以上都不对
A
O
CH3—C—O—H
酸性
酯化
官能团
结构决定性质
官能团的结构
决定
物质的化学性质
课堂小结:
1、写出 HCOOH 与 CH3CH2CH2OH 在浓硫酸
催化下的酯化反应方程式。
2、课本课后习题及练习册相应练习。
课后作业:
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
