【考点精讲】人教版化学九年级上册 6.1金刚石、石墨 和C60 同步学案
文档属性
| 名称 | 【考点精讲】人教版化学九年级上册 6.1金刚石、石墨 和C60 同步学案 |

|
|
| 格式 | doc | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-26 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
第六单元课题1 金刚石、石墨和C60
思维导图
二、考点精讲
考点一:碳单质的物理性质和用途
【精讲1】比较金刚石和石墨,下列说法中正确的是( )
A.都可以用作电极 B.都由碳元素组成
C.都能切割大理石 D.都是无色透明固体
【答案】B
【解析】A、金刚石没有导电性,不能用作电极,故A错误;B、金刚石和石墨都是由碳元素组成的,故B正确;C、石墨质软,不能用于切割大理石;金刚石是天然存在的硬度最大物质,可用于切割大理石,故C错误;D、石墨是灰黑色的固体,不透明,故D错误。故选:B。
【精讲2】认真阅读下列材料,回答有关问题。
举世瞩目的北京冬奥会既是体育盛会,也是科技盛会。冬奥会颁奖礼仪服装,不仅外观典雅大方,而且衣服内胆中添加了一块能够发热的“布”——石墨烯发热材料。这一新材料在通电时,碳分子团之间相互摩擦、碰撞而产生热能,热能通过远红外线以平面方式均匀地辐射出来,被入体接收,产生一种由内而外的温暖。
(1)石墨烯由 元素组成,属于 (填“化合物”或“单质”)。
(2)从上述材料中可得出石墨烯具有的物理性质有 性(写一点)。
【答案】碳;单质;导热
【解析】(1)石墨烯是由碳元素组成的纯净物,属于单质;
(2)从上述材料中可得出石墨烯具有的物理性质有导热性;
【跟踪练1】活性炭口罩具有防毒、除臭、滤菌、阻尘等功效,其中除臭是利用了活性炭的( )
A.导电性 B.导热性 C.滑腻感 D.吸附性
【答案】D
【解析】活性炭具有疏松多孔的结构,具有吸附性,因此可用活性炭来吸附色素和异味,可除臭。故选:D。
【跟踪练2】12.金刚石、石墨、石墨烯组成元素相同,有关说法不正确的是( )
A.金刚石是天然存在的最硬物质
B.石墨可用于制作电极
C.每个C60由60个碳原子构成
D.石墨烯属于化合物
【答案】D
【解析】A、金刚石是天然存在的最硬物质,故A正确;B、石墨具有优良的导电性,可用于制作电极,故B正确;C、由化学式可知,每个C60由60个碳原子构成,故C正确;D、石墨烯是由碳元素组成的纯净物,属于单质,故D错误。故选:D。
考点二: 单质碳的化学性质
【精讲1】在2Fe2O3+3C4Fe+3CO2↑反应中,还原剂是( )
A.C B.CO2 C.Fe2O3 D.Fe
【答案】A
【解析】由反应的化学方程式2Fe2O3+3C4Fe+3CO2↑可知,氧化铁失去氧生成铁发生了还原反应,是氧化剂;碳得到氧生成二氧化碳发生了氧化反应,是还原剂。故选:A。
【精讲2】如图是木炭还原氧化铜的装置图,回答下列问题。
(1)写出该装置图中用于固定的仪器名称 。
(2)酒精灯加网罩的目的 。
(3)加热一会后观察到右边试管中产生的现象是 。
(4)左边试管内发生反应的化学方程式为 。
(5)小明在做该实验时,一观察到黑色固体变成红色后,就立即拆开装置将红色固体倒出,发现红色固体又变成了黑色,其中的原因 。
【答案】(1)铁架台;(2)集中火焰,提高温度;(3)澄清的石灰水变浑浊;
(4)C+2CuO2Cu+CO2↑;(5)还原出的铜重新被氧化。
【解析】(1)由图示可知,装置图中用于固定的仪器名称是铁架台。
(2)酒精灯加网罩的目的集中火焰,提高温度。
(3)加热一会后,碳在高温时与氧化铜反应生成的二氧化碳能与氢氧化钙反应生成了碳酸钙和水,所以观察到右边试管中产生的现象是:澄清的石灰水变浑浊。
(4)左边试管内在高温时碳与与氧化铜反应生成了铜和二氧化碳,发生反应的化学方程式为:C+2CuO2Cu+CO2↑。
(5)由于热的铜能与氧气反应生成了氧化铜,小明在做该实验时,一观察到黑色固体变成红色后,就立即拆开装置将红色固体倒出,发现红色固体又变成了黑色,其中的原因是还原出的铜重新被氧化。
【跟踪练1】已知A、B、C、D、E五种物质均为初中化学中常见的物质,它们相互转化的关系如图所示。A、B均为黑色固体,C是造成温室效应的主要气体,D是一种紫红色固体。
回答下列问题:
(1)E的化学式是 。
(2)写出反应①的化学方程式 。
(3)还原反应中发挥还原作用的物质是还原剂,具有还原性。反应①中作还原剂的
是 (写化学式)。
(4)写出反应③的基本反应类型 。
(5)写出物质A的一条用途 。
【答案】(1)O2;(2)C+2CuO2Cu+CO2↑;(3)C;(4)化合反应;(5)炼铁;
【解析】C是造成温室效应的主要气体,所以C是二氧化碳,D是一种紫红色的金属单质,所以D是铜,如果A和B均为黑色固体,常见的黑色固体有氧化铜、木炭、二氧化锰、四氧化三铁等,A与B反应会生成二氧化碳和铜,所以A、B是氧化铜或木炭中的一种,A和E会转化成二氧化碳,所以A是木炭,E就是氧气,铜和E又会转化成,所以B就是氧化铜。
(1)E是氧气,其化学式是O2;
(2)①是碳和氧化铜的反应,该反应的方程式为:C+2CuO2Cu+CO2↑;
(3)在①的反应中,碳是还原剂,具有还原性,化学式为C;
(4)③是铜和氧气的反应,产物是氧化铜,该反应的特征是“多变一”,属于化合反应;
(5)物质A是木炭,可以用来炼铁;
【跟踪练2】如图是木炭还原氧化铜的实验示意图
(1)酒精灯上加一个金属网罩的作用是 。
(2)刚开始预热时,试管②中立即看到有气泡产生,但澄清石灰水未变浑浊,其原因是 ,继续加热一段时间,看到试管①中的现象是 ,反应的化学方程式是 ,试管②中出现 的现象,反应的化学方程式 。
(3)实验完毕后,要先 (选“A、先熄灭酒精灯”或“B、先将导管从石灰水中拿出”)。
(4)该实验得出的结论是碳在高温下具有 性。
【答案】(1)使酒精灯火焰更加集中,提高温度;
(2)刚开始排出的气体是装置内的空气;黑色粉末逐渐变红;C+2CuO2Cu+CO2↑;澄清石灰水变浑浊;Ca(OH)2+CO2═CaCO3↓+H2O;
(3)将导管从石灰水中拿出;
(4)还原。
【解析】(1)酒精灯火焰加上网罩后火焰会集中,从而提高了火焰的温度;
(2)刚开始预热时,导管口有气泡产生,但B中没有变浑浊,是因为此时排出的气体是装置内的空气;碳和氧化铜在高温的条件下生成铜和二氧化碳,继续加热一段时间,看到试管①中的现象是:黑色粉末逐渐变红,化学方程式是:C+2CuO2Cu+CO2↑;二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以试管②中出现澄清石灰水变浑浊的现象,化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;
(3)实验完毕后,要先将导管从石灰水中拿出,防止石灰水倒流,炸裂试管;
(4)该实验得出的结论是碳在高温下具有还原性。
知识梳理:
1、金刚石和石墨的物理性质及用途:
2、C60的物理性质和用途:
形似足球,几乎不导电,不导热,用于制备新材料、超导、医学及生物等领域。
3、无定性碳:木炭、活性炭、焦炭、炭黑
(1)活性炭、木炭:具有疏散多孔的结构,因此具有强烈的吸附性。木炭可用于食品、工业产品中除去色素、异味等;活性炭可用于防毒面具中除去毒气、制糖业中脱色以制白糖;
(2)焦炭用于冶铁,炭黑加到橡胶里能够增加轮胎的耐磨性。
【知识点睛】
碳单质物理性质差别的原因为碳原子的排列顺序不同。金刚石中碳原子排列呈正四面体结构,石墨中碳原子排列呈片层结构,C60中碳原子排列呈足球状结构;
关于碳单质的物理性质及用途,可以根据“结构性质用途”这个相互关系来互推巧记和理解;
书写碳元素组成的单质的名称时,一定要规范,不可写错别字。特别是,碳与炭不可弄混了.其中,“碳”是元素名称,是核电荷数(即核内质子数)为6的一类原子的总称;它用来描述元素、原子或由碳元素组成的物质的名称(但并不具体指某种物质),如碳元素、碳原子、二氧化碳、一氧化碳、碳酸钙、碳水化合
物等。而“炭”是用来专指由碳元素组成的部分单质(即没有固定形状的碳单质),主要有木炭、焦炭、活性炭、炭黑等。
【命题方向】
该考点的命题方向主要是通过创设相关问题情景或图表信息等,来考查学生对碳单质的物理性质及用途的理解和掌握情况;以及阅读、分析、推断能力和对知识的迁移能力.并且,经常将其与物质的组成和构成、碳元素组成的单质、碳单质的化学性质、金属的物理性质及其用途、吸附剂、水的净化、物质的推断和鉴别、铁的冶炼等相关知识联系起来,进行综合考查。
【解题方法点拨】
要想解答好这类题目,首先,要理解和熟记碳单质的物理性质及用途等相关知识.然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,以及自己的生活经验所得,细致地分析题意或图表信息等各种信息资源,联系起来综合分析,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可。
知识梳理:
碳的化学性质主要有三个:
1.常温时,具有稳定性。如,我国古代用墨书写或绘制的字画,虽年深日久仍不变色;就是利用了碳的这个性质;
2.点燃时,具有可燃性。它的燃烧还有两种情况:
(1)当碳在氧气或空气里充分燃烧时,生成二氧化碳,同时放出大量的热;
(2)当碳燃烧不充分的时候,生成一氧化碳,同时也放出热;
利用单质碳的可燃性,可以把碳用作燃料。
3. 高温时,具有还原性。在较高温度下碳能夺取某些含氧化合物里的氧,使其它元素被还原。
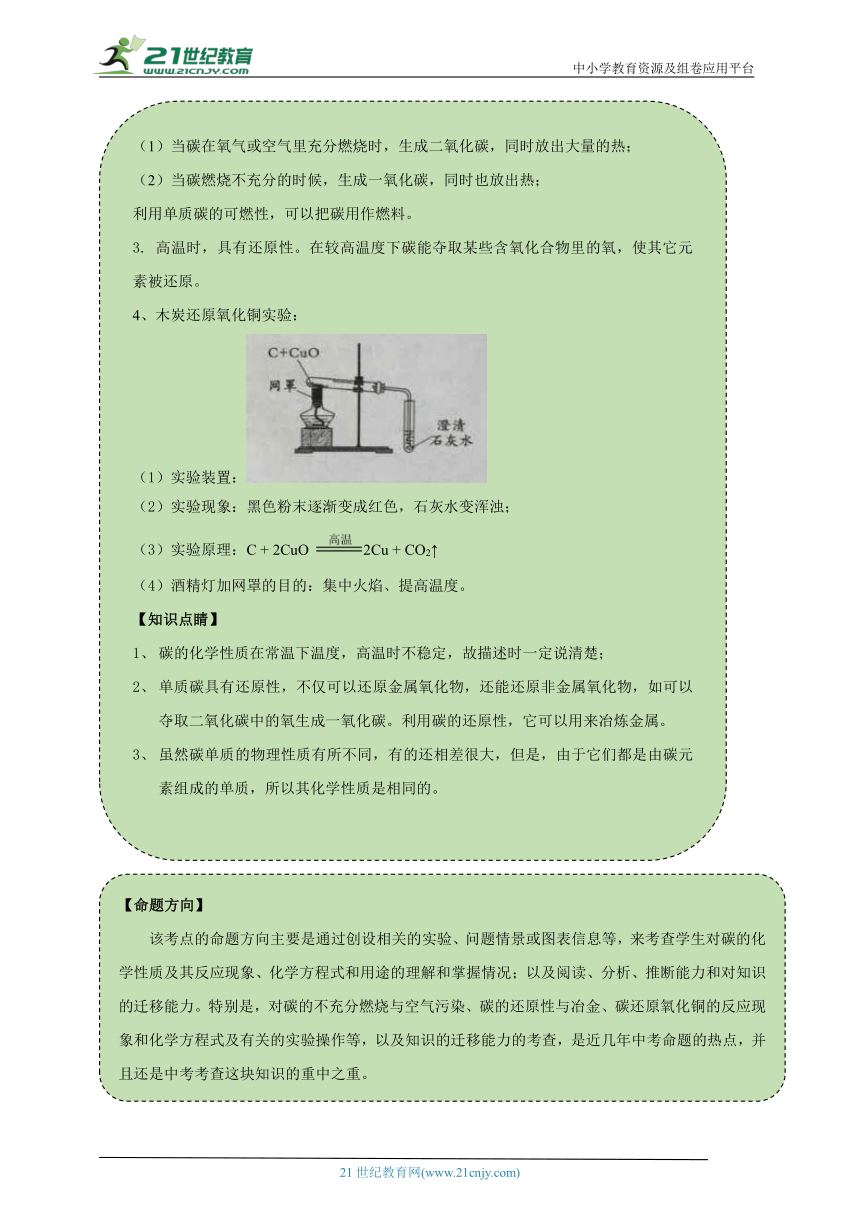
4、木炭还原氧化铜实验:
(1)实验装置:
(2)实验现象:黑色粉末逐渐变成红色,石灰水变浑浊;
(3)实验原理:C + 2CuO 2Cu + CO2↑
(4)酒精灯加网罩的目的:集中火焰、提高温度。
【知识点睛】
碳的化学性质在常温下温度,高温时不稳定,故描述时一定说清楚;
单质碳具有还原性,不仅可以还原金属氧化物,还能还原非金属氧化物,如可以夺取二氧化碳中的氧生成一氧化碳。利用碳的还原性,它可以用来冶炼金属。
虽然碳单质的物理性质有所不同,有的还相差很大,但是,由于它们都是由碳元素组成的单质,所以其化学性质是相同的。
【命题方向】
该考点的命题方向主要是通过创设相关的实验、问题情景或图表信息等,来考查学生对碳的化学性质及其反应现象、化学方程式和用途的理解和掌握情况;以及阅读、分析、推断能力和对知识的迁移能力。特别是,对碳的不充分燃烧与空气污染、碳的还原性与冶金、碳还原氧化铜的反应现象和化学方程式及有关的实验操作等,以及知识的迁移能力的考查,是近几年中考命题的热点,并且还是中考考查这块知识的重中之重。
【解题方法点拨】
要想解答好这类题目,首先,要理解和熟记碳的化学性质及其反应现象、化学方程式和用途等相关知识.然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,以及自己的生产或生活经验所得,细致地分析题意或图表信息等各种信息资源,联系起来综合分析,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
第六单元课题1 金刚石、石墨和C60
思维导图
二、考点精讲
考点一:碳单质的物理性质和用途
【精讲1】比较金刚石和石墨,下列说法中正确的是( )
A.都可以用作电极 B.都由碳元素组成
C.都能切割大理石 D.都是无色透明固体
【答案】B
【解析】A、金刚石没有导电性,不能用作电极,故A错误;B、金刚石和石墨都是由碳元素组成的,故B正确;C、石墨质软,不能用于切割大理石;金刚石是天然存在的硬度最大物质,可用于切割大理石,故C错误;D、石墨是灰黑色的固体,不透明,故D错误。故选:B。
【精讲2】认真阅读下列材料,回答有关问题。
举世瞩目的北京冬奥会既是体育盛会,也是科技盛会。冬奥会颁奖礼仪服装,不仅外观典雅大方,而且衣服内胆中添加了一块能够发热的“布”——石墨烯发热材料。这一新材料在通电时,碳分子团之间相互摩擦、碰撞而产生热能,热能通过远红外线以平面方式均匀地辐射出来,被入体接收,产生一种由内而外的温暖。
(1)石墨烯由 元素组成,属于 (填“化合物”或“单质”)。
(2)从上述材料中可得出石墨烯具有的物理性质有 性(写一点)。
【答案】碳;单质;导热
【解析】(1)石墨烯是由碳元素组成的纯净物,属于单质;
(2)从上述材料中可得出石墨烯具有的物理性质有导热性;
【跟踪练1】活性炭口罩具有防毒、除臭、滤菌、阻尘等功效,其中除臭是利用了活性炭的( )
A.导电性 B.导热性 C.滑腻感 D.吸附性
【答案】D
【解析】活性炭具有疏松多孔的结构,具有吸附性,因此可用活性炭来吸附色素和异味,可除臭。故选:D。
【跟踪练2】12.金刚石、石墨、石墨烯组成元素相同,有关说法不正确的是( )
A.金刚石是天然存在的最硬物质
B.石墨可用于制作电极
C.每个C60由60个碳原子构成
D.石墨烯属于化合物
【答案】D
【解析】A、金刚石是天然存在的最硬物质,故A正确;B、石墨具有优良的导电性,可用于制作电极,故B正确;C、由化学式可知,每个C60由60个碳原子构成,故C正确;D、石墨烯是由碳元素组成的纯净物,属于单质,故D错误。故选:D。
考点二: 单质碳的化学性质
【精讲1】在2Fe2O3+3C4Fe+3CO2↑反应中,还原剂是( )
A.C B.CO2 C.Fe2O3 D.Fe
【答案】A
【解析】由反应的化学方程式2Fe2O3+3C4Fe+3CO2↑可知,氧化铁失去氧生成铁发生了还原反应,是氧化剂;碳得到氧生成二氧化碳发生了氧化反应,是还原剂。故选:A。
【精讲2】如图是木炭还原氧化铜的装置图,回答下列问题。
(1)写出该装置图中用于固定的仪器名称 。
(2)酒精灯加网罩的目的 。
(3)加热一会后观察到右边试管中产生的现象是 。
(4)左边试管内发生反应的化学方程式为 。
(5)小明在做该实验时,一观察到黑色固体变成红色后,就立即拆开装置将红色固体倒出,发现红色固体又变成了黑色,其中的原因 。
【答案】(1)铁架台;(2)集中火焰,提高温度;(3)澄清的石灰水变浑浊;
(4)C+2CuO2Cu+CO2↑;(5)还原出的铜重新被氧化。
【解析】(1)由图示可知,装置图中用于固定的仪器名称是铁架台。
(2)酒精灯加网罩的目的集中火焰,提高温度。
(3)加热一会后,碳在高温时与氧化铜反应生成的二氧化碳能与氢氧化钙反应生成了碳酸钙和水,所以观察到右边试管中产生的现象是:澄清的石灰水变浑浊。
(4)左边试管内在高温时碳与与氧化铜反应生成了铜和二氧化碳,发生反应的化学方程式为:C+2CuO2Cu+CO2↑。
(5)由于热的铜能与氧气反应生成了氧化铜,小明在做该实验时,一观察到黑色固体变成红色后,就立即拆开装置将红色固体倒出,发现红色固体又变成了黑色,其中的原因是还原出的铜重新被氧化。
【跟踪练1】已知A、B、C、D、E五种物质均为初中化学中常见的物质,它们相互转化的关系如图所示。A、B均为黑色固体,C是造成温室效应的主要气体,D是一种紫红色固体。
回答下列问题:
(1)E的化学式是 。
(2)写出反应①的化学方程式 。
(3)还原反应中发挥还原作用的物质是还原剂,具有还原性。反应①中作还原剂的
是 (写化学式)。
(4)写出反应③的基本反应类型 。
(5)写出物质A的一条用途 。
【答案】(1)O2;(2)C+2CuO2Cu+CO2↑;(3)C;(4)化合反应;(5)炼铁;
【解析】C是造成温室效应的主要气体,所以C是二氧化碳,D是一种紫红色的金属单质,所以D是铜,如果A和B均为黑色固体,常见的黑色固体有氧化铜、木炭、二氧化锰、四氧化三铁等,A与B反应会生成二氧化碳和铜,所以A、B是氧化铜或木炭中的一种,A和E会转化成二氧化碳,所以A是木炭,E就是氧气,铜和E又会转化成,所以B就是氧化铜。
(1)E是氧气,其化学式是O2;
(2)①是碳和氧化铜的反应,该反应的方程式为:C+2CuO2Cu+CO2↑;
(3)在①的反应中,碳是还原剂,具有还原性,化学式为C;
(4)③是铜和氧气的反应,产物是氧化铜,该反应的特征是“多变一”,属于化合反应;
(5)物质A是木炭,可以用来炼铁;
【跟踪练2】如图是木炭还原氧化铜的实验示意图
(1)酒精灯上加一个金属网罩的作用是 。
(2)刚开始预热时,试管②中立即看到有气泡产生,但澄清石灰水未变浑浊,其原因是 ,继续加热一段时间,看到试管①中的现象是 ,反应的化学方程式是 ,试管②中出现 的现象,反应的化学方程式 。
(3)实验完毕后,要先 (选“A、先熄灭酒精灯”或“B、先将导管从石灰水中拿出”)。
(4)该实验得出的结论是碳在高温下具有 性。
【答案】(1)使酒精灯火焰更加集中,提高温度;
(2)刚开始排出的气体是装置内的空气;黑色粉末逐渐变红;C+2CuO2Cu+CO2↑;澄清石灰水变浑浊;Ca(OH)2+CO2═CaCO3↓+H2O;
(3)将导管从石灰水中拿出;
(4)还原。
【解析】(1)酒精灯火焰加上网罩后火焰会集中,从而提高了火焰的温度;
(2)刚开始预热时,导管口有气泡产生,但B中没有变浑浊,是因为此时排出的气体是装置内的空气;碳和氧化铜在高温的条件下生成铜和二氧化碳,继续加热一段时间,看到试管①中的现象是:黑色粉末逐渐变红,化学方程式是:C+2CuO2Cu+CO2↑;二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以试管②中出现澄清石灰水变浑浊的现象,化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;
(3)实验完毕后,要先将导管从石灰水中拿出,防止石灰水倒流,炸裂试管;
(4)该实验得出的结论是碳在高温下具有还原性。
知识梳理:
1、金刚石和石墨的物理性质及用途:
2、C60的物理性质和用途:
形似足球,几乎不导电,不导热,用于制备新材料、超导、医学及生物等领域。
3、无定性碳:木炭、活性炭、焦炭、炭黑
(1)活性炭、木炭:具有疏散多孔的结构,因此具有强烈的吸附性。木炭可用于食品、工业产品中除去色素、异味等;活性炭可用于防毒面具中除去毒气、制糖业中脱色以制白糖;
(2)焦炭用于冶铁,炭黑加到橡胶里能够增加轮胎的耐磨性。
【知识点睛】
碳单质物理性质差别的原因为碳原子的排列顺序不同。金刚石中碳原子排列呈正四面体结构,石墨中碳原子排列呈片层结构,C60中碳原子排列呈足球状结构;
关于碳单质的物理性质及用途,可以根据“结构性质用途”这个相互关系来互推巧记和理解;
书写碳元素组成的单质的名称时,一定要规范,不可写错别字。特别是,碳与炭不可弄混了.其中,“碳”是元素名称,是核电荷数(即核内质子数)为6的一类原子的总称;它用来描述元素、原子或由碳元素组成的物质的名称(但并不具体指某种物质),如碳元素、碳原子、二氧化碳、一氧化碳、碳酸钙、碳水化合
物等。而“炭”是用来专指由碳元素组成的部分单质(即没有固定形状的碳单质),主要有木炭、焦炭、活性炭、炭黑等。
【命题方向】
该考点的命题方向主要是通过创设相关问题情景或图表信息等,来考查学生对碳单质的物理性质及用途的理解和掌握情况;以及阅读、分析、推断能力和对知识的迁移能力.并且,经常将其与物质的组成和构成、碳元素组成的单质、碳单质的化学性质、金属的物理性质及其用途、吸附剂、水的净化、物质的推断和鉴别、铁的冶炼等相关知识联系起来,进行综合考查。
【解题方法点拨】
要想解答好这类题目,首先,要理解和熟记碳单质的物理性质及用途等相关知识.然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,以及自己的生活经验所得,细致地分析题意或图表信息等各种信息资源,联系起来综合分析,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可。
知识梳理:
碳的化学性质主要有三个:
1.常温时,具有稳定性。如,我国古代用墨书写或绘制的字画,虽年深日久仍不变色;就是利用了碳的这个性质;
2.点燃时,具有可燃性。它的燃烧还有两种情况:
(1)当碳在氧气或空气里充分燃烧时,生成二氧化碳,同时放出大量的热;
(2)当碳燃烧不充分的时候,生成一氧化碳,同时也放出热;
利用单质碳的可燃性,可以把碳用作燃料。
3. 高温时,具有还原性。在较高温度下碳能夺取某些含氧化合物里的氧,使其它元素被还原。
4、木炭还原氧化铜实验:
(1)实验装置:
(2)实验现象:黑色粉末逐渐变成红色,石灰水变浑浊;
(3)实验原理:C + 2CuO 2Cu + CO2↑
(4)酒精灯加网罩的目的:集中火焰、提高温度。
【知识点睛】
碳的化学性质在常温下温度,高温时不稳定,故描述时一定说清楚;
单质碳具有还原性,不仅可以还原金属氧化物,还能还原非金属氧化物,如可以夺取二氧化碳中的氧生成一氧化碳。利用碳的还原性,它可以用来冶炼金属。
虽然碳单质的物理性质有所不同,有的还相差很大,但是,由于它们都是由碳元素组成的单质,所以其化学性质是相同的。
【命题方向】
该考点的命题方向主要是通过创设相关的实验、问题情景或图表信息等,来考查学生对碳的化学性质及其反应现象、化学方程式和用途的理解和掌握情况;以及阅读、分析、推断能力和对知识的迁移能力。特别是,对碳的不充分燃烧与空气污染、碳的还原性与冶金、碳还原氧化铜的反应现象和化学方程式及有关的实验操作等,以及知识的迁移能力的考查,是近几年中考命题的热点,并且还是中考考查这块知识的重中之重。
【解题方法点拨】
要想解答好这类题目,首先,要理解和熟记碳的化学性质及其反应现象、化学方程式和用途等相关知识.然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,以及自己的生产或生活经验所得,细致地分析题意或图表信息等各种信息资源,联系起来综合分析,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
