化学人教版(2019)必修二 7.3.1 乙醇 课件(21张)
文档属性
| 名称 | 化学人教版(2019)必修二 7.3.1 乙醇 课件(21张) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-27 00:00:00 | ||
图片预览





文档简介
(共21张PPT)
第三节 乙醇与乙酸
第1课时 乙醇
第七章 有机化合物
【引入】
早在几千年前,人类就掌握了发酵法酿酒的技术。各种酒类都含有浓度不等的乙醇。
请同学们说一些含有酒的诗句?
这些诗句中体现出乙醇的哪些性质?
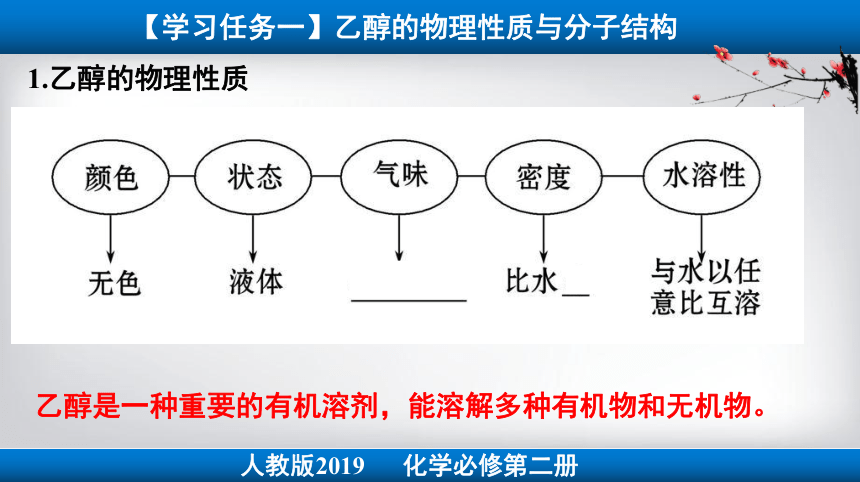
1.乙醇的物理性质
【学习任务一】乙醇的物理性质与分子结构
乙醇是一种重要的有机溶剂,能溶解多种有机物和无机物。
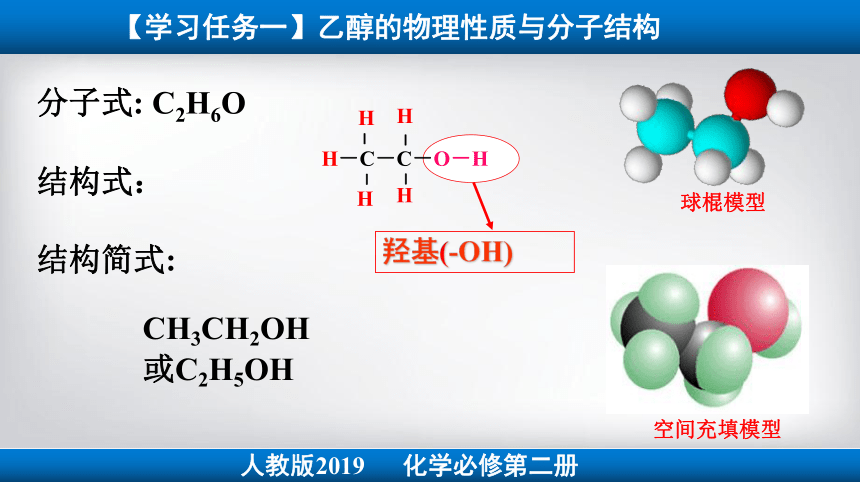
分子式: C2H6O
结构式:
结构简式:
CH3CH2OH
或C2H5OH
羟基(-OH)
H-C-C-O-H
-
H
-
-
-
H
H
H
球棍模型
空间充填模型
【学习任务一】乙醇的物理性质与分子结构
【学习任务一】乙醇的物理性质与分子结构
CH3CH3
CH3CH2OH
烃的衍生物:烃分子中的H原子被其他原子或原子团所取代而生成的一系列化合物。
思考1:因取代基团的不同,预测乙醇与乙烷相比可能会有哪些不同的化学性质?
【实验7-4】
在盛有少量无水乙醇的试管中,加入一小块新切的、用滤纸吸干表面煤油的钠,在试管口迅速塞上带尖嘴导管的橡胶塞,用小试管收集气体并检验其纯度,然后点燃(如图7-19),在将干燥的小烧杯罩在火焰上。待烧杯璧上出现液滴后,迅速倒转烧杯,想其中加入少量澄清石灰水。观察现象,并与前面做过的水与钠反应的实现现象进行比较。
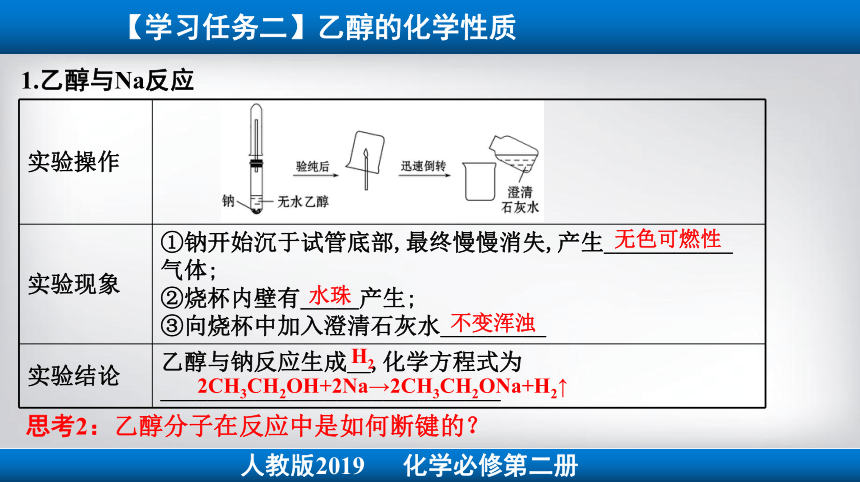
【学习任务二】乙醇的化学性质
1.乙醇与Na反应
实验操作
实验现象 ①钠开始沉于试管底部,最终慢慢消失,产生___________
气体;
②烧杯内壁有_____产生;
③向烧杯中加入澄清石灰水_________
实验结论 乙醇与钠反应生成__,化学方程式为
_____________________________
无色可燃性
水珠
不变浑浊
H2
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
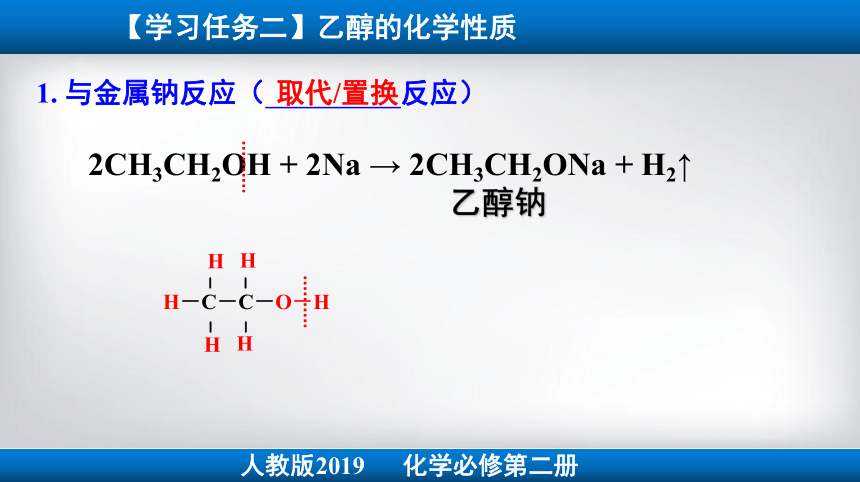
【学习任务二】乙醇的化学性质
思考2:乙醇分子在反应中是如何断键的?
1. 与金属钠反应( 反应)
2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑
乙醇钠
取代/置换
H-C-C-O-H
-
H
-
-
-
H
H
H
【学习任务二】乙醇的化学性质
思考与交流:
钠与水、与乙醇反应对比
1、从二者均能反应放出氢气,可得出什么结论?
2、从二者反应剧烈程度不同分析,乙醇 和水分子的羟基中的H原子哪个较活泼?乙基对乙醇的性质有无影响?
[结论] 1、羟基决定乙醇能和钠反应生成氢气
2、羟基中的H原子的活泼性:醇<水
乙醇羟基中的氢原子不如水分子中的氢原子活泼。实验表明,乙醇与钠的反应相同条件下比水与钠的反应缓和得多。
【学习任务二】乙醇的化学性质
官能团:决定有机化合物特性的原子或原子团。
如醇类:羟基(—OH);烯烃:碳碳双键;炔烃:碳碳三键
乙醇具有与乙烷不同的性质,从分子结构角度分析,是因为取代氢原子的羟基对乙醇的性质产生了影响。
烃分子失去1个氢原子后所剩余的部分叫做烃基,可以用一R来表示。如一CH3叫甲基,一CH2CH3,叫乙基。烃的衍生物分子一般可以看成是烃基和官能团相互结合组成的。例如,乙醇分子可以看成是由乙基和羟基组成的:CH3CH2-OH。
2.氧化反应:
①燃烧:
C2H5OH + 3O2 2CO2+3H2O
点燃
乙醇汽油
固体酒精
【学习任务二】乙醇的化学性质
现象:产生淡蓝色火焰,同时放出大量热。
【情景创设】工匠焊接银器、铜器时,表面会生成发黑的氧化膜,这时可以先把铜、银在火上烧热,马上蘸一下酒精,铜银会光亮如初。你知道为什么吗?【学习任务二】乙醇的化学性质
实验7-5向试管中加入少量乙醇,取一根铜丝,下端绕成螺旋状,在酒精灯上灼烧后插入乙醇中,反复几次,注意观察反应现象,并小心闻试管中液体产生的气味。
红色铜丝
Δ
变黑
有刺激性气味
插入乙醇溶液中
又变红
【学习任务二】乙醇的化学性质
红色铜丝
变黑
又变红
产生刺激性气味
2.氧化反应
(2)乙醇的催化氧化
【学习任务二】乙醇的化学性质
官能团:醛基
(—CHO)
如何断键(成键)?
【情景创设】据交警介绍,在机动车驾驶人的每100毫升血液中,酒精含量达到20毫克为饮酒驾车,大致相当于饮用一杯啤酒;每100毫升血液中酒精含量达到和超过80毫克可以认定为醉酒驾车,相当于饮用3两低度白酒或者两瓶啤酒。这是日前国家质量监督检验检疫总局正式发布并实施的中华人民共和国《车辆驾驶人员血液、呼气酒精含量阈值与检验》国家标准(GB19522-2004)(以下简称标准)规定的。你知道酒精检测仪的工作原理吗?
(3)乙醇与强氧化剂反应
2.氧化反应
K2Cr2O7
Cr2(SO4)3
(橙色)
(绿色)
乙醇
CH3CH2OH
KMnO4(H+) 或
K2Cr2O7 (H+)
CH3COOH(乙酸)
【学习任务二】乙醇的化学性质
五十六度:
酒精度=56%(V/V)
【资料卡片】酒常识
酒类产品标签中的酒精度是指乙醇的体积分数,白酒一般在25%~ 68%,啤酒一般在3%~ 5%。
酒的主要成分是乙醇,少量饮酒对人体有益,但酗酒有害健康。科学研究表明酒量的大小与人体内某些酶有关。乙醇进入人体后,会在肝中通过酶的催化作用被氧化为乙醛和乙酸,最终被氧化为二氧化碳和水。过量饮酒会加重肝负担,血液中较高浓度的乙醇和乙醛也会对人体产生毒害作用。
【资料卡片】酒常识
(1) 用作酒精灯、火锅、内燃机等的燃料。
(2) 用作化工原料、香料、化妆品、涂料等。
(3) 医疗上常用体积分数为75%的乙醇溶液作消毒剂。
【学习任务三】乙醇的用途
与Na反应,断_____键
催化氧化,断______键
燃烧,断__________键
①
① ③
【课堂小结】
∣
H—C—C—O—H
H
①
②
③
④
∣
∣
∣
H
H
H
⑤
①② ③④⑤
(金榜P70:情境应用)几乎所有的保湿类护肤品都少不了甘油,其中重要的一个原因是甘油吸水性强具有保湿作用。甘油学名为丙三醇,甘油可以吸取空气中的水分给皮肤保湿,也能将皮肤中的水分锁住,将水分留在角质层,不让它流失。
【学习评价一】
第三节 乙醇与乙酸
第1课时 乙醇
第七章 有机化合物
【引入】
早在几千年前,人类就掌握了发酵法酿酒的技术。各种酒类都含有浓度不等的乙醇。
请同学们说一些含有酒的诗句?
这些诗句中体现出乙醇的哪些性质?
1.乙醇的物理性质
【学习任务一】乙醇的物理性质与分子结构
乙醇是一种重要的有机溶剂,能溶解多种有机物和无机物。
分子式: C2H6O
结构式:
结构简式:
CH3CH2OH
或C2H5OH
羟基(-OH)
H-C-C-O-H
-
H
-
-
-
H
H
H
球棍模型
空间充填模型
【学习任务一】乙醇的物理性质与分子结构
【学习任务一】乙醇的物理性质与分子结构
CH3CH3
CH3CH2OH
烃的衍生物:烃分子中的H原子被其他原子或原子团所取代而生成的一系列化合物。
思考1:因取代基团的不同,预测乙醇与乙烷相比可能会有哪些不同的化学性质?
【实验7-4】
在盛有少量无水乙醇的试管中,加入一小块新切的、用滤纸吸干表面煤油的钠,在试管口迅速塞上带尖嘴导管的橡胶塞,用小试管收集气体并检验其纯度,然后点燃(如图7-19),在将干燥的小烧杯罩在火焰上。待烧杯璧上出现液滴后,迅速倒转烧杯,想其中加入少量澄清石灰水。观察现象,并与前面做过的水与钠反应的实现现象进行比较。
【学习任务二】乙醇的化学性质
1.乙醇与Na反应
实验操作
实验现象 ①钠开始沉于试管底部,最终慢慢消失,产生___________
气体;
②烧杯内壁有_____产生;
③向烧杯中加入澄清石灰水_________
实验结论 乙醇与钠反应生成__,化学方程式为
_____________________________
无色可燃性
水珠
不变浑浊
H2
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
【学习任务二】乙醇的化学性质
思考2:乙醇分子在反应中是如何断键的?
1. 与金属钠反应( 反应)
2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑
乙醇钠
取代/置换
H-C-C-O-H
-
H
-
-
-
H
H
H
【学习任务二】乙醇的化学性质
思考与交流:
钠与水、与乙醇反应对比
1、从二者均能反应放出氢气,可得出什么结论?
2、从二者反应剧烈程度不同分析,乙醇 和水分子的羟基中的H原子哪个较活泼?乙基对乙醇的性质有无影响?
[结论] 1、羟基决定乙醇能和钠反应生成氢气
2、羟基中的H原子的活泼性:醇<水
乙醇羟基中的氢原子不如水分子中的氢原子活泼。实验表明,乙醇与钠的反应相同条件下比水与钠的反应缓和得多。
【学习任务二】乙醇的化学性质
官能团:决定有机化合物特性的原子或原子团。
如醇类:羟基(—OH);烯烃:碳碳双键;炔烃:碳碳三键
乙醇具有与乙烷不同的性质,从分子结构角度分析,是因为取代氢原子的羟基对乙醇的性质产生了影响。
烃分子失去1个氢原子后所剩余的部分叫做烃基,可以用一R来表示。如一CH3叫甲基,一CH2CH3,叫乙基。烃的衍生物分子一般可以看成是烃基和官能团相互结合组成的。例如,乙醇分子可以看成是由乙基和羟基组成的:CH3CH2-OH。
2.氧化反应:
①燃烧:
C2H5OH + 3O2 2CO2+3H2O
点燃
乙醇汽油
固体酒精
【学习任务二】乙醇的化学性质
现象:产生淡蓝色火焰,同时放出大量热。
【情景创设】工匠焊接银器、铜器时,表面会生成发黑的氧化膜,这时可以先把铜、银在火上烧热,马上蘸一下酒精,铜银会光亮如初。你知道为什么吗?【学习任务二】乙醇的化学性质
实验7-5向试管中加入少量乙醇,取一根铜丝,下端绕成螺旋状,在酒精灯上灼烧后插入乙醇中,反复几次,注意观察反应现象,并小心闻试管中液体产生的气味。
红色铜丝
Δ
变黑
有刺激性气味
插入乙醇溶液中
又变红
【学习任务二】乙醇的化学性质
红色铜丝
变黑
又变红
产生刺激性气味
2.氧化反应
(2)乙醇的催化氧化
【学习任务二】乙醇的化学性质
官能团:醛基
(—CHO)
如何断键(成键)?
【情景创设】据交警介绍,在机动车驾驶人的每100毫升血液中,酒精含量达到20毫克为饮酒驾车,大致相当于饮用一杯啤酒;每100毫升血液中酒精含量达到和超过80毫克可以认定为醉酒驾车,相当于饮用3两低度白酒或者两瓶啤酒。这是日前国家质量监督检验检疫总局正式发布并实施的中华人民共和国《车辆驾驶人员血液、呼气酒精含量阈值与检验》国家标准(GB19522-2004)(以下简称标准)规定的。你知道酒精检测仪的工作原理吗?
(3)乙醇与强氧化剂反应
2.氧化反应
K2Cr2O7
Cr2(SO4)3
(橙色)
(绿色)
乙醇
CH3CH2OH
KMnO4(H+) 或
K2Cr2O7 (H+)
CH3COOH(乙酸)
【学习任务二】乙醇的化学性质
五十六度:
酒精度=56%(V/V)
【资料卡片】酒常识
酒类产品标签中的酒精度是指乙醇的体积分数,白酒一般在25%~ 68%,啤酒一般在3%~ 5%。
酒的主要成分是乙醇,少量饮酒对人体有益,但酗酒有害健康。科学研究表明酒量的大小与人体内某些酶有关。乙醇进入人体后,会在肝中通过酶的催化作用被氧化为乙醛和乙酸,最终被氧化为二氧化碳和水。过量饮酒会加重肝负担,血液中较高浓度的乙醇和乙醛也会对人体产生毒害作用。
【资料卡片】酒常识
(1) 用作酒精灯、火锅、内燃机等的燃料。
(2) 用作化工原料、香料、化妆品、涂料等。
(3) 医疗上常用体积分数为75%的乙醇溶液作消毒剂。
【学习任务三】乙醇的用途
与Na反应,断_____键
催化氧化,断______键
燃烧,断__________键
①
① ③
【课堂小结】
∣
H—C—C—O—H
H
①
②
③
④
∣
∣
∣
H
H
H
⑤
①② ③④⑤
(金榜P70:情境应用)几乎所有的保湿类护肤品都少不了甘油,其中重要的一个原因是甘油吸水性强具有保湿作用。甘油学名为丙三醇,甘油可以吸取空气中的水分给皮肤保湿,也能将皮肤中的水分锁住,将水分留在角质层,不让它流失。
【学习评价一】
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
