4.4化学式与化合价(第二课时化合价)课件 --2022-2023学年九年级化学人教版上册(共41张PPT 内嵌音频)
文档属性
| 名称 | 4.4化学式与化合价(第二课时化合价)课件 --2022-2023学年九年级化学人教版上册(共41张PPT 内嵌音频) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-28 00:00:00 | ||
图片预览





文档简介
(共41张PPT)
化合价
开始学习
温故知新
写出下列物质的化学式
氯化钠 硫化锌 氧化汞
氯化镁 氯化铝 氧化镁
思考
目前已知的物质有数千万种,我们可以依据实验的结果来测定物质的组成并写出物质的化学式
观察下列物质组成元素的原子个数比
NaCl MgCl 2 H2O HCl
1:1 1:2 2:1 1:1
导入新课
如果每个化学式的书写都像英语单词一样依靠记忆,我背的只想哭!
导入新课
小明,有没有更简单的办法来解决化学式的书写问题呢?
……………………………………?
导入新课
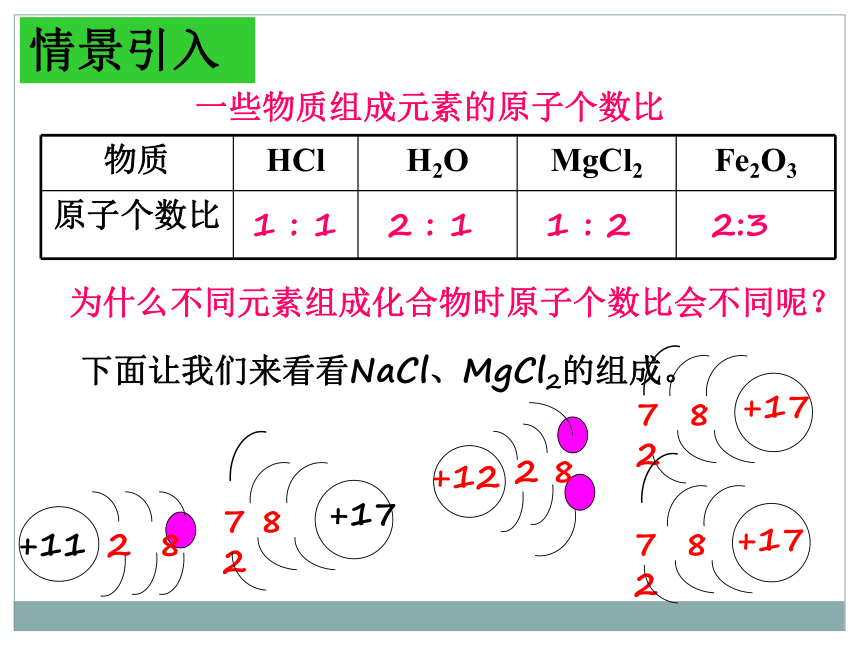
一些物质组成元素的原子个数比
物质 HCl H2O MgCl2 Fe2O3
原子个数比
1 : 1
2 : 1
1 : 2
2:3
为什么不同元素组成化合物时原子个数比会不同呢?
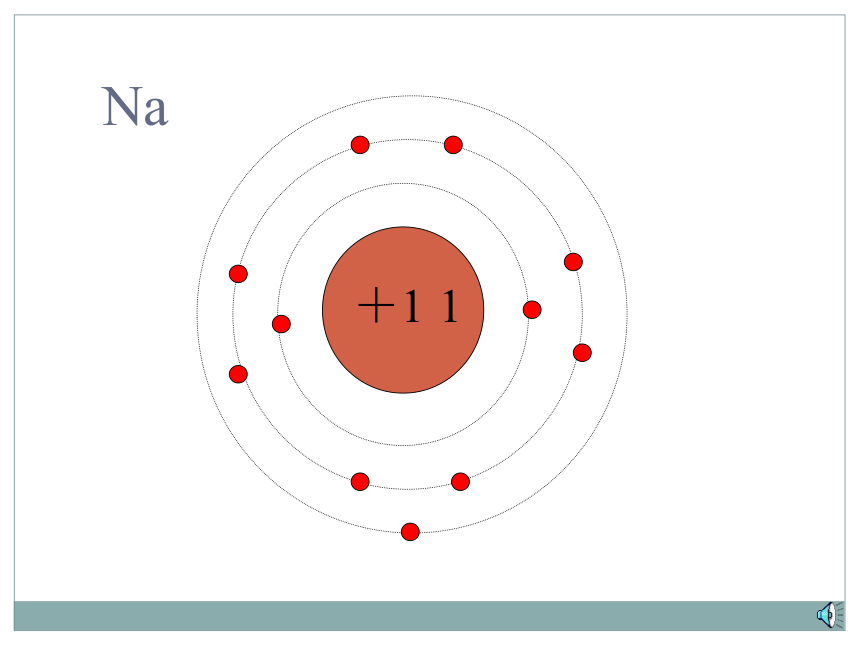
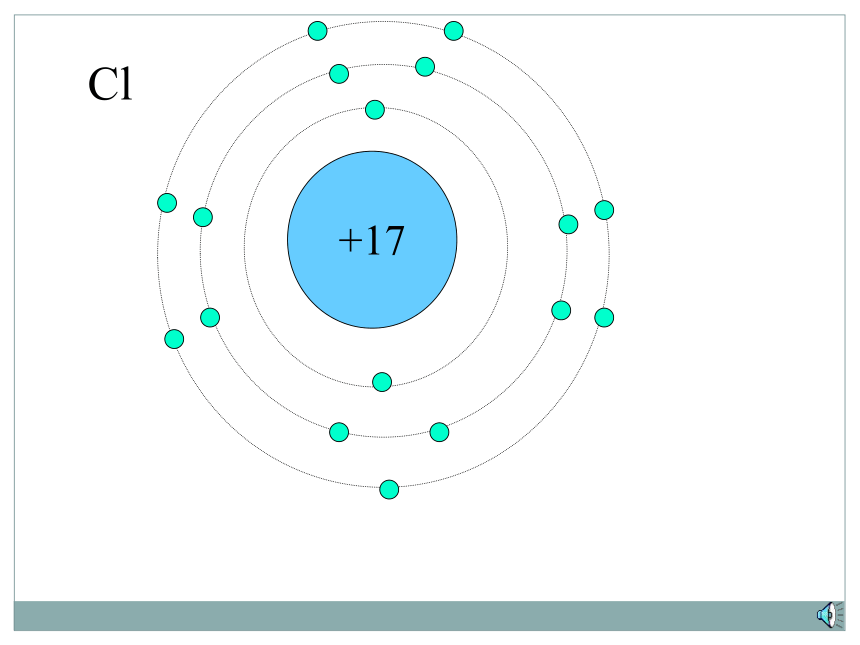
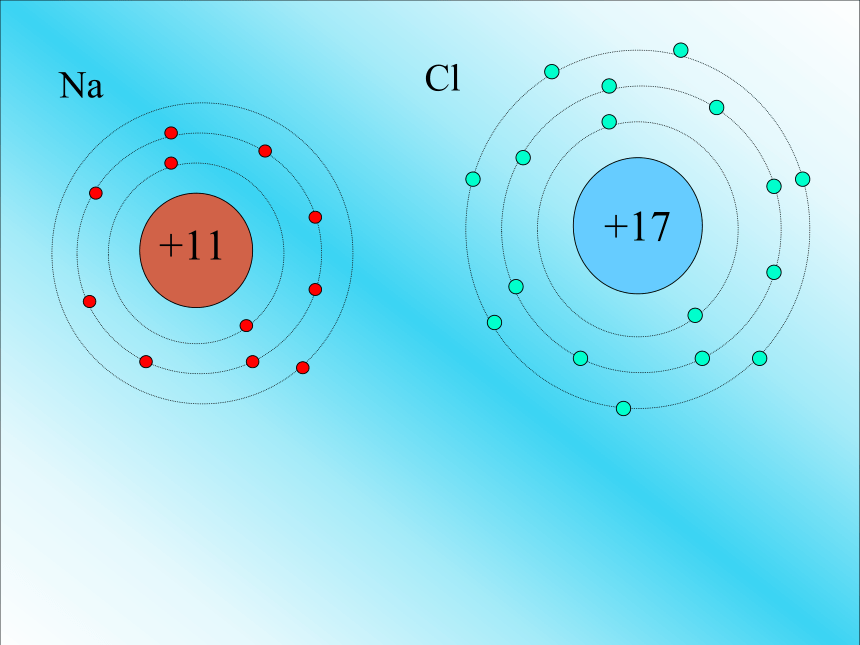
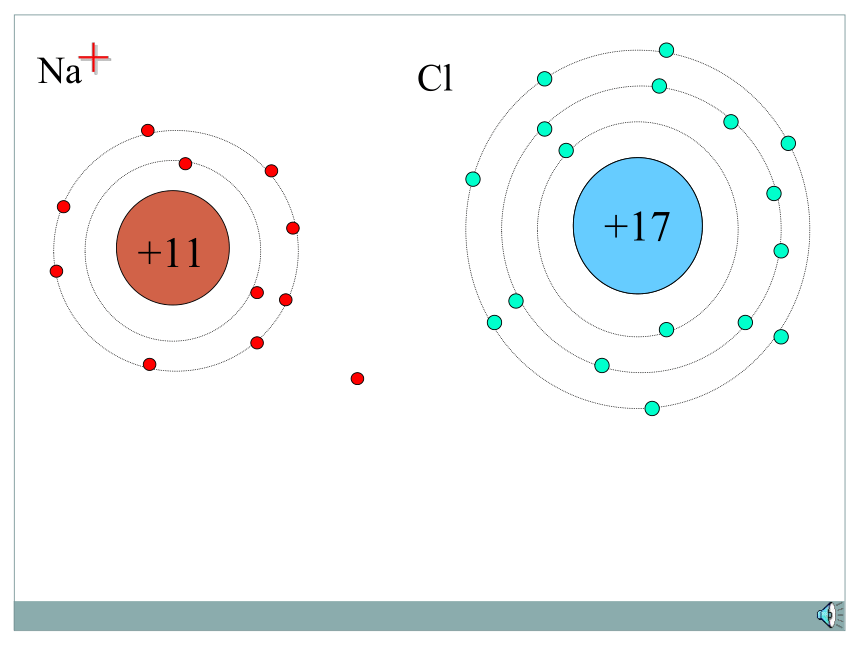
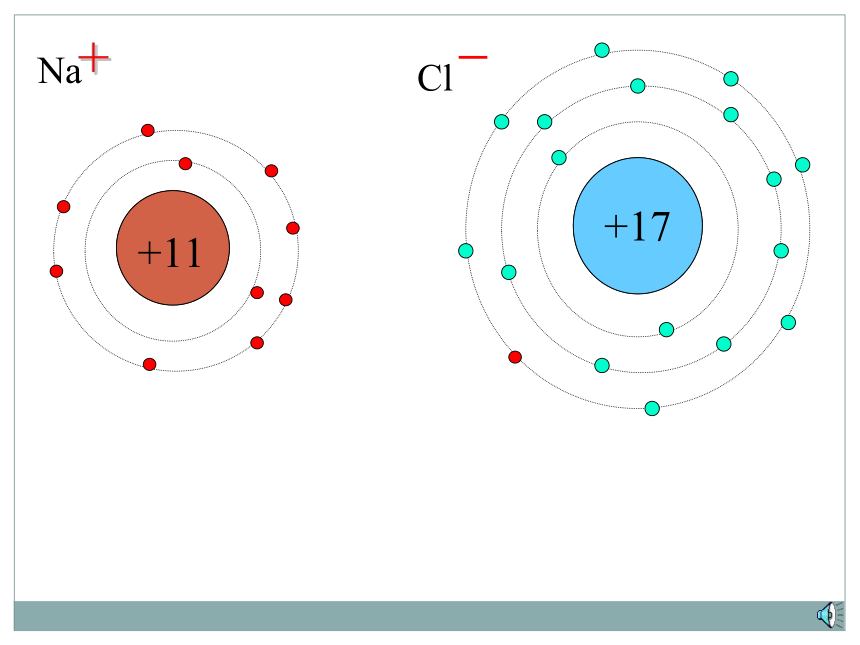
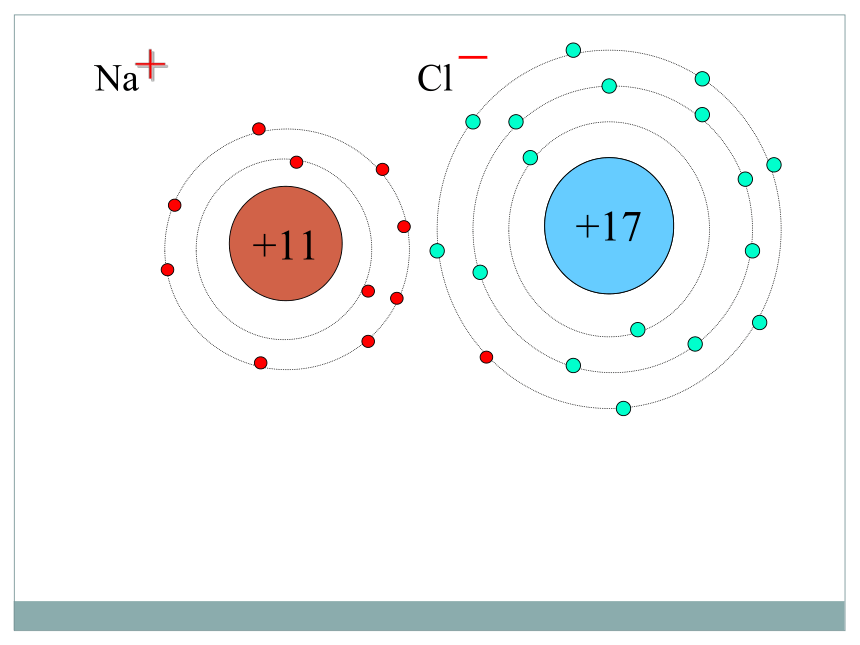
下面让我们来看看NaCl、MgCl2的组成。
+11
+12
2 8
+17
7 8 2
+17
7 8 2
+17
7 8 2
情景引入
2 8
+1 1
Na
+17
Cl
Na
+17
Cl
+11
Cl
+
Na
+17
Cl
+11
Na
Cl
+
+
Na
+17
Cl
+11
Na
Cl
+
+
Na
+17
Cl
+11
+11
+17
Na Cl
+1 -1
实验测定 化学式的书写必须依据实验的结果
我们还可以根据组成元素的化合价来推求化合物中组成元素的原子个数比。
化学上用化合价来表示原子间相化合的数目
【注意】元素的化合价是元素的原子在形成化合物时表现出来的一种性质,因此,通常称为元素的化合价而不应称为原子的化合价。
一、化合价的表示方法:
1 写在元素符号的正上方。
2. “+”、“—” 符号在前,数值在后。
3. “1”不能省略。
NaCl MgCl 2 H2O HCl
+1 -1 +2 -1 +1 -2 +1 -1
化合价
NaCl MgO N2 Al2O3 H2O SO2 MnO2
+1
-1
+2
-2
0
+3
-2
+1
-2
-2
+4
+4
-2
化合价的原则:
在化合物里,正、负化合价的代数和为零。
单质分子中元素的化合价为零。
【观察】下列化合物中,正、负化合价的代数和有什么特点?
想一想
离子符号的书写与元素化合价的书写比较:
H+
H
+1
Na+
Na
+1
Mg2+
Mg
+2
Al3+
Al
+3
NH4+
NH4
+1
Cl-
O2-
NO3-
Cl
-1
O
-2
NO3
-1
MnO4-
MnO4
-1
(KMnO4)
MnO42-
MnO4
-2
(K2MnO4)
高锰酸根离子
锰酸根离子
你发现了什么规律?
Mg
+2
写出下列符号中数字表示的意义:
镁元素的化合价为正二价
一个镁离子带两个单位的正电荷
写出下列符号中数字的含义:
Mg2+
离子符号和化合价的表示方法不同:
离子:数字在前,“+”“-”号在后;写在右上角。
化合价:数字在后,“+”“-”号在前;写在正上方。
化合价与离子所带电荷的联系:数字相同,正负号相同。
离子符号与化合价的比较:
观察与思考
离子符号 Na+ Mg2+ Al3+ F- O2-
化合价 Na Mg Al F O
+1
+2
+3
-1
-2
讲授新课
背诵出化合价,就能
顺利写出离子符号。
化合价的标法与离子符号的区别与联系
化合价的表示 方法 Na 离子符号 Na+
区 别 1.记号的位置不同 标在元素符号 的正上方 标在元素符号的右上角
2.“+ - ”与数字的位置不同 “+ -”在数字之前 “+ -”在数字之后
3. “1”的处理不同 “1”必标 “1”不必标
联系 化合价的数值与离子所带电荷的数值相同,符号一致
+1
+2
Zn
锌
-3、+3、+5
P
磷
+2.+4.+6.+7
Mn
锰
-3.+2.+4.+5
N
氮
+3
Al
铝
+4
Si
硅
+2、+3
Fe
铁
+2、+4
C
碳
+1、+2
Cu
铜
-2、+4、+6
S
硫
+2
Ba
钡
-2
O
氧
+2
Mg
镁
-1
Br
溴
+2
Ca
钙
-1.+1.+5.+7
Cl
氯
+1
Ag
银
-1
F
氟
+1
Na
钠
+1
H
氢
+1
K
钾
常见化合价
元素符号
元素
常见化合价
元素符号
元素
元素 元素符号 常见化合价 元素 元素符号 常见化合价
钾 K +1 氢 H +1
钠 Na +1 氟 F -1
银 Ag +1 氯 Cl -1.+1.+5.+7
钙 Ca +2 溴 Br -1
镁 Mg +2 氧 O -2
钡 Ba +2 硫 S -2、+4、+6
铜 Cu +1、+2 碳 C +2、+4
铁 Fe +2、+3 硅 Si +4
铝 Al +3 氮 N -3.+2.+4.+5
锰 Mn +2.+4.+6.+7 磷 P -3、+3、+5
锌 Zn +2
金属元素的化合价
金属元素跟非金属元素化合时,
金属元素显正价。
(1)在任何化合物里,正负化合价的代数和为零。
(2)在化合物里氢通常显+1价,氧通常显-2价。
(3)金属元素显正价
(4)元素只有在形成化合物时,才讲化合价单质里元素的化合价为零。
(5)许多元素具有可变化合价,同种元素在不同的化合物里可显不同的化合价,如:FeO,Fe2O3中铁元素的化合价分别为+2和+3。
化合价的有关规律
化合价的应用
二
1.根据化学式求某一元素化合价
原则:化合物里正负化合价的代数和为零。
例1:试确定氯酸钾(KClO3)中氯元素的化合价
解:设氯元素的化合价为x,则
(+1)+ x +(-2)×3=0
x = +5
答:在氯酸钾中,氯元素的化合价为+5价
根据化学式求锰元素的化合价
先确定氢、氧、金属元素的化合价
根据化学式标(横线)元素的化合价
当堂检测
H2SO4 CaCO3 AgNO3
O2 KClO3 NH4Cl
NO
NO2
NH3
同种元素在不同的化合物里可显不同的化合价
1.冲洗照片时,需将底片浸泡在大苏打(Na2S2O3)溶液中,使影像固定下来,这一过程叫“定影”。大苏打中硫元素的化合价为( )
A.0 B.+2
C.+4 D.+6
训练
讲授新课
原子团:作为一个整体参加反应的原子集团(就好像一个原子一样),原子团也叫作根。
注意:①原子团不能单独存在;
②带电荷的原子团也是离子。
③原子团(根)是一个整体,不能随意拆开。
NaOH、Ca(OH)2、Cu(OH)2、Fe(OH)3
读氢氧化某
H2CO3、H2SO4、HNO3
读某酸[中间元素的名称]
CaCO3、CuSO4、NaNO3
读某[酸根]酸某
推求下列原子团(根)的化合价:
原子团的化合价
NaNO3、 NH4NO3、 NaOH、
H2SO4、 Na2CO3、 H3PO4
+1
-1
-1
+1
+1
+1
+1
+1
-1
-2
-2
-3
推求的依据:化合物中元素的化合价代数和为零。
例:求NH4NO3中带横线元素的化合价
思路:
设原子团NH4中氮元素的化合价为X
设原子团NO3中氮元素的化合价为Y
NH4NO3
-3
+5
同种元素在同种物质中可以呈现不同的化合价
NaCl MgCl2 Al2O3 P2O5
Fe2O3 Ag2O H2O BaCl2
+1 -1 +2 -1 +3 -2 +5 -2
+3 -2 +1 -2 +1 -2 +2 -1
如何写角码?请分析找规律
探究--找规律:
NaCl MgCl2 Al2O3 P2O5
Fe2O3 Ag2O H2O BaCl2
+1 -1 +2 -1 +3 -2 +5 -2
+3 -2 +1 -2 +1 -2 +2 -1
化合价交叉写角码
探究--找规律:
三、根据化合价书写化学式
方法:一排顺序,二标价,三要约简 ,四交叉,
最后记住要检查
.
点拨
写出元素符号,正价在左,负价在右。(有些化合物书写时负价元素在左边,正价元素在右边,如NH3、CH4等)
1、特殊物质:过氧化氢、四氧化二氮
2、带有原子团的化学式且原子团个数不为1时,需要为原子团加上小括号。
化 合 价 的 计 算 小 结
【问】:如果碰到有原子团的化学式又怎样书写呢?如已知铝为+3价,硫酸根(SO4)为-2价,写出硫酸铝的化学式。
Al2(SO4)3
小 结
数字交叉法书写化学式的一般步骤:
①写出组成的元素符号:正价先写,负价后写;
②标出元素的化合价;
③定原子或原子团个数:
化合价的绝对值斜交叉下来得个数;
能约简的要先约简再交叉;
有2个以上原子团要加括号;
右下角数字是“1”的省略不写;
思路:正前 负后 化简 交叉
1.写出下列物质的化学式
(1)氧化钠 (2)氯化镁 (3)氧化镁(4)氧化钙
(5)氧化铝(6)氟化钠. (7)氯化钾(8)氯化氢
(9)硝酸铝(10)硫酸钾
(11) 氯化银(12)氢氧化钙
当堂检测
3、填空:
下列化学式如有错误请改在横线上:
氧化钙Ca2O2 ______, 氯化铁 FeCl2 _____
氯化锌 ZnCl ______, 硫化铝 Al3S2 ______
氢氧化铜CuOH _____ , 氯化钠ClNa ______
CaO
FeCl3
ZnCl2
Al2S3
Cu(OH)2
NaCl
课堂教学展示
典例剖析
例1 交警常用装有重铬酸钾(K2Cr2O7)的仪器检测司机是否酒后驾车,因为酒中的乙醇分子能使橙红色的重铬酸钾变为绿色的硫酸铬[Cr2(SO4)3],重铬酸钾和硫酸铬中铬的化合价依次是( )
A.+6、+3
B.+3、+5
C.+3、+3
D.+3、+6
A
已知钾元素为+1价,氧元素为-2价,硫酸根离子为-2价,设在这两种化合物中铬元素的化合价依次为x、y,则有:
(+1)×2+2x+(-2)×7=0
y×2+(-2)×3=0
解得 x=+6
y=+3
1.高铁酸钠(Na2FeO4)是一种“绿色环保高效”消毒剂,比目前国内外广泛使用的含氯饮用水消毒剂性能更为优良。高铁酸钠(Na2FeO4)中铁元素的化合
价为( )
A.0 B.+2 C.+3 D.+6
2.元素R在化合物中只有一种化合价,它的氧化物的化学式为R2O3,则下列化学式正确的是( )
A.R(OH)2 B.RNO3 C.R2(SO4)3 D.RCO3
训练
1、已知在H3RO4中,氢元素为+1价,氧为-2价,则其中R的化合价为( )
A、+3 B、+4 C、+5 D、+6
2、下列化合物中,氮元素为+5价的是( )
A、N0 B、NO2 C、HNO2 D、KNO3
3、元素R的氧化物的化学式为R2O3,则R元素与OH-组成的物质的化学式为( )
A、ROH B、R(OH)2 C、R(OH)3 D、R(OH)4
C
D
C
总结:化合价的运用
1. 根据元素化合价推出实际存在的物质的化学式
(1). 排列元素 符号------正价在前负价在后
(2). 确定原子个数-------求两种元素正负化合价绝对值的最小公倍数
(3). 写出化学式----------把原子个数写在各元素 符号的右下方
(4). 检查化学式----------依据: 化合价代数和为0
例.写出氧化铝的化学式
2. 根据化学式判断元素的化合价
求 MnO2, FeO,Fe2O3, NH4NO3中 Mn , Fe , N 三种元素的
化合价
依据 :化合物里正负化合价代数和为0
结论:1.同种元素 在不同的化合物里有不同的化合价
2.同一化合物里同种元素 也可能有不同的化合价
化合价
开始学习
温故知新
写出下列物质的化学式
氯化钠 硫化锌 氧化汞
氯化镁 氯化铝 氧化镁
思考
目前已知的物质有数千万种,我们可以依据实验的结果来测定物质的组成并写出物质的化学式
观察下列物质组成元素的原子个数比
NaCl MgCl 2 H2O HCl
1:1 1:2 2:1 1:1
导入新课
如果每个化学式的书写都像英语单词一样依靠记忆,我背的只想哭!
导入新课
小明,有没有更简单的办法来解决化学式的书写问题呢?
……………………………………?
导入新课
一些物质组成元素的原子个数比
物质 HCl H2O MgCl2 Fe2O3
原子个数比
1 : 1
2 : 1
1 : 2
2:3
为什么不同元素组成化合物时原子个数比会不同呢?
下面让我们来看看NaCl、MgCl2的组成。
+11
+12
2 8
+17
7 8 2
+17
7 8 2
+17
7 8 2
情景引入
2 8
+1 1
Na
+17
Cl
Na
+17
Cl
+11
Cl
+
Na
+17
Cl
+11
Na
Cl
+
+
Na
+17
Cl
+11
Na
Cl
+
+
Na
+17
Cl
+11
+11
+17
Na Cl
+1 -1
实验测定 化学式的书写必须依据实验的结果
我们还可以根据组成元素的化合价来推求化合物中组成元素的原子个数比。
化学上用化合价来表示原子间相化合的数目
【注意】元素的化合价是元素的原子在形成化合物时表现出来的一种性质,因此,通常称为元素的化合价而不应称为原子的化合价。
一、化合价的表示方法:
1 写在元素符号的正上方。
2. “+”、“—” 符号在前,数值在后。
3. “1”不能省略。
NaCl MgCl 2 H2O HCl
+1 -1 +2 -1 +1 -2 +1 -1
化合价
NaCl MgO N2 Al2O3 H2O SO2 MnO2
+1
-1
+2
-2
0
+3
-2
+1
-2
-2
+4
+4
-2
化合价的原则:
在化合物里,正、负化合价的代数和为零。
单质分子中元素的化合价为零。
【观察】下列化合物中,正、负化合价的代数和有什么特点?
想一想
离子符号的书写与元素化合价的书写比较:
H+
H
+1
Na+
Na
+1
Mg2+
Mg
+2
Al3+
Al
+3
NH4+
NH4
+1
Cl-
O2-
NO3-
Cl
-1
O
-2
NO3
-1
MnO4-
MnO4
-1
(KMnO4)
MnO42-
MnO4
-2
(K2MnO4)
高锰酸根离子
锰酸根离子
你发现了什么规律?
Mg
+2
写出下列符号中数字表示的意义:
镁元素的化合价为正二价
一个镁离子带两个单位的正电荷
写出下列符号中数字的含义:
Mg2+
离子符号和化合价的表示方法不同:
离子:数字在前,“+”“-”号在后;写在右上角。
化合价:数字在后,“+”“-”号在前;写在正上方。
化合价与离子所带电荷的联系:数字相同,正负号相同。
离子符号与化合价的比较:
观察与思考
离子符号 Na+ Mg2+ Al3+ F- O2-
化合价 Na Mg Al F O
+1
+2
+3
-1
-2
讲授新课
背诵出化合价,就能
顺利写出离子符号。
化合价的标法与离子符号的区别与联系
化合价的表示 方法 Na 离子符号 Na+
区 别 1.记号的位置不同 标在元素符号 的正上方 标在元素符号的右上角
2.“+ - ”与数字的位置不同 “+ -”在数字之前 “+ -”在数字之后
3. “1”的处理不同 “1”必标 “1”不必标
联系 化合价的数值与离子所带电荷的数值相同,符号一致
+1
+2
Zn
锌
-3、+3、+5
P
磷
+2.+4.+6.+7
Mn
锰
-3.+2.+4.+5
N
氮
+3
Al
铝
+4
Si
硅
+2、+3
Fe
铁
+2、+4
C
碳
+1、+2
Cu
铜
-2、+4、+6
S
硫
+2
Ba
钡
-2
O
氧
+2
Mg
镁
-1
Br
溴
+2
Ca
钙
-1.+1.+5.+7
Cl
氯
+1
Ag
银
-1
F
氟
+1
Na
钠
+1
H
氢
+1
K
钾
常见化合价
元素符号
元素
常见化合价
元素符号
元素
元素 元素符号 常见化合价 元素 元素符号 常见化合价
钾 K +1 氢 H +1
钠 Na +1 氟 F -1
银 Ag +1 氯 Cl -1.+1.+5.+7
钙 Ca +2 溴 Br -1
镁 Mg +2 氧 O -2
钡 Ba +2 硫 S -2、+4、+6
铜 Cu +1、+2 碳 C +2、+4
铁 Fe +2、+3 硅 Si +4
铝 Al +3 氮 N -3.+2.+4.+5
锰 Mn +2.+4.+6.+7 磷 P -3、+3、+5
锌 Zn +2
金属元素的化合价
金属元素跟非金属元素化合时,
金属元素显正价。
(1)在任何化合物里,正负化合价的代数和为零。
(2)在化合物里氢通常显+1价,氧通常显-2价。
(3)金属元素显正价
(4)元素只有在形成化合物时,才讲化合价单质里元素的化合价为零。
(5)许多元素具有可变化合价,同种元素在不同的化合物里可显不同的化合价,如:FeO,Fe2O3中铁元素的化合价分别为+2和+3。
化合价的有关规律
化合价的应用
二
1.根据化学式求某一元素化合价
原则:化合物里正负化合价的代数和为零。
例1:试确定氯酸钾(KClO3)中氯元素的化合价
解:设氯元素的化合价为x,则
(+1)+ x +(-2)×3=0
x = +5
答:在氯酸钾中,氯元素的化合价为+5价
根据化学式求锰元素的化合价
先确定氢、氧、金属元素的化合价
根据化学式标(横线)元素的化合价
当堂检测
H2SO4 CaCO3 AgNO3
O2 KClO3 NH4Cl
NO
NO2
NH3
同种元素在不同的化合物里可显不同的化合价
1.冲洗照片时,需将底片浸泡在大苏打(Na2S2O3)溶液中,使影像固定下来,这一过程叫“定影”。大苏打中硫元素的化合价为( )
A.0 B.+2
C.+4 D.+6
训练
讲授新课
原子团:作为一个整体参加反应的原子集团(就好像一个原子一样),原子团也叫作根。
注意:①原子团不能单独存在;
②带电荷的原子团也是离子。
③原子团(根)是一个整体,不能随意拆开。
NaOH、Ca(OH)2、Cu(OH)2、Fe(OH)3
读氢氧化某
H2CO3、H2SO4、HNO3
读某酸[中间元素的名称]
CaCO3、CuSO4、NaNO3
读某[酸根]酸某
推求下列原子团(根)的化合价:
原子团的化合价
NaNO3、 NH4NO3、 NaOH、
H2SO4、 Na2CO3、 H3PO4
+1
-1
-1
+1
+1
+1
+1
+1
-1
-2
-2
-3
推求的依据:化合物中元素的化合价代数和为零。
例:求NH4NO3中带横线元素的化合价
思路:
设原子团NH4中氮元素的化合价为X
设原子团NO3中氮元素的化合价为Y
NH4NO3
-3
+5
同种元素在同种物质中可以呈现不同的化合价
NaCl MgCl2 Al2O3 P2O5
Fe2O3 Ag2O H2O BaCl2
+1 -1 +2 -1 +3 -2 +5 -2
+3 -2 +1 -2 +1 -2 +2 -1
如何写角码?请分析找规律
探究--找规律:
NaCl MgCl2 Al2O3 P2O5
Fe2O3 Ag2O H2O BaCl2
+1 -1 +2 -1 +3 -2 +5 -2
+3 -2 +1 -2 +1 -2 +2 -1
化合价交叉写角码
探究--找规律:
三、根据化合价书写化学式
方法:一排顺序,二标价,三要约简 ,四交叉,
最后记住要检查
.
点拨
写出元素符号,正价在左,负价在右。(有些化合物书写时负价元素在左边,正价元素在右边,如NH3、CH4等)
1、特殊物质:过氧化氢、四氧化二氮
2、带有原子团的化学式且原子团个数不为1时,需要为原子团加上小括号。
化 合 价 的 计 算 小 结
【问】:如果碰到有原子团的化学式又怎样书写呢?如已知铝为+3价,硫酸根(SO4)为-2价,写出硫酸铝的化学式。
Al2(SO4)3
小 结
数字交叉法书写化学式的一般步骤:
①写出组成的元素符号:正价先写,负价后写;
②标出元素的化合价;
③定原子或原子团个数:
化合价的绝对值斜交叉下来得个数;
能约简的要先约简再交叉;
有2个以上原子团要加括号;
右下角数字是“1”的省略不写;
思路:正前 负后 化简 交叉
1.写出下列物质的化学式
(1)氧化钠 (2)氯化镁 (3)氧化镁(4)氧化钙
(5)氧化铝(6)氟化钠. (7)氯化钾(8)氯化氢
(9)硝酸铝(10)硫酸钾
(11) 氯化银(12)氢氧化钙
当堂检测
3、填空:
下列化学式如有错误请改在横线上:
氧化钙Ca2O2 ______, 氯化铁 FeCl2 _____
氯化锌 ZnCl ______, 硫化铝 Al3S2 ______
氢氧化铜CuOH _____ , 氯化钠ClNa ______
CaO
FeCl3
ZnCl2
Al2S3
Cu(OH)2
NaCl
课堂教学展示
典例剖析
例1 交警常用装有重铬酸钾(K2Cr2O7)的仪器检测司机是否酒后驾车,因为酒中的乙醇分子能使橙红色的重铬酸钾变为绿色的硫酸铬[Cr2(SO4)3],重铬酸钾和硫酸铬中铬的化合价依次是( )
A.+6、+3
B.+3、+5
C.+3、+3
D.+3、+6
A
已知钾元素为+1价,氧元素为-2价,硫酸根离子为-2价,设在这两种化合物中铬元素的化合价依次为x、y,则有:
(+1)×2+2x+(-2)×7=0
y×2+(-2)×3=0
解得 x=+6
y=+3
1.高铁酸钠(Na2FeO4)是一种“绿色环保高效”消毒剂,比目前国内外广泛使用的含氯饮用水消毒剂性能更为优良。高铁酸钠(Na2FeO4)中铁元素的化合
价为( )
A.0 B.+2 C.+3 D.+6
2.元素R在化合物中只有一种化合价,它的氧化物的化学式为R2O3,则下列化学式正确的是( )
A.R(OH)2 B.RNO3 C.R2(SO4)3 D.RCO3
训练
1、已知在H3RO4中,氢元素为+1价,氧为-2价,则其中R的化合价为( )
A、+3 B、+4 C、+5 D、+6
2、下列化合物中,氮元素为+5价的是( )
A、N0 B、NO2 C、HNO2 D、KNO3
3、元素R的氧化物的化学式为R2O3,则R元素与OH-组成的物质的化学式为( )
A、ROH B、R(OH)2 C、R(OH)3 D、R(OH)4
C
D
C
总结:化合价的运用
1. 根据元素化合价推出实际存在的物质的化学式
(1). 排列元素 符号------正价在前负价在后
(2). 确定原子个数-------求两种元素正负化合价绝对值的最小公倍数
(3). 写出化学式----------把原子个数写在各元素 符号的右下方
(4). 检查化学式----------依据: 化合价代数和为0
例.写出氧化铝的化学式
2. 根据化学式判断元素的化合价
求 MnO2, FeO,Fe2O3, NH4NO3中 Mn , Fe , N 三种元素的
化合价
依据 :化合物里正负化合价代数和为0
结论:1.同种元素 在不同的化合物里有不同的化合价
2.同一化合物里同种元素 也可能有不同的化合价
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
