2014中考化学必考题眼检测
图片预览



文档简介
姓名 ☆ 2014中考化学必考“题眼”归类☆
1、必考固体(化学式)
红色固体: 、 蓝色沉淀: 红褐色沉淀: 黑色粉末: 、 、 、 、
白色沉淀: 、 、 、 、 、 白色固体: 、 、 、 、 、
2、有色溶液:① 浅绿色、 黄色、 蓝色。②紫色石蕊、无色酚酞
3、①不溶于稀硝酸的沉淀只有 、 。
②常见的可溶于稀硝酸也溶于稀盐酸的白色沉淀 、 、 、 。
③在某沉淀中加入稀硝酸,会有三种情况:
沉淀全部溶解,说明此沉淀中一定不含 和 。
沉淀不溶解,说明此沉淀中至少含 和 中的 种。
沉淀部分溶解,说明此沉淀中至少含BaSO4和AgCl中的 种,另外还含有其他的沉淀。
④在某溶液中加入BaCl2溶液,产生了不溶于稀硝酸的白色沉淀,说明此溶液中可能含有 ,也可能含有 。
⑤其他情况:
在某溶液中加入AgNO3溶液,产生了不溶于稀硝酸的白色沉淀,说明此溶液中含有 。
在某溶液中加入Ba(NO3)2溶液,产生了不溶于稀硝酸的白色沉淀,说明此溶液中含有 。)
在某溶液中加入稀盐酸无沉淀,加入BaCl2溶液产生了不溶于稀硝酸的白色沉淀,说明此溶液中一定含有 -。
①在某物质中加入酸溶液,产生了使澄清石灰水变浑浊的无色气体,说明此物质中一定含有 离子。
(CO32-检验试剂稀盐酸和澄清石灰水) 以上内容一定要会 灰常重要!
②在某物质中加入碱溶液,产生了使红色石蕊试纸变蓝色的气体(或有刺激性气味的气体,或其水溶液可以做氮肥的气体),此气体是氨气 ,说明此物质中一定含有 。(NH4+检验试剂是碱溶液和红色石蕊试纸)
5、在复分解反应中产生的气体,常见的有 和NH3。(某物质与其他物质反应若既有可能产生CO2,又有可能产生NH3,那么这种是NH4HCO3。)
6、* 一种气体与某溶液的反应,一般是非金属氧化物与碱溶液的反应,而最常见的是 与Ca(OH)2溶液或NaOH溶液的反应。SO2与NaON反应等。
7、①改良酸性土壤或处理酸量超标的工业废水用 石灰;②中和胃酸过多的一般用Mg(OH)2、Al(OH)3 、NaHCO3,
绝不能用 或Ca(OH)2(因为它们都有强烈的腐蚀性)。
一些国家正在试用碳酸水浇灌某些植物,其作用是促进植物的 合作用;在植物上方形成 室;调节土壤的
pH,改良 性土壤;提高农作物产量
8、①溶液呈蓝色,说明溶液中含有 (硫酸铜CuSO4、氯化铜CuCl2、硝酸铜);
②溶液呈黄色,说明溶液中含有 (硫酸铁Fe2(SO4)3、氯化铁FeCl3、硝酸铁);
③溶液呈浅绿色色,说明溶液中含有 (硫酸亚铁FeSO4、氯化亚铁FeCl2、硝酸亚铁);
④其他离子的溶液一般为无色。
说明
微溶不是沉淀 ,但量多了就沉淀 。
微溶时,溶解的是溶质,未溶解的是沉淀,
常见的微溶物有CaSO4、Ag2SO4、MgCO3、Ca(OH)2等。 一般难溶才打↓,一般不看做沉淀
9、单质铁与酸溶液或盐溶液的反应(置换反应),都生成 铁盐(即含Fe2+的盐)。
10、①无水硫酸铜为白色粉末,遇水(或水蒸气)变 色,常用于检验水分。
②澄清石灰水[Ca(OH)2]常用于检验 ,氢氧化钠NaOH溶液常用于吸收(或除去) 。
③常用作干燥剂的有 硫酸(液体)、固体 化钠NaOH、固体 化钙(生石灰CaO);
既要检验水又要检验其他气体,应把检验 的装置放在检验其他气体装置的前面;
既要吸收(除去)水,又要吸收(除去)其他气体杂质,应把除水装置放在除去其他气体装置的 面。
即气体的净化顺序:先除 ,后干燥。 气体的验证顺序:先验 ,后验气。
11、①淡蓝色火焰:氢气在空气中燃烧; ②蓝色火焰:一氧化碳、甲烷在空气中燃烧;
③白光:镁在空气中燃烧发出耀眼的白光;乙炔(C2H2)、蜡烛在氧气中燃烧发出白光。
12、常见气体的检验:
①能使带火星木条复燃的气体是 气; ②能使澄清石灰水变浑浊的气体是 化碳;
③溶于水呈碱性,且能使湿润的红色石蕊试纸变蓝的是 气的特性;
④在空气中燃烧产生淡蓝色火焰,且燃烧产物仅为水的是 气;⑤无色无味,能使人煤气中毒的是 氧化碳;
⑥具有刺激性气味的大气污染物是 氧化硫。
13、化学之最
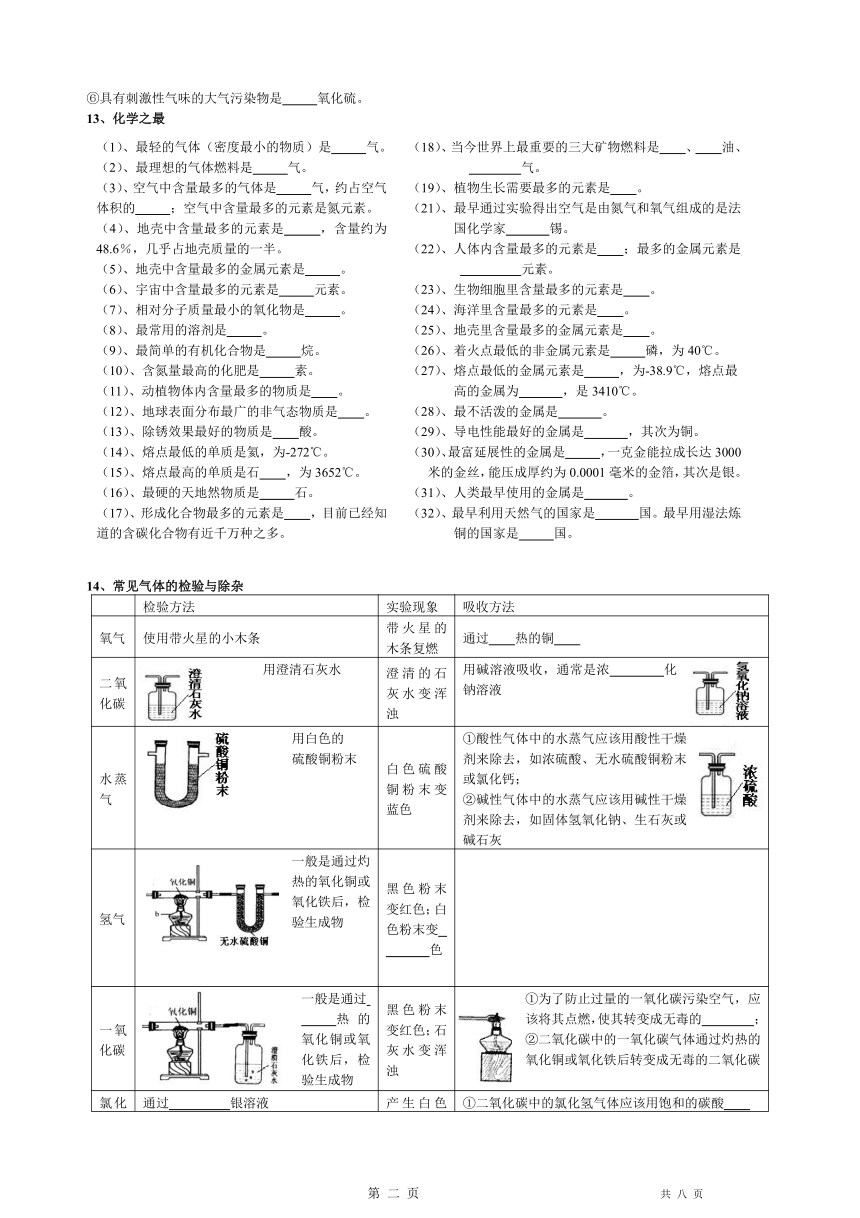
14、常见气体的检验与除杂
检验方法
实验现象
吸收方法
氧气
使用带火星的小木条
带火星的木条复燃
通过 热的铜
二氧化碳
用澄清石灰水
澄清的石灰水变浑浊
用碱溶液吸收,通常是浓 化钠溶液
水蒸气
用白色的
硫酸铜粉末
白色硫酸铜粉末变蓝色
①酸性气体中的水蒸气应该用酸性干燥剂来除去,如浓硫酸、无水硫酸铜粉末或氯化钙;
②碱性气体中的水蒸气应该用碱性干燥剂来除去,如固体氢氧化钠、生石灰或碱石灰
氢气
一般是通过灼热的氧化铜或氧化铁后,检验生成物
黑色粉末变红色;白色粉末变
色
一氧化碳
一般是通过
热的氧化铜或氧化铁后,检验生成物
黑色粉末变红色;石灰水变浑浊
①为了防止过量的一氧化碳污染空气,应该将其点燃,使其转变成无毒的 ;②二氧化碳中的一氧化碳气体通过灼热的氧化铜或氧化铁后转变成无毒的二氧化碳
氯化氢
通过 银溶液
产生白色沉淀
①二氧化碳中的氯化氢气体应该用饱和的碳酸
钠溶液或硝酸银溶液来除去;②氢气中的氯化氢气体应该用浓碱溶液(如氢氧化钠溶液)来除去
氨气
有刺激性气味,使用湿润的红色石蕊试纸
湿润的红色石蕊试纸变
色
用 或酸溶液吸收
15、常见离子的检验
常见阳离子的检验:
(1)、Mg2+:加入Na 溶液,生成白色沉淀〔Mg( )2〕。该沉淀能溶于盐酸
(2)、Al3+:加入Na 溶液,生成白色絮状沉淀,该沉淀能溶于盐酸。
(3)、Ba2+:加入稀 酸或可溶性 酸盐溶液,生成白色沉淀(BaSO4),该沉淀不溶于稀 酸。
(4)、Ag+:加入稀 酸或可溶性 酸盐,生成白色沉淀(AgCl),该沉淀不溶于稀 酸。
(5)、Fe3+:加入Na 溶液,生成红 色沉淀。该沉淀能溶于 酸
(6)、Cu2+:①加入Na 溶液,生成蓝色沉淀〔Cu( )2〕。 ②插入 片或锌片,有红色的铜析出。
(7)、NH4+:加入浓Na 溶液,加热,产生刺激性气味气体(NH3),该气体能使湿润的红色石蕊试纸变 。
(8)、H+:①加入锌或Na2 溶液,产生无色气体;②能使紫色石蕊试液、pH试纸变红。
常见阴离子的检验
(1)、OH-:能使无色酚酞、紫色石蕊等指示剂分别变为红色、蓝色;能使红色石蕊试纸、pH试纸变蓝。
(2)、SO42-:加入Ba 2溶液,生成白色沉淀(BaSO4),该沉淀不溶于稀 酸。
(3)、CO32-:①加入 Cl2或 Cl2溶液,生成白色沉淀(CaCO3或BaCO3),将沉淀溶于强酸,产生无色、无味的
气体(CO2),该气体能使澄清的石灰水变混浊。
②加入 酸,产生无色、无味的气体,该气体能使澄清的石灰水变浑浊。
(4)、Cl-:加入 溶液和稀 酸(Ag+起作用),生成白色沉淀,该沉淀不溶于稀 酸
16、离子的共存问题
离子的共存问题是中考化学的基础性考题,该类考题涉及到酸、碱、盐间相互反应的方方面面,可以说涉及面广、考查范围大,学生不易把握解题要点,常常感到思路模糊,不知从何处入手、分析和解答,现将有关知识结合和例题解释如下:
1、离子间不能共存的条件:
两种离子相互作用如果有水、气体或沉淀等物质生成,则这两种离子不能共存于同一溶液中。
初中化学阶段常见不共存离子如下:
(1)H+ + →H2O (2)H++ →CO2↑ (3)NH4++ →NH3↑
(4)Ba2++ →BaSO4 ↓ (5)Ag++ →AgCl ↓ (6)Ca2+ + →CaCO3 ↓
(7)Ba2++ →BaCO3 ↓ (8)Mg2++ →Mg(OH)2↓ (9)Cu2++ →Cu(OH)2↓
(10)Fe3++ →Fe(OH)3↓
2、不共存离子间相互反应所得产物的特征: * 判断依据 ,解题思路
(1)CO2通常情况下为使澄清的石灰水变 的无色气体;
(2)NH3通常情况下为无色有刺激性气味,且能使湿润的红色石蕊试纸变 的气体;
(3)AgCl、BaSO4二者均为 色沉淀,且不溶于稀 酸;
(4)CaCO3、BaCO3二者均为 色沉淀,且与盐酸(或稀硝酸)反应产生 气体;
(5)Mg(OH)2为 色沉淀,Fe(OH)3为红 色沉淀,Cu(OH)2为 色沉淀,三者均溶于 酸(或稀硝酸)。
17、常见物质的俗称与化学式
学名
俗名
化学式
学名
俗名
化学式
氧化钙
石灰
石墨
C
氢氧化钠
碱
碱、
性钠
Na
固体二氧化碳
CO2
碳酸钠
碱
、 打
Na2
氢氧化钙
石灰
石灰
Ca( )2
五水合
硫酸铜
胆矾、蓝矾
CuSO4·5H2O
碳酸氢钠
苏打
酸式碳酸钠
甲 烷
气
乙 酸
酸
乙 醇
精
铜 绿
碱式碳酸铜
Cu2(OH)2CO3
18、常见混合物中主要成分及其化学式
混合物
主要成分名称及化学式
混合物
主要成分名称及化学式
食 盐
氯化钠
铁 锈
氧化铁
大理石、石灰石、
鸡蛋壳、贝壳、珍珠
碳酸钙
天然气、沼 气
甲烷
澄清石灰水
氢氧化钙 溶液
石灰乳、石灰浆
生铁、钢
赤铁矿石
波尔多液
CuSO4和Ca(OH)2
氯化氢水溶液
酸、氢氯酸
爆鸣气
氢气和 气
工业用盐
亚硝酸钠
了解内容
微溶不是沉淀 ,但量多了就沉淀 。
微溶时,溶解的是溶质,未溶解的是沉淀,
常见的微溶物有CaSO4、Ag2SO4、MgCO3、Ca(OH)2等。
一般难溶才打↓,一般微溶不看做沉淀 。
参考答案
2013中考化学必考“题眼”归类
1、必考固体
红色固体:Cu(亮红或紫红色)、Fe2O3(棕红色)……红色粉末
蓝色沉淀:Cu(OH)2
红褐色沉淀:Fe(OH)3
黑色粉末:木炭粉C、CuO、MnO2、Fe3O4、铁粉(铁片铁丝为银白色)
白色沉淀:BaSO4、AgCl、CaCO3、BaCO3、Mg(OH)2、Al(OH)3
白色固体:MgO、P2O5、CaO、无水CuSO4;
铁、镁为银白色、汞(银白色液体)。
2、有色溶液:
①Fe2+(浅绿色)、Fe3+(黄色)、Cu2+(蓝色)
②紫色石蕊、无色酚酞
3、①不溶于稀硝酸的沉淀只有BaSO4、AgCl。
②常见的可溶于稀硝酸的白色沉淀CaCO3、BaCO3、Mg(OH)2、Al(OH)3,也能溶于稀盐酸。
③在某沉淀中加入稀硝酸,会有三种情况:
沉淀全部溶解,说明此沉淀中一定不含BaSO4和AgCl。
沉淀不溶解,说明此沉淀中至少含BaSO4和AgCl中的一种。
沉淀部分溶解,说明此沉淀中至少含BaSO4和AgCl中的一种,另外还含有其他的沉淀。
④在某溶液中加入BaCl2溶液,产生了不溶于稀硝酸的白色沉淀,说明此溶液中可能含有SO42-,也可能含有Ag+。
⑤其他情况:
在某溶液中加入AgNO3溶液,产生了不溶于稀硝酸的白色沉淀,说明此溶液中含有Cl-。
在某溶液中加入Ba(NO3)2溶液,产生了不溶于稀硝酸的白色沉淀,说明此溶液中含有SO42-。)
在某溶液中加入稀盐酸无沉淀,加入BaCl2溶液产生了不溶于稀硝酸的白色沉淀,说明此溶液中一定含有SO42-。
①在某物质中加入酸溶液,产生了使澄清石灰水变浑浊的无色气体,说明此物质中一定含有CO32-。
(CO32-检验试剂稀盐酸和澄清石灰水)
②在某物质中加入碱溶液,产生了使红色石蕊试纸变蓝色的气体(或有刺激性气味的气体,或其水溶液可以做氮肥的气体),此气体是氨气NH3,说明此物质中一定含有NH4+。(NH4+检验试剂是碱溶液和红色石蕊试纸)
5、在复分解反应中产生的气体常见的有CO2和NH3。(某物质与其他物质反应若既有可能产生CO2,又有可能产生NH3,那么这种是NH4HCO3。)
6、一种气体与某溶液的反应,一般是非金属氧化物与碱溶液的反应,而最常见的是CO2与Ca(OH)2溶液或NaOH溶液的反应。
7、①改良酸性土壤或处理酸量超标的工业废水用熟石灰;②中和胃酸过多的一般用Mg(OH)2、Al(OH)3 、NaHCO3,
绝不能用NaOH或Ca(OH)2(因为它们都有强烈的腐蚀性)。
8、①溶液呈蓝色,说明溶液中含有Cu2+(硫酸铜CuSO4、氯化铜CuCl2、硝酸铜);
②溶液呈黄色,说明溶液中含有Fe3+(硫酸铁Fe2(SO4)3、氯化铁FeCl3、硝酸铁);
③溶液呈浅绿色色,说明溶液中含有Fe2+(硫酸亚铁FeSO4、氯化亚铁FeCl2、硝酸亚铁);
④其他离子的溶液一般为无色。
了解内容
微溶不是沉淀 ,但量多了就沉淀 。
微溶时,溶解的是溶质,未溶解的是沉淀,
常见的微溶物有CaSO4、Ag2SO4、MgCO3、Ca(OH)2等。 一般难溶才打↓,一般不看做沉淀
9、单质铁与酸溶液或盐溶液的反应(置换反应),都生成亚铁盐(即含Fe2+的盐)。
10、①无水硫酸铜为白色粉末,遇水(或水蒸气)变蓝色,常用于检验水分。
②澄清石灰水[Ca(OH)2]常用于检验CO2,氢氧化钠NaOH溶液常用于吸收(或除去)CO2。
③常用作干燥剂的有浓硫酸(液体)、固体氢氧化钠NaOH、固体氧化钙(生石灰CaO);
既要检验水又要检验其他气体,应把检验水的装置放在检验其他气体装置的前面;
既要吸收(除去)水,又要吸收(除去)其他气体杂质,应把除水装置放在除去其他气体装置的后面。
即气体的净化顺序:先除杂,后干燥。 气体的验证顺序:先验水,后验气。
11、①淡蓝色火焰:氢气在空气中燃烧; ②蓝色火焰:一氧化碳、甲烷在空气中燃烧;
③白光:镁在空气中燃烧发出耀眼的白光;乙炔(C2H2)、蜡烛在氧气中燃烧发出白光。
12、常见气体的检验:
①能使带火星木条复燃的气体是氧气; ②能使澄清石灰水变浑浊的气体是二氧化碳;
③溶于水呈碱性,且能使湿润的红色石蕊试纸变蓝的氨气的特性;
④在空气中燃烧产生淡蓝色火焰,且燃烧产物仅为水石氢气;⑤无色无味,能使人煤气中毒的是一氧化碳;
⑥具有刺激性气味的大气污染物是二氧化硫。
13、化学之最
14、常见气体的检验与除杂
检验方法
实验现象
吸收方法
氧气
使用带火星的小木条
带火星的木条复燃
通过灼热的铜网
二氧化碳
用澄清石灰水
澄清的石灰水变浑浊
用碱溶液吸收,通常是浓氢氧化钠溶液
水蒸气
用白色的硫酸铜粉末
白色硫酸铜粉末变蓝色
①酸性气体中的水蒸气应该用酸性干燥剂来除去,如浓硫酸、无水硫酸铜粉末或氯化钙;
②碱性气体中的水蒸气应该用碱性干燥剂来除去,如固体氢氧化钠、生石灰或碱石灰
氢气
一般是通过灼热的氧化铜或氧化铁后,检验生成物
黑色粉末变红色;白色粉末变蓝色
一氧化碳
一般是通过灼热的氧化铜或氧化铁后,检验生成物
黑色粉末变红色;石灰水变浑浊
①为了防止过量的一氧化碳污染空气,应该将其点燃,使其转变成无毒的二氧化碳;②二氧化碳中的一氧化碳气体通过灼热的氧化铜或氧化铁后转变成无毒的二氧化碳
氯化氢
通过硝酸银溶液
产生白色沉淀
①二氧化碳中的氯化氢气体应该用饱和的碳酸氢钠溶液或硝酸银溶液来除去;②氢气中的氯化氢气体应该用浓碱溶液(如氢氧化钠溶液)来除去
氨气
有刺激性气味,使用湿润的红色石蕊试纸
湿润的红色石蕊试纸变蓝色
用水或酸溶液吸收
15、常见离子的检验
常见阳离子的检验:
(1)、Mg2+:加入NaOH溶液,生成白色沉淀〔Mg(OH)2〕。该沉淀能溶于盐酸
(2)、Al3+:加入NaOH溶液,生成白色絮状沉淀,该沉淀能溶于盐酸。
(3)、Ba2+:加入稀硫酸或可溶性硫酸盐溶液,生成白色沉淀(BaSO4),该沉淀不溶于稀硝酸。
(4)、Ag+:加入稀盐酸或可溶性盐酸盐,生成白色沉淀(AgCl),该沉淀不溶于稀硝酸。
(5)、Fe3+:加入NaOH溶液,生成红褐色沉淀。该沉淀能溶于盐酸
(6)、Cu2+:①加入NaOH溶液,生成蓝色沉淀〔Cu(OH)2〕。②插入铁片或锌片,有红色的铜析出。
(7)、NH4+:加入浓NaOH溶液,加热,产生刺激性气味气体(NH3),该气体能使湿润的红色石蕊试纸变蓝。
(8)、H+:①加入锌或Na2CO3溶液,产生无色气体;②能使紫色石蕊试液、pH试纸变红。
常见阴离子的检验
(1)、OH-:能使无色酚酞、紫色石蕊等指示剂分别变为红色、蓝色;能使红色石蕊试纸、pH试纸变蓝。
(2)、SO42-:加入BaCl2溶液,生成白色沉淀(BaSO4),该沉淀不溶于稀硝酸。
(3)、CO32-:①加入CaCl2或BaCl2溶液,生成白色沉淀(CaCO3或BaCO3),将沉淀溶于强酸,产生无色、无味的气体(CO2),该气体能使澄清的石灰水变混浊。②加入盐酸,产生无色、无味的气体,该气体能使澄清的石灰水变浑浊。
(4)、Cl-:加入AgNO3溶液和稀硝酸(Ag+起作用),生成白色沉淀,该沉淀不溶于稀硝酸
16、离子的共存问题
离子的共存问题是中考化学的基础性考题,该类考题涉及到酸、碱、盐间相互反应的方方面面,可以说涉及面广、考查范围大,学生不易把握解题要点,常常感到思路模糊,不知从何处入手、分析和解答,现将有关知识结合和例题解释如下:
1、离子间不能共存的条件:
两种离子相互作用如果有水、气体或沉淀等物质生成,则这两种离子不能共存于同一溶液中。
初中化学阶段常见不共存离子如下:
(1)H++OH-→H2O (2)H++CO32-→CO2↑ (3)NH4++OH-→NH3↑
(4)Ba2++SO42-→BaSO4 ↓ (5)Ag++Cl-→AgCl ↓ (6)Ca2++CO32-→CaCO3 ↓
(7)Ba2++CO32-→BaCO3 ↓ (8)Mg2++OH-→Mg(OH)2↓ (9)Cu2++OH-→Cu(OH)2↓
(10)Fe3++OH-→Fe(OH)3↓
2、不共存离子间相互反应所得产物的特征:
(1)CO2通常情况下为使澄清的石灰水变混浊的无色气体;
(2)NH3通常情况下为无色有刺激性气味,且能使湿润的红色石蕊试纸变蓝的气体;
(3)AgCl、BaSO4二者均为白色沉淀,且不溶于稀硝酸;
(4)CaCO3、BaCO3二者均为白色沉淀,且与盐酸(或稀硝酸)反应产生CO2气体;
(5)Mg(OH)2为白色沉淀,Fe(OH)3为红褐色沉淀,Cu(OH)2为蓝色沉淀,三者均溶于盐酸(或稀硝酸)。
17、常见物质的俗称与化学式
学名
俗名
化学式
学名
俗名
化学式
氧化钙
生石灰
CaO
石墨
C
氢氧化钠
烧碱、火碱、苛性钠
NaOH
固体二氧化碳
干冰
CO2
碳酸钠
纯碱、苏打
Na2CO3
氢氧化钙
熟石灰、消石灰
Ca(OH)2
五水合硫酸铜
胆矾、蓝矾
CuSO4·5H2O
碳酸氢钠
小苏打
酸式碳酸钠
NaHCO3
甲烷
沼气
CH4
乙酸
醋酸
CH3COOH
乙醇
酒精
C2H5OH
铜绿
碱式碳酸铜
Cu2(OH)2CO3
18、常见混合物中主要成分及其化学式
混合物
主要成分名称及化学式
混合物
主要成分名称及化学式
食盐
氯化钠NaCl
铁锈
氧化铁Fe2O3
大理石、石灰石、
鸡蛋壳、贝壳、珍珠
碳酸钙)CaCO3
天然气、沼气
甲烷CH4
澄清石灰水
氢氧化钙Ca(OH)2溶液
石灰乳、石灰浆
Ca(OH)2
生铁、钢
Fe
赤铁矿石
Fe2O3
波尔多液
CuSO4和Ca(OH)2
氯化氢水溶液
盐酸、氢氯酸 HCl
爆鸣气
氢气和氧气
工业用盐
亚硝酸钠NaNO2
了解内容
微溶不是沉淀 ,但量多了就沉淀 。
微溶时,溶解的是溶质,未溶解的是沉淀,
常见的微溶物有CaSO4、Ag2SO4、MgCO3、Ca(OH)2等。 一般难溶才打↓,一般不看做沉淀
1、必考固体(化学式)
红色固体: 、 蓝色沉淀: 红褐色沉淀: 黑色粉末: 、 、 、 、
白色沉淀: 、 、 、 、 、 白色固体: 、 、 、 、 、
2、有色溶液:① 浅绿色、 黄色、 蓝色。②紫色石蕊、无色酚酞
3、①不溶于稀硝酸的沉淀只有 、 。
②常见的可溶于稀硝酸也溶于稀盐酸的白色沉淀 、 、 、 。
③在某沉淀中加入稀硝酸,会有三种情况:
沉淀全部溶解,说明此沉淀中一定不含 和 。
沉淀不溶解,说明此沉淀中至少含 和 中的 种。
沉淀部分溶解,说明此沉淀中至少含BaSO4和AgCl中的 种,另外还含有其他的沉淀。
④在某溶液中加入BaCl2溶液,产生了不溶于稀硝酸的白色沉淀,说明此溶液中可能含有 ,也可能含有 。
⑤其他情况:
在某溶液中加入AgNO3溶液,产生了不溶于稀硝酸的白色沉淀,说明此溶液中含有 。
在某溶液中加入Ba(NO3)2溶液,产生了不溶于稀硝酸的白色沉淀,说明此溶液中含有 。)
在某溶液中加入稀盐酸无沉淀,加入BaCl2溶液产生了不溶于稀硝酸的白色沉淀,说明此溶液中一定含有 -。
①在某物质中加入酸溶液,产生了使澄清石灰水变浑浊的无色气体,说明此物质中一定含有 离子。
(CO32-检验试剂稀盐酸和澄清石灰水) 以上内容一定要会 灰常重要!
②在某物质中加入碱溶液,产生了使红色石蕊试纸变蓝色的气体(或有刺激性气味的气体,或其水溶液可以做氮肥的气体),此气体是氨气 ,说明此物质中一定含有 。(NH4+检验试剂是碱溶液和红色石蕊试纸)
5、在复分解反应中产生的气体,常见的有 和NH3。(某物质与其他物质反应若既有可能产生CO2,又有可能产生NH3,那么这种是NH4HCO3。)
6、* 一种气体与某溶液的反应,一般是非金属氧化物与碱溶液的反应,而最常见的是 与Ca(OH)2溶液或NaOH溶液的反应。SO2与NaON反应等。
7、①改良酸性土壤或处理酸量超标的工业废水用 石灰;②中和胃酸过多的一般用Mg(OH)2、Al(OH)3 、NaHCO3,
绝不能用 或Ca(OH)2(因为它们都有强烈的腐蚀性)。
一些国家正在试用碳酸水浇灌某些植物,其作用是促进植物的 合作用;在植物上方形成 室;调节土壤的
pH,改良 性土壤;提高农作物产量
8、①溶液呈蓝色,说明溶液中含有 (硫酸铜CuSO4、氯化铜CuCl2、硝酸铜);
②溶液呈黄色,说明溶液中含有 (硫酸铁Fe2(SO4)3、氯化铁FeCl3、硝酸铁);
③溶液呈浅绿色色,说明溶液中含有 (硫酸亚铁FeSO4、氯化亚铁FeCl2、硝酸亚铁);
④其他离子的溶液一般为无色。
说明
微溶不是沉淀 ,但量多了就沉淀 。
微溶时,溶解的是溶质,未溶解的是沉淀,
常见的微溶物有CaSO4、Ag2SO4、MgCO3、Ca(OH)2等。 一般难溶才打↓,一般不看做沉淀
9、单质铁与酸溶液或盐溶液的反应(置换反应),都生成 铁盐(即含Fe2+的盐)。
10、①无水硫酸铜为白色粉末,遇水(或水蒸气)变 色,常用于检验水分。
②澄清石灰水[Ca(OH)2]常用于检验 ,氢氧化钠NaOH溶液常用于吸收(或除去) 。
③常用作干燥剂的有 硫酸(液体)、固体 化钠NaOH、固体 化钙(生石灰CaO);
既要检验水又要检验其他气体,应把检验 的装置放在检验其他气体装置的前面;
既要吸收(除去)水,又要吸收(除去)其他气体杂质,应把除水装置放在除去其他气体装置的 面。
即气体的净化顺序:先除 ,后干燥。 气体的验证顺序:先验 ,后验气。
11、①淡蓝色火焰:氢气在空气中燃烧; ②蓝色火焰:一氧化碳、甲烷在空气中燃烧;
③白光:镁在空气中燃烧发出耀眼的白光;乙炔(C2H2)、蜡烛在氧气中燃烧发出白光。
12、常见气体的检验:
①能使带火星木条复燃的气体是 气; ②能使澄清石灰水变浑浊的气体是 化碳;
③溶于水呈碱性,且能使湿润的红色石蕊试纸变蓝的是 气的特性;
④在空气中燃烧产生淡蓝色火焰,且燃烧产物仅为水的是 气;⑤无色无味,能使人煤气中毒的是 氧化碳;
⑥具有刺激性气味的大气污染物是 氧化硫。
13、化学之最
14、常见气体的检验与除杂
检验方法
实验现象
吸收方法
氧气
使用带火星的小木条
带火星的木条复燃
通过 热的铜
二氧化碳
用澄清石灰水
澄清的石灰水变浑浊
用碱溶液吸收,通常是浓 化钠溶液
水蒸气
用白色的
硫酸铜粉末
白色硫酸铜粉末变蓝色
①酸性气体中的水蒸气应该用酸性干燥剂来除去,如浓硫酸、无水硫酸铜粉末或氯化钙;
②碱性气体中的水蒸气应该用碱性干燥剂来除去,如固体氢氧化钠、生石灰或碱石灰
氢气
一般是通过灼热的氧化铜或氧化铁后,检验生成物
黑色粉末变红色;白色粉末变
色
一氧化碳
一般是通过
热的氧化铜或氧化铁后,检验生成物
黑色粉末变红色;石灰水变浑浊
①为了防止过量的一氧化碳污染空气,应该将其点燃,使其转变成无毒的 ;②二氧化碳中的一氧化碳气体通过灼热的氧化铜或氧化铁后转变成无毒的二氧化碳
氯化氢
通过 银溶液
产生白色沉淀
①二氧化碳中的氯化氢气体应该用饱和的碳酸
钠溶液或硝酸银溶液来除去;②氢气中的氯化氢气体应该用浓碱溶液(如氢氧化钠溶液)来除去
氨气
有刺激性气味,使用湿润的红色石蕊试纸
湿润的红色石蕊试纸变
色
用 或酸溶液吸收
15、常见离子的检验
常见阳离子的检验:
(1)、Mg2+:加入Na 溶液,生成白色沉淀〔Mg( )2〕。该沉淀能溶于盐酸
(2)、Al3+:加入Na 溶液,生成白色絮状沉淀,该沉淀能溶于盐酸。
(3)、Ba2+:加入稀 酸或可溶性 酸盐溶液,生成白色沉淀(BaSO4),该沉淀不溶于稀 酸。
(4)、Ag+:加入稀 酸或可溶性 酸盐,生成白色沉淀(AgCl),该沉淀不溶于稀 酸。
(5)、Fe3+:加入Na 溶液,生成红 色沉淀。该沉淀能溶于 酸
(6)、Cu2+:①加入Na 溶液,生成蓝色沉淀〔Cu( )2〕。 ②插入 片或锌片,有红色的铜析出。
(7)、NH4+:加入浓Na 溶液,加热,产生刺激性气味气体(NH3),该气体能使湿润的红色石蕊试纸变 。
(8)、H+:①加入锌或Na2 溶液,产生无色气体;②能使紫色石蕊试液、pH试纸变红。
常见阴离子的检验
(1)、OH-:能使无色酚酞、紫色石蕊等指示剂分别变为红色、蓝色;能使红色石蕊试纸、pH试纸变蓝。
(2)、SO42-:加入Ba 2溶液,生成白色沉淀(BaSO4),该沉淀不溶于稀 酸。
(3)、CO32-:①加入 Cl2或 Cl2溶液,生成白色沉淀(CaCO3或BaCO3),将沉淀溶于强酸,产生无色、无味的
气体(CO2),该气体能使澄清的石灰水变混浊。
②加入 酸,产生无色、无味的气体,该气体能使澄清的石灰水变浑浊。
(4)、Cl-:加入 溶液和稀 酸(Ag+起作用),生成白色沉淀,该沉淀不溶于稀 酸
16、离子的共存问题
离子的共存问题是中考化学的基础性考题,该类考题涉及到酸、碱、盐间相互反应的方方面面,可以说涉及面广、考查范围大,学生不易把握解题要点,常常感到思路模糊,不知从何处入手、分析和解答,现将有关知识结合和例题解释如下:
1、离子间不能共存的条件:
两种离子相互作用如果有水、气体或沉淀等物质生成,则这两种离子不能共存于同一溶液中。
初中化学阶段常见不共存离子如下:
(1)H+ + →H2O (2)H++ →CO2↑ (3)NH4++ →NH3↑
(4)Ba2++ →BaSO4 ↓ (5)Ag++ →AgCl ↓ (6)Ca2+ + →CaCO3 ↓
(7)Ba2++ →BaCO3 ↓ (8)Mg2++ →Mg(OH)2↓ (9)Cu2++ →Cu(OH)2↓
(10)Fe3++ →Fe(OH)3↓
2、不共存离子间相互反应所得产物的特征: * 判断依据 ,解题思路
(1)CO2通常情况下为使澄清的石灰水变 的无色气体;
(2)NH3通常情况下为无色有刺激性气味,且能使湿润的红色石蕊试纸变 的气体;
(3)AgCl、BaSO4二者均为 色沉淀,且不溶于稀 酸;
(4)CaCO3、BaCO3二者均为 色沉淀,且与盐酸(或稀硝酸)反应产生 气体;
(5)Mg(OH)2为 色沉淀,Fe(OH)3为红 色沉淀,Cu(OH)2为 色沉淀,三者均溶于 酸(或稀硝酸)。
17、常见物质的俗称与化学式
学名
俗名
化学式
学名
俗名
化学式
氧化钙
石灰
石墨
C
氢氧化钠
碱
碱、
性钠
Na
固体二氧化碳
CO2
碳酸钠
碱
、 打
Na2
氢氧化钙
石灰
石灰
Ca( )2
五水合
硫酸铜
胆矾、蓝矾
CuSO4·5H2O
碳酸氢钠
苏打
酸式碳酸钠
甲 烷
气
乙 酸
酸
乙 醇
精
铜 绿
碱式碳酸铜
Cu2(OH)2CO3
18、常见混合物中主要成分及其化学式
混合物
主要成分名称及化学式
混合物
主要成分名称及化学式
食 盐
氯化钠
铁 锈
氧化铁
大理石、石灰石、
鸡蛋壳、贝壳、珍珠
碳酸钙
天然气、沼 气
甲烷
澄清石灰水
氢氧化钙 溶液
石灰乳、石灰浆
生铁、钢
赤铁矿石
波尔多液
CuSO4和Ca(OH)2
氯化氢水溶液
酸、氢氯酸
爆鸣气
氢气和 气
工业用盐
亚硝酸钠
了解内容
微溶不是沉淀 ,但量多了就沉淀 。
微溶时,溶解的是溶质,未溶解的是沉淀,
常见的微溶物有CaSO4、Ag2SO4、MgCO3、Ca(OH)2等。
一般难溶才打↓,一般微溶不看做沉淀 。
参考答案
2013中考化学必考“题眼”归类
1、必考固体
红色固体:Cu(亮红或紫红色)、Fe2O3(棕红色)……红色粉末
蓝色沉淀:Cu(OH)2
红褐色沉淀:Fe(OH)3
黑色粉末:木炭粉C、CuO、MnO2、Fe3O4、铁粉(铁片铁丝为银白色)
白色沉淀:BaSO4、AgCl、CaCO3、BaCO3、Mg(OH)2、Al(OH)3
白色固体:MgO、P2O5、CaO、无水CuSO4;
铁、镁为银白色、汞(银白色液体)。
2、有色溶液:
①Fe2+(浅绿色)、Fe3+(黄色)、Cu2+(蓝色)
②紫色石蕊、无色酚酞
3、①不溶于稀硝酸的沉淀只有BaSO4、AgCl。
②常见的可溶于稀硝酸的白色沉淀CaCO3、BaCO3、Mg(OH)2、Al(OH)3,也能溶于稀盐酸。
③在某沉淀中加入稀硝酸,会有三种情况:
沉淀全部溶解,说明此沉淀中一定不含BaSO4和AgCl。
沉淀不溶解,说明此沉淀中至少含BaSO4和AgCl中的一种。
沉淀部分溶解,说明此沉淀中至少含BaSO4和AgCl中的一种,另外还含有其他的沉淀。
④在某溶液中加入BaCl2溶液,产生了不溶于稀硝酸的白色沉淀,说明此溶液中可能含有SO42-,也可能含有Ag+。
⑤其他情况:
在某溶液中加入AgNO3溶液,产生了不溶于稀硝酸的白色沉淀,说明此溶液中含有Cl-。
在某溶液中加入Ba(NO3)2溶液,产生了不溶于稀硝酸的白色沉淀,说明此溶液中含有SO42-。)
在某溶液中加入稀盐酸无沉淀,加入BaCl2溶液产生了不溶于稀硝酸的白色沉淀,说明此溶液中一定含有SO42-。
①在某物质中加入酸溶液,产生了使澄清石灰水变浑浊的无色气体,说明此物质中一定含有CO32-。
(CO32-检验试剂稀盐酸和澄清石灰水)
②在某物质中加入碱溶液,产生了使红色石蕊试纸变蓝色的气体(或有刺激性气味的气体,或其水溶液可以做氮肥的气体),此气体是氨气NH3,说明此物质中一定含有NH4+。(NH4+检验试剂是碱溶液和红色石蕊试纸)
5、在复分解反应中产生的气体常见的有CO2和NH3。(某物质与其他物质反应若既有可能产生CO2,又有可能产生NH3,那么这种是NH4HCO3。)
6、一种气体与某溶液的反应,一般是非金属氧化物与碱溶液的反应,而最常见的是CO2与Ca(OH)2溶液或NaOH溶液的反应。
7、①改良酸性土壤或处理酸量超标的工业废水用熟石灰;②中和胃酸过多的一般用Mg(OH)2、Al(OH)3 、NaHCO3,
绝不能用NaOH或Ca(OH)2(因为它们都有强烈的腐蚀性)。
8、①溶液呈蓝色,说明溶液中含有Cu2+(硫酸铜CuSO4、氯化铜CuCl2、硝酸铜);
②溶液呈黄色,说明溶液中含有Fe3+(硫酸铁Fe2(SO4)3、氯化铁FeCl3、硝酸铁);
③溶液呈浅绿色色,说明溶液中含有Fe2+(硫酸亚铁FeSO4、氯化亚铁FeCl2、硝酸亚铁);
④其他离子的溶液一般为无色。
了解内容
微溶不是沉淀 ,但量多了就沉淀 。
微溶时,溶解的是溶质,未溶解的是沉淀,
常见的微溶物有CaSO4、Ag2SO4、MgCO3、Ca(OH)2等。 一般难溶才打↓,一般不看做沉淀
9、单质铁与酸溶液或盐溶液的反应(置换反应),都生成亚铁盐(即含Fe2+的盐)。
10、①无水硫酸铜为白色粉末,遇水(或水蒸气)变蓝色,常用于检验水分。
②澄清石灰水[Ca(OH)2]常用于检验CO2,氢氧化钠NaOH溶液常用于吸收(或除去)CO2。
③常用作干燥剂的有浓硫酸(液体)、固体氢氧化钠NaOH、固体氧化钙(生石灰CaO);
既要检验水又要检验其他气体,应把检验水的装置放在检验其他气体装置的前面;
既要吸收(除去)水,又要吸收(除去)其他气体杂质,应把除水装置放在除去其他气体装置的后面。
即气体的净化顺序:先除杂,后干燥。 气体的验证顺序:先验水,后验气。
11、①淡蓝色火焰:氢气在空气中燃烧; ②蓝色火焰:一氧化碳、甲烷在空气中燃烧;
③白光:镁在空气中燃烧发出耀眼的白光;乙炔(C2H2)、蜡烛在氧气中燃烧发出白光。
12、常见气体的检验:
①能使带火星木条复燃的气体是氧气; ②能使澄清石灰水变浑浊的气体是二氧化碳;
③溶于水呈碱性,且能使湿润的红色石蕊试纸变蓝的氨气的特性;
④在空气中燃烧产生淡蓝色火焰,且燃烧产物仅为水石氢气;⑤无色无味,能使人煤气中毒的是一氧化碳;
⑥具有刺激性气味的大气污染物是二氧化硫。
13、化学之最
14、常见气体的检验与除杂
检验方法
实验现象
吸收方法
氧气
使用带火星的小木条
带火星的木条复燃
通过灼热的铜网
二氧化碳
用澄清石灰水
澄清的石灰水变浑浊
用碱溶液吸收,通常是浓氢氧化钠溶液
水蒸气
用白色的硫酸铜粉末
白色硫酸铜粉末变蓝色
①酸性气体中的水蒸气应该用酸性干燥剂来除去,如浓硫酸、无水硫酸铜粉末或氯化钙;
②碱性气体中的水蒸气应该用碱性干燥剂来除去,如固体氢氧化钠、生石灰或碱石灰
氢气
一般是通过灼热的氧化铜或氧化铁后,检验生成物
黑色粉末变红色;白色粉末变蓝色
一氧化碳
一般是通过灼热的氧化铜或氧化铁后,检验生成物
黑色粉末变红色;石灰水变浑浊
①为了防止过量的一氧化碳污染空气,应该将其点燃,使其转变成无毒的二氧化碳;②二氧化碳中的一氧化碳气体通过灼热的氧化铜或氧化铁后转变成无毒的二氧化碳
氯化氢
通过硝酸银溶液
产生白色沉淀
①二氧化碳中的氯化氢气体应该用饱和的碳酸氢钠溶液或硝酸银溶液来除去;②氢气中的氯化氢气体应该用浓碱溶液(如氢氧化钠溶液)来除去
氨气
有刺激性气味,使用湿润的红色石蕊试纸
湿润的红色石蕊试纸变蓝色
用水或酸溶液吸收
15、常见离子的检验
常见阳离子的检验:
(1)、Mg2+:加入NaOH溶液,生成白色沉淀〔Mg(OH)2〕。该沉淀能溶于盐酸
(2)、Al3+:加入NaOH溶液,生成白色絮状沉淀,该沉淀能溶于盐酸。
(3)、Ba2+:加入稀硫酸或可溶性硫酸盐溶液,生成白色沉淀(BaSO4),该沉淀不溶于稀硝酸。
(4)、Ag+:加入稀盐酸或可溶性盐酸盐,生成白色沉淀(AgCl),该沉淀不溶于稀硝酸。
(5)、Fe3+:加入NaOH溶液,生成红褐色沉淀。该沉淀能溶于盐酸
(6)、Cu2+:①加入NaOH溶液,生成蓝色沉淀〔Cu(OH)2〕。②插入铁片或锌片,有红色的铜析出。
(7)、NH4+:加入浓NaOH溶液,加热,产生刺激性气味气体(NH3),该气体能使湿润的红色石蕊试纸变蓝。
(8)、H+:①加入锌或Na2CO3溶液,产生无色气体;②能使紫色石蕊试液、pH试纸变红。
常见阴离子的检验
(1)、OH-:能使无色酚酞、紫色石蕊等指示剂分别变为红色、蓝色;能使红色石蕊试纸、pH试纸变蓝。
(2)、SO42-:加入BaCl2溶液,生成白色沉淀(BaSO4),该沉淀不溶于稀硝酸。
(3)、CO32-:①加入CaCl2或BaCl2溶液,生成白色沉淀(CaCO3或BaCO3),将沉淀溶于强酸,产生无色、无味的气体(CO2),该气体能使澄清的石灰水变混浊。②加入盐酸,产生无色、无味的气体,该气体能使澄清的石灰水变浑浊。
(4)、Cl-:加入AgNO3溶液和稀硝酸(Ag+起作用),生成白色沉淀,该沉淀不溶于稀硝酸
16、离子的共存问题
离子的共存问题是中考化学的基础性考题,该类考题涉及到酸、碱、盐间相互反应的方方面面,可以说涉及面广、考查范围大,学生不易把握解题要点,常常感到思路模糊,不知从何处入手、分析和解答,现将有关知识结合和例题解释如下:
1、离子间不能共存的条件:
两种离子相互作用如果有水、气体或沉淀等物质生成,则这两种离子不能共存于同一溶液中。
初中化学阶段常见不共存离子如下:
(1)H++OH-→H2O (2)H++CO32-→CO2↑ (3)NH4++OH-→NH3↑
(4)Ba2++SO42-→BaSO4 ↓ (5)Ag++Cl-→AgCl ↓ (6)Ca2++CO32-→CaCO3 ↓
(7)Ba2++CO32-→BaCO3 ↓ (8)Mg2++OH-→Mg(OH)2↓ (9)Cu2++OH-→Cu(OH)2↓
(10)Fe3++OH-→Fe(OH)3↓
2、不共存离子间相互反应所得产物的特征:
(1)CO2通常情况下为使澄清的石灰水变混浊的无色气体;
(2)NH3通常情况下为无色有刺激性气味,且能使湿润的红色石蕊试纸变蓝的气体;
(3)AgCl、BaSO4二者均为白色沉淀,且不溶于稀硝酸;
(4)CaCO3、BaCO3二者均为白色沉淀,且与盐酸(或稀硝酸)反应产生CO2气体;
(5)Mg(OH)2为白色沉淀,Fe(OH)3为红褐色沉淀,Cu(OH)2为蓝色沉淀,三者均溶于盐酸(或稀硝酸)。
17、常见物质的俗称与化学式
学名
俗名
化学式
学名
俗名
化学式
氧化钙
生石灰
CaO
石墨
C
氢氧化钠
烧碱、火碱、苛性钠
NaOH
固体二氧化碳
干冰
CO2
碳酸钠
纯碱、苏打
Na2CO3
氢氧化钙
熟石灰、消石灰
Ca(OH)2
五水合硫酸铜
胆矾、蓝矾
CuSO4·5H2O
碳酸氢钠
小苏打
酸式碳酸钠
NaHCO3
甲烷
沼气
CH4
乙酸
醋酸
CH3COOH
乙醇
酒精
C2H5OH
铜绿
碱式碳酸铜
Cu2(OH)2CO3
18、常见混合物中主要成分及其化学式
混合物
主要成分名称及化学式
混合物
主要成分名称及化学式
食盐
氯化钠NaCl
铁锈
氧化铁Fe2O3
大理石、石灰石、
鸡蛋壳、贝壳、珍珠
碳酸钙)CaCO3
天然气、沼气
甲烷CH4
澄清石灰水
氢氧化钙Ca(OH)2溶液
石灰乳、石灰浆
Ca(OH)2
生铁、钢
Fe
赤铁矿石
Fe2O3
波尔多液
CuSO4和Ca(OH)2
氯化氢水溶液
盐酸、氢氯酸 HCl
爆鸣气
氢气和氧气
工业用盐
亚硝酸钠NaNO2
了解内容
微溶不是沉淀 ,但量多了就沉淀 。
微溶时,溶解的是溶质,未溶解的是沉淀,
常见的微溶物有CaSO4、Ag2SO4、MgCO3、Ca(OH)2等。 一般难溶才打↓,一般不看做沉淀
