人教版九年级化学上册实验专练(10)实验室制取二氧化碳(含解析)
文档属性
| 名称 | 人教版九年级化学上册实验专练(10)实验室制取二氧化碳(含解析) |
|
|
| 格式 | docx | ||
| 文件大小 | 216.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-31 00:00:00 | ||
图片预览

文档简介
(10)实验室制取二氧化碳
课本实验再现
1、药品:稀盐酸与石灰石(或大理石)
2、反应原理:CaCO3+2HCl=CaCl2+H2O+CO2↑
易错提示:
①不能选用浓盐酸,因浓盐酸挥发性太强,能挥发出大量的氯化氢气体,使制得的二氧化碳不纯;
②不能选用稀硫酸,因稀硫酸与碳酸钙反应生成微溶性的硫酸钙,覆盖在石灰石(或大理石)的表面,会阻止反应继续进行;
③不能选用碳酸钠、碳酸钾粉末代替大理石或石灰石,因为它们易溶于水,反应速率快,不易控制,难以收集。
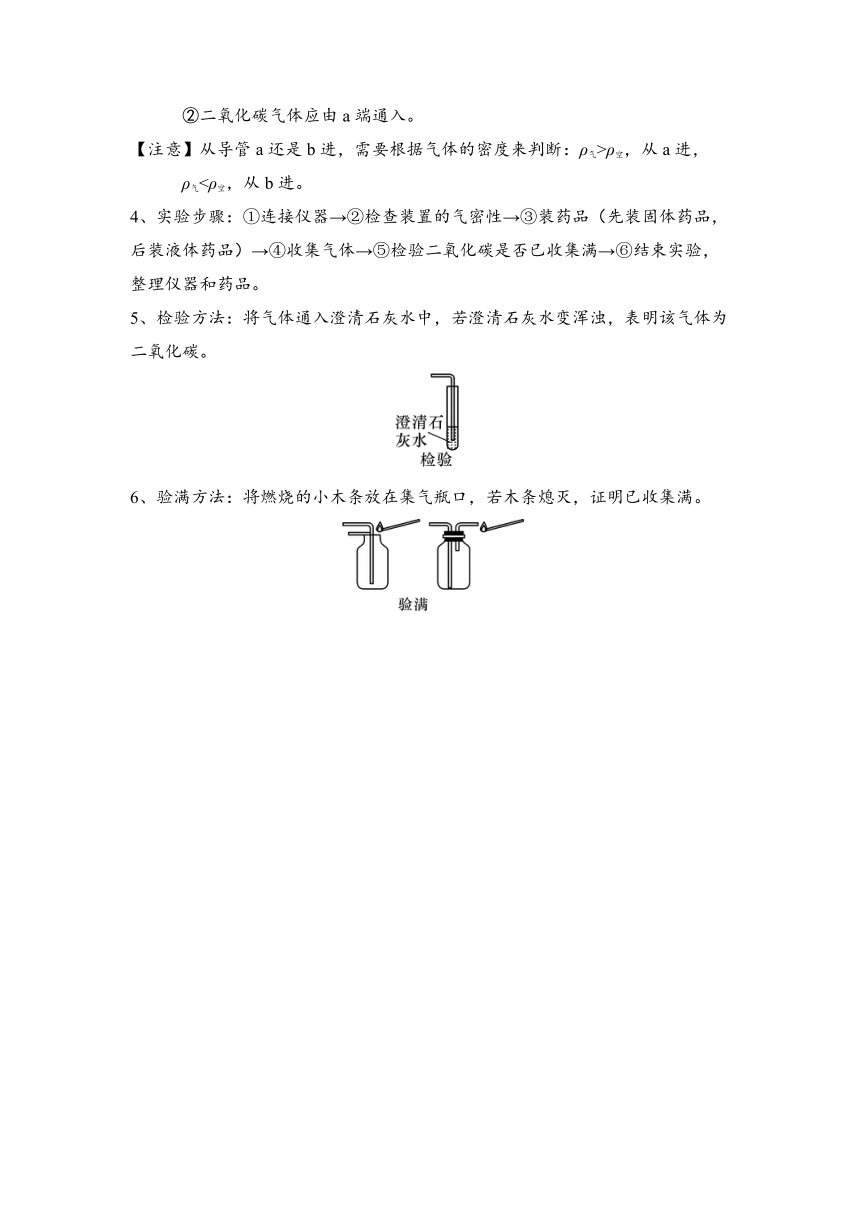
3、实验装置
(1)发生装置:固液常温型
实验装置 A B C D
装置 优点 安装简单 便于添加液体 能控制 反应速率 可随时控制反应的发生和停止
注意事项 ①以上装置中导管均需刚露出橡胶塞即可,否则不利于气体导出;②B、D装置中长颈漏斗末端必须伸入液面以下,形成液封,防止生成的气体从长颈漏斗的上端逸出。
(2)收集装置:二氧化碳能溶于水,且密度比空气大。
①收集时,导管的下端要伸至集气瓶底部,以便排尽空气;
②二氧化碳气体应由a端通入。
【注意】从导管a还是b进,需要根据气体的密度来判断:ρ气>ρ空,从a进,
ρ气<ρ空,从b进。
4、实验步骤:①连接仪器→②检查装置的气密性→③装药品(先装固体药品,后装液体药品)→④收集气体→⑤检验二氧化碳是否已收集满→⑥结束实验,整理仪器和药品。
5、检验方法:将气体通入澄清石灰水中,若澄清石灰水变浑浊,表明该气体为二氧化碳。
6、验满方法:将燃烧的小木条放在集气瓶口,若木条熄灭,证明已收集满。
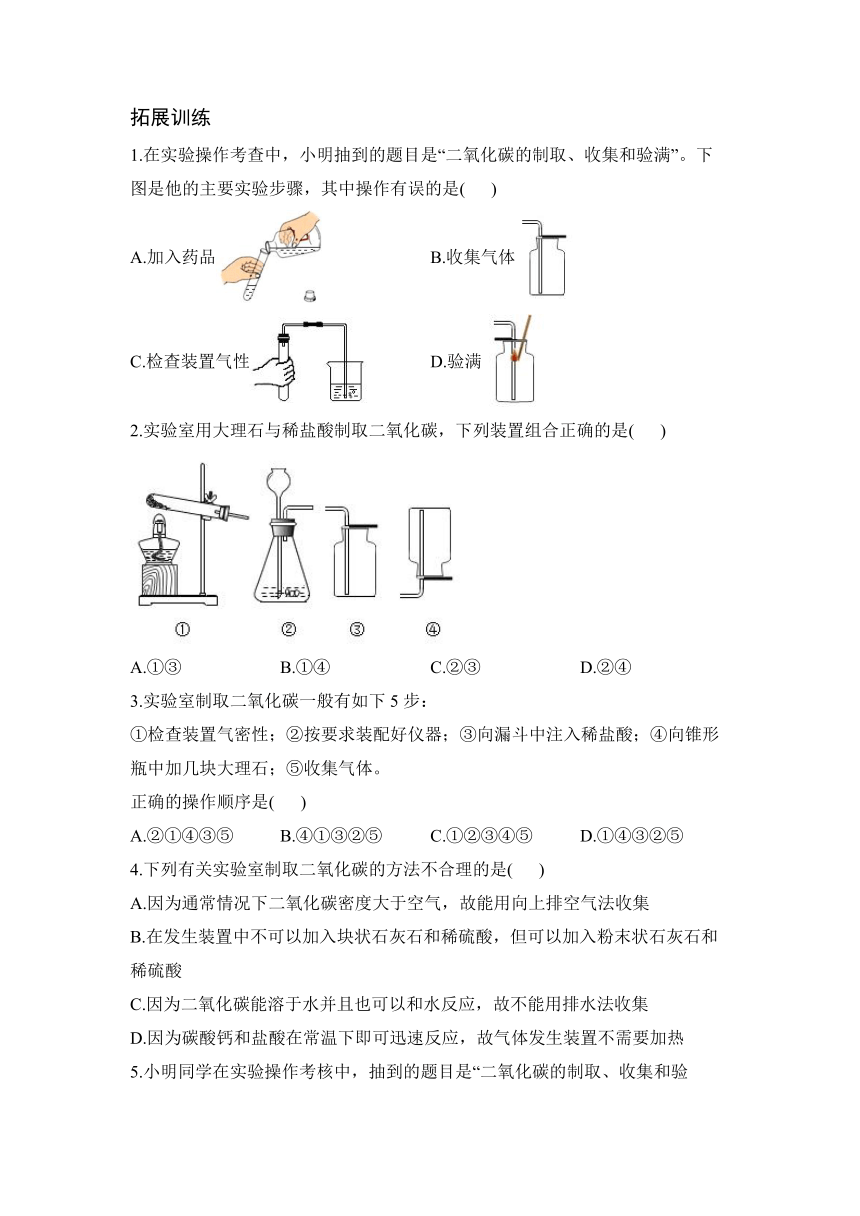
拓展训练
1.在实验操作考查中,小明抽到的题目是“二氧化碳的制取、收集和验满”。下图是他的主要实验步骤,其中操作有误的是( )
A.加入药品 B.收集气体
C.检查装置气性 D.验满
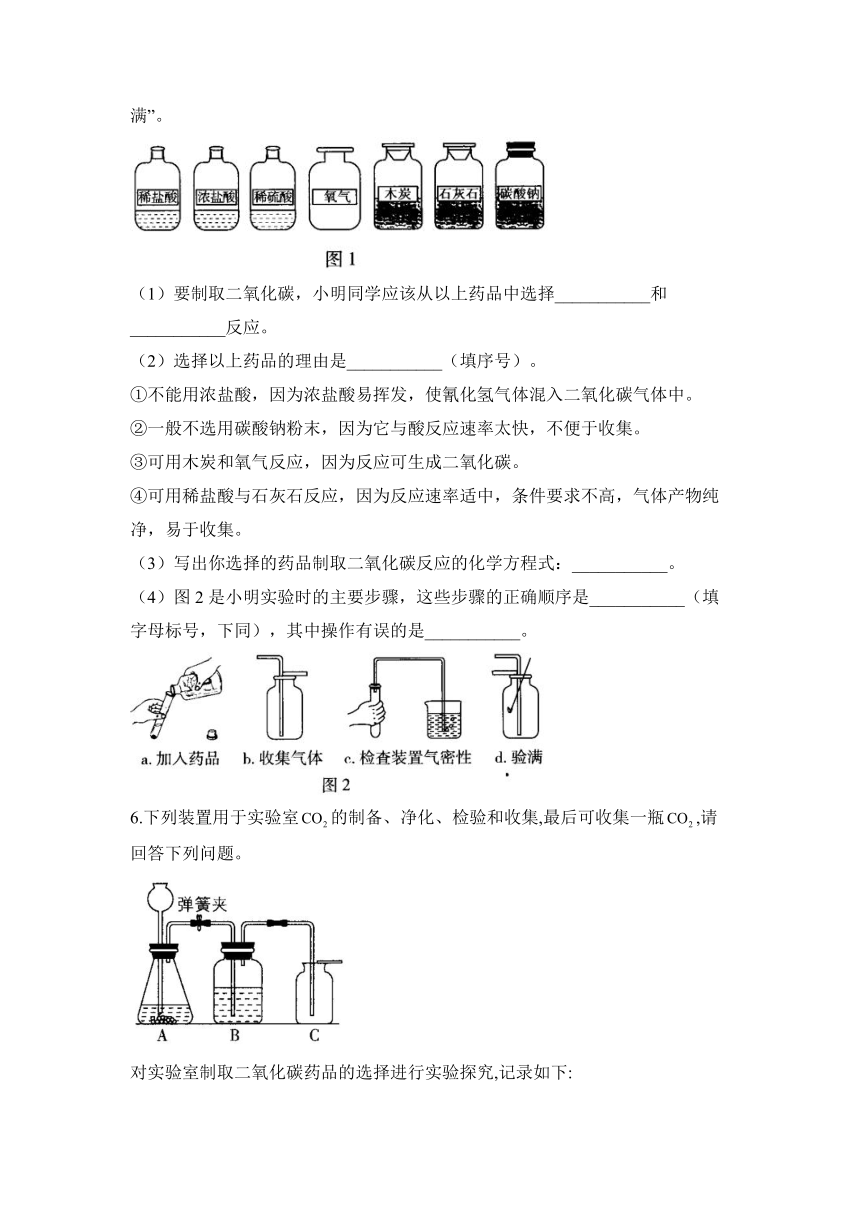
2.实验室用大理石与稀盐酸制取二氧化碳,下列装置组合正确的是( )
A.①③ B.①④ C.②③ D.②④
3.实验室制取二氧化碳一般有如下5步:
①检查装置气密性;②按要求装配好仪器;③向漏斗中注入稀盐酸;④向锥形瓶中加几块大理石;⑤收集气体。
正确的操作顺序是( )
A.②①④③⑤ B.④①③②⑤ C.①②③④⑤ D.①④③②⑤
4.下列有关实验室制取二氧化碳的方法不合理的是( )
A.因为通常情况下二氧化碳密度大于空气,故能用向上排空气法收集
B.在发生装置中不可以加入块状石灰石和稀硫酸,但可以加入粉末状石灰石和稀硫酸
C.因为二氧化碳能溶于水并且也可以和水反应,故不能用排水法收集
D.因为碳酸钙和盐酸在常温下即可迅速反应,故气体发生装置不需要加热
5.小明同学在实验操作考核中,抽到的题目是“二氧化碳的制取、收集和验满”。
(1)要制取二氧化碳,小明同学应该从以上药品中选择___________和___________反应。
(2)选择以上药品的理由是___________(填序号)。
①不能用浓盐酸,因为浓盐酸易挥发,使氰化氢气体混入二氧化碳气体中。
②一般不选用碳酸钠粉末,因为它与酸反应速率太快,不便于收集。
③可用木炭和氧气反应,因为反应可生成二氧化碳。
④可用稀盐酸与石灰石反应,因为反应速率适中,条件要求不高,气体产物纯净,易于收集。
(3)写出你选择的药品制取二氧化碳反应的化学方程式:___________。
(4)图2是小明实验时的主要步骤,这些步骤的正确顺序是___________(填字母标号,下同),其中操作有误的是___________。
6.下列装置用于实验室的制备、净化、检验和收集,最后可收集一瓶,请回答下列问题。
对实验室制取二氧化碳药品的选择进行实验探究,记录如下:
组别 药品 实验现象
① 碳酸钠粉末和稀盐酸 产生气泡速率很快
② 块状石灰石和稀硫酸 产生气泡速率缓慢并逐渐停止
③ 块状石灰石和稀盐酸 产生气泡速率适中
(1)从制取和收集的角度分析,一般选择第__________(填序号)组药品,所发生反应的化学方程式为________________________________。
(2)B装置用于检验二氧化碳气体,则B中所盛放的物质是__________,发生反应的化学方程式是________________________________。
(3)反应过程中将弹簧夹关闭,在A中观察到的现象是_______________。
(4)C中的收集方法说明二氧化碳具有的物理性质是_____________________。
7.如图为实验室常用仪器或装置,请回答以下问题:
(1)仪器a的名称是__________,实验时使用它的优点是____________;实验室制取时,应选择的发生装置是________(填字母,下同),收集装置是________,实验室制取的原理是__________(写化学方程式)。
(2)实验室制取时,不能用浓盐酸,原因是__________。
(3)的验满方法是___________。
(4)B装置除了实验室制取外,还能用来制取的气体是_________。
(5)制取时可选用如图G、H两种仪器代替仪器a,选用这两种仪器的优点是_____________。
8.某研究小组在实验室制取二氧化碳的研究中发现,通常不选用大理石与稀硫酸反应制取二氧化碳,其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止.为此,该小组设立研究课题:选择合适浓度的硫酸和适当的反应温度制取二氧化碳.
[实验一]选择合适浓度的硫酸
操作:在28时,用装有5mL硫酸溶液的注射器向盛有1g直径为2mm大理石的大试管中注入硫酸,记录15分钟内生成气体的体积,见下表:
试管编号 1 2 3 4 5
硫酸浓度(%) 15 20 25 30 35
气体体积(mL) 35 47 55 51 42
[实验二]选择合适的反应温度
操作:往盛有1g直径为2mm大理石的大试管中分别加入5mL相同合适浓度而不同温度的硫酸溶液,观察反应的情况,记录如下表:
试管编号 A B C D E
温度() 40 50 60 70 80
现象和比较 有少量气泡 气泡比A号试管多 气泡明显比B号试管多 大量气泡产生,与常温用盐酸反应相似 反应激烈,迅速产生大量气体
请根据本次活动的研究目的,分析处理以上两个表中数据,得出结论:
(1)稀硫酸与大理石反应,在28时,选用硫酸的浓度最合适为______%.
(2)在合适的硫酸浓度下,应选择最合适的反应温度为________.
(3)除选用适当的温度和合适浓度的硫酸之外,在反应过程中,为防止硫酸钙覆盖在大理石上,应增加________操作,更有利于气体的制备.
(4)你认为该研究小组还可以研究________对该反应速率的影响.
答案以及解析
1.答案:D
解析:A、取用液体药品时:试剂瓶瓶口紧挨试管口,能防止液体流出;标签向着手心,能防止液体流出腐蚀标签;瓶塞倒放桌面上,能防止污染瓶塞,污染药品。图中操作正确,不符合题意;B、二氧化碳的密度比空气大,可用向上排空气法收集,故导气管要伸入集气瓶底部,操作正确,不符合题意;C、检查装置的气感性:导管放入水中,用手紧握试管,试管内的气体受热膨胀,气压增大,若装置气密性良好,导管口有气泡冒出,操作正确,不符合题意;D、二氧化碳不能燃烧也不能支持燃烧,二氧化碳气体验满时,要把燃着的木条放在瓶口,不能放在焦气瓶内部,操作错误,符合题意。故选D。
2.答案:C
解析:实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,属于固液常温型,发生装置可选图中②;二氧化碳密度比空气大,二氧化碳能溶于水,只能用向上排空气法收集,收集装置选③。故选C。
3.答案:A
解析:实验室制取二氧化碳,首先按要求装配好仪器,然后检查装置气密性,向锥形瓶中加几块大理石,向漏斗中注入稀盐酸,收集气体,则正确的操作顺序是②①④③⑤,故选A。
4.答案:C
解析:A、因为通常情况下二氧化碳密度大于空气,所以能用向上排空气法收集,正确。
B、碳酸钙和硫酸反应生成微溶于水的硫酸钙,如用块状石灰石水附着在石灰石表面阻碍反应进行。但用粉末状石灰石,与硫酸接触面积较大,生成的硫酸钙几乎不影响石灰石和硫酸反应,正确。
C、因为二氧化碳溶于水的速度远小于二氧化碳从水中逸出的速度,所以可以用排水法收集。错误。
D、因为碳酸钙和盐酸在常温下即可迅速反应,故气体发生装置不需要加热,使用固液常温型发生装置。正确。
故选C。
5.答案:(1)石灰石;稀盐酸
(2)①②④
(3)
(4)c、a、b、d;d
解析:本题运用比较法解答。实验室制取二氧化碳气体选用石灰石与稀盐酸反应,不能用浓盐酸,因为浓盐酸有挥发性,使制得的二氧化碳气体不纯;不能用碳酸钠粉末,因为它与酸反应速率太快,不便于收集;也不能用木炭与氧气反应,虽然木炭与氧气反应能生成二氧化碳,但无法控制反应物的量,使制得的二氧化碳不纯;稀盐酸与石灰石反应速率适中,不需加热,制得的气体较纯净,易于收集,所以实验室常用石灰石与稀盐酸反应制取二氧化碳气体。
6.答案:(1)③;
(2)澄清石灰水;
(3)A中长颈漏斗内液面上升
(4)密度比空气大
解析:(1)从制取和收集的角度分析,实验室制取气体应选择反应速率适中的药品,这样便于收集到气体,且收集到的气体的纯度更高,故选③;碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳。(2)二氧化碳能使澄清石灰水变浑浊,故用澄清石灰水来检验二氧化碳;二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水。(3)石灰石和稀盐酸反应生成二氧化碳,反应过程中将弹簧夹关闭,锥形瓶中的压强增大,A中锥形瓶内液体被压入长颈漏斗内,长颈漏斗内液面上升。(4)二氧化碳能用向上排空气法收集,说明其密度比空气大。
7.答案:(1)长颈漏斗;方便添加液体;B或C;F;
(2)浓盐酸有挥发性,使收集到的不纯
(3)将燃烧的小木条放到集气瓶口,若小木条熄灭,则已收集满
(4)氧气(或)
(5)可控制液体的滴加速度
解析:(1)仪器a为长颈漏斗,使用它方便添加液体;实验室在常温下用固体和液体药品制取二氧化碳,二氧化碳密度比空气大,能溶于水,应选择发生装置B或C,收集装置F。(2)浓盐酸有挥发性,收集的二氧化碳中会含有氯化氢气体,因此实验室制取不能用浓盐酸。
(3)二氧化碳不支持燃烧,验满方法是将燃着的小木条放在集气瓶口,若小木条熄灭,则已收集满。
(4)B装置除了实验室制取外,还能用过氧化氢溶液和二氧化锰制取氧气。
8.答案:(1)25.
(2)70.
(3)摇动(振荡)试管.
(4)大理石颗粒大小.
解析:(1)观察实验一中的表格中数据可以知道,3号试管收集的气体最多,此时管中硫酸浓度是25%.浓度大于或小于此浓度值生成的气体体积都少.
(2)观察实验二中表格中的数据,可知应选择最合适的反应温度为70;低于70时,生成的气体少并且反应慢,高于70反应速率过快,不易收集.
(3)为防止硫酸钙覆盖在大理石上,可以用摇动试管的方法除去覆盖在大理石上的硫酸钙.
(4)碳酸钙固体颗粒大小也会影响反应的速率,也可作为研究课题.
课本实验再现
1、药品:稀盐酸与石灰石(或大理石)
2、反应原理:CaCO3+2HCl=CaCl2+H2O+CO2↑
易错提示:
①不能选用浓盐酸,因浓盐酸挥发性太强,能挥发出大量的氯化氢气体,使制得的二氧化碳不纯;
②不能选用稀硫酸,因稀硫酸与碳酸钙反应生成微溶性的硫酸钙,覆盖在石灰石(或大理石)的表面,会阻止反应继续进行;
③不能选用碳酸钠、碳酸钾粉末代替大理石或石灰石,因为它们易溶于水,反应速率快,不易控制,难以收集。
3、实验装置
(1)发生装置:固液常温型
实验装置 A B C D
装置 优点 安装简单 便于添加液体 能控制 反应速率 可随时控制反应的发生和停止
注意事项 ①以上装置中导管均需刚露出橡胶塞即可,否则不利于气体导出;②B、D装置中长颈漏斗末端必须伸入液面以下,形成液封,防止生成的气体从长颈漏斗的上端逸出。
(2)收集装置:二氧化碳能溶于水,且密度比空气大。
①收集时,导管的下端要伸至集气瓶底部,以便排尽空气;
②二氧化碳气体应由a端通入。
【注意】从导管a还是b进,需要根据气体的密度来判断:ρ气>ρ空,从a进,
ρ气<ρ空,从b进。
4、实验步骤:①连接仪器→②检查装置的气密性→③装药品(先装固体药品,后装液体药品)→④收集气体→⑤检验二氧化碳是否已收集满→⑥结束实验,整理仪器和药品。
5、检验方法:将气体通入澄清石灰水中,若澄清石灰水变浑浊,表明该气体为二氧化碳。
6、验满方法:将燃烧的小木条放在集气瓶口,若木条熄灭,证明已收集满。
拓展训练
1.在实验操作考查中,小明抽到的题目是“二氧化碳的制取、收集和验满”。下图是他的主要实验步骤,其中操作有误的是( )
A.加入药品 B.收集气体
C.检查装置气性 D.验满
2.实验室用大理石与稀盐酸制取二氧化碳,下列装置组合正确的是( )
A.①③ B.①④ C.②③ D.②④
3.实验室制取二氧化碳一般有如下5步:
①检查装置气密性;②按要求装配好仪器;③向漏斗中注入稀盐酸;④向锥形瓶中加几块大理石;⑤收集气体。
正确的操作顺序是( )
A.②①④③⑤ B.④①③②⑤ C.①②③④⑤ D.①④③②⑤
4.下列有关实验室制取二氧化碳的方法不合理的是( )
A.因为通常情况下二氧化碳密度大于空气,故能用向上排空气法收集
B.在发生装置中不可以加入块状石灰石和稀硫酸,但可以加入粉末状石灰石和稀硫酸
C.因为二氧化碳能溶于水并且也可以和水反应,故不能用排水法收集
D.因为碳酸钙和盐酸在常温下即可迅速反应,故气体发生装置不需要加热
5.小明同学在实验操作考核中,抽到的题目是“二氧化碳的制取、收集和验满”。
(1)要制取二氧化碳,小明同学应该从以上药品中选择___________和___________反应。
(2)选择以上药品的理由是___________(填序号)。
①不能用浓盐酸,因为浓盐酸易挥发,使氰化氢气体混入二氧化碳气体中。
②一般不选用碳酸钠粉末,因为它与酸反应速率太快,不便于收集。
③可用木炭和氧气反应,因为反应可生成二氧化碳。
④可用稀盐酸与石灰石反应,因为反应速率适中,条件要求不高,气体产物纯净,易于收集。
(3)写出你选择的药品制取二氧化碳反应的化学方程式:___________。
(4)图2是小明实验时的主要步骤,这些步骤的正确顺序是___________(填字母标号,下同),其中操作有误的是___________。
6.下列装置用于实验室的制备、净化、检验和收集,最后可收集一瓶,请回答下列问题。
对实验室制取二氧化碳药品的选择进行实验探究,记录如下:
组别 药品 实验现象
① 碳酸钠粉末和稀盐酸 产生气泡速率很快
② 块状石灰石和稀硫酸 产生气泡速率缓慢并逐渐停止
③ 块状石灰石和稀盐酸 产生气泡速率适中
(1)从制取和收集的角度分析,一般选择第__________(填序号)组药品,所发生反应的化学方程式为________________________________。
(2)B装置用于检验二氧化碳气体,则B中所盛放的物质是__________,发生反应的化学方程式是________________________________。
(3)反应过程中将弹簧夹关闭,在A中观察到的现象是_______________。
(4)C中的收集方法说明二氧化碳具有的物理性质是_____________________。
7.如图为实验室常用仪器或装置,请回答以下问题:
(1)仪器a的名称是__________,实验时使用它的优点是____________;实验室制取时,应选择的发生装置是________(填字母,下同),收集装置是________,实验室制取的原理是__________(写化学方程式)。
(2)实验室制取时,不能用浓盐酸,原因是__________。
(3)的验满方法是___________。
(4)B装置除了实验室制取外,还能用来制取的气体是_________。
(5)制取时可选用如图G、H两种仪器代替仪器a,选用这两种仪器的优点是_____________。
8.某研究小组在实验室制取二氧化碳的研究中发现,通常不选用大理石与稀硫酸反应制取二氧化碳,其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止.为此,该小组设立研究课题:选择合适浓度的硫酸和适当的反应温度制取二氧化碳.
[实验一]选择合适浓度的硫酸
操作:在28时,用装有5mL硫酸溶液的注射器向盛有1g直径为2mm大理石的大试管中注入硫酸,记录15分钟内生成气体的体积,见下表:
试管编号 1 2 3 4 5
硫酸浓度(%) 15 20 25 30 35
气体体积(mL) 35 47 55 51 42
[实验二]选择合适的反应温度
操作:往盛有1g直径为2mm大理石的大试管中分别加入5mL相同合适浓度而不同温度的硫酸溶液,观察反应的情况,记录如下表:
试管编号 A B C D E
温度() 40 50 60 70 80
现象和比较 有少量气泡 气泡比A号试管多 气泡明显比B号试管多 大量气泡产生,与常温用盐酸反应相似 反应激烈,迅速产生大量气体
请根据本次活动的研究目的,分析处理以上两个表中数据,得出结论:
(1)稀硫酸与大理石反应,在28时,选用硫酸的浓度最合适为______%.
(2)在合适的硫酸浓度下,应选择最合适的反应温度为________.
(3)除选用适当的温度和合适浓度的硫酸之外,在反应过程中,为防止硫酸钙覆盖在大理石上,应增加________操作,更有利于气体的制备.
(4)你认为该研究小组还可以研究________对该反应速率的影响.
答案以及解析
1.答案:D
解析:A、取用液体药品时:试剂瓶瓶口紧挨试管口,能防止液体流出;标签向着手心,能防止液体流出腐蚀标签;瓶塞倒放桌面上,能防止污染瓶塞,污染药品。图中操作正确,不符合题意;B、二氧化碳的密度比空气大,可用向上排空气法收集,故导气管要伸入集气瓶底部,操作正确,不符合题意;C、检查装置的气感性:导管放入水中,用手紧握试管,试管内的气体受热膨胀,气压增大,若装置气密性良好,导管口有气泡冒出,操作正确,不符合题意;D、二氧化碳不能燃烧也不能支持燃烧,二氧化碳气体验满时,要把燃着的木条放在瓶口,不能放在焦气瓶内部,操作错误,符合题意。故选D。
2.答案:C
解析:实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,属于固液常温型,发生装置可选图中②;二氧化碳密度比空气大,二氧化碳能溶于水,只能用向上排空气法收集,收集装置选③。故选C。
3.答案:A
解析:实验室制取二氧化碳,首先按要求装配好仪器,然后检查装置气密性,向锥形瓶中加几块大理石,向漏斗中注入稀盐酸,收集气体,则正确的操作顺序是②①④③⑤,故选A。
4.答案:C
解析:A、因为通常情况下二氧化碳密度大于空气,所以能用向上排空气法收集,正确。
B、碳酸钙和硫酸反应生成微溶于水的硫酸钙,如用块状石灰石水附着在石灰石表面阻碍反应进行。但用粉末状石灰石,与硫酸接触面积较大,生成的硫酸钙几乎不影响石灰石和硫酸反应,正确。
C、因为二氧化碳溶于水的速度远小于二氧化碳从水中逸出的速度,所以可以用排水法收集。错误。
D、因为碳酸钙和盐酸在常温下即可迅速反应,故气体发生装置不需要加热,使用固液常温型发生装置。正确。
故选C。
5.答案:(1)石灰石;稀盐酸
(2)①②④
(3)
(4)c、a、b、d;d
解析:本题运用比较法解答。实验室制取二氧化碳气体选用石灰石与稀盐酸反应,不能用浓盐酸,因为浓盐酸有挥发性,使制得的二氧化碳气体不纯;不能用碳酸钠粉末,因为它与酸反应速率太快,不便于收集;也不能用木炭与氧气反应,虽然木炭与氧气反应能生成二氧化碳,但无法控制反应物的量,使制得的二氧化碳不纯;稀盐酸与石灰石反应速率适中,不需加热,制得的气体较纯净,易于收集,所以实验室常用石灰石与稀盐酸反应制取二氧化碳气体。
6.答案:(1)③;
(2)澄清石灰水;
(3)A中长颈漏斗内液面上升
(4)密度比空气大
解析:(1)从制取和收集的角度分析,实验室制取气体应选择反应速率适中的药品,这样便于收集到气体,且收集到的气体的纯度更高,故选③;碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳。(2)二氧化碳能使澄清石灰水变浑浊,故用澄清石灰水来检验二氧化碳;二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水。(3)石灰石和稀盐酸反应生成二氧化碳,反应过程中将弹簧夹关闭,锥形瓶中的压强增大,A中锥形瓶内液体被压入长颈漏斗内,长颈漏斗内液面上升。(4)二氧化碳能用向上排空气法收集,说明其密度比空气大。
7.答案:(1)长颈漏斗;方便添加液体;B或C;F;
(2)浓盐酸有挥发性,使收集到的不纯
(3)将燃烧的小木条放到集气瓶口,若小木条熄灭,则已收集满
(4)氧气(或)
(5)可控制液体的滴加速度
解析:(1)仪器a为长颈漏斗,使用它方便添加液体;实验室在常温下用固体和液体药品制取二氧化碳,二氧化碳密度比空气大,能溶于水,应选择发生装置B或C,收集装置F。(2)浓盐酸有挥发性,收集的二氧化碳中会含有氯化氢气体,因此实验室制取不能用浓盐酸。
(3)二氧化碳不支持燃烧,验满方法是将燃着的小木条放在集气瓶口,若小木条熄灭,则已收集满。
(4)B装置除了实验室制取外,还能用过氧化氢溶液和二氧化锰制取氧气。
8.答案:(1)25.
(2)70.
(3)摇动(振荡)试管.
(4)大理石颗粒大小.
解析:(1)观察实验一中的表格中数据可以知道,3号试管收集的气体最多,此时管中硫酸浓度是25%.浓度大于或小于此浓度值生成的气体体积都少.
(2)观察实验二中表格中的数据,可知应选择最合适的反应温度为70;低于70时,生成的气体少并且反应慢,高于70反应速率过快,不易收集.
(3)为防止硫酸钙覆盖在大理石上,可以用摇动试管的方法除去覆盖在大理石上的硫酸钙.
(4)碳酸钙固体颗粒大小也会影响反应的速率,也可作为研究课题.
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
