化学人教版(2019)必修第二册7.3 .2乙酸 (共32张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册7.3 .2乙酸 (共32张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-13 00:00:00 | ||
图片预览











文档简介
(共32张PPT)
第二单元 食品中的有机化合物
人教版(2019)必修二
乙 酸
生活中常用的调味品食醋,它就是约含3%~5%的乙酸。
乙酸又称醋酸。它有什么样的结构?它都有那些性质呢?
混合物
纯净物
课堂导入
C
H
O
O
C
H
H
H
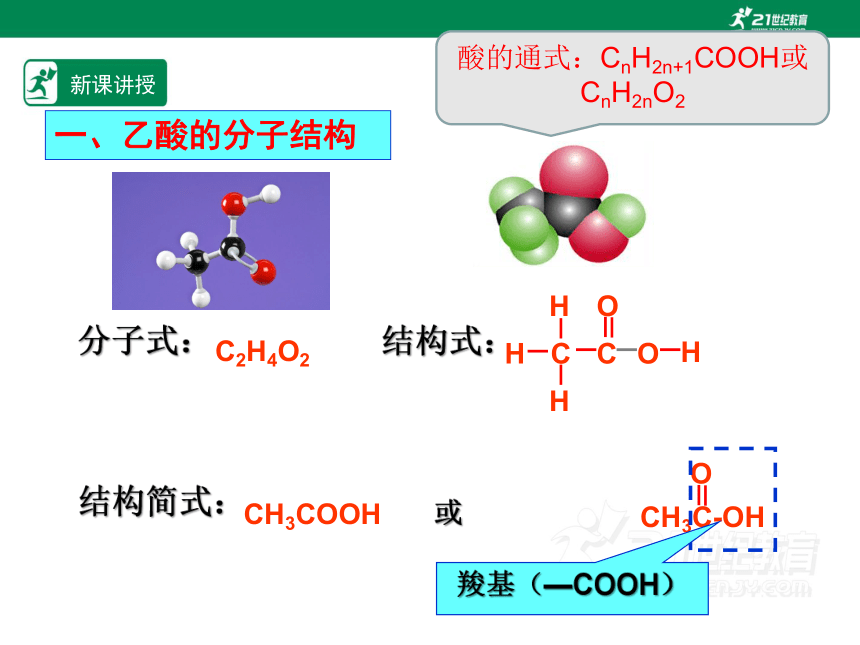
分子式: 结构式:
结构简式:
C2H4O2
CH3COOH
O
CH3C-OH
或
一、乙酸的分子结构
羧基(—COOH)
酸的通式:CnH2n+1COOH或CnH2nO2
新课讲授
常温下为液体
强烈刺激性气味
与水、酒精以任意比互溶
熔沸点较低,易挥发。熔点:16.6 0C,易结成冰一样的晶体。(冰醋酸由此得名)
气味 :
颜色 :
状态 :
溶解性 :
熔沸点 :
无色
二、乙酸的物理性质
新课讲授
想一想:家用的食醋除了调味外还有哪些用途?
1.巧除水垢
2.您知道醋为什么能解酒吗?
碳酸钙
利用了乙酸的酸性。
新课讲授
在温热的洗澡水中,加少许醋,洗浴后会感觉格外凉爽、舒适。 将醋与甘油以五比一的比例混合,经常擦用,能使粗糙的皮肤变得细嫩。 醋还有保健与食疗的作用。醋还有降血压防止动脉硬化和治疗冠心病及高血压的效果。用醋的蒸气薰蒸居室也能杀灭病毒与病菌,防止感冒与传染病。酒醉时喝一点醋可以醒酒。在食用大量油腻荤腥食品后可用醋做成羹汤来解除油腻与帮助消化。
新课讲授
生活常识
1、下列物质不能与乙酸反应的是( )
A、氢氧化钠溶液 B、铁
C、铜 D、碳酸氢钠溶液
2、下列物质可用来鉴别乙酸、乙醇和苯的是 ( )双选
A、澄清石灰水 B、溴水
C、碳酸钠溶液 D、紫色石蕊试液
C
CD
课堂练习
3、右图是某有机分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子。
下列说法正确的是 ( )
A、该物质的水溶液可除去热水瓶瓶胆中的水垢
B、该物质是室内装潢的夹板中散发出的一种对人体有害的气体
C、该物质属于电解质,在熔融状态下能导电
D、该物质中重要的基团是-OH
A
课堂练习
1. 酸性
试管 现象 结论
I
II
三、乙酸的化学性质
石蕊变红
产生气泡
乙酸显酸性
乙酸酸性比碳酸强
请用化学方程式或电离方程式表示产生以上现象的原因
I
II
CH3COOH CH3COO- + H+
2CH3COOH + Na2CO3 = 2CH3COONa + H2O + CO2↑
弱酸
4、下列能说明 CH3COOH是弱酸的是( )
A、同浓度的HCl溶液与CH3COOH溶液分别与Zn反应,前者反应速率大
B、CH3COOH能与Na2CO3溶液反应
C、CH3COOH能使紫色石蕊试液变红色
D、CH3COOH与H2O能以任意比混溶
A
5.为了使稀硫酸和锌反应的速率减慢,可选择加入下列物质,正确的是 。
1、水 2、CH3COONa 3、加热 4、浓硫酸
1、2
课堂练习
6、钠与下列物质反应都能够产生氢气:① H2O,②CH3COOH,③ CH3CH2OH。请判断这三种物质电离出H+的难易程度 (从难到易的顺序) ( )
A、 ①②③ B、②③①
C、③①② D、②①③
C
课堂练习
实验设计:根据下列药品设计实验
方案证明乙酸的确有酸性
药品:镁粉、NaOH溶液、Na2CO3粉未、
Na2SO3粉未、乙酸溶液、
石蕊、CuSO4 溶液
新课讲授
可行方案有:
方案一:往乙酸溶液中加石蕊
方案二:往镁粉中加入乙酸溶液
方案三:往Na2CO3粉未中加入乙酸溶液
方案四:NaOH溶液与乙酸溶液混和
方案五:往CuSO4溶液中滴入少量NaOH
溶液,再加入乙酸溶液。
课本P67 演示实验1:
新课讲授
判断实验现象
乙酸溶液2mL加紫色石蕊试液2-3滴
乙酸溶液2mL加Zn粒1-2粒
少量CuO粉与2-3mL乙酸溶液共热
向2mL乙酸溶液中滴入Na2CO3溶液
讨论:
1、上述实验说明乙酸具有什么性质?
2、乙酸的酸性比碳酸的酸性强还是弱?为什么?
3、写出上述反应的化学方程式
新课讲授
三、乙酸的化学性质
(重点与难点)
1、乙酸的弱酸性
Mg + 2CH3COOH → (CH3COO)2Mg + H2↑
Na2CO3 + 2CH3COOH → 2CH3COONa + CO2↑+H2O
CuO + 2CH3COOH → (CH3COO)2Cu + H2O
NaOH+ CH3COOH → CH3COONa + H2O
酸性比较:CH3COOH > H2CO3 >HClO
电离方程式:CH3COOH CH3COO— + H+
新课讲授
乙酸乙酯的实验室制备
1、装药品的顺序如何?
2、浓硫酸的作用是什么?
3、如何提高乙酸乙酯的产率?
4、得到的反应产物是否纯净?主要杂质有哪些?如何除去?
5、 饱和Na2CO3溶液有什么作用?
6、 为什么导管不插入饱和Na2CO3溶液中?
有无其它防倒吸的方法?
新课讲授
饱和碳酸钠溶液的液面上有透
明的油状液体,并可闻到香味。
乙酸乙酯:CH3COOCH2CH3
3、用酒精灯小心加热,观察现象。
1、在试管中先加入3mL乙醇,再慢慢加入2mL浓硫酸,摇动试管混合均匀,用手感觉温度变化。
2、再加入2mL冰醋酸,如图连好装置。接上导管到3mL饱和碳酸钠的液面上(不接触液面)。
2.酯化反应
酯化反应:酸和醇作用,生成酯和水的反应
新课讲授
实验注意点:
先加乙醇再加浓H2SO4,冷却,最后加乙酸
催化剂、吸水剂
提高反应速率
导气、冷凝
1、混合酸的顺序:
2、浓H2SO4作用:
3、加热的目的:
4、导管的作用:
5、饱和Na2CO3的作用:
中和乙酸;溶解乙醇;
降低乙酸乙酯在水中的溶解
不能伸到液面下(防倒吸)
注意:
新课讲授
1、为什么要先加酒精,后加浓硫酸?
2、乙酸乙酯为什么浮在液面上?
3、蒸出的乙酸乙酯中含有哪些杂质?
物 质 沸点(0C) 密度(g/mL) 水溶性
乙 酸 117.9 1.05 易溶
乙 醇 78.5 0.7893 易溶
乙酸乙酯 77 0.90 微溶于水
不溶于盐溶液
交流讨论:
浓硫酸稀释放出热量;若酒精加在后,则会沸腾飞溅
乙酸乙酯不溶于碳酸钠溶液,且密度比水小。
乙醇、乙酸
新课讲授
2、酯化反应
定义:酸和醇 作用,生成酯和水的反应叫做酯化反应
乙酸乙酯
三、乙酸的化学性质
CH3COOH + HOC2H5 CH3COOC2H5+H2O
浓H2SO4
△
特殊香味
新课讲授
6、下图是分离乙酸乙酯、乙酸和乙醇混合物的实验操作流程图:
上述实验过程中涉及的三次分离操作分别是( )
A、①蒸馏 ,②过滤 ,③ 分液
B、①分液 ,②蒸馏 ,③蒸馏
C、①蒸馏 ,②分液 ,③分液
D,①分液 ,②蒸馏 ,③结晶、过滤
B
新课讲授
探究酯化反应可能的反应方式
浓H2SO4
b、 O O
CH3—C—O—H+HO—C2H5 CH3—C—O—C2H5 + H2O
a、
CH3—C—OH+H—O—C2H5 CH3—C—O—C2H5 + H2O
浓H2SO4
=
=
O
O
可能一
可能二
新课讲授
酯化反应实质:
酸脱羟基,醇脱羟基上的氢原子。
CH3 C OH + H 18O C2H5
浓H2SO4
=
O
CH3 C 18O C2H5 + H2O
=
O
同位素原子示踪法
思考: 酯化反应中酸和醇分子内的化学键
怎样断裂?
新课讲授
浓H2SO4
CH3-C-OH + HO-CH2CH3 CH3-C-O-CH2CH3 + H2O
O
O
△
乙酸
乙醇
乙酸乙酯
CH3-C-O-CH2CH3
O
酯化反应实质:
取代反应。
新课讲授
7、酯化反应是有机化学中的一类重要反应,下列对酯化反应的理解不正确的是( )
A、酯化反应的产物只有酯
B、酯化反应可看成取代反应的一种
C、酯化反应是有限度的
D、浓硫酸可用作酯化反应的催化剂
A
8、下列关于乙酸性质的叙述错误的是( )
A、有强烈刺激性气味的无色液体
B、乙酸加人水中会分层,乙酸在下层
C、乙酸可用来除去热水瓶中的水垢(主要成分为碳酸钙)
D、在发生酯化反应时,乙酸分子中羟基上的氢原子跟醇分子中的羟基结合生成水
D
课堂练习
9、下列关于乙酸性质的叙述错误的是( ) 双选
A,乙酸具有氧化性,它能被氧化成乙醛
B、乙酸具有消毒杀菌作用
C,乙酸分子中含有碳氧双键,所以它能使溴的四氯化碳溶液褪色
D、乙酸在催化剂存在和加热条件下能与乙醇反应
AC
2CH3CHO + O2 → 2CH3COOH
课堂练习
乙醇
羟基 -OH
羧基
-COOH
官能团:反映一类有机物的共同特征的基团。
思考:乙酸的化学性质与它的哪部分结构有关?
碳碳双键 C=C
O
CH3—C—OH
官能团
结论:乙酸的化学性质与羧基有关。
碳碳叁键
有机物CH2=CH-COOH可以与下列哪些物质发生反应?
它表现了哪个官能团的性质特征?
溴水
乙醇
NaOH溶液
高锰酸钾溶液
碳碳双键
羧基
羧基
碳碳双键
知识拓展:
结论:有什么样的官能团就有什么样的化学性质
新课讲授
一.乙酸的物理性质
二.乙酸的分子结构
结构简式: 官能团:
三.乙酸的化学性质
1.乙酸的酸性
2.乙酸的酯化反应
CH3COOH
—COOH(羧基)
概念:酸和醇作用生成酯和水的反应
条件:浓硫酸、加热
规律:酸脱羟基醇脱氢
(无色、液体、有刺激性气味、易溶于水和乙醇)
CH3-C-O-H+H-O-CH2-CH3 CH3-C-O-CH2-CH3+H2O
O
O
△
浓H2SO4
课堂小结
10,如下图所示,在试管甲中先加人2mL95%的乙醇,并边振荡边缓缓加人2mL浓硫酸,充分摇匀,冷却后再加人2g无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上。在试管乙中加人5mL饱和碳酸钠溶液。按图连接装置,用酒精灯对试管甲加热,当观察到试管乙中有明显现象时停止实验。
(1)试管乙中观察到的现象是 。
(2)加人的浓硫酸的作用是 。
(3)该实验使用球形干燥管除起冷凝作用外,另一重要作用是 。
(4)试管乙中饱和碳酸钠溶液的作用是 。
有一层无色油状物浮在液面上
与 CH3COONa反应制取 CH3COOH、 催化剂 、吸水剂
防止倒吸
除去乙酸;溶解乙醇;有利于乙酸乙酯的分离
课堂练习
1. 分离乙醇和乙酸的方法最好的是( )
A. 分液漏斗分液
B. 加入碳酸钠饱和溶液,通过分液分离
C. 加热蒸馏
D. 加入氢氧化钠后,蒸出乙醇,再加硫酸蒸出乙酸
D
课堂练习
2. 除去乙酸乙酯中混有少量的CH3COOH,
最好的处理方法是( )
A.蒸馏
B.水洗后分液
C.用过量饱和Na2CO3溶液洗涤后分液
D.加乙醇和浓硫酸,加热
C
课堂练习
第二单元 食品中的有机化合物
人教版(2019)必修二
乙 酸
生活中常用的调味品食醋,它就是约含3%~5%的乙酸。
乙酸又称醋酸。它有什么样的结构?它都有那些性质呢?
混合物
纯净物
课堂导入
C
H
O
O
C
H
H
H
分子式: 结构式:
结构简式:
C2H4O2
CH3COOH
O
CH3C-OH
或
一、乙酸的分子结构
羧基(—COOH)
酸的通式:CnH2n+1COOH或CnH2nO2
新课讲授
常温下为液体
强烈刺激性气味
与水、酒精以任意比互溶
熔沸点较低,易挥发。熔点:16.6 0C,易结成冰一样的晶体。(冰醋酸由此得名)
气味 :
颜色 :
状态 :
溶解性 :
熔沸点 :
无色
二、乙酸的物理性质
新课讲授
想一想:家用的食醋除了调味外还有哪些用途?
1.巧除水垢
2.您知道醋为什么能解酒吗?
碳酸钙
利用了乙酸的酸性。
新课讲授
在温热的洗澡水中,加少许醋,洗浴后会感觉格外凉爽、舒适。 将醋与甘油以五比一的比例混合,经常擦用,能使粗糙的皮肤变得细嫩。 醋还有保健与食疗的作用。醋还有降血压防止动脉硬化和治疗冠心病及高血压的效果。用醋的蒸气薰蒸居室也能杀灭病毒与病菌,防止感冒与传染病。酒醉时喝一点醋可以醒酒。在食用大量油腻荤腥食品后可用醋做成羹汤来解除油腻与帮助消化。
新课讲授
生活常识
1、下列物质不能与乙酸反应的是( )
A、氢氧化钠溶液 B、铁
C、铜 D、碳酸氢钠溶液
2、下列物质可用来鉴别乙酸、乙醇和苯的是 ( )双选
A、澄清石灰水 B、溴水
C、碳酸钠溶液 D、紫色石蕊试液
C
CD
课堂练习
3、右图是某有机分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子。
下列说法正确的是 ( )
A、该物质的水溶液可除去热水瓶瓶胆中的水垢
B、该物质是室内装潢的夹板中散发出的一种对人体有害的气体
C、该物质属于电解质,在熔融状态下能导电
D、该物质中重要的基团是-OH
A
课堂练习
1. 酸性
试管 现象 结论
I
II
三、乙酸的化学性质
石蕊变红
产生气泡
乙酸显酸性
乙酸酸性比碳酸强
请用化学方程式或电离方程式表示产生以上现象的原因
I
II
CH3COOH CH3COO- + H+
2CH3COOH + Na2CO3 = 2CH3COONa + H2O + CO2↑
弱酸
4、下列能说明 CH3COOH是弱酸的是( )
A、同浓度的HCl溶液与CH3COOH溶液分别与Zn反应,前者反应速率大
B、CH3COOH能与Na2CO3溶液反应
C、CH3COOH能使紫色石蕊试液变红色
D、CH3COOH与H2O能以任意比混溶
A
5.为了使稀硫酸和锌反应的速率减慢,可选择加入下列物质,正确的是 。
1、水 2、CH3COONa 3、加热 4、浓硫酸
1、2
课堂练习
6、钠与下列物质反应都能够产生氢气:① H2O,②CH3COOH,③ CH3CH2OH。请判断这三种物质电离出H+的难易程度 (从难到易的顺序) ( )
A、 ①②③ B、②③①
C、③①② D、②①③
C
课堂练习
实验设计:根据下列药品设计实验
方案证明乙酸的确有酸性
药品:镁粉、NaOH溶液、Na2CO3粉未、
Na2SO3粉未、乙酸溶液、
石蕊、CuSO4 溶液
新课讲授
可行方案有:
方案一:往乙酸溶液中加石蕊
方案二:往镁粉中加入乙酸溶液
方案三:往Na2CO3粉未中加入乙酸溶液
方案四:NaOH溶液与乙酸溶液混和
方案五:往CuSO4溶液中滴入少量NaOH
溶液,再加入乙酸溶液。
课本P67 演示实验1:
新课讲授
判断实验现象
乙酸溶液2mL加紫色石蕊试液2-3滴
乙酸溶液2mL加Zn粒1-2粒
少量CuO粉与2-3mL乙酸溶液共热
向2mL乙酸溶液中滴入Na2CO3溶液
讨论:
1、上述实验说明乙酸具有什么性质?
2、乙酸的酸性比碳酸的酸性强还是弱?为什么?
3、写出上述反应的化学方程式
新课讲授
三、乙酸的化学性质
(重点与难点)
1、乙酸的弱酸性
Mg + 2CH3COOH → (CH3COO)2Mg + H2↑
Na2CO3 + 2CH3COOH → 2CH3COONa + CO2↑+H2O
CuO + 2CH3COOH → (CH3COO)2Cu + H2O
NaOH+ CH3COOH → CH3COONa + H2O
酸性比较:CH3COOH > H2CO3 >HClO
电离方程式:CH3COOH CH3COO— + H+
新课讲授
乙酸乙酯的实验室制备
1、装药品的顺序如何?
2、浓硫酸的作用是什么?
3、如何提高乙酸乙酯的产率?
4、得到的反应产物是否纯净?主要杂质有哪些?如何除去?
5、 饱和Na2CO3溶液有什么作用?
6、 为什么导管不插入饱和Na2CO3溶液中?
有无其它防倒吸的方法?
新课讲授
饱和碳酸钠溶液的液面上有透
明的油状液体,并可闻到香味。
乙酸乙酯:CH3COOCH2CH3
3、用酒精灯小心加热,观察现象。
1、在试管中先加入3mL乙醇,再慢慢加入2mL浓硫酸,摇动试管混合均匀,用手感觉温度变化。
2、再加入2mL冰醋酸,如图连好装置。接上导管到3mL饱和碳酸钠的液面上(不接触液面)。
2.酯化反应
酯化反应:酸和醇作用,生成酯和水的反应
新课讲授
实验注意点:
先加乙醇再加浓H2SO4,冷却,最后加乙酸
催化剂、吸水剂
提高反应速率
导气、冷凝
1、混合酸的顺序:
2、浓H2SO4作用:
3、加热的目的:
4、导管的作用:
5、饱和Na2CO3的作用:
中和乙酸;溶解乙醇;
降低乙酸乙酯在水中的溶解
不能伸到液面下(防倒吸)
注意:
新课讲授
1、为什么要先加酒精,后加浓硫酸?
2、乙酸乙酯为什么浮在液面上?
3、蒸出的乙酸乙酯中含有哪些杂质?
物 质 沸点(0C) 密度(g/mL) 水溶性
乙 酸 117.9 1.05 易溶
乙 醇 78.5 0.7893 易溶
乙酸乙酯 77 0.90 微溶于水
不溶于盐溶液
交流讨论:
浓硫酸稀释放出热量;若酒精加在后,则会沸腾飞溅
乙酸乙酯不溶于碳酸钠溶液,且密度比水小。
乙醇、乙酸
新课讲授
2、酯化反应
定义:酸和醇 作用,生成酯和水的反应叫做酯化反应
乙酸乙酯
三、乙酸的化学性质
CH3COOH + HOC2H5 CH3COOC2H5+H2O
浓H2SO4
△
特殊香味
新课讲授
6、下图是分离乙酸乙酯、乙酸和乙醇混合物的实验操作流程图:
上述实验过程中涉及的三次分离操作分别是( )
A、①蒸馏 ,②过滤 ,③ 分液
B、①分液 ,②蒸馏 ,③蒸馏
C、①蒸馏 ,②分液 ,③分液
D,①分液 ,②蒸馏 ,③结晶、过滤
B
新课讲授
探究酯化反应可能的反应方式
浓H2SO4
b、 O O
CH3—C—O—H+HO—C2H5 CH3—C—O—C2H5 + H2O
a、
CH3—C—OH+H—O—C2H5 CH3—C—O—C2H5 + H2O
浓H2SO4
=
=
O
O
可能一
可能二
新课讲授
酯化反应实质:
酸脱羟基,醇脱羟基上的氢原子。
CH3 C OH + H 18O C2H5
浓H2SO4
=
O
CH3 C 18O C2H5 + H2O
=
O
同位素原子示踪法
思考: 酯化反应中酸和醇分子内的化学键
怎样断裂?
新课讲授
浓H2SO4
CH3-C-OH + HO-CH2CH3 CH3-C-O-CH2CH3 + H2O
O
O
△
乙酸
乙醇
乙酸乙酯
CH3-C-O-CH2CH3
O
酯化反应实质:
取代反应。
新课讲授
7、酯化反应是有机化学中的一类重要反应,下列对酯化反应的理解不正确的是( )
A、酯化反应的产物只有酯
B、酯化反应可看成取代反应的一种
C、酯化反应是有限度的
D、浓硫酸可用作酯化反应的催化剂
A
8、下列关于乙酸性质的叙述错误的是( )
A、有强烈刺激性气味的无色液体
B、乙酸加人水中会分层,乙酸在下层
C、乙酸可用来除去热水瓶中的水垢(主要成分为碳酸钙)
D、在发生酯化反应时,乙酸分子中羟基上的氢原子跟醇分子中的羟基结合生成水
D
课堂练习
9、下列关于乙酸性质的叙述错误的是( ) 双选
A,乙酸具有氧化性,它能被氧化成乙醛
B、乙酸具有消毒杀菌作用
C,乙酸分子中含有碳氧双键,所以它能使溴的四氯化碳溶液褪色
D、乙酸在催化剂存在和加热条件下能与乙醇反应
AC
2CH3CHO + O2 → 2CH3COOH
课堂练习
乙醇
羟基 -OH
羧基
-COOH
官能团:反映一类有机物的共同特征的基团。
思考:乙酸的化学性质与它的哪部分结构有关?
碳碳双键 C=C
O
CH3—C—OH
官能团
结论:乙酸的化学性质与羧基有关。
碳碳叁键
有机物CH2=CH-COOH可以与下列哪些物质发生反应?
它表现了哪个官能团的性质特征?
溴水
乙醇
NaOH溶液
高锰酸钾溶液
碳碳双键
羧基
羧基
碳碳双键
知识拓展:
结论:有什么样的官能团就有什么样的化学性质
新课讲授
一.乙酸的物理性质
二.乙酸的分子结构
结构简式: 官能团:
三.乙酸的化学性质
1.乙酸的酸性
2.乙酸的酯化反应
CH3COOH
—COOH(羧基)
概念:酸和醇作用生成酯和水的反应
条件:浓硫酸、加热
规律:酸脱羟基醇脱氢
(无色、液体、有刺激性气味、易溶于水和乙醇)
CH3-C-O-H+H-O-CH2-CH3 CH3-C-O-CH2-CH3+H2O
O
O
△
浓H2SO4
课堂小结
10,如下图所示,在试管甲中先加人2mL95%的乙醇,并边振荡边缓缓加人2mL浓硫酸,充分摇匀,冷却后再加人2g无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上。在试管乙中加人5mL饱和碳酸钠溶液。按图连接装置,用酒精灯对试管甲加热,当观察到试管乙中有明显现象时停止实验。
(1)试管乙中观察到的现象是 。
(2)加人的浓硫酸的作用是 。
(3)该实验使用球形干燥管除起冷凝作用外,另一重要作用是 。
(4)试管乙中饱和碳酸钠溶液的作用是 。
有一层无色油状物浮在液面上
与 CH3COONa反应制取 CH3COOH、 催化剂 、吸水剂
防止倒吸
除去乙酸;溶解乙醇;有利于乙酸乙酯的分离
课堂练习
1. 分离乙醇和乙酸的方法最好的是( )
A. 分液漏斗分液
B. 加入碳酸钠饱和溶液,通过分液分离
C. 加热蒸馏
D. 加入氢氧化钠后,蒸出乙醇,再加硫酸蒸出乙酸
D
课堂练习
2. 除去乙酸乙酯中混有少量的CH3COOH,
最好的处理方法是( )
A.蒸馏
B.水洗后分液
C.用过量饱和Na2CO3溶液洗涤后分液
D.加乙醇和浓硫酸,加热
C
课堂练习
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
