第九单元课题3溶液的浓度习题—2022-2023学年九年级化学人教版下册(有答案)
文档属性
| 名称 | 第九单元课题3溶液的浓度习题—2022-2023学年九年级化学人教版下册(有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 115.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-01 00:00:00 | ||
图片预览


文档简介
第九单元课题3溶液的浓度习题
一、单选题
1.实验室配制50g溶质质量分数为6%的氯化钠溶液,下列做法正确的是
A.用托盘天平称取5g氯化钠
B.用50mL量筒量取所需水的体积
C.溶解氯化钠时,使用的玻璃仪器有量筒、玻璃棒
D.将配制好的溶液装入广口瓶中,塞好瓶塞并贴上标签
2.硝酸钾可作为无土栽培的一种营养液。现将 25%的硝酸钾溶液稀释成 200g 10%来用于培植营养液,则需加水( )
A.80g B.300g C.120g D.100g
3.20℃时,KCl溶解于水的实验数据如下表,④中溶液的溶质质量分数约为( )
实验序号 水的质量/g 加入KCl质量/g 溶液的质量/g
① 10 1.4 11.4
② 10 2.4 12.4
③ 10 3.4 13.4
④ 10 4.4 13.4
A.25% B.30% C.34% D.44%
4.要使质量分数为10%的氯化钠溶液50g 变成质量分数为20%的氯化钠溶液,可采取的方法是
A.加入5g氯化钠 B.蒸发20g水
C.加入50g的30%氯化钠溶液 D.将溶液取出25g
5.常温下,对100mL氯化钠的饱和溶液进行图示实验。下列分析错误的是
A.实验2后,甲中溶液为氯化钠的不饱和溶液
B.实验2后,乙中比甲中氯化钠的溶解度大
C.实验2后,甲、乙中溶液的溶质质量分数不相等
D.实验1后的甲和实验2后的乙中溶液所含溶质质量相等
6.如图是a、b、c三种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是
A.a的溶解度大于b的溶解度
B.P点表示t1℃时a、c两物质溶解度相等
C.将t1℃饱和的c溶液升温到t2℃,得到的是不饱和溶液
D.将t2℃,a、b、c三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数由大到小的顺序为:b>a=c
7.甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是
A.t1 ℃时,甲的溶解度大于乙的溶解度
B.t2 ℃时,乙的饱和溶液升温或降温均会析出晶体
C.乙溶液从t3 ℃降温到t1 ℃,乙溶液中的溶质质量分数会发生改变
D.t3 ℃时,50 g水中加入40 g的甲物质充分溶解可得到90 g甲的饱和溶液
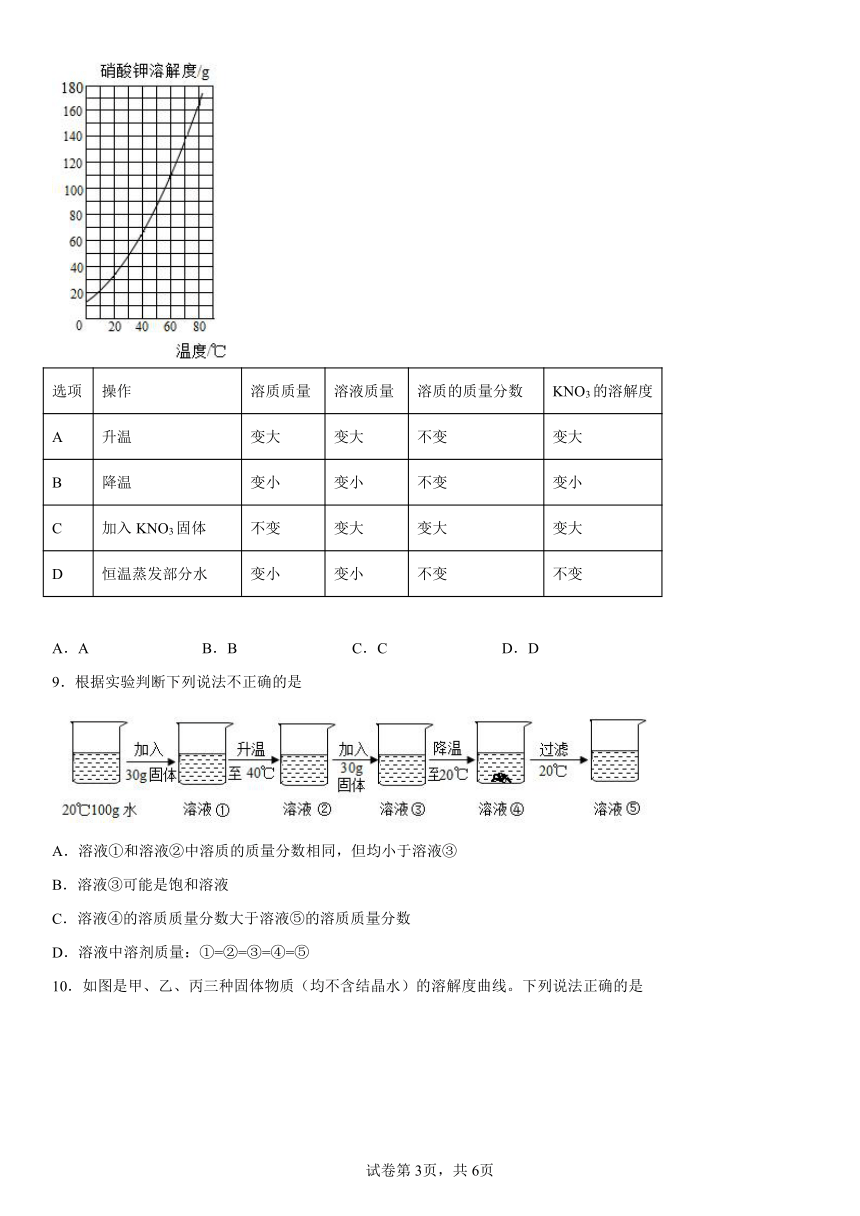
8.硝酸钾的溶解度曲线如图所示,将100g60℃的KNO3饱和溶液分别进行如下操作后,,所得溶液与原溶液相比,变化结果完全正确的是
选项 操作 溶质质量 溶液质量 溶质的质量分数 KNO3的溶解度
A 升温 变大 变大 不变 变大
B 降温 变小 变小 不变 变小
C 加入KNO3固体 不变 变大 变大 变大
D 恒温蒸发部分水 变小 变小 不变 不变
A.A B.B C.C D.D
9.根据实验判断下列说法不正确的是
A.溶液①和溶液②中溶质的质量分数相同,但均小于溶液③
B.溶液③可能是饱和溶液
C.溶液④的溶质质量分数大于溶液⑤的溶质质量分数
D.溶液中溶剂质量:①=②=③=④=⑤
10.如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。下列说法正确的是
A.三种物质的溶解度大小关系为甲>乙>丙
B.t2℃时,将20g甲加入50g水中,得到70g溶液
C.t3℃时,用等质量的甲、乙、丙固体配成饱和溶液,需要水的质量大小关系是乙>甲>丙
D.将t2℃的三种物质的饱和溶液分别降温到t1℃,所得溶液的溶质质量分数大小关系为乙>丙>甲
11.用氯化钠固体配制溶质质量分数为5%的氯化钠溶液。下列仪器中必须用到的是( )
A.②④⑥⑦ B.①④⑤⑥ C.①③⑤⑦ D.①②④⑦
12.将质量均为30g的甲、乙两种固体分别加入到50g水中,充分搅拌后,剩余固体物质与温度的关系如图所示,下列说法正确的是( )
A.甲的溶解度随温度升高而增大
B.t1℃时,甲、乙的溶解度均为20g
C.温度由t2℃降低到t1℃时,甲溶液析出5g固体
D.a,b,c三点中溶质的质量分数由大到小的顺序是:c>a>b
二、填空题
13.如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:
(1)P点含义是_________。
(2)t2 ℃时,将15 g A物质放入50 g水中,充分溶解后,形成溶液的质量为_________。
(3)若A物质中含有少量的B物质,提纯A物质的方法是_________ (填“降温结晶”或“蒸发结晶”)。
(4)t3℃时,将A、B、C三种物质的饱和溶液降温到t1℃,三种溶液中溶质的质量分数由大到小的顺序为_________。
14.在一定温度下,向100g水中依次加入一定质量的KCl固体,充分溶解,加入KCl固体的质量与所得溶液质量的关系如图所示:
(1)该温度下,实验①所得溶液是______溶液填“饱和”或“不饱和”。
(2)该温度下,KCl的溶解度为______。
(3)实验③所得溶液中溶质的质量分数是______。填选项序号。
a.40% b.37.5% c.28.6%
15.将30g固体物质X(不含结晶水)投入盛有20g水的烧杯中,搅拌,测得0℃、t1℃、t2℃、t3℃时烧杯中溶液的质量分别如图中A、B、C、D点所示。
回答下列问题:
(1)A、B两点对应的溶液中溶质的质量分数较大的是____________(填字母编号)。
(2)0℃时,物质X的溶解度是____________。
(3)A、B、C、D四点对应的溶液中,一定属于饱和溶液的是____________(填字母编号)。
(4)下列说法正确的是_____________(填序号)。
①t1℃时,若向B点对应的烧杯中再加入30g水,搅拌,所得溶液为不饱和溶液
②若要从D点对应的溶液中得到全部固体X,可采用降温结晶的方法
③t2℃时,将物质X的饱和溶液变为不饱和溶液,溶质的质量可能增大
16.下图是对某固体物质的溶液在一定温度下进行恒温蒸发操作的实验记录,请回答:
(1)乙中的溶液为__________(填“饱和”或“不饱和”)溶液;
(2)该固体物质在当时温度下的溶解度为__________。
(3)甲、乙、丙、丁中溶液的溶质质量分数的大小关系是__________。
三、计算题
17.某兴趣小组用73g溶质质量分数为20%的盐酸与足量锌粒反应,可制得氢气的质量是多少?
18.73g质量分数为20%的盐酸与足量的大理石反应,生成二氧化碳的质量是多少?这些二氧化碳的体积(标准状况)是多少?(在标准状况下,二氧化碳的密度为1.977g/L)
19.为测定某种贝壳中碳酸钙的含量,取25g贝壳,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不能与稀盐酸反应,也不溶于水)。请计算:
(1)这种贝壳中碳酸钙的质量分数是多少。
(2)25g贝壳与稀盐酸恰好完全反应时,所用稀盐酸中溶质的质量分数。(写出计算过程,最后结果保留1位小数)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.C
3.A
4.C
5.B
6.B
7.B
8.D
9.C
10.D
11.B
12.D
13. (1) t1 ℃时,A、C两物质的溶解度相等 (2)60g 降温结晶 B>A>C
14. (1) 不饱和 (2)40g c
15. (1) B 20g (2) A、B ③
16. (1) 不饱和 (2)15g 丙=丁>乙>甲
17.0.4g
18.解:设生成二氧化碳的质量是x
x=8.8g;
这些二氧化碳的体积为:8.8g÷1.977g/L≈4.45L。
答:生成二氧化碳的质量是8.8g;这些二氧化碳的体积(标准状况)是4.45L。
19.(1)80%(2)14.7%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.实验室配制50g溶质质量分数为6%的氯化钠溶液,下列做法正确的是
A.用托盘天平称取5g氯化钠
B.用50mL量筒量取所需水的体积
C.溶解氯化钠时,使用的玻璃仪器有量筒、玻璃棒
D.将配制好的溶液装入广口瓶中,塞好瓶塞并贴上标签
2.硝酸钾可作为无土栽培的一种营养液。现将 25%的硝酸钾溶液稀释成 200g 10%来用于培植营养液,则需加水( )
A.80g B.300g C.120g D.100g
3.20℃时,KCl溶解于水的实验数据如下表,④中溶液的溶质质量分数约为( )
实验序号 水的质量/g 加入KCl质量/g 溶液的质量/g
① 10 1.4 11.4
② 10 2.4 12.4
③ 10 3.4 13.4
④ 10 4.4 13.4
A.25% B.30% C.34% D.44%
4.要使质量分数为10%的氯化钠溶液50g 变成质量分数为20%的氯化钠溶液,可采取的方法是
A.加入5g氯化钠 B.蒸发20g水
C.加入50g的30%氯化钠溶液 D.将溶液取出25g
5.常温下,对100mL氯化钠的饱和溶液进行图示实验。下列分析错误的是
A.实验2后,甲中溶液为氯化钠的不饱和溶液
B.实验2后,乙中比甲中氯化钠的溶解度大
C.实验2后,甲、乙中溶液的溶质质量分数不相等
D.实验1后的甲和实验2后的乙中溶液所含溶质质量相等
6.如图是a、b、c三种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是
A.a的溶解度大于b的溶解度
B.P点表示t1℃时a、c两物质溶解度相等
C.将t1℃饱和的c溶液升温到t2℃,得到的是不饱和溶液
D.将t2℃,a、b、c三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数由大到小的顺序为:b>a=c
7.甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是
A.t1 ℃时,甲的溶解度大于乙的溶解度
B.t2 ℃时,乙的饱和溶液升温或降温均会析出晶体
C.乙溶液从t3 ℃降温到t1 ℃,乙溶液中的溶质质量分数会发生改变
D.t3 ℃时,50 g水中加入40 g的甲物质充分溶解可得到90 g甲的饱和溶液
8.硝酸钾的溶解度曲线如图所示,将100g60℃的KNO3饱和溶液分别进行如下操作后,,所得溶液与原溶液相比,变化结果完全正确的是
选项 操作 溶质质量 溶液质量 溶质的质量分数 KNO3的溶解度
A 升温 变大 变大 不变 变大
B 降温 变小 变小 不变 变小
C 加入KNO3固体 不变 变大 变大 变大
D 恒温蒸发部分水 变小 变小 不变 不变
A.A B.B C.C D.D
9.根据实验判断下列说法不正确的是
A.溶液①和溶液②中溶质的质量分数相同,但均小于溶液③
B.溶液③可能是饱和溶液
C.溶液④的溶质质量分数大于溶液⑤的溶质质量分数
D.溶液中溶剂质量:①=②=③=④=⑤
10.如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。下列说法正确的是
A.三种物质的溶解度大小关系为甲>乙>丙
B.t2℃时,将20g甲加入50g水中,得到70g溶液
C.t3℃时,用等质量的甲、乙、丙固体配成饱和溶液,需要水的质量大小关系是乙>甲>丙
D.将t2℃的三种物质的饱和溶液分别降温到t1℃,所得溶液的溶质质量分数大小关系为乙>丙>甲
11.用氯化钠固体配制溶质质量分数为5%的氯化钠溶液。下列仪器中必须用到的是( )
A.②④⑥⑦ B.①④⑤⑥ C.①③⑤⑦ D.①②④⑦
12.将质量均为30g的甲、乙两种固体分别加入到50g水中,充分搅拌后,剩余固体物质与温度的关系如图所示,下列说法正确的是( )
A.甲的溶解度随温度升高而增大
B.t1℃时,甲、乙的溶解度均为20g
C.温度由t2℃降低到t1℃时,甲溶液析出5g固体
D.a,b,c三点中溶质的质量分数由大到小的顺序是:c>a>b
二、填空题
13.如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:
(1)P点含义是_________。
(2)t2 ℃时,将15 g A物质放入50 g水中,充分溶解后,形成溶液的质量为_________。
(3)若A物质中含有少量的B物质,提纯A物质的方法是_________ (填“降温结晶”或“蒸发结晶”)。
(4)t3℃时,将A、B、C三种物质的饱和溶液降温到t1℃,三种溶液中溶质的质量分数由大到小的顺序为_________。
14.在一定温度下,向100g水中依次加入一定质量的KCl固体,充分溶解,加入KCl固体的质量与所得溶液质量的关系如图所示:
(1)该温度下,实验①所得溶液是______溶液填“饱和”或“不饱和”。
(2)该温度下,KCl的溶解度为______。
(3)实验③所得溶液中溶质的质量分数是______。填选项序号。
a.40% b.37.5% c.28.6%
15.将30g固体物质X(不含结晶水)投入盛有20g水的烧杯中,搅拌,测得0℃、t1℃、t2℃、t3℃时烧杯中溶液的质量分别如图中A、B、C、D点所示。
回答下列问题:
(1)A、B两点对应的溶液中溶质的质量分数较大的是____________(填字母编号)。
(2)0℃时,物质X的溶解度是____________。
(3)A、B、C、D四点对应的溶液中,一定属于饱和溶液的是____________(填字母编号)。
(4)下列说法正确的是_____________(填序号)。
①t1℃时,若向B点对应的烧杯中再加入30g水,搅拌,所得溶液为不饱和溶液
②若要从D点对应的溶液中得到全部固体X,可采用降温结晶的方法
③t2℃时,将物质X的饱和溶液变为不饱和溶液,溶质的质量可能增大
16.下图是对某固体物质的溶液在一定温度下进行恒温蒸发操作的实验记录,请回答:
(1)乙中的溶液为__________(填“饱和”或“不饱和”)溶液;
(2)该固体物质在当时温度下的溶解度为__________。
(3)甲、乙、丙、丁中溶液的溶质质量分数的大小关系是__________。
三、计算题
17.某兴趣小组用73g溶质质量分数为20%的盐酸与足量锌粒反应,可制得氢气的质量是多少?
18.73g质量分数为20%的盐酸与足量的大理石反应,生成二氧化碳的质量是多少?这些二氧化碳的体积(标准状况)是多少?(在标准状况下,二氧化碳的密度为1.977g/L)
19.为测定某种贝壳中碳酸钙的含量,取25g贝壳,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不能与稀盐酸反应,也不溶于水)。请计算:
(1)这种贝壳中碳酸钙的质量分数是多少。
(2)25g贝壳与稀盐酸恰好完全反应时,所用稀盐酸中溶质的质量分数。(写出计算过程,最后结果保留1位小数)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.C
3.A
4.C
5.B
6.B
7.B
8.D
9.C
10.D
11.B
12.D
13. (1) t1 ℃时,A、C两物质的溶解度相等 (2)60g 降温结晶 B>A>C
14. (1) 不饱和 (2)40g c
15. (1) B 20g (2) A、B ③
16. (1) 不饱和 (2)15g 丙=丁>乙>甲
17.0.4g
18.解:设生成二氧化碳的质量是x
x=8.8g;
这些二氧化碳的体积为:8.8g÷1.977g/L≈4.45L。
答:生成二氧化碳的质量是8.8g;这些二氧化碳的体积(标准状况)是4.45L。
19.(1)80%(2)14.7%
答案第1页,共2页
答案第1页,共2页
同课章节目录
