第十一单元《盐化肥》综合训练2022-2023学年九年级化学人教版下册(有答案)
文档属性
| 名称 | 第十一单元《盐化肥》综合训练2022-2023学年九年级化学人教版下册(有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 142.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-01 00:00:00 | ||
图片预览


文档简介
第十一单元《盐化肥》 综合训练
一、单选题
1.下列物质的名称和俗名相对应的是( )
A.碳酸钙﹣纯碱 B.氯化钠﹣食盐 C.碳酸钙﹣小苏打 D.氧化钙﹣熟石灰
2.在“粗盐的提纯”实验中,一定用不到的仪器是
A.铁架台、蒸发皿 B.酒精灯、漏斗
C.细口瓶、试管 D.量筒、烧杯
3.紫甘蓝汁性质稳定,其颜色随pH改变而发生如下变化:
pH ﹤6.5 7.0—7.1 7.5—8.5 8.5—12.0 ﹥12.5
颜色 粉红色 紫色 蓝色 绿色 黄色
下列分析错误的是A.紫甘蓝汁可用作酸碱指示剂
B.将紫甘蓝汁加入到不同碱性溶液中,可能显示出多种颜色
C.与石蕊相比,紫甘蓝汁可更准确检验溶液的酸碱性强弱程度
D.向滴有紫甘蓝汁的氢氧化钠溶液中加入盐酸,若溶液变色则说明一定恰好完全反应
4.下列做法正确的是
A.植树造林,防沙降尘 B.焚烧垃圾,净化环境
C.禁用农药,保护水源 D.深埋电池,消除污染
5.在“粗盐中难溶性杂质去除”实验中,操作错误的是
A.称量时,在托盘天平左右两盘垫上相同质量的纸片
B.溶解时,用玻璃棒搅拌加快粗盐溶解
C.过滤时,用玻璃棒搅拌漏斗内的液体加快过滤
D.蒸发时,当蒸发皿中出现较多固体时停止加热
6.进行下列对比实验,不需要控制变量的是
A.用红磷和白磷探究可燃物燃烧的条件
B.用铁钉探究钢铁生锈的条件
C.用足量稀盐酸区分氯化钾溶液和碳酸钾溶液
D.用镁、锌与稀硫酸反应,比较镁、锌的金属活动性强弱
7.利用图1装置进行实验,先后将溶液快速全部推入,测得一段时间内压强变化如图2所示。下列说法不正确的是
A.先推入的是NaOH溶液
B.BC段,CO2与NaOH反应基本停止
C.D点压强比初始瓶内压强大,此时瓶内二氧化碳气体的量比初始多
D.最终压强比初始压强小,可能是因为有部分二氧化碳溶于水
8.河道两旁有甲、乙两厂,它们排放的工业废水中共含有H+、Na+、Ba2+、Cl-、SO、CO六种离子。两厂废水中各含三种离子,其中甲厂的废水明显呈酸性,甲厂废水中的离子是( )
A.H+、Na+、Ba2+
B.H+、Ba2+、Cl-
C.Na+、SO、CO
D.H+、SO、CO
二、简答题
9.写出下列反应的化学方程式:
(1)红磷在空气中燃烧:___________________________________________________。
(2)氯化铵与熟石灰加热制氨气:____________________________________________________。
10.请你判断,下列家庭小实验“能”或“不能”达到预期目的,并说明其理由。
(1)“品尝”:鉴别厨房中的白糖和食盐________________。
(2)“加食醋”:鉴别苏打和食盐___________________________。
(3)“观察”:鉴别黄铜和黄金___________________________。
11.春节是中华民族的传统佳节,在访亲拜友中迎接新年的到来。表达自己的观点。
(1)花馍是最具山西特色的美食之一。春节蒸花馍会用到发酵粉,其主要成分是小苏打,化学式为______。蒸好的花馍松软多孔是______气体受热膨胀所留下的空隙。
(2)美食之后,洗碗—碗盘上附着的油污常用洗涤剂清洗,这是因为洗涤剂具有______作用。泡茶使用茶漏可以很好的分离茶叶和茶水,这相当于化学实验操作中的______。
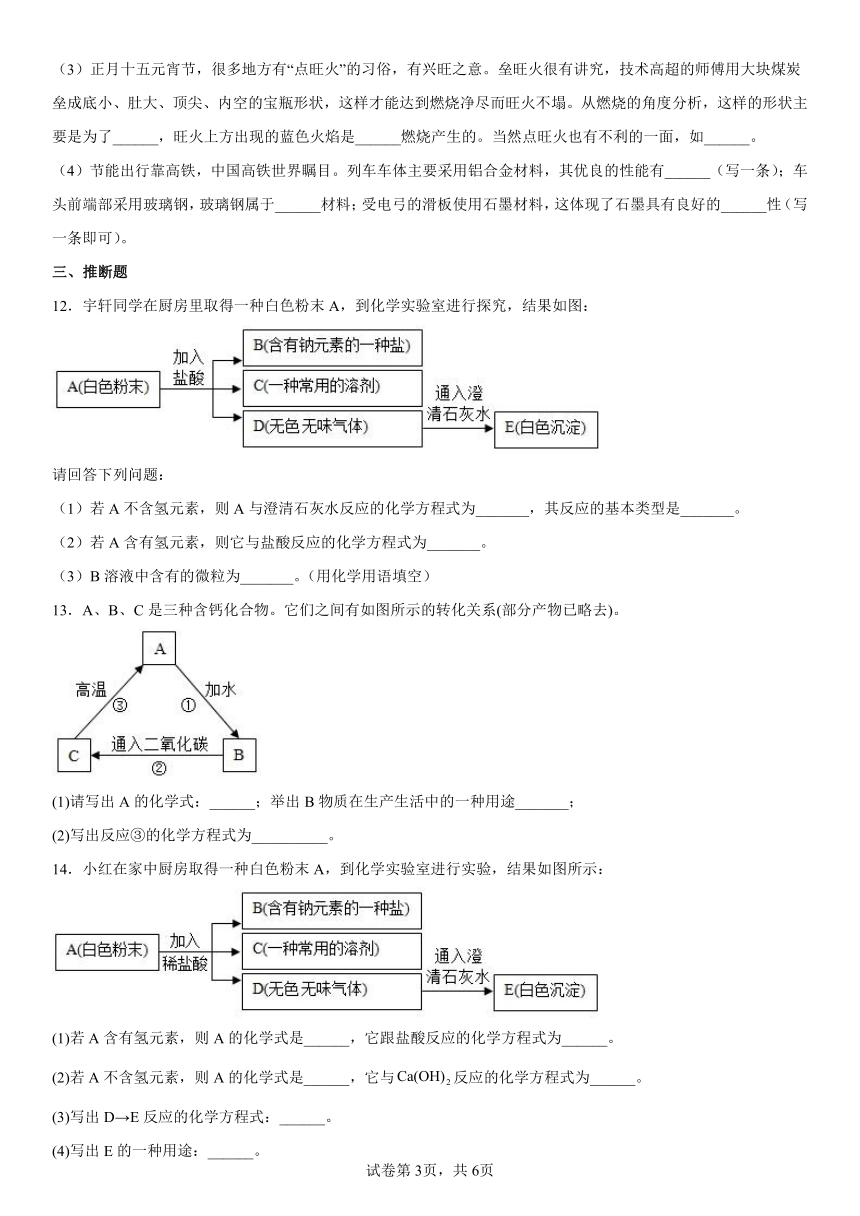
(3)正月十五元宵节,很多地方有“点旺火”的习俗,有兴旺之意。垒旺火很有讲究,技术高超的师傅用大块煤炭垒成底小、肚大、顶尖、内空的宝瓶形状,这样才能达到燃烧净尽而旺火不塌。从燃烧的角度分析,这样的形状主要是为了______,旺火上方出现的蓝色火焰是______燃烧产生的。当然点旺火也有不利的一面,如______。
(4)节能出行靠高铁,中国高铁世界瞩目。列车车体主要采用铝合金材料,其优良的性能有______(写一条);车头前端部采用玻璃钢,玻璃钢属于______材料;受电弓的滑板使用石墨材料,这体现了石墨具有良好的______性(写一条即可)。
三、推断题
12.宇轩同学在厨房里取得一种白色粉末A,到化学实验室进行探究,结果如图:
请回答下列问题:
(1)若A不含氢元素,则A与澄清石灰水反应的化学方程式为_______,其反应的基本类型是_______。
(2)若A含有氢元素,则它与盐酸反应的化学方程式为_______。
(3)B溶液中含有的微粒为_______。(用化学用语填空)
13.A、B、C是三种含钙化合物。它们之间有如图所示的转化关系(部分产物已略去)。
(1)请写出A的化学式:______;举出B物质在生产生活中的一种用途_______;
(2)写出反应③的化学方程式为__________。
14.小红在家中厨房取得一种白色粉末A,到化学实验室进行实验,结果如图所示:
(1)若A含有氢元素,则A的化学式是______,它跟盐酸反应的化学方程式为______。
(2)若A不含氢元素,则A的化学式是______,它与反应的化学方程式为______。
(3)写出D→E反应的化学方程式:______。
(4)写出E的一种用途:______。
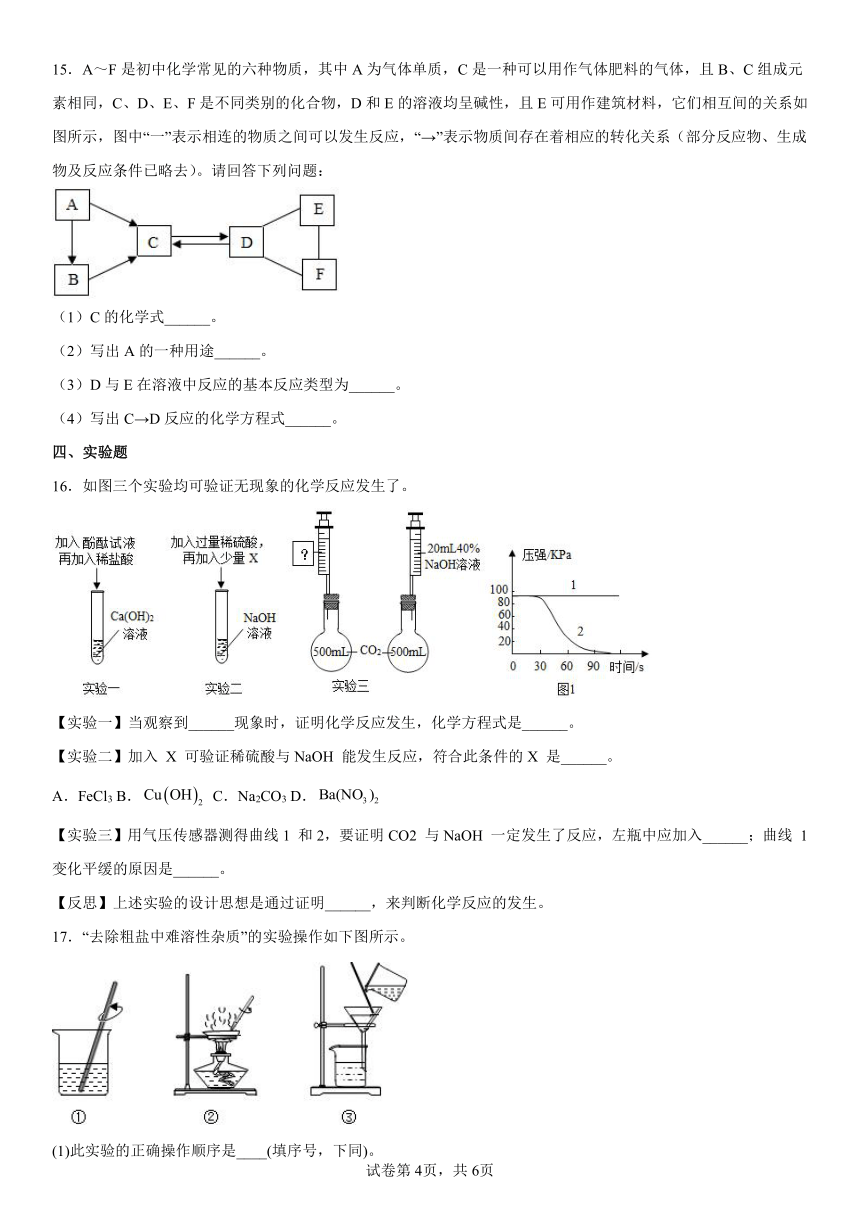
15.A~F是初中化学常见的六种物质,其中A为气体单质,C是一种可以用作气体肥料的气体,且B、C组成元素相同,C、D、E、F是不同类别的化合物,D和E的溶液均呈碱性,且E可用作建筑材料,它们相互间的关系如图所示,图中“一”表示相连的物质之间可以发生反应,“→”表示物质间存在着相应的转化关系(部分反应物、生成物及反应条件已略去)。请回答下列问题:
(1)C的化学式______。
(2)写出A的一种用途______。
(3)D与E在溶液中反应的基本反应类型为______。
(4)写出C→D反应的化学方程式______。
四、实验题
16.如图三个实验均可验证无现象的化学反应发生了。
【实验一】当观察到______现象时,证明化学反应发生,化学方程式是______。
【实验二】加入 X 可验证稀硫酸与NaOH 能发生反应,符合此条件的X 是______。
A.FeCl3 B. C.Na2CO3 D.
【实验三】用气压传感器测得曲线1 和2,要证明CO2 与NaOH 一定发生了反应,左瓶中应加入______;曲线 1 变化平缓的原因是______。
【反思】上述实验的设计思想是通过证明______,来判断化学反应的发生。
17.“去除粗盐中难溶性杂质”的实验操作如下图所示。
(1)此实验的正确操作顺序是____(填序号,下同)。
(2)操作②中,玻璃棒的作用是____。
A 引流 B 加快溶解 C 防止局部温度过高,液滴飞溅
18.烧杯A中盛有一定量的碳酸钠溶液,进行如图所示的实验。
(1)碳酸钠溶液显碱性,得出此结论的依据是_______。
(2)步骤②中发生反应的化学方程式为_______。
(3)步骤③观察到的现象是烧杯中产生气泡,红色褪去,_______。
19.某兴趣小组做了如下提纯NaCl的实验。
请根据实验回答下列问题:
(1)操作②的名称为 ________________ ;操作②中玻璃棒的作用是 ____________________ ;操作③中,当看到 ____________ 时,应停止加热。
(2)若得到NaCl的产率偏低,则可能的原因是(填序号) ____________ 。
(产率=提纯后盐的质量÷粗盐的质量×100%)
A过滤时滤纸有破损
B蒸发时有固体溅出
C把晶体从蒸发皿转移到天平上称量时,有少量沾在了蒸发皿上
D溶解11g含有泥沙的NaCl时,加入的水量不足
(3)用上述实验所得的NaCl配制溶质质量分数为5%的NaCl 溶液50g,不需要的仪器为(填序号) __________ 。
A量筒 B天平 C烧杯 D漏斗 E蒸发皿 F玻璃棒 G酒精灯
五、计算题
20.如图是某化肥厂生产的碳酸氢铵的包装袋上的部分说明。
(1)避免高温天气施用的原因是___________(用化学方程式表示)。
(2)一袋该化肥中至少含有纯净的NH4HCO3的质量为______Kg(直接写出计算结果)。
21.0.9%的氯化钠溶液称作生理盐水。
(1)生理盐水中的溶剂是 。
(2)若氯化钠来配制100g0.9%的生理盐水,需加水 g。
22.现有碳酸钠和氯化钠的混合物14.4g,加入到烧杯中,向其中滴入稀盐酸,直至不再产生气体为止,共用去90g稀盐酸,反应后得到100g溶液。请计算:
(1)原混合物中碳酸钠的质量。
(2)反应后所得溶液中溶质的质量分数。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.C
3.D
4.A
5.C
6.C
7.C
8.B
9.(1)4P+ 5O22P2O5 (2)2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O
10. (1)能,白糖有甜味,食盐有咸味 (2)能,食醋中的醋酸与苏打中的碳酸钠能反应有气泡冒出,醋酸与食盐中的氯化钠不反应,没有气泡冒出; (3)不能,黄铜和黄金都呈黄色。
11. (1)NaHCO3 CO2 乳化 (2)过滤 增大与氧气的接触面积,使燃烧更充分 CO (3)造成空气污染 密度小 复合材料 导电
12. (1) 复分解反应 (2) (3)Na+、Cl- 、H2O
13.(1) CaO 建筑材料
(2)CaCO3CaO+CO2↑
14.(1)
(2)
(3)
(4)补钙剂、建筑材料等(合理即可)
15.(1) CO2 医疗急救(合理即可) (2)复分解反应 CO2+2NaOH=Na2CO3+H2O
16.(1) 溶液由红色变为无色 (2)A 20mL水 (3)CO2 在水中的溶解度较小且与水反应的量小 (3)反应物已转化为其他物质
17.(1) ①③② (2)C
18. (1) B烧杯中溶液变红 (2)溶液变澄清
19.(1)过滤 引流 (2)蒸发皿中出现较多固体 (3)BCD DEG
20.(1)
(2)39.5
21.(1)水 (2)99.1
22.(1)反应生成二氧化碳质量为:14.4g+90g-100g=4.4g,设碳酸钠质量为x,反应生成氯化钠质量为y,
x=10.6g,y=11.7g,
答:原混合物中碳酸钠的质量是10.6g。
(2)反应后所得溶液中溶质的质量分数为:
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列物质的名称和俗名相对应的是( )
A.碳酸钙﹣纯碱 B.氯化钠﹣食盐 C.碳酸钙﹣小苏打 D.氧化钙﹣熟石灰
2.在“粗盐的提纯”实验中,一定用不到的仪器是
A.铁架台、蒸发皿 B.酒精灯、漏斗
C.细口瓶、试管 D.量筒、烧杯
3.紫甘蓝汁性质稳定,其颜色随pH改变而发生如下变化:
pH ﹤6.5 7.0—7.1 7.5—8.5 8.5—12.0 ﹥12.5
颜色 粉红色 紫色 蓝色 绿色 黄色
下列分析错误的是A.紫甘蓝汁可用作酸碱指示剂
B.将紫甘蓝汁加入到不同碱性溶液中,可能显示出多种颜色
C.与石蕊相比,紫甘蓝汁可更准确检验溶液的酸碱性强弱程度
D.向滴有紫甘蓝汁的氢氧化钠溶液中加入盐酸,若溶液变色则说明一定恰好完全反应
4.下列做法正确的是
A.植树造林,防沙降尘 B.焚烧垃圾,净化环境
C.禁用农药,保护水源 D.深埋电池,消除污染
5.在“粗盐中难溶性杂质去除”实验中,操作错误的是
A.称量时,在托盘天平左右两盘垫上相同质量的纸片
B.溶解时,用玻璃棒搅拌加快粗盐溶解
C.过滤时,用玻璃棒搅拌漏斗内的液体加快过滤
D.蒸发时,当蒸发皿中出现较多固体时停止加热
6.进行下列对比实验,不需要控制变量的是
A.用红磷和白磷探究可燃物燃烧的条件
B.用铁钉探究钢铁生锈的条件
C.用足量稀盐酸区分氯化钾溶液和碳酸钾溶液
D.用镁、锌与稀硫酸反应,比较镁、锌的金属活动性强弱
7.利用图1装置进行实验,先后将溶液快速全部推入,测得一段时间内压强变化如图2所示。下列说法不正确的是
A.先推入的是NaOH溶液
B.BC段,CO2与NaOH反应基本停止
C.D点压强比初始瓶内压强大,此时瓶内二氧化碳气体的量比初始多
D.最终压强比初始压强小,可能是因为有部分二氧化碳溶于水
8.河道两旁有甲、乙两厂,它们排放的工业废水中共含有H+、Na+、Ba2+、Cl-、SO、CO六种离子。两厂废水中各含三种离子,其中甲厂的废水明显呈酸性,甲厂废水中的离子是( )
A.H+、Na+、Ba2+
B.H+、Ba2+、Cl-
C.Na+、SO、CO
D.H+、SO、CO
二、简答题
9.写出下列反应的化学方程式:
(1)红磷在空气中燃烧:___________________________________________________。
(2)氯化铵与熟石灰加热制氨气:____________________________________________________。
10.请你判断,下列家庭小实验“能”或“不能”达到预期目的,并说明其理由。
(1)“品尝”:鉴别厨房中的白糖和食盐________________。
(2)“加食醋”:鉴别苏打和食盐___________________________。
(3)“观察”:鉴别黄铜和黄金___________________________。
11.春节是中华民族的传统佳节,在访亲拜友中迎接新年的到来。表达自己的观点。
(1)花馍是最具山西特色的美食之一。春节蒸花馍会用到发酵粉,其主要成分是小苏打,化学式为______。蒸好的花馍松软多孔是______气体受热膨胀所留下的空隙。
(2)美食之后,洗碗—碗盘上附着的油污常用洗涤剂清洗,这是因为洗涤剂具有______作用。泡茶使用茶漏可以很好的分离茶叶和茶水,这相当于化学实验操作中的______。
(3)正月十五元宵节,很多地方有“点旺火”的习俗,有兴旺之意。垒旺火很有讲究,技术高超的师傅用大块煤炭垒成底小、肚大、顶尖、内空的宝瓶形状,这样才能达到燃烧净尽而旺火不塌。从燃烧的角度分析,这样的形状主要是为了______,旺火上方出现的蓝色火焰是______燃烧产生的。当然点旺火也有不利的一面,如______。
(4)节能出行靠高铁,中国高铁世界瞩目。列车车体主要采用铝合金材料,其优良的性能有______(写一条);车头前端部采用玻璃钢,玻璃钢属于______材料;受电弓的滑板使用石墨材料,这体现了石墨具有良好的______性(写一条即可)。
三、推断题
12.宇轩同学在厨房里取得一种白色粉末A,到化学实验室进行探究,结果如图:
请回答下列问题:
(1)若A不含氢元素,则A与澄清石灰水反应的化学方程式为_______,其反应的基本类型是_______。
(2)若A含有氢元素,则它与盐酸反应的化学方程式为_______。
(3)B溶液中含有的微粒为_______。(用化学用语填空)
13.A、B、C是三种含钙化合物。它们之间有如图所示的转化关系(部分产物已略去)。
(1)请写出A的化学式:______;举出B物质在生产生活中的一种用途_______;
(2)写出反应③的化学方程式为__________。
14.小红在家中厨房取得一种白色粉末A,到化学实验室进行实验,结果如图所示:
(1)若A含有氢元素,则A的化学式是______,它跟盐酸反应的化学方程式为______。
(2)若A不含氢元素,则A的化学式是______,它与反应的化学方程式为______。
(3)写出D→E反应的化学方程式:______。
(4)写出E的一种用途:______。
15.A~F是初中化学常见的六种物质,其中A为气体单质,C是一种可以用作气体肥料的气体,且B、C组成元素相同,C、D、E、F是不同类别的化合物,D和E的溶液均呈碱性,且E可用作建筑材料,它们相互间的关系如图所示,图中“一”表示相连的物质之间可以发生反应,“→”表示物质间存在着相应的转化关系(部分反应物、生成物及反应条件已略去)。请回答下列问题:
(1)C的化学式______。
(2)写出A的一种用途______。
(3)D与E在溶液中反应的基本反应类型为______。
(4)写出C→D反应的化学方程式______。
四、实验题
16.如图三个实验均可验证无现象的化学反应发生了。
【实验一】当观察到______现象时,证明化学反应发生,化学方程式是______。
【实验二】加入 X 可验证稀硫酸与NaOH 能发生反应,符合此条件的X 是______。
A.FeCl3 B. C.Na2CO3 D.
【实验三】用气压传感器测得曲线1 和2,要证明CO2 与NaOH 一定发生了反应,左瓶中应加入______;曲线 1 变化平缓的原因是______。
【反思】上述实验的设计思想是通过证明______,来判断化学反应的发生。
17.“去除粗盐中难溶性杂质”的实验操作如下图所示。
(1)此实验的正确操作顺序是____(填序号,下同)。
(2)操作②中,玻璃棒的作用是____。
A 引流 B 加快溶解 C 防止局部温度过高,液滴飞溅
18.烧杯A中盛有一定量的碳酸钠溶液,进行如图所示的实验。
(1)碳酸钠溶液显碱性,得出此结论的依据是_______。
(2)步骤②中发生反应的化学方程式为_______。
(3)步骤③观察到的现象是烧杯中产生气泡,红色褪去,_______。
19.某兴趣小组做了如下提纯NaCl的实验。
请根据实验回答下列问题:
(1)操作②的名称为 ________________ ;操作②中玻璃棒的作用是 ____________________ ;操作③中,当看到 ____________ 时,应停止加热。
(2)若得到NaCl的产率偏低,则可能的原因是(填序号) ____________ 。
(产率=提纯后盐的质量÷粗盐的质量×100%)
A过滤时滤纸有破损
B蒸发时有固体溅出
C把晶体从蒸发皿转移到天平上称量时,有少量沾在了蒸发皿上
D溶解11g含有泥沙的NaCl时,加入的水量不足
(3)用上述实验所得的NaCl配制溶质质量分数为5%的NaCl 溶液50g,不需要的仪器为(填序号) __________ 。
A量筒 B天平 C烧杯 D漏斗 E蒸发皿 F玻璃棒 G酒精灯
五、计算题
20.如图是某化肥厂生产的碳酸氢铵的包装袋上的部分说明。
(1)避免高温天气施用的原因是___________(用化学方程式表示)。
(2)一袋该化肥中至少含有纯净的NH4HCO3的质量为______Kg(直接写出计算结果)。
21.0.9%的氯化钠溶液称作生理盐水。
(1)生理盐水中的溶剂是 。
(2)若氯化钠来配制100g0.9%的生理盐水,需加水 g。
22.现有碳酸钠和氯化钠的混合物14.4g,加入到烧杯中,向其中滴入稀盐酸,直至不再产生气体为止,共用去90g稀盐酸,反应后得到100g溶液。请计算:
(1)原混合物中碳酸钠的质量。
(2)反应后所得溶液中溶质的质量分数。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.C
3.D
4.A
5.C
6.C
7.C
8.B
9.(1)4P+ 5O22P2O5 (2)2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O
10. (1)能,白糖有甜味,食盐有咸味 (2)能,食醋中的醋酸与苏打中的碳酸钠能反应有气泡冒出,醋酸与食盐中的氯化钠不反应,没有气泡冒出; (3)不能,黄铜和黄金都呈黄色。
11. (1)NaHCO3 CO2 乳化 (2)过滤 增大与氧气的接触面积,使燃烧更充分 CO (3)造成空气污染 密度小 复合材料 导电
12. (1) 复分解反应 (2) (3)Na+、Cl- 、H2O
13.(1) CaO 建筑材料
(2)CaCO3CaO+CO2↑
14.(1)
(2)
(3)
(4)补钙剂、建筑材料等(合理即可)
15.(1) CO2 医疗急救(合理即可) (2)复分解反应 CO2+2NaOH=Na2CO3+H2O
16.(1) 溶液由红色变为无色 (2)A 20mL水 (3)CO2 在水中的溶解度较小且与水反应的量小 (3)反应物已转化为其他物质
17.(1) ①③② (2)C
18. (1) B烧杯中溶液变红 (2)溶液变澄清
19.(1)过滤 引流 (2)蒸发皿中出现较多固体 (3)BCD DEG
20.(1)
(2)39.5
21.(1)水 (2)99.1
22.(1)反应生成二氧化碳质量为:14.4g+90g-100g=4.4g,设碳酸钠质量为x,反应生成氯化钠质量为y,
x=10.6g,y=11.7g,
答:原混合物中碳酸钠的质量是10.6g。
(2)反应后所得溶液中溶质的质量分数为:
答案第1页,共2页
答案第1页,共2页
同课章节目录
