第五单元课题2 如何正确书写化学反应方程式课件—2022-2023学年九年级化学人教版上册(共32张PPT)
文档属性
| 名称 | 第五单元课题2 如何正确书写化学反应方程式课件—2022-2023学年九年级化学人教版上册(共32张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 10.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-06 00:00:00 | ||
图片预览











文档简介
(共32张PPT)
如何正确书写
化学反应方程式
Chemical
主讲人:张老师
九年级化学上册unit5
本节知识点
九年级化学(上册)
一、化学反应方程式定义
二、书写化学反应方程式应遵循的原则
本节知识点
三、化学反应方程书写的步骤
三、化学反应方程式配平的方法
九年级化学(上册)
1.1
化学反应方程式的定义:(P96)
用化学式和数字来表示化学反应的式子,叫做化学反应方程式。
我们为什么要学习化学反应方程式呢?
以铁的燃烧为例
九年级化学(上册)
铁丝的燃烧
1.1
【图示现象】铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
【中文陈述】铁在氧气中燃烧,生成四氧化三铁
【文字表达式】铁+氧气 四氧化三铁
点燃
【符号表达式】Fe + O2 Fe3O4
【化学方程式】3Fe + 2O2 Fe3O4
点燃
点燃
文字表达式相对于现象和中文陈述就显得准确且精炼了,但这个式子老外能看懂吗?
当我们用符号表达式来表示一个化学反应,不仅准确、精炼,而且还能国际通用
最后用一定的方法在化学式前面加上系数,就写出了化学反应方程式。
这个式子不仅表明了反应物、生成物和反应条件,同时,通过相对分子质量(或相对原子质量),还可以表示各物质之间的质量关系,即各物质之间的质量比
我们知道了什么是化学反应方程式,接下来就要学习如何去书写它了,书写化学反应方程式需要遵循两点原则
要以客观事实为基础,是什么,就是什么,生成什么,就是什么,切勿凭空捏造。
原则一
九年级化学(上册)
1.2
要遵循质量守恒定律,即等号两边各原子的种类和数目必须相等。
原则二
九年级化学(上册)
化学方程式书写方法
C原子个数
O原子个数
原子总个数
1
1
2
2
_____________________
3
3
该化学方程式等号两边的原子种类和数目都相等,我们就称化学方程式配平了。
C + O2 CO2
点燃
九年级化学(上册)
化学方程式书写方法
这个式子是否遵循化学反应方程式书写的两点原则?为什么?这个式子配平了吗?
H2 + O2 H2O
H原子个数
O原子个数
原子总个数
_____________________
2
2
2
1
3
4
点燃
九年级化学(上册)
化学方程式书写方法
H原子个数
O原子个数
原子总个数
4
4
2
2
6
6
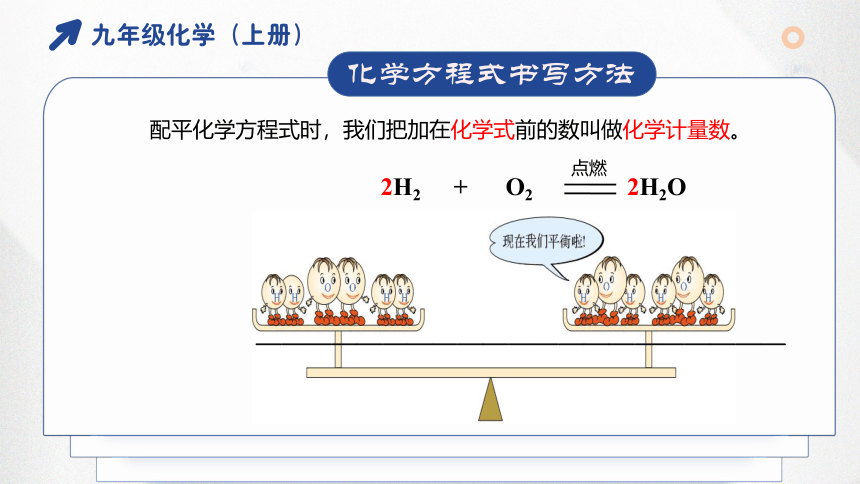
配平化学方程式时,我们把加在化学式前的数叫做化学计量数。
2H2 + O2 2H2O
点燃
_____________________
九年级化学(上册)
化学方程式书写步骤
P
O2
+
P2O5
左边写反应物的化学式;
右边写生成物的化学式;
反应物与生成物之间用一条短线连接。
写
以红磷在空气中的燃烧为例
九年级化学(上册)
化学方程式书写步骤
配平化学方程式
化学式前面配上适当的化学计量数使
等号两边各原子的种类和数目相等
4P
5O2
+
2P2O5
配
九年级化学(上册)
化学方程式书写步骤
注明反应条件
生成物的状态
把短线改成等号
4P
5O2
+
2P2O5
点燃
注
反应发生的条件写在等号上方,如加热(常用“△”号表示)、点燃、高温、催化剂等。若反应是在常温下进行,则不需注明。
九年级化学(上册)
化学方程式书写步骤
“↑” 和“↓”符号 的使用
1.如生成物中有气体,在气体的化学式右边要注“↑”号
反应物和生成物中都有气体,气体生成物就不注“↑”号
如:S + O2 SO2
点燃
如:2KMnO4 K2MnO4 + MnO2 + O2↑
△
无气生气,加“↑”;
有气生气,不加“↑”
九年级化学(上册)
化学方程式书写步骤
“↑” 和“↓”符号 的使用
2.溶液中反应如果生成物中有固体,在固体生成物的化学式右边要注“↓”号
如:CuSO4 + 2NaOH Na2SO4 + Cu(OH)2↓
溶液中反应如果反应物和生成物中都有固体,固体生成物也不需注“↓”号
如:Fe + CuSO4 Cu + FeSO4
九年级化学(上册)
化学方程式书写步骤
4P
5O2
+
2P2O5
点燃
检查反应物和生成物中各原子的个数是否相等
左边 右边
磷原子数
氧原子数
4
2×2=4
2×5=10
5×2=10
检
九年级化学(上册)
一、最小公倍数法
配平方法
方法步骤:
①找出式子左右两边只出现一次、且原子个数相差较大的原子,将该原子作为配平的起点。
②求该原子在方程式两边的个数的最小公倍数。
③用求得的最小公倍数分别除以两边原子个数,得化学计量数。
④按原子出现次数由少到多逐一配平其他原子。
O2
O2
1.2
九年级化学(上册)
最小公倍数法配平示范
P + O2 → P2O5
4 P + 5O2 2P2O5
点燃
第一步 :以O为起点。2和5的最小公倍数为10,分别除以相应数目,得5和2
P+5O2— 2P2O5
第二步:配平其他物质。
4P+5O2— 2P2O5
第三步:短线改等号、添加反应条件等,形成完整的化学方程式并检查。
九年级化学(上册)
二、奇偶法
配平方法
适用范围:
在化学方程式中某一种元素在反应物与生成物中出现多次,且方程式一边该元素原子数目总和是偶数,另一边该元素原子数目总和是奇数,这时可考虑用奇偶法配平。先变奇数为偶数,再用观察法配平。
O2
O2
1.2
九年级化学(上册)
先观察式子两侧,氧元素在O2、CO2、H2O中都出现,且式子左边氧原子总数和是偶数,右边氧原子总数和是奇数,所以将H2O中氧原子变成偶数,H2O前面配“2”,然后配平H原子,在C2H2前面配“2”,再配C原子,在CO2的前面配“4”;最后配平O原子,在O2前面配“5”,使得左右原子守恒,整个配平完成。即得到:
奇偶法配平示范
C2H2 + O2 → CO2 + H2O
2C2H2 + 5O2 4CO2 + 2H2O
点燃
九年级化学(上册)
三、定一法
配平方法
适用范围:
大多数含C、H或含C、H、O元素的化合物(如:CH4、C2H5OH、CH3COOH等)与氧气的反应;化合反应;分解反应等。
O2
O2
1.2
九年级化学(上册)
将含元素种类最多的化合物系数设为1,若元素种类相同,则将原子个数最多的化合物系数设为1。这里的“元素种类最多”、“原子个数最多”一般指:含C、H或含C、H、O元素的化合物,化合反应的生成物,分解反应的反应物。按原子出现次数由少到多逐一配平其他原子。(同一元素在同一化学式中出现多处仅算一次,如C2H5OH中两处出现H,算一次), 若配平后系数出现分数或可以约分,需调整成最简整数比。
定一法配平
示范
C2H5OH + O2 → CO2 + H2O
九年级化学(上册)
定一法配平示范
C2H5OH + O2 → CO2 + H2O
第一步:
设定C2H5OH的系数为1。
1C2H5OH+O2 — CO2+H2O
第二步:
原子出现次数分别为C2次,H2次,O4次。C、H均出现2次,首先配平。根据C2H5OH的系数为1,可确定CO2的系数为2,H2O的系数为3。
1C2H5OH+O2 — 2CO2+3H2O
第三步:
配平出现4次的O。根据左右两边氧原子个数相等确定,计算出O2的系数为3。
1C2H5OH+3O2 — 2CO2+3H2O
第四步:
形成完整的化学方程式并检查。系数1省略不写。
C2H5OH + 3 O2 2 CO2 + 3 H2O
点燃
九年级化学(上册)
四、待定系数法
配平方法
方法步骤:
1.设a、b、c、d等未知数,分别作为待配平的化学方程式两端各项化学式的系数。
2.根据质量守恒定律,反应前后各元素的原子种类和个数相等,列出每种元素的原子数与化学式系数a、b、c、d……关系的代数式,这些代数式可联立成一待定方程组:
3.解此待定方程组、就可求得各未知数之间的倍数关系。a=xb=yc=zd=...
4.令某未知数为某一正整数,使其它未知数成为最小正整数,将所得的a、b、c、d等值代入原化学反应式的待定位置,配平即告完成。
O2
O2
1.2
九年级化学(上册)
第一步:设a、b、c、d分别为反应式中各物质化学式的系数:
aFe2O3十bCO→cFe十dCO2
第二步:依据质量守恒定律:反应前后各元素的原子数目必须相等,列出a、b、c、d的关系式:对Fe原子有:2a=c①;对O原子有:3a十b=2d②;对C原于有:b=d③
第三步:解①一②的联立方程组,可得下列关系:a=1/3 b=1/2 c=1/3 d
第四步:为了使各个系数成为最小的正整数,而无公约数,令d=3,则a=1,b=3,c=2。将a、b、c、d的值代人原化学反应式的相应位置,即得配平的方程式为:
待定系数法配平示范
Fe2O3 + CO Fe + CO2
高温
Fe2O3 + 3 CO 2 Fe + 3 CO2
高温
九年级化学(上册)
小结
1、定义:用化学式表示化学反应的式子。
2、书写原则
1.3
一是必须以客观事实为基础
二是要遵守质量守恒定律,等号两边各原子种类与数目必须相等
3、书写步骤
写:左反右生一横线
配:配平
注:注明反应条件、生成物的状态、横线改等号
检:检查反应前后各原子的个数是否相等
4、配平方法:最小公倍数法、奇偶法、定一法、待定系数法等
九年级化学(上册)
题型训练
GO!
准备好了吗?
九年级化学(上册)
牛刀小试
写出下列化学反应的化学方程式:
2H2O2 ══ 2H2O +O2↑
MnO2
2KMnO4 K2MnO4 + MnO2 + O2↑
2KClO3 ══ 2KCl + 3O2 ↑
△
MnO2
△
(1)过氧化氢溶液分解生成水和氧气
(2)高锰酸钾加热生成锰酸钾、二氧化锰和氧气
(3)氯酸钾在加热条件下反应生成氯化钾和氧气
A. 2Al + O2 = 2AlO
九年级化学(上册)
能力提升
解释下列化学方程式书写违背了什么原则
A. 2Al + O2 = 2AlO
B. HgO = Hg + O2↑
要以客观事实为基础,切勿凭空捏造,氧化铝中的铝元素为+3价,应为Al2O3。
要遵循质量守恒定律,即等号两边各原子的种类和数目必须相等。这个方程式没有配平。
九年级化学(上册)
1
选择专练
下列化学方程式书写正确的是( )
B
A.S+O2 SO2↑ B.4Al+3O2 2Al2O3
C.C+O2 2CO2 D.2Mg+O2 2MgO
点燃
点燃
点燃
点燃
九年级化学(上册)
根据化学方程式A3B4+4CB=3A+4X,确定X的化学式为( )
2
CB
C2B3
CB2
A
C
D
B
CB3
物质变化类型的判断
B
九年级化学(上册)
加热氯酸钾和二氧化锰的混合物制取氧气时,反应前后二氧化锰
在固体混合物中的质量分数(不变、增大、减小) 。
3
物质性质类型的判断
增大
九年级化学(上册)
PRACTICE
课后练习题
请写出我们以前学过的化学反应方程式,比一比谁写的最多。
国内外研究现状
九年级化学(上册)
感谢聆听!
如何正确书写化学反应方程式
如何正确书写
化学反应方程式
Chemical
主讲人:张老师
九年级化学上册unit5
本节知识点
九年级化学(上册)
一、化学反应方程式定义
二、书写化学反应方程式应遵循的原则
本节知识点
三、化学反应方程书写的步骤
三、化学反应方程式配平的方法
九年级化学(上册)
1.1
化学反应方程式的定义:(P96)
用化学式和数字来表示化学反应的式子,叫做化学反应方程式。
我们为什么要学习化学反应方程式呢?
以铁的燃烧为例
九年级化学(上册)
铁丝的燃烧
1.1
【图示现象】铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
【中文陈述】铁在氧气中燃烧,生成四氧化三铁
【文字表达式】铁+氧气 四氧化三铁
点燃
【符号表达式】Fe + O2 Fe3O4
【化学方程式】3Fe + 2O2 Fe3O4
点燃
点燃
文字表达式相对于现象和中文陈述就显得准确且精炼了,但这个式子老外能看懂吗?
当我们用符号表达式来表示一个化学反应,不仅准确、精炼,而且还能国际通用
最后用一定的方法在化学式前面加上系数,就写出了化学反应方程式。
这个式子不仅表明了反应物、生成物和反应条件,同时,通过相对分子质量(或相对原子质量),还可以表示各物质之间的质量关系,即各物质之间的质量比
我们知道了什么是化学反应方程式,接下来就要学习如何去书写它了,书写化学反应方程式需要遵循两点原则
要以客观事实为基础,是什么,就是什么,生成什么,就是什么,切勿凭空捏造。
原则一
九年级化学(上册)
1.2
要遵循质量守恒定律,即等号两边各原子的种类和数目必须相等。
原则二
九年级化学(上册)
化学方程式书写方法
C原子个数
O原子个数
原子总个数
1
1
2
2
_____________________
3
3
该化学方程式等号两边的原子种类和数目都相等,我们就称化学方程式配平了。
C + O2 CO2
点燃
九年级化学(上册)
化学方程式书写方法
这个式子是否遵循化学反应方程式书写的两点原则?为什么?这个式子配平了吗?
H2 + O2 H2O
H原子个数
O原子个数
原子总个数
_____________________
2
2
2
1
3
4
点燃
九年级化学(上册)
化学方程式书写方法
H原子个数
O原子个数
原子总个数
4
4
2
2
6
6
配平化学方程式时,我们把加在化学式前的数叫做化学计量数。
2H2 + O2 2H2O
点燃
_____________________
九年级化学(上册)
化学方程式书写步骤
P
O2
+
P2O5
左边写反应物的化学式;
右边写生成物的化学式;
反应物与生成物之间用一条短线连接。
写
以红磷在空气中的燃烧为例
九年级化学(上册)
化学方程式书写步骤
配平化学方程式
化学式前面配上适当的化学计量数使
等号两边各原子的种类和数目相等
4P
5O2
+
2P2O5
配
九年级化学(上册)
化学方程式书写步骤
注明反应条件
生成物的状态
把短线改成等号
4P
5O2
+
2P2O5
点燃
注
反应发生的条件写在等号上方,如加热(常用“△”号表示)、点燃、高温、催化剂等。若反应是在常温下进行,则不需注明。
九年级化学(上册)
化学方程式书写步骤
“↑” 和“↓”符号 的使用
1.如生成物中有气体,在气体的化学式右边要注“↑”号
反应物和生成物中都有气体,气体生成物就不注“↑”号
如:S + O2 SO2
点燃
如:2KMnO4 K2MnO4 + MnO2 + O2↑
△
无气生气,加“↑”;
有气生气,不加“↑”
九年级化学(上册)
化学方程式书写步骤
“↑” 和“↓”符号 的使用
2.溶液中反应如果生成物中有固体,在固体生成物的化学式右边要注“↓”号
如:CuSO4 + 2NaOH Na2SO4 + Cu(OH)2↓
溶液中反应如果反应物和生成物中都有固体,固体生成物也不需注“↓”号
如:Fe + CuSO4 Cu + FeSO4
九年级化学(上册)
化学方程式书写步骤
4P
5O2
+
2P2O5
点燃
检查反应物和生成物中各原子的个数是否相等
左边 右边
磷原子数
氧原子数
4
2×2=4
2×5=10
5×2=10
检
九年级化学(上册)
一、最小公倍数法
配平方法
方法步骤:
①找出式子左右两边只出现一次、且原子个数相差较大的原子,将该原子作为配平的起点。
②求该原子在方程式两边的个数的最小公倍数。
③用求得的最小公倍数分别除以两边原子个数,得化学计量数。
④按原子出现次数由少到多逐一配平其他原子。
O2
O2
1.2
九年级化学(上册)
最小公倍数法配平示范
P + O2 → P2O5
4 P + 5O2 2P2O5
点燃
第一步 :以O为起点。2和5的最小公倍数为10,分别除以相应数目,得5和2
P+5O2— 2P2O5
第二步:配平其他物质。
4P+5O2— 2P2O5
第三步:短线改等号、添加反应条件等,形成完整的化学方程式并检查。
九年级化学(上册)
二、奇偶法
配平方法
适用范围:
在化学方程式中某一种元素在反应物与生成物中出现多次,且方程式一边该元素原子数目总和是偶数,另一边该元素原子数目总和是奇数,这时可考虑用奇偶法配平。先变奇数为偶数,再用观察法配平。
O2
O2
1.2
九年级化学(上册)
先观察式子两侧,氧元素在O2、CO2、H2O中都出现,且式子左边氧原子总数和是偶数,右边氧原子总数和是奇数,所以将H2O中氧原子变成偶数,H2O前面配“2”,然后配平H原子,在C2H2前面配“2”,再配C原子,在CO2的前面配“4”;最后配平O原子,在O2前面配“5”,使得左右原子守恒,整个配平完成。即得到:
奇偶法配平示范
C2H2 + O2 → CO2 + H2O
2C2H2 + 5O2 4CO2 + 2H2O
点燃
九年级化学(上册)
三、定一法
配平方法
适用范围:
大多数含C、H或含C、H、O元素的化合物(如:CH4、C2H5OH、CH3COOH等)与氧气的反应;化合反应;分解反应等。
O2
O2
1.2
九年级化学(上册)
将含元素种类最多的化合物系数设为1,若元素种类相同,则将原子个数最多的化合物系数设为1。这里的“元素种类最多”、“原子个数最多”一般指:含C、H或含C、H、O元素的化合物,化合反应的生成物,分解反应的反应物。按原子出现次数由少到多逐一配平其他原子。(同一元素在同一化学式中出现多处仅算一次,如C2H5OH中两处出现H,算一次), 若配平后系数出现分数或可以约分,需调整成最简整数比。
定一法配平
示范
C2H5OH + O2 → CO2 + H2O
九年级化学(上册)
定一法配平示范
C2H5OH + O2 → CO2 + H2O
第一步:
设定C2H5OH的系数为1。
1C2H5OH+O2 — CO2+H2O
第二步:
原子出现次数分别为C2次,H2次,O4次。C、H均出现2次,首先配平。根据C2H5OH的系数为1,可确定CO2的系数为2,H2O的系数为3。
1C2H5OH+O2 — 2CO2+3H2O
第三步:
配平出现4次的O。根据左右两边氧原子个数相等确定,计算出O2的系数为3。
1C2H5OH+3O2 — 2CO2+3H2O
第四步:
形成完整的化学方程式并检查。系数1省略不写。
C2H5OH + 3 O2 2 CO2 + 3 H2O
点燃
九年级化学(上册)
四、待定系数法
配平方法
方法步骤:
1.设a、b、c、d等未知数,分别作为待配平的化学方程式两端各项化学式的系数。
2.根据质量守恒定律,反应前后各元素的原子种类和个数相等,列出每种元素的原子数与化学式系数a、b、c、d……关系的代数式,这些代数式可联立成一待定方程组:
3.解此待定方程组、就可求得各未知数之间的倍数关系。a=xb=yc=zd=...
4.令某未知数为某一正整数,使其它未知数成为最小正整数,将所得的a、b、c、d等值代入原化学反应式的待定位置,配平即告完成。
O2
O2
1.2
九年级化学(上册)
第一步:设a、b、c、d分别为反应式中各物质化学式的系数:
aFe2O3十bCO→cFe十dCO2
第二步:依据质量守恒定律:反应前后各元素的原子数目必须相等,列出a、b、c、d的关系式:对Fe原子有:2a=c①;对O原子有:3a十b=2d②;对C原于有:b=d③
第三步:解①一②的联立方程组,可得下列关系:a=1/3 b=1/2 c=1/3 d
第四步:为了使各个系数成为最小的正整数,而无公约数,令d=3,则a=1,b=3,c=2。将a、b、c、d的值代人原化学反应式的相应位置,即得配平的方程式为:
待定系数法配平示范
Fe2O3 + CO Fe + CO2
高温
Fe2O3 + 3 CO 2 Fe + 3 CO2
高温
九年级化学(上册)
小结
1、定义:用化学式表示化学反应的式子。
2、书写原则
1.3
一是必须以客观事实为基础
二是要遵守质量守恒定律,等号两边各原子种类与数目必须相等
3、书写步骤
写:左反右生一横线
配:配平
注:注明反应条件、生成物的状态、横线改等号
检:检查反应前后各原子的个数是否相等
4、配平方法:最小公倍数法、奇偶法、定一法、待定系数法等
九年级化学(上册)
题型训练
GO!
准备好了吗?
九年级化学(上册)
牛刀小试
写出下列化学反应的化学方程式:
2H2O2 ══ 2H2O +O2↑
MnO2
2KMnO4 K2MnO4 + MnO2 + O2↑
2KClO3 ══ 2KCl + 3O2 ↑
△
MnO2
△
(1)过氧化氢溶液分解生成水和氧气
(2)高锰酸钾加热生成锰酸钾、二氧化锰和氧气
(3)氯酸钾在加热条件下反应生成氯化钾和氧气
A. 2Al + O2 = 2AlO
九年级化学(上册)
能力提升
解释下列化学方程式书写违背了什么原则
A. 2Al + O2 = 2AlO
B. HgO = Hg + O2↑
要以客观事实为基础,切勿凭空捏造,氧化铝中的铝元素为+3价,应为Al2O3。
要遵循质量守恒定律,即等号两边各原子的种类和数目必须相等。这个方程式没有配平。
九年级化学(上册)
1
选择专练
下列化学方程式书写正确的是( )
B
A.S+O2 SO2↑ B.4Al+3O2 2Al2O3
C.C+O2 2CO2 D.2Mg+O2 2MgO
点燃
点燃
点燃
点燃
九年级化学(上册)
根据化学方程式A3B4+4CB=3A+4X,确定X的化学式为( )
2
CB
C2B3
CB2
A
C
D
B
CB3
物质变化类型的判断
B
九年级化学(上册)
加热氯酸钾和二氧化锰的混合物制取氧气时,反应前后二氧化锰
在固体混合物中的质量分数(不变、增大、减小) 。
3
物质性质类型的判断
增大
九年级化学(上册)
PRACTICE
课后练习题
请写出我们以前学过的化学反应方程式,比一比谁写的最多。
国内外研究现状
九年级化学(上册)
感谢聆听!
如何正确书写化学反应方程式
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
