3.1《从铝土矿到铝合金-第三课时》
图片预览







文档简介
课件29张PPT。第1课时 从铝土矿中提取铝专题3 从矿物到基础材料 第一单元 从铝土矿到铝合金火箭的铝合金材料“嫦娥一号”上首次使用的铝锂合金月球车上
泡沫铝防护服3厨房里的铝制品铝合金门窗镁合金制品纯正镁合金
机身铝质饮料罐铝导线(一)在国宴上,
拿破仑三世使用一
套珍藏的铝制餐具,
而大臣们使用的是
银制餐具。
(二)门捷列夫创建了元素周期表,受到英国皇家学会的表彰,奖品是一只铝制奖杯。
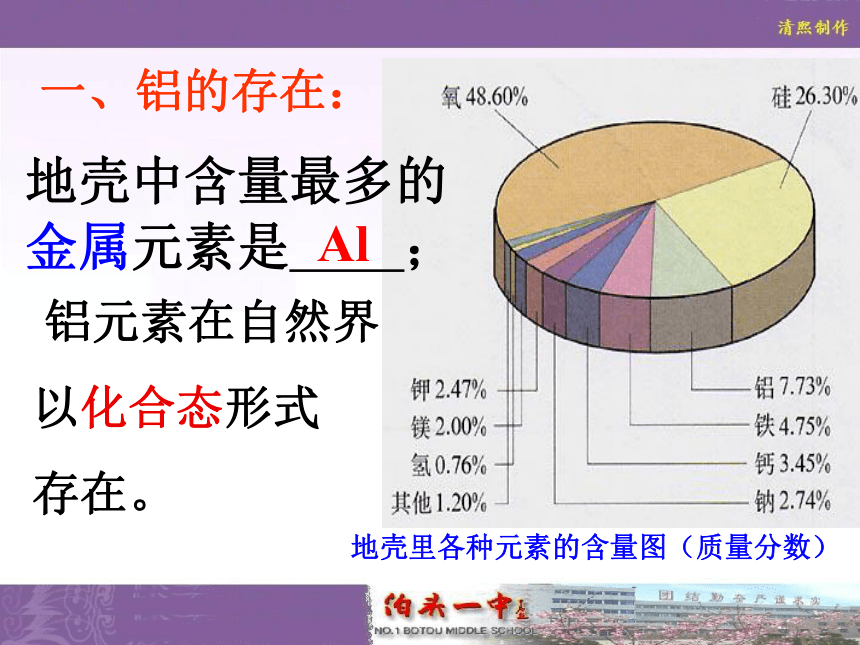
“铝的趣史”一、铝的存在: 铝元素在自然界
以化合态形式
存在。 地壳中含量最多的金属元素是 ;
地壳里各种元素的含量图(质量分数)Al二、从铝土矿中提炼铝溶解铝土矿NaOH溶液过滤残渣二氧化碳酸化过滤滤液灼烧H2O电解铝铝土矿:主要成分为Al2O3还有少量的Fe2O3等杂质?①②③④用NaOH溶液溶解铝土矿中什么物质?问题一 :实验验证:预测:结论:可能溶解了Al2O3向装有Al2O3的试管(1号)中加入NaOH向装有Fe2O3的试管(2号)中加入NaOHFe2O3不与NaOH反应Al2O3+2NaOH=2NaAlO2+H2O偏铝酸钠问题二:NaOH溶解铝土矿后,滤液中的主要成分是什么?残渣是什么?滤液:过量的NaOH、NaAlO2残渣:Fe2O3等杂质问题三:把滤液酸化的目的是什么? 两试管都有白色沉淀生成。把滤液酸化的作用是中和过量的NaOH溶液并和NaAlO2反应产生沉淀 实验:现象:结论:向3号试管中加入NaAlO2溶液,再滴加盐酸向4号试管中加入NaAlO2溶液,再通入CO2Al(OH)3问题四:为什么工艺流程中不是用盐酸来酸化,而是通足量的CO2酸化? 实验:现象:加稀盐酸的试管中沉淀溶解通CO2的试管中沉淀不溶解结论:Al(OH)3可以溶于强酸,但不能溶于H2CO3等弱酸。NaAlO2+CO2+2H2O=Al(OH)3 +NaHCO3向3号试管中继续滴加稀盐酸至过量。向4号试管中继续通入CO2气体至过量。问题五:过滤后的白色固体是什么?经灼烧后得到了什么物质?写出有关的化学方程式。Al(OH)3 1886年,美国化学家霍尔法国埃鲁通过不断摸索, 把氧化铝熔化在熔融的冰晶石(Na3AlF6)中进行电解, 终于看到小球状的铝聚集在阴极上。电解铝方法的发明冰晶石(Na3AlF6)做助熔剂,大大降低了Al2O3 的熔点。我们的收获知道 方面知识铝元素的存在形式
提炼铝的工艺流程3锻炼 种能力2实验探究能力
合作学习能力培养 种情感1珍惜资源 保护环境例题. 从铝土矿制备铝所涉及的下列有关反应中,属于氧化还原反应的是: ( )
A.铝土矿溶于NaOH溶液中
B.偏铝酸钠溶液的酸化
C.灼烧氢氧化铝固体
D.电解熔融的氧化铝
D
Al2O3+2NaOH=2NaAlO2+H2O
NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3巩固与练习 1.下列有关铝土矿中提炼铝的说法不正确的是
( )
A.铝土矿中的铝元素是以化合态存在的,需用化学方 法把铝元素变成游离态。
B.提炼过程中,先将铝土矿净化提取氧化铝,再进行冶炼。
C.可用常见的还原剂把氧化铝中的铝还原出来。
D.冶炼铝的方法同工业冶炼钠、镁相似, 可用电解法。C
Al2O3+2NaOH=2NaAlO2+H2ONaAlO2+CO2+2H2O=Al(OH)3 +NaHCO32. 从铝土矿制备铝所涉及的前两个反应,改写成离子方程式。Al2O3 + 2OH- = 2AlO2- + H2O
3. 铝及其化合物因其有优良的性能决定了具有
下列用途: ①制包装糖果和食品用的铝箔
②制易拉罐 ③制电线电缆 ④制备牙膏皮
⑤制炊具 ⑥铝合金门窗 ⑦制飞机构件
(1)由铝的良好的延展性决定的是:
(2)由铝的良好的导电导热性决定的是:
(3)由铝的合金的密度小,强度高,抗腐蚀
能力强的性质决定的是:
(4)铝元素在人体中积累可使人慢性中毒,在
食品污染源中加以控制的是:①②③④③⑤⑥⑦①②④⑤18练习:书写以下有关反应的离子方程式.Al3+Al(OH)3AlO2-①②③④⑤⑥重点:铝三角191.向AlCl3溶液中逐滴加入NaOH溶液至过量202.向NaOH溶液中逐滴加入AlCl3 溶液至过量213.向NaAlO2溶液中逐滴滴入盐酸至过量Al(OH)3+3H+=Al3++3H2O224.向HCl溶液中逐滴加入NaAlO2溶液至过量235.向AlCl3溶液中逐滴加入氨水溶液至过量246.向NaAlO2溶液中通入CO2至过量25 7.向含有物质的量相等的MgCl2 、AlCl3、HCl混合溶液中逐 滴加入NaOH至过量26练习1下面有四个实验: ①向NaOH溶液中逐滴加入AlCl3 溶液至过量 ②在明矾溶液中逐滴加入NaOH溶液至过量 ③在HCl溶液中逐滴加入NaAlO2溶液至过量 ④向NaAlO2溶液中逐滴滴入盐酸至过量 根据实验绘制出下列四种图象(y表示沉淀的 物质的量/mol, x表示加入的物质的物质的量/mol) yx0bcd实验与图像对应关系正确的是:A. ①和cB. ②和a C. ③和B D. ④和dD27练习2 有一硫酸铝和硫酸镁的混合溶液,向其中逐滴加入氢氧化钠溶液,析出沉淀的量与加入氢氧化钠溶液的体积的关系如下图所示.根据图中所标的数据求原混合液中硫酸铝和硫酸镁的物质的量之比.0沉淀量NaOH溶液体积v5V/41:128练习3、把a g铁铝合金粉末溶于足量盐酸中,加入过量NaOH溶液。过滤出沉淀,经洗涤、干燥、灼烧,得到红棕色粉末的质量仍为a g,则原合金中铁的质量分数为
A.70% B.52.4% C.47.6% D.30%A29再见
泡沫铝防护服3厨房里的铝制品铝合金门窗镁合金制品纯正镁合金
机身铝质饮料罐铝导线(一)在国宴上,
拿破仑三世使用一
套珍藏的铝制餐具,
而大臣们使用的是
银制餐具。
(二)门捷列夫创建了元素周期表,受到英国皇家学会的表彰,奖品是一只铝制奖杯。
“铝的趣史”一、铝的存在: 铝元素在自然界
以化合态形式
存在。 地壳中含量最多的金属元素是 ;
地壳里各种元素的含量图(质量分数)Al二、从铝土矿中提炼铝溶解铝土矿NaOH溶液过滤残渣二氧化碳酸化过滤滤液灼烧H2O电解铝铝土矿:主要成分为Al2O3还有少量的Fe2O3等杂质?①②③④用NaOH溶液溶解铝土矿中什么物质?问题一 :实验验证:预测:结论:可能溶解了Al2O3向装有Al2O3的试管(1号)中加入NaOH向装有Fe2O3的试管(2号)中加入NaOHFe2O3不与NaOH反应Al2O3+2NaOH=2NaAlO2+H2O偏铝酸钠问题二:NaOH溶解铝土矿后,滤液中的主要成分是什么?残渣是什么?滤液:过量的NaOH、NaAlO2残渣:Fe2O3等杂质问题三:把滤液酸化的目的是什么? 两试管都有白色沉淀生成。把滤液酸化的作用是中和过量的NaOH溶液并和NaAlO2反应产生沉淀 实验:现象:结论:向3号试管中加入NaAlO2溶液,再滴加盐酸向4号试管中加入NaAlO2溶液,再通入CO2Al(OH)3问题四:为什么工艺流程中不是用盐酸来酸化,而是通足量的CO2酸化? 实验:现象:加稀盐酸的试管中沉淀溶解通CO2的试管中沉淀不溶解结论:Al(OH)3可以溶于强酸,但不能溶于H2CO3等弱酸。NaAlO2+CO2+2H2O=Al(OH)3 +NaHCO3向3号试管中继续滴加稀盐酸至过量。向4号试管中继续通入CO2气体至过量。问题五:过滤后的白色固体是什么?经灼烧后得到了什么物质?写出有关的化学方程式。Al(OH)3 1886年,美国化学家霍尔法国埃鲁通过不断摸索, 把氧化铝熔化在熔融的冰晶石(Na3AlF6)中进行电解, 终于看到小球状的铝聚集在阴极上。电解铝方法的发明冰晶石(Na3AlF6)做助熔剂,大大降低了Al2O3 的熔点。我们的收获知道 方面知识铝元素的存在形式
提炼铝的工艺流程3锻炼 种能力2实验探究能力
合作学习能力培养 种情感1珍惜资源 保护环境例题. 从铝土矿制备铝所涉及的下列有关反应中,属于氧化还原反应的是: ( )
A.铝土矿溶于NaOH溶液中
B.偏铝酸钠溶液的酸化
C.灼烧氢氧化铝固体
D.电解熔融的氧化铝
D
Al2O3+2NaOH=2NaAlO2+H2O
NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3巩固与练习 1.下列有关铝土矿中提炼铝的说法不正确的是
( )
A.铝土矿中的铝元素是以化合态存在的,需用化学方 法把铝元素变成游离态。
B.提炼过程中,先将铝土矿净化提取氧化铝,再进行冶炼。
C.可用常见的还原剂把氧化铝中的铝还原出来。
D.冶炼铝的方法同工业冶炼钠、镁相似, 可用电解法。C
Al2O3+2NaOH=2NaAlO2+H2ONaAlO2+CO2+2H2O=Al(OH)3 +NaHCO32. 从铝土矿制备铝所涉及的前两个反应,改写成离子方程式。Al2O3 + 2OH- = 2AlO2- + H2O
3. 铝及其化合物因其有优良的性能决定了具有
下列用途: ①制包装糖果和食品用的铝箔
②制易拉罐 ③制电线电缆 ④制备牙膏皮
⑤制炊具 ⑥铝合金门窗 ⑦制飞机构件
(1)由铝的良好的延展性决定的是:
(2)由铝的良好的导电导热性决定的是:
(3)由铝的合金的密度小,强度高,抗腐蚀
能力强的性质决定的是:
(4)铝元素在人体中积累可使人慢性中毒,在
食品污染源中加以控制的是:①②③④③⑤⑥⑦①②④⑤18练习:书写以下有关反应的离子方程式.Al3+Al(OH)3AlO2-①②③④⑤⑥重点:铝三角191.向AlCl3溶液中逐滴加入NaOH溶液至过量202.向NaOH溶液中逐滴加入AlCl3 溶液至过量213.向NaAlO2溶液中逐滴滴入盐酸至过量Al(OH)3+3H+=Al3++3H2O224.向HCl溶液中逐滴加入NaAlO2溶液至过量235.向AlCl3溶液中逐滴加入氨水溶液至过量246.向NaAlO2溶液中通入CO2至过量25 7.向含有物质的量相等的MgCl2 、AlCl3、HCl混合溶液中逐 滴加入NaOH至过量26练习1下面有四个实验: ①向NaOH溶液中逐滴加入AlCl3 溶液至过量 ②在明矾溶液中逐滴加入NaOH溶液至过量 ③在HCl溶液中逐滴加入NaAlO2溶液至过量 ④向NaAlO2溶液中逐滴滴入盐酸至过量 根据实验绘制出下列四种图象(y表示沉淀的 物质的量/mol, x表示加入的物质的物质的量/mol) yx0bcd实验与图像对应关系正确的是:A. ①和cB. ②和a C. ③和B D. ④和dD27练习2 有一硫酸铝和硫酸镁的混合溶液,向其中逐滴加入氢氧化钠溶液,析出沉淀的量与加入氢氧化钠溶液的体积的关系如下图所示.根据图中所标的数据求原混合液中硫酸铝和硫酸镁的物质的量之比.0沉淀量NaOH溶液体积v5V/41:128练习3、把a g铁铝合金粉末溶于足量盐酸中,加入过量NaOH溶液。过滤出沉淀,经洗涤、干燥、灼烧,得到红棕色粉末的质量仍为a g,则原合金中铁的质量分数为
A.70% B.52.4% C.47.6% D.30%A29再见
