人教版化学九上第六单元 课题3 二氧化碳和一氧化碳 提优练(word 含解析)
文档属性
| 名称 | 人教版化学九上第六单元 课题3 二氧化碳和一氧化碳 提优练(word 含解析) |
|
|
| 格式 | docx | ||
| 文件大小 | 629.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-10 00:00:00 | ||
图片预览

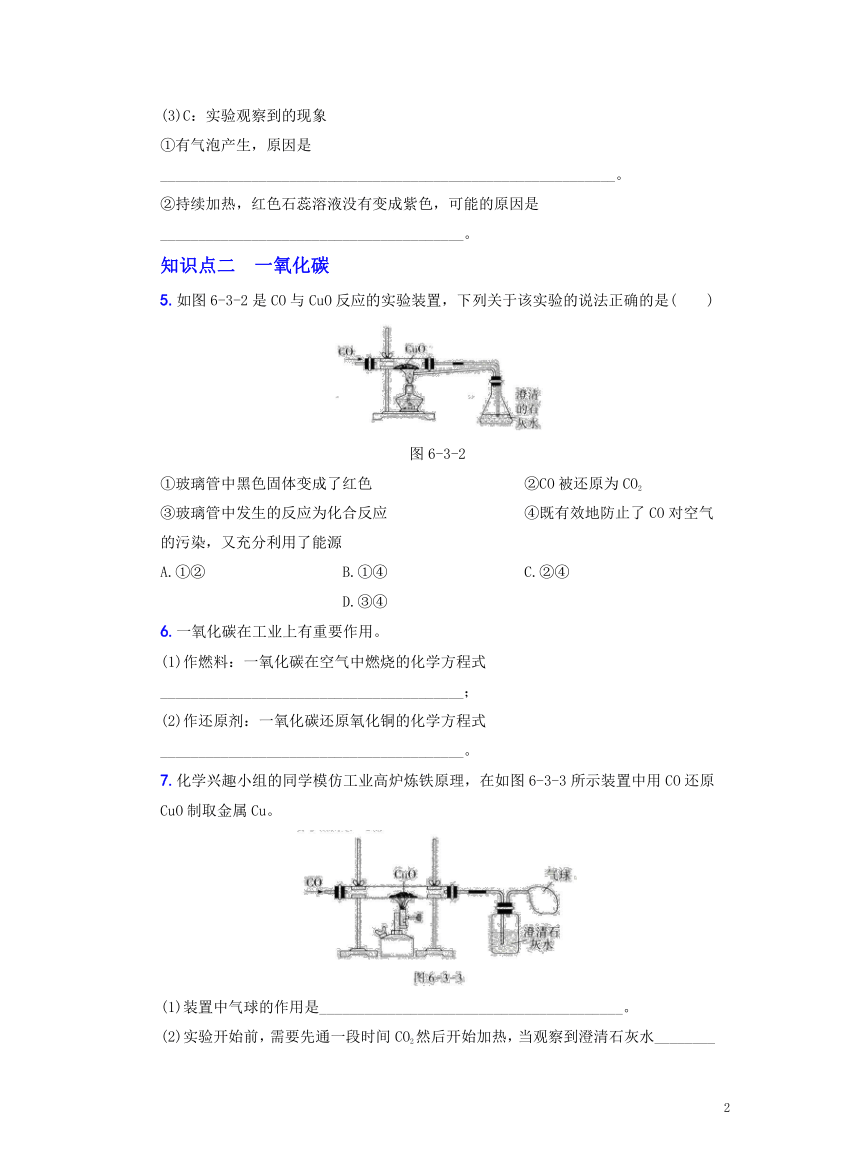
文档简介
第六单元 碳和碳的氧化物
课题3 二氧化碳和一氧化碳
知识能力全练
知识点一 二氧化碳
1.关于二氧化碳的说法中,正确的是( )
A.由一个碳原子和一个氧分子构成 B.由一个碳原子和两个氧原子构成
C.由碳元素和氧元素组成 D.大气中CO2的消耗途径主要是绿色植物的呼吸作用
2.下列实验或现象不能说明二氧化碳的密度比空气大的是( )
3.某班同学在对CO2进行功与过的讨论时,列举的以下事实既可以体现CO2的功,又可以体现CO2的过的是( )
A.CO2可以使人窒息 B.CO2可以作气体肥料 C.CO2可以产生温室效应 D.固态CO2可用于人工降雨
4.实验课上,小明和同学们完成了实验室制取二氧化碳和验证二氧化碳性质的实验,并进行了相关问题的思考。请结合图文信息完成下列任务。
(1)仪器a的名称是________。
(2)A:制取二氧化碳的化学方程式为________________
(3)C:实验观察到的现象
①有气泡产生,原因是____________________________________________________________。
②持续加热,红色石蕊溶液没有变成紫色,可能的原因是________________________________________。
知识点二 一氧化碳
5.如图6-3-2是CO与CuO反应的实验装置,下列关于该实验的说法正确的是( )
图6-3-2
①玻璃管中黑色固体变成了红色 ②CO被还原为CO2
③玻璃管中发生的反应为化合反应 ④既有效地防止了CO对空气的污染,又充分利用了能源
A.①② B.①④ C.②④ D.③④
6.一氧化碳在工业上有重要作用。
(1)作燃料:一氧化碳在空气中燃烧的化学方程式________________________________________;
(2)作还原剂:一氧化碳还原氧化铜的化学方程式________________________________________。
7.化学兴趣小组的同学模仿工业高炉炼铁原理,在如图6-3-3所示装置中用CO还原CuO制取金属Cu。
(1)装置中气球的作用是________________________________________。
(2)实验开始前,需要先通一段时间CO2然后开始加热,当观察到澄清石灰水________的现象,说明CO与CuO已经发生反应。
(3)为确定反应的最佳温度,兴趣小组利用原位X射线粉末衍射仪来测定不同温度下反应4小时后的固体物质成分,实验结果如图6-3-4所示(该图谱可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同),据图回答下列问题:
①400℃时,反应的固体产物中含有Cu和________。
②500℃时,该反应的化学方程式为________________________________________。
③用CO还原CuO制取纯净的Cu,反应温度至少要控制在________℃以上。
模拟全练
8.将二氧化碳通人紫色石蕊溶液中,然后将其进行加热,冷却后再加入一定量的活性炭,充分振荡后静止。在这个过程中,液体颜色变化的顺序是( )
A.紫→红→紫→无 B.紫→红→蓝→无 C.紫→蓝→红→无 D.紫→红→蓝→紫
9.下列关于碳及其化合物的说法,正确的是( )
A.CO和CO2都可将氧化铜还原成铜
B.大气中二氧化碳消耗的途径主要是绿色植物的光合作用
C.在室内放一盆澄清石灰水可防止CO中毒
D.温室效应严重影响了人类的生存,我们应想方设法消除二氧化碳等导致的温室效应
《参考答案及解析》
课题3 二氧化碳和一氧化碳
知识能力全练
1.C 二氧化碳是由二氧化碳分子构成的,A错;一个碳原子和两个氧原子只能构成一个二氧化碳分子,B错;物质是由元素组成的,二氧化碳由碳元素和氧元素组成,C正确;二氧化碳是绿色植物光合作用的原料,大气中二氧化碳的消耗途径主要是光合作用,D错。
2.B 用向上排空气法收集二氧化碳,说明二氧化碳的密度比空气的大;往盛有二氧化碳的塑料瓶中倒入一定量水,振荡后发现塑料瓶变瘪,说明二氧化碳能溶于水;往烧杯中倒入二氧化碳气体,充满空气的气球上浮,说明二氧化碳的密度比空气的大;倒入二氧化碳的纸袋下沉,充分证明了二氧化碳的密度比空气的大。
3.C A项仅体现了CO2的过;B.D项均只体现了CO2的功;正是因为有了温室效应,全球平均地表温度才提高到目前适合人类生存的15℃,但是全球变暖已使人类的生存环境受到了严重的威胁,因此,温室效应既体现了二氧化碳的功,又体现了二氧化碳的过.故选C。
4.【答案】(1)锥形瓶
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)①碳酸受热分解有二氧化碳气体生成(合理即可)
②二氧化碳气体中混有氯化氢气体或溶液中含有盐酸(合理即可)
【解析】(1)由图可知,仪器a的名称是锥形瓶。
(2)实验室通常用石灰石或大理石和稀盐酸反应制取二氧化碳,石灰石或大理石的主要成分是碳酸钙,碳酸钙与稀盐酸反应生成氯化钙、二氧化碳和水,该反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑。
(3)①碳酸受热分解为二氧化碳和水,故有气泡产生;②盐酸具有挥发性,二氧化碳气体中可能混有氯化氢气体,氯化氢溶于水形成盐酸,盐酸显酸性,能使紫色石蕊溶液变红,故持续加热,红色石蕊溶液没有变成紫色。
5.B 一氧化碳具有还原性,能与氧化铜反应生成铜和二氧化碳,会观察到玻璃管中黑色固体变成了红色,①正确;一氧化碳夺取了氧化铜中的氧,CO被氧化为CO2②错误;一氧化碳与氧化铜反应生成铜和二氧化碳,两种物质反应生成两种物质,不属于化合反应,③错误;一氧化碳燃烧生成二氧化碳,利用一氧化碳燃烧产生的热量给玻璃管加热,既有效地防止了CO对空气的污染,又充分利用了能源,④正确.故选B。
6.【答案】(1)2CO+022CO2 (2)CuO+COCu+CO2
【解析】(1)一氧化碳在空气中燃烧生成二氧化碳,反应的化学方程式点燃是2CO+022CO2;
(2)一氧化碳还原氧化铜生成铜和二氧化碳,反△应的化学方程式是CuO+COCu+CO2
7.【答案】(1)收集尾气,防止污染环境 (2)变浑浊 (3)①Cu20 ②CO+CuOCu+CO2 ③500
【解析】:(1)尾气中含有有毒的一氧化碳,装置中气球的作用是收集尾气,防止污染环境。
(2)当观察到澄清石灰水变浑浊的现象时,说明CO与CuO已经发生反应,因为加热条件下一氧化碳与氧化铜反应会生成二氧化碳,二氧化碳能使澄清石灰水变浑浊。
(3)①根据图示可知,400℃时,反应的固体产物中含有Cu和Cu20。②根据图示可知,500℃时,固体产物中只含有Cu,即一氧化碳与氧化铜在加热条件下反应生成铜和二氧化碳,该反应的化学方程式为CO+CuOCu+CO2。③根据图示可知,500℃及以上温度时,固体产物只有铜,故用CO还原CuO制取纯净的Cu,反应温度至少要控制在500℃以上。
模拟全练
8.A 二氧化碳通入紫色石蕊溶液中,二氧化碳与水反应生成碳酸,碳酸使紫色石蕊溶液由紫色变为红色;加热后碳酸分解,溶液又由红变紫;冷却后加入活性炭,活性炭具有吸附性,吸附溶液中的颜色,最终溶液变为无色.故选A。
9.B 一氧化碳具有还原性,可将氧化铜还原成铜;二氧化碳不具有还原性,不能将氧化铜还原成铜,A错误。大气中二氧化碳消耗的途径主要是绿色植物的光合作用,B正确。一氧化碳难溶于水且不与澄清石灰水反应,在室内放一盆澄清石灰水不能防止CO中毒,C错误。因为有了温室效应,全球平均地表温度才提高到目前适合人类生存的15℃,因此不能消除二氧化碳等导致的温室效应,D错误。
1
课题3 二氧化碳和一氧化碳
知识能力全练
知识点一 二氧化碳
1.关于二氧化碳的说法中,正确的是( )
A.由一个碳原子和一个氧分子构成 B.由一个碳原子和两个氧原子构成
C.由碳元素和氧元素组成 D.大气中CO2的消耗途径主要是绿色植物的呼吸作用
2.下列实验或现象不能说明二氧化碳的密度比空气大的是( )
3.某班同学在对CO2进行功与过的讨论时,列举的以下事实既可以体现CO2的功,又可以体现CO2的过的是( )
A.CO2可以使人窒息 B.CO2可以作气体肥料 C.CO2可以产生温室效应 D.固态CO2可用于人工降雨
4.实验课上,小明和同学们完成了实验室制取二氧化碳和验证二氧化碳性质的实验,并进行了相关问题的思考。请结合图文信息完成下列任务。
(1)仪器a的名称是________。
(2)A:制取二氧化碳的化学方程式为________________
(3)C:实验观察到的现象
①有气泡产生,原因是____________________________________________________________。
②持续加热,红色石蕊溶液没有变成紫色,可能的原因是________________________________________。
知识点二 一氧化碳
5.如图6-3-2是CO与CuO反应的实验装置,下列关于该实验的说法正确的是( )
图6-3-2
①玻璃管中黑色固体变成了红色 ②CO被还原为CO2
③玻璃管中发生的反应为化合反应 ④既有效地防止了CO对空气的污染,又充分利用了能源
A.①② B.①④ C.②④ D.③④
6.一氧化碳在工业上有重要作用。
(1)作燃料:一氧化碳在空气中燃烧的化学方程式________________________________________;
(2)作还原剂:一氧化碳还原氧化铜的化学方程式________________________________________。
7.化学兴趣小组的同学模仿工业高炉炼铁原理,在如图6-3-3所示装置中用CO还原CuO制取金属Cu。
(1)装置中气球的作用是________________________________________。
(2)实验开始前,需要先通一段时间CO2然后开始加热,当观察到澄清石灰水________的现象,说明CO与CuO已经发生反应。
(3)为确定反应的最佳温度,兴趣小组利用原位X射线粉末衍射仪来测定不同温度下反应4小时后的固体物质成分,实验结果如图6-3-4所示(该图谱可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同),据图回答下列问题:
①400℃时,反应的固体产物中含有Cu和________。
②500℃时,该反应的化学方程式为________________________________________。
③用CO还原CuO制取纯净的Cu,反应温度至少要控制在________℃以上。
模拟全练
8.将二氧化碳通人紫色石蕊溶液中,然后将其进行加热,冷却后再加入一定量的活性炭,充分振荡后静止。在这个过程中,液体颜色变化的顺序是( )
A.紫→红→紫→无 B.紫→红→蓝→无 C.紫→蓝→红→无 D.紫→红→蓝→紫
9.下列关于碳及其化合物的说法,正确的是( )
A.CO和CO2都可将氧化铜还原成铜
B.大气中二氧化碳消耗的途径主要是绿色植物的光合作用
C.在室内放一盆澄清石灰水可防止CO中毒
D.温室效应严重影响了人类的生存,我们应想方设法消除二氧化碳等导致的温室效应
《参考答案及解析》
课题3 二氧化碳和一氧化碳
知识能力全练
1.C 二氧化碳是由二氧化碳分子构成的,A错;一个碳原子和两个氧原子只能构成一个二氧化碳分子,B错;物质是由元素组成的,二氧化碳由碳元素和氧元素组成,C正确;二氧化碳是绿色植物光合作用的原料,大气中二氧化碳的消耗途径主要是光合作用,D错。
2.B 用向上排空气法收集二氧化碳,说明二氧化碳的密度比空气的大;往盛有二氧化碳的塑料瓶中倒入一定量水,振荡后发现塑料瓶变瘪,说明二氧化碳能溶于水;往烧杯中倒入二氧化碳气体,充满空气的气球上浮,说明二氧化碳的密度比空气的大;倒入二氧化碳的纸袋下沉,充分证明了二氧化碳的密度比空气的大。
3.C A项仅体现了CO2的过;B.D项均只体现了CO2的功;正是因为有了温室效应,全球平均地表温度才提高到目前适合人类生存的15℃,但是全球变暖已使人类的生存环境受到了严重的威胁,因此,温室效应既体现了二氧化碳的功,又体现了二氧化碳的过.故选C。
4.【答案】(1)锥形瓶
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)①碳酸受热分解有二氧化碳气体生成(合理即可)
②二氧化碳气体中混有氯化氢气体或溶液中含有盐酸(合理即可)
【解析】(1)由图可知,仪器a的名称是锥形瓶。
(2)实验室通常用石灰石或大理石和稀盐酸反应制取二氧化碳,石灰石或大理石的主要成分是碳酸钙,碳酸钙与稀盐酸反应生成氯化钙、二氧化碳和水,该反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑。
(3)①碳酸受热分解为二氧化碳和水,故有气泡产生;②盐酸具有挥发性,二氧化碳气体中可能混有氯化氢气体,氯化氢溶于水形成盐酸,盐酸显酸性,能使紫色石蕊溶液变红,故持续加热,红色石蕊溶液没有变成紫色。
5.B 一氧化碳具有还原性,能与氧化铜反应生成铜和二氧化碳,会观察到玻璃管中黑色固体变成了红色,①正确;一氧化碳夺取了氧化铜中的氧,CO被氧化为CO2②错误;一氧化碳与氧化铜反应生成铜和二氧化碳,两种物质反应生成两种物质,不属于化合反应,③错误;一氧化碳燃烧生成二氧化碳,利用一氧化碳燃烧产生的热量给玻璃管加热,既有效地防止了CO对空气的污染,又充分利用了能源,④正确.故选B。
6.【答案】(1)2CO+022CO2 (2)CuO+COCu+CO2
【解析】(1)一氧化碳在空气中燃烧生成二氧化碳,反应的化学方程式点燃是2CO+022CO2;
(2)一氧化碳还原氧化铜生成铜和二氧化碳,反△应的化学方程式是CuO+COCu+CO2
7.【答案】(1)收集尾气,防止污染环境 (2)变浑浊 (3)①Cu20 ②CO+CuOCu+CO2 ③500
【解析】:(1)尾气中含有有毒的一氧化碳,装置中气球的作用是收集尾气,防止污染环境。
(2)当观察到澄清石灰水变浑浊的现象时,说明CO与CuO已经发生反应,因为加热条件下一氧化碳与氧化铜反应会生成二氧化碳,二氧化碳能使澄清石灰水变浑浊。
(3)①根据图示可知,400℃时,反应的固体产物中含有Cu和Cu20。②根据图示可知,500℃时,固体产物中只含有Cu,即一氧化碳与氧化铜在加热条件下反应生成铜和二氧化碳,该反应的化学方程式为CO+CuOCu+CO2。③根据图示可知,500℃及以上温度时,固体产物只有铜,故用CO还原CuO制取纯净的Cu,反应温度至少要控制在500℃以上。
模拟全练
8.A 二氧化碳通入紫色石蕊溶液中,二氧化碳与水反应生成碳酸,碳酸使紫色石蕊溶液由紫色变为红色;加热后碳酸分解,溶液又由红变紫;冷却后加入活性炭,活性炭具有吸附性,吸附溶液中的颜色,最终溶液变为无色.故选A。
9.B 一氧化碳具有还原性,可将氧化铜还原成铜;二氧化碳不具有还原性,不能将氧化铜还原成铜,A错误。大气中二氧化碳消耗的途径主要是绿色植物的光合作用,B正确。一氧化碳难溶于水且不与澄清石灰水反应,在室内放一盆澄清石灰水不能防止CO中毒,C错误。因为有了温室效应,全球平均地表温度才提高到目前适合人类生存的15℃,因此不能消除二氧化碳等导致的温室效应,D错误。
1
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
