第7章化学反应的定量研究单元测试题--2022-2023学年九年级化学京改版(2013)上册(有答案)
文档属性
| 名称 | 第7章化学反应的定量研究单元测试题--2022-2023学年九年级化学京改版(2013)上册(有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 166.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-10 00:00:00 | ||
图片预览



文档简介
第7章化学反应的定量研究单元测试题--2022-2023学年九年级化学京改版(2013)上册
一、单选题
1.连花清瘟胶囊源自传统中医名方,可用于治疗流感,现代仪器测得其成分之一是没食子酸(化学式为C7H6O5)。下列有关没食子酸的说法,正确的是( )
A.属于氧化物 B.碳、氢、氧元素的质量比为12∶1∶16
C.含有3个原子 D.完全燃烧生成CO2和H2O
2.石笋和钟乳石的形成蕴含许多化学原理,其反应之一为: 则X的化学式为
A.CaCO3 B.Ca(OH)2 C.CaO D.CaH2
3.石灰氮(化学式为CaCN2)是一种固态肥料,遇水发生反应的现象为CaCN2+3H2O=CaCO3+2X,则x化学式为
A.NO B.N2 C.CO2 D.NH3
4.在实验室和化工生产中常用到硝酸。硝酸是一种强氧化剂,能与碳发生氧化还原反应,现象为。则X是
A.NO2
B.CO
C.NO
D.N2O5
5.下列现象书写完全正确的是( )
A.CO+CuOCu+CO2↑ B.2P+5O22P2O5
C.3Fe+2O2Fe3O4 D.Al+2HCl=AlCl2+H2↑
6.甲酸(HCOOH)具有清洁制氢的巨大潜力,其分解前后分子种类变化的微观示意图如下:
下列说法正确的是
A.甲酸分子中氢、氧原子个数比为1:2
B.乙中碳、氧元素质量比为1:2
C.46g甲酸中氢元素质量为2g
D.生成甲与乙的分子个数比为2:1
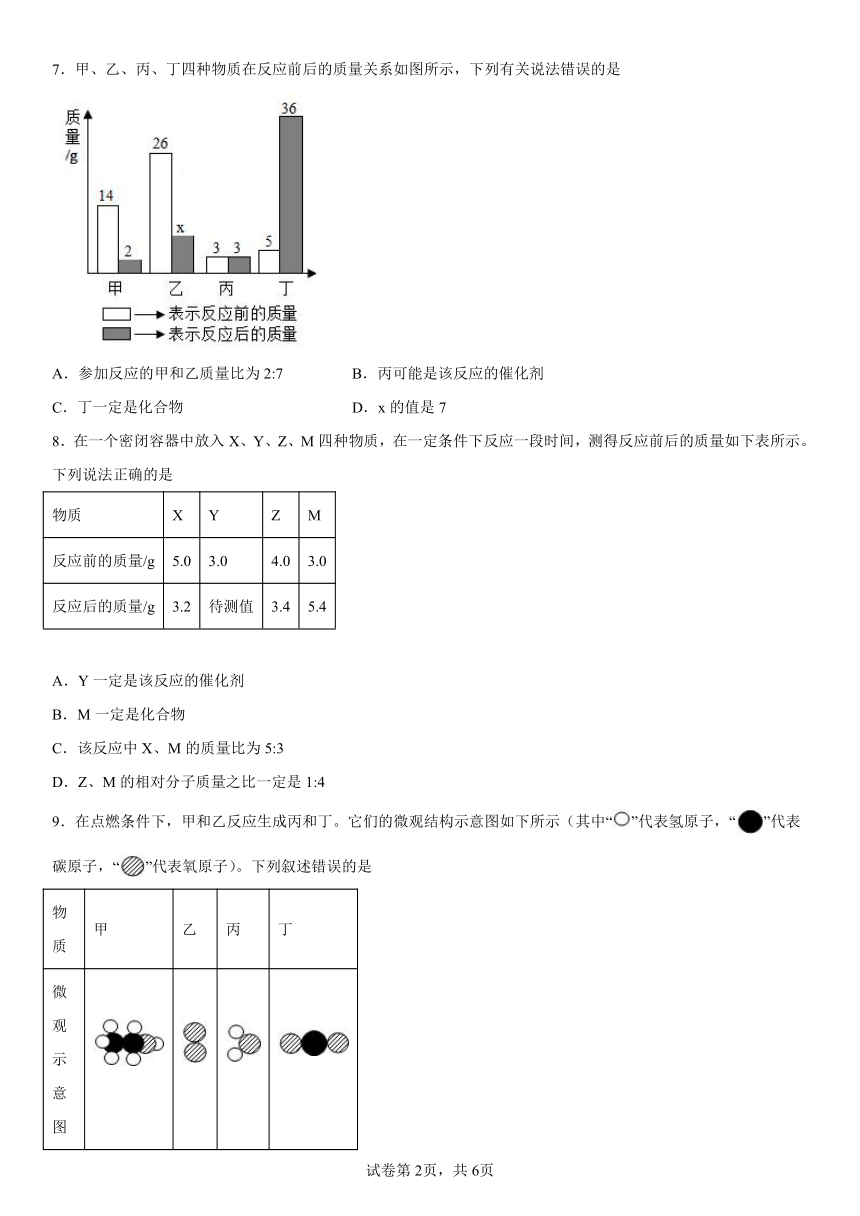
7.甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是
A.参加反应的甲和乙质量比为2:7 B.丙可能是该反应的催化剂
C.丁一定是化合物 D.x的值是7
8.在一个密闭容器中放入X、Y、Z、M四种物质,在一定条件下反应一段时间,测得反应前后的质量如下表所示。下列说法正确的是
物质 X Y Z M
反应前的质量/g 5.0 3.0 4.0 3.0
反应后的质量/g 3.2 待测值 3.4 5.4
A.Y一定是该反应的催化剂
B.M一定是化合物
C.该反应中X、M的质量比为5:3
D.Z、M的相对分子质量之比一定是1:4
9.在点燃条件下,甲和乙反应生成丙和丁。它们的微观结构示意图如下所示(其中“”代表氢原子,“”代表碳原子,“”代表氧原子)。下列叙述错误的是
物质 甲 乙 丙 丁
微观示意图
A.生成物均为氧化物
B.甲中碳、氢、氧三种元素的质量比为12:3:8
C.在该反应中,生成丙和丁的质量比为3:11
D.在该反应中,甲和乙的分子个数比为1:3
10.某化合物完全燃烧,需要氧气,同时生成二氧化碳和水,则该化合物( )
A.含有碳、氢、氧三种元素 B.只含碳、氧两种元素
C.只含碳、氢两种元素 D.无法确定
11.在宏观、微观和符号之间建立联系是化学学科的特点,如图是某化学反应的微观过程示意图(“○”表示 A 原子,“●”表示 B 原子),下列说法不正确的是
A.该反应属于化合反应
B.从宏观角度看,物质丙属于混合物
C.化学反应前后原子的种类、数目均不变
D.参加反应的甲、乙两物质的微粒个数比为 3:2
12.创新改进实验是学习化学的有效方法。下列对实验的创新改进能够达到实验目的的是
A.测定空气中氧气的含量
B.证明分子在不停地运动
C.验证质量守恒定律
D.探究燃烧的条件
二、填空题
13.硫在氧气中燃烧的现象是:S+O2SO2.这个式子不仅表明了反应物是_______,生成物是______,反应条件是______,还表示了参与反应的各物质之间的质量关系,即在点燃条件下,每______份质量的硫 ______份质量的氧气恰好完全反应生成______份质量的二氧化硫.
14.如图所示的是硫在氧气中燃烧的实验。燃烧停止后,取出燃烧匙,用毛玻璃片盖紧集气瓶,振荡,悬空倒置,发现毛玻璃片不脱落。
(1)硫在氧气中燃烧的现象为___,水的的作用是___。
(2)毛玻璃片不脱落时,大气压强___(选填"大于”“小于”或“等于”)瓶内气体压强。
15.水是生命之源,是人类宝贵的自然资源。
Ⅰ:节约用水
(1)下列图标是我国“国家节水标志”的是_______(填字母)。
A. B. C. D.
(2)预防和治理水污染,保护和改善水质,下列做法错误的是_______(填字母序号)。
A.生活污水处理后再排放 B.合理使用农药和化肥 C.为降低成本,工业废水直接排放
Ⅱ:水的净化
(3)“沉降池”中可用明矾作混凝剂,其作用为__________。
(4)过滤的操作可以除去难溶性杂质,实验室中过滤操作需要的玻璃仪器有烧杯、漏斗和_____。
(5)“吸附池”中常用________(填物质名称)吸附色素和异味。
Ⅲ:废水处理
(6)废水中氨氮(以 NH3形式存在)含量过高,直接排放会导致水体富营养化。次氯酸(HClO)可除去废水中的 NH3,发生的反应为:。X 的化学式为_______。
IV:验证水的组成可以进行电解水的实验(如图 A)。
(7)试管 a 中的气体是__________(填化学式)。
(8)电解水的现象为____________。
(9)电解水的实验证明水是由____________组成的。
16.下图是某反应的微观示意图。
请回答:
(1)B框中的物质属于___________(填序号:①化合物、②单质、③纯净物、④混合物)。
(2)此反应的现象为_____________________________,此图说明化学反应前后发生改变的微粒是_________。
三、实验题
17.小明利用如图1装置,称量了白磷被引燃前后整个装置的总质量,验证了质量守恒定律。
(1)白磷燃烧属于化学反应基本类型中的_____反应。
(2)实验过程中可观察到气球体积变化情况是_____。
(3)图2中,锥形瓶中固态物质的质量m随时间t的变化关系正确的是_____。
18.小明用蜡烛进行了下列活动。
(1)活动1:点燃蜡烛后,电子称示数逐渐减小。蜡烛减小的质量_______(填“大于”“等于”或“小于”)燃烧后生成物的总质量。
(2)活动2:加入泡腾片(主要成分含柠檬酸、碳酸氢钠等),观察到水中产生大量气泡,蜡烛逐渐熄灭。产生上述现象的原因是___________。
(3)活动3:用玻璃杯迅速扣住燃烧的蜡烛,并使杯口始终浸没在水中。下列说法正确的是_______(填序号)。
A可观察到蜡烛熄灭 B最终杯中液面高于碗中液面 C该方法能准确测定空气中氧气的含量
四、计算题
19.电解法是金属的冶炼方法之一。工业上制取金属钠的现象为:2NaCl(熔融)2Na+Cl2↑,生产 92 吨金属钠,消耗多少吨氯化钠?
20.氢气的储存是科学研究热点之一。X是一种储存氢气的材料,取11.2g X在O2中完全燃烧后只生成8.0g CuO、8.0g MgO。
(1)上述燃烧过程中消耗O2的质量为多少克。
(2)通过计算求X中各元素的原子个数比?试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.A
3.D
4.A
5.C
6.C
7.A
8.B
9.C
10.A
11.D
12.A
13. (1) 硫和氧气 二氧化硫 (2) 点燃 32 32 64
14.(1) 吸收二氧化硫,防止污染空气
(2)大于
15.(1)B
(2)C
(3)吸附沉降
(4)玻璃棒
(5)活性炭
(6)N2
(7)H2
(8)氢元素、氧元素
16.(1) ② (2) 分子
17. (1) 化合 (2) 开始变大后来变小 C
18. (1) 小于 (2)柠檬酸和碳酸氢钠生成的CO2比空气密度大而将空气挤走,导致蜡烛周围没有O2(隔绝O2) A、B
19.解:设消耗NaCl的质量为x
x=234t。
答:消耗NaCl的质量为234吨。
20.(1)4.8(2)1:2
答案第1页,共2页
答案第1页,共2页
一、单选题
1.连花清瘟胶囊源自传统中医名方,可用于治疗流感,现代仪器测得其成分之一是没食子酸(化学式为C7H6O5)。下列有关没食子酸的说法,正确的是( )
A.属于氧化物 B.碳、氢、氧元素的质量比为12∶1∶16
C.含有3个原子 D.完全燃烧生成CO2和H2O
2.石笋和钟乳石的形成蕴含许多化学原理,其反应之一为: 则X的化学式为
A.CaCO3 B.Ca(OH)2 C.CaO D.CaH2
3.石灰氮(化学式为CaCN2)是一种固态肥料,遇水发生反应的现象为CaCN2+3H2O=CaCO3+2X,则x化学式为
A.NO B.N2 C.CO2 D.NH3
4.在实验室和化工生产中常用到硝酸。硝酸是一种强氧化剂,能与碳发生氧化还原反应,现象为。则X是
A.NO2
B.CO
C.NO
D.N2O5
5.下列现象书写完全正确的是( )
A.CO+CuOCu+CO2↑ B.2P+5O22P2O5
C.3Fe+2O2Fe3O4 D.Al+2HCl=AlCl2+H2↑
6.甲酸(HCOOH)具有清洁制氢的巨大潜力,其分解前后分子种类变化的微观示意图如下:
下列说法正确的是
A.甲酸分子中氢、氧原子个数比为1:2
B.乙中碳、氧元素质量比为1:2
C.46g甲酸中氢元素质量为2g
D.生成甲与乙的分子个数比为2:1
7.甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是
A.参加反应的甲和乙质量比为2:7 B.丙可能是该反应的催化剂
C.丁一定是化合物 D.x的值是7
8.在一个密闭容器中放入X、Y、Z、M四种物质,在一定条件下反应一段时间,测得反应前后的质量如下表所示。下列说法正确的是
物质 X Y Z M
反应前的质量/g 5.0 3.0 4.0 3.0
反应后的质量/g 3.2 待测值 3.4 5.4
A.Y一定是该反应的催化剂
B.M一定是化合物
C.该反应中X、M的质量比为5:3
D.Z、M的相对分子质量之比一定是1:4
9.在点燃条件下,甲和乙反应生成丙和丁。它们的微观结构示意图如下所示(其中“”代表氢原子,“”代表碳原子,“”代表氧原子)。下列叙述错误的是
物质 甲 乙 丙 丁
微观示意图
A.生成物均为氧化物
B.甲中碳、氢、氧三种元素的质量比为12:3:8
C.在该反应中,生成丙和丁的质量比为3:11
D.在该反应中,甲和乙的分子个数比为1:3
10.某化合物完全燃烧,需要氧气,同时生成二氧化碳和水,则该化合物( )
A.含有碳、氢、氧三种元素 B.只含碳、氧两种元素
C.只含碳、氢两种元素 D.无法确定
11.在宏观、微观和符号之间建立联系是化学学科的特点,如图是某化学反应的微观过程示意图(“○”表示 A 原子,“●”表示 B 原子),下列说法不正确的是
A.该反应属于化合反应
B.从宏观角度看,物质丙属于混合物
C.化学反应前后原子的种类、数目均不变
D.参加反应的甲、乙两物质的微粒个数比为 3:2
12.创新改进实验是学习化学的有效方法。下列对实验的创新改进能够达到实验目的的是
A.测定空气中氧气的含量
B.证明分子在不停地运动
C.验证质量守恒定律
D.探究燃烧的条件
二、填空题
13.硫在氧气中燃烧的现象是:S+O2SO2.这个式子不仅表明了反应物是_______,生成物是______,反应条件是______,还表示了参与反应的各物质之间的质量关系,即在点燃条件下,每______份质量的硫 ______份质量的氧气恰好完全反应生成______份质量的二氧化硫.
14.如图所示的是硫在氧气中燃烧的实验。燃烧停止后,取出燃烧匙,用毛玻璃片盖紧集气瓶,振荡,悬空倒置,发现毛玻璃片不脱落。
(1)硫在氧气中燃烧的现象为___,水的的作用是___。
(2)毛玻璃片不脱落时,大气压强___(选填"大于”“小于”或“等于”)瓶内气体压强。
15.水是生命之源,是人类宝贵的自然资源。
Ⅰ:节约用水
(1)下列图标是我国“国家节水标志”的是_______(填字母)。
A. B. C. D.
(2)预防和治理水污染,保护和改善水质,下列做法错误的是_______(填字母序号)。
A.生活污水处理后再排放 B.合理使用农药和化肥 C.为降低成本,工业废水直接排放
Ⅱ:水的净化
(3)“沉降池”中可用明矾作混凝剂,其作用为__________。
(4)过滤的操作可以除去难溶性杂质,实验室中过滤操作需要的玻璃仪器有烧杯、漏斗和_____。
(5)“吸附池”中常用________(填物质名称)吸附色素和异味。
Ⅲ:废水处理
(6)废水中氨氮(以 NH3形式存在)含量过高,直接排放会导致水体富营养化。次氯酸(HClO)可除去废水中的 NH3,发生的反应为:。X 的化学式为_______。
IV:验证水的组成可以进行电解水的实验(如图 A)。
(7)试管 a 中的气体是__________(填化学式)。
(8)电解水的现象为____________。
(9)电解水的实验证明水是由____________组成的。
16.下图是某反应的微观示意图。
请回答:
(1)B框中的物质属于___________(填序号:①化合物、②单质、③纯净物、④混合物)。
(2)此反应的现象为_____________________________,此图说明化学反应前后发生改变的微粒是_________。
三、实验题
17.小明利用如图1装置,称量了白磷被引燃前后整个装置的总质量,验证了质量守恒定律。
(1)白磷燃烧属于化学反应基本类型中的_____反应。
(2)实验过程中可观察到气球体积变化情况是_____。
(3)图2中,锥形瓶中固态物质的质量m随时间t的变化关系正确的是_____。
18.小明用蜡烛进行了下列活动。
(1)活动1:点燃蜡烛后,电子称示数逐渐减小。蜡烛减小的质量_______(填“大于”“等于”或“小于”)燃烧后生成物的总质量。
(2)活动2:加入泡腾片(主要成分含柠檬酸、碳酸氢钠等),观察到水中产生大量气泡,蜡烛逐渐熄灭。产生上述现象的原因是___________。
(3)活动3:用玻璃杯迅速扣住燃烧的蜡烛,并使杯口始终浸没在水中。下列说法正确的是_______(填序号)。
A可观察到蜡烛熄灭 B最终杯中液面高于碗中液面 C该方法能准确测定空气中氧气的含量
四、计算题
19.电解法是金属的冶炼方法之一。工业上制取金属钠的现象为:2NaCl(熔融)2Na+Cl2↑,生产 92 吨金属钠,消耗多少吨氯化钠?
20.氢气的储存是科学研究热点之一。X是一种储存氢气的材料,取11.2g X在O2中完全燃烧后只生成8.0g CuO、8.0g MgO。
(1)上述燃烧过程中消耗O2的质量为多少克。
(2)通过计算求X中各元素的原子个数比?试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.A
3.D
4.A
5.C
6.C
7.A
8.B
9.C
10.A
11.D
12.A
13. (1) 硫和氧气 二氧化硫 (2) 点燃 32 32 64
14.(1) 吸收二氧化硫,防止污染空气
(2)大于
15.(1)B
(2)C
(3)吸附沉降
(4)玻璃棒
(5)活性炭
(6)N2
(7)H2
(8)氢元素、氧元素
16.(1) ② (2) 分子
17. (1) 化合 (2) 开始变大后来变小 C
18. (1) 小于 (2)柠檬酸和碳酸氢钠生成的CO2比空气密度大而将空气挤走,导致蜡烛周围没有O2(隔绝O2) A、B
19.解:设消耗NaCl的质量为x
x=234t。
答:消耗NaCl的质量为234吨。
20.(1)4.8(2)1:2
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第1章 走进化学
- 第一节 化学让世界更美好
- 第二节 实验是化学的基础
- 第2章 空气之谜
- 第一节 空气
- 第二节 氧气的制法
- 第三节 氧气的性质
- 第3章 构成物质的微粒
- 第一节 原子
- 第二节 原子核外电子的排布 离子
- 第三节 分子
- 第4章 最常见的液体——水
- 第一节 水的净化
- 第二节 水的变化
- 第三节 水资源的开发、利用和保护
- 第5章 化学元素与物质组成的表示
- 第一节 初步认识化学元素
- 第二节 物质组成的表示——化学式
- 第三节 化合价
- 第6章 燃烧的学问
- 第一节 探索燃烧与灭火
- 第二节 化学反应中的能量变化
- 第三节 化石燃料
- 第7章 化学反应的定量研究
- 第一节 质量守恒定律
- 第二节 化学方程式
- 第三节 依据化学方程式的简单计算
- 第8章 碳的世界
- 第一节 碳的单质
- 第二节 二氧化碳的性质和用途
- 第三节 二氧化碳的实验室制法
