第6章《常用的金属和盐》基础练习 九年级化学沪教版(上海)第二学期(有答案)
文档属性
| 名称 | 第6章《常用的金属和盐》基础练习 九年级化学沪教版(上海)第二学期(有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 139.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-10 00:00:00 | ||
图片预览



文档简介
第6章《常用的金属和盐》基础练习
一、单选题
1.下列有关金属的说法正确的是
A.所有金属都呈银白色 B.常温下所有的金属都是固体
C.合金的硬度一般比各成分金属小 D.铝制品耐腐蚀是因为表面生成致密氧化膜
2.金属材料在生产,生活中使用广泛。下列金属的用途利用了金属导电性的是
A.铜制电线 B.铁质铁锅 C.金制项链 D.铝制饮料罐
3.小玲家的水稻出现了倒伏现象,急需施用的化肥是( )
A.CO(NH2)2 B.Ca3(PO4)2 C.K2SO4 D.NH4Cl
4.金属材料在人类活动中已得到越来越广泛的应用。下列性质属于金属共性的是
A.熔点很高 B.有良好的导电性、导热性
C.银白色的固体 D.硬度很大
5.下列物质的名称或俗名,属同一种物质的是
A.生石灰 熟石灰 消石灰 B.冰 干冰 可燃冰
C.烧碱 苛性钠 火碱 D.石灰石 熟石灰 大理石
6.某同学总结的Ca(OH)2的化学性质如图,下列说法错误的是
A.甲一定是碳酸盐
B.反应②为放热反应
C.反应③可用于检验某种温室气体
D.向澄清石灰水中加入紫色石蕊试液,试液由紫色变为蓝色
7.港珠澳大桥的桥、岛、隧以及“雪龙2号”的船身等主要由金属材料制成。下列金属防护措施不正确的是
A.在金属制品表面镀保护层
B.改变金属结构制成合金使用
C.在金属制品表面涂油漆
D.用稀盐酸定期清洗金属制品
8.下图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。下列说法不正确的是
A.①中甲、乙、丙三处比较,生锈最明显的地方是甲
B.①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水
C.③中附着在棉花上的氯化钙的作用是作干燥剂
D.四个实验中,生锈最快的是④中的铁钉
9.草木灰是一种农家肥,其主要成分是K2CO3,它属于( )
A.钾肥 B.磷肥 C.氮肥 D.复合肥
10.将一定质量的铁粉加入到Mg(NO3)2、AgNO3的混合溶液中,充分反应后过滤,得到滤液和滤渣。向滤液中加入稀盐酸,无明显现象。下列叙述正确的是( )
A.滤液中一定含有Mg2+和Fe3+
B.滤液中含有Mg2+和Ag+
C.滤渣中一定含有Ag
D.滤渣中可能含有Mg
11.下列关于金属的说法中,不正确的是
A.铜有良好的导电性,常用于制作导线
B.所有的金属都能与稀盐酸反应
C.铁制品在干燥的空气中不易生锈
D.不锈钢具有较强的耐腐蚀性,可用于制作医疗器械
二、简答题
12.化学与人类的生产生活密切相关,人类的衣食住行都与化学有关,请回答下列问题:
(1)中国古代的丝绸享誉世界,鉴别某面料是真丝而非全棉的方法是_____,洗涤衣物上的油污通常可用洗衣液,主要是利用了洗衣液的_____作用;有膳食专家说青少年的饮食只要“一把蔬菜一把豆,一个鸡蛋加点肉”就行,其中蔬菜给人提供的主要营养素是_____,从营养全面的角度,你发现该说法中除水、无机盐外,还缺少的一种主要的营养素是_____。厨房中最常用的调味品中含有的阴离子是_____(填符号)
(2)化学使人类出行更便利,住宅跟安全,现代建筑大量使用的钢筋混凝土是_____(填“金属材料”“合成材料”或“复合材料”),汽车通常表面进行刷漆处理,除了美观外,其主要作用是_____,现在汽车汽油中常加入乙醇以减少污染,节约石油,乙醇是由_____构成的。
13.下图为我国发行的人民币硬币,主要材料含有铁、铝、铜等。
(1)工业上用赤铁矿(主要成分Fe2O3)炼铁的化学方程式为 _____ 。
(2)选择铸造硬币的材料,需要考虑的因素是 _____ (填序号)。
A 金属的硬度 B 金属的导电性 C 金属的耐腐蚀性
三、推断题
14.有A,B,C,D四种可溶性的物质,每种由以下两组中的离子构成。(每种离子只能选用一次)
阳离子
阴离子
四种物质之间的反应有如下现象:
(1)A+B→白色沉淀,不溶于稀硝酸。
(2)B+D→蓝色沉淀。
(3)C+B→白色沉淀,再加稀硝酸沉淀溶解并生成C。
由此可推知:A为_____,B为_____,C为_____,D为_____。(写化学式)
15.下列字母A-H表示初中化学常见的物质,它们由氢、碳、氧、钠、氯、钙中的2-3种元素组成。
(1)A俗称生石灰,则A是_____。A与B(胃液中含有的酸)反应放出大量的热,该反应的化学方程式是_____。
(2)B与C在溶液中发生的中和反应可表示为:B+C→D+E,其中D是食盐的主要成分,E是水。能证明B、C恰好完全反应,可选用的试剂是_____(填字母序号)。
A.石蕊溶液 B.酚酞溶液 C.酚酞溶液和锌粒 D.pH试纸
(3)F能与B反应,G能与C反应生成H,且F与G反应生成白色沉淀。写出F与H反应的化学方程式_____。
四、实验题
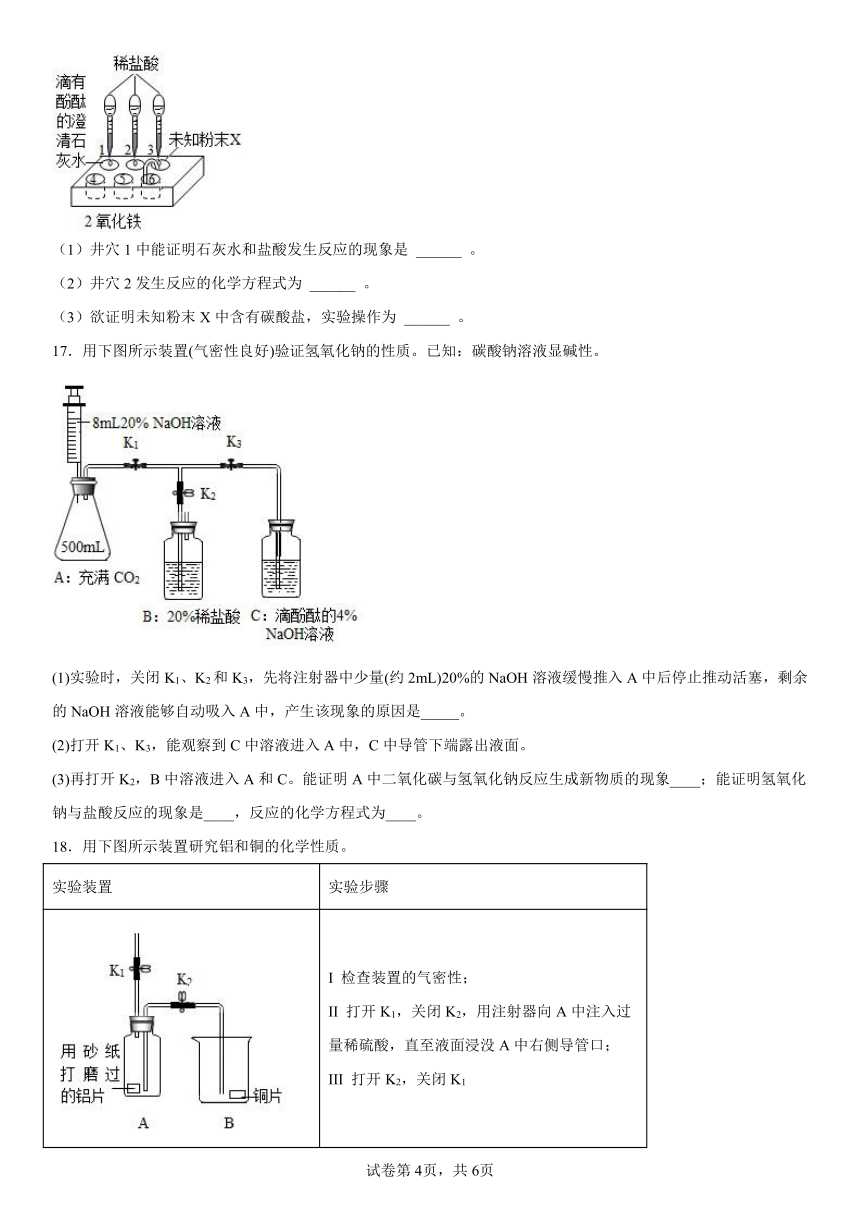
16.如图,利用井穴板、打孔透明盖子、滴管和导管进行微型实验。
(1)井穴1中能证明石灰水和盐酸发生反应的现象是 ______ 。
(2)井穴2发生反应的化学方程式为 ______ 。
(3)欲证明未知粉末X中含有碳酸盐,实验操作为 ______ 。
17.用下图所示装置(气密性良好)验证氢氧化钠的性质。已知:碳酸钠溶液显碱性。
(1)实验时,关闭K1、K2和K3,先将注射器中少量(约2mL)20%的NaOH溶液缓慢推入A中后停止推动活塞,剩余的NaOH溶液能够自动吸入A中,产生该现象的原因是_____。
(2)打开K1、K3,能观察到C中溶液进入A中,C中导管下端露出液面。
(3)再打开K2,B中溶液进入A和C。能证明A中二氧化碳与氢氧化钠反应生成新物质的现象____;能证明氢氧化钠与盐酸反应的现象是____,反应的化学方程式为____。
18.用下图所示装置研究铝和铜的化学性质。
实验装置 实验步骤
I 检查装置的气密性; II 打开K1,关闭K2,用注射器向A中注入过量稀硫酸,直至液面浸没A中右侧导管口; III 打开K2,关闭K1
(1)用砂纸打磨铝片的目的是_____。
(2)检查装置气密性的操作;向B中加入蒸馏水至浸没导管口,关闭K1,打开K2,_____。
(3)步骤II,A中可以观察到的现象有_____。
(4)步骤III,A中液体进入B后,未观察到明显现象,原因是_____。
五、计算题
19.早在西汉时期的《淮南万毕术》中就记载“曾青得铁则化为铜”,成为现代湿法冶金的先驱。现有含16kg硫酸铜的工业废液,加入铁粉回收铜,请计算:
(1)硫酸铜中铜元素质量分数_____。
(2)理论上与硫酸铜反应消耗铁粉的质量_____。
20.黄铜是铜和锌的合金,常用来制造机械零件、仪表等。化学小组想测定黄铜中锌的含量,将10g黄铜粉末放入烧杯中,加入93.7g稀硫酸恰好完全反应,烧杯中剩余物质总质量变为103.5g。请计算:
(1)反应生成氢气的质量为______g。
(2)求黄铜样品中锌的质量分数。(写出计算过程)
21.家庭中常用洁厕剂的有效成分是盐酸。小明同学想测定某品牌洁厕剂中氯化氢的质量分数,他将足量的石灰石加入洁厕剂样品中(石灰石中的杂质既不与酸反应,也不溶于水),有关实验数据如下表:
反应前 反应后
实验数据 洁厕剂样 品的质量 加入石灰 石的质量 剩余物的总质量
36.5 g 25 g 57.1 g
请计算:
(1)反应后生成二氧化碳的质量为________。
(2)该洁厕剂中氯化氢的质量分数为________。
22.《天工开物》中记载“凡铁分生、熟,出中未炒则生,既炒则熟。生熟相和,炼成则钢”为测定某生铁样品中铁的质量分数,实验小组称取8.75g该生铁样品于烧杯中,然后向其中加入100g稀硫酸,恰好完全反应(假设杂质不参与反应),称得反应前后烧杯内物质的总质量随时间的变化关系如图所示。
(1)生成氢气的质量为______g。
(2)计算该生铁样品中铁的质量分数。(写出计算过程)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.A
3.C
4.B
5.C
6.A
7.D
8.A
9.A
10.C
11.B
12. 取样在火中灼烧,灼烧时会产生烧焦羽毛气味的是真丝,有烧纸气味的是棉花 乳化 维生素 糖类 Cl- 复合材料 防止生锈 乙醇分子
13. 3CO + Fe2O3 3CO2 + 2Fe AC
14. Na2SO4 Ba(OH)2 Mg(NO3)2 CuCl2
15. CaO CaO+2HCl=CaCl2+H2O ACD Na2CO3+Ca(OH)2=2NaOH+CaCO3↓
16. 红色溶液变成无色 6HCl+Fe2O3=2FeCl3 +3H2O 在孔穴6中加入澄清石灰水,将稀盐酸挤入孔穴3
17. CO2与NaOH溶液反应而消耗,使A中压强低于外界大气压,NaOH溶液被压入 A中有气泡产生 C中红色溶液褪为无色 NaOH+HCl=NaCl+H2O
18. 除去铝片表面的氧化物 向B中加入蒸馏水至浸没导管口,关闭K1,打开K2,双手紧握A装置外壁,若B装置的导管口有气泡冒出,则装置气密性良好 有气泡生成,且A中的的溶液会流入烧杯B中 硫酸与铜不反应,且硫酸与铝反应生成的硫酸铝与铜也不反应
19.(1)40%
硫酸铜中铜元素质量分数为;
(2)5.6kg
解:设消耗铁粉的质量为
答:消耗铁粉5.6kg。
20.(1)0.2g
(2)设样品中锌的质量为x,
锌的质量分数为:=65%
答:黄铜样品中锌的质量分数为65%。
21.(1)4.4 g(2)20%
22.(1)0.3
(2)解:设该生铁样品中铁的质量为x
该生铁样品中铁的质量分数为
答:该生铁样品中铁的质量分数为96%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列有关金属的说法正确的是
A.所有金属都呈银白色 B.常温下所有的金属都是固体
C.合金的硬度一般比各成分金属小 D.铝制品耐腐蚀是因为表面生成致密氧化膜
2.金属材料在生产,生活中使用广泛。下列金属的用途利用了金属导电性的是
A.铜制电线 B.铁质铁锅 C.金制项链 D.铝制饮料罐
3.小玲家的水稻出现了倒伏现象,急需施用的化肥是( )
A.CO(NH2)2 B.Ca3(PO4)2 C.K2SO4 D.NH4Cl
4.金属材料在人类活动中已得到越来越广泛的应用。下列性质属于金属共性的是
A.熔点很高 B.有良好的导电性、导热性
C.银白色的固体 D.硬度很大
5.下列物质的名称或俗名,属同一种物质的是
A.生石灰 熟石灰 消石灰 B.冰 干冰 可燃冰
C.烧碱 苛性钠 火碱 D.石灰石 熟石灰 大理石
6.某同学总结的Ca(OH)2的化学性质如图,下列说法错误的是
A.甲一定是碳酸盐
B.反应②为放热反应
C.反应③可用于检验某种温室气体
D.向澄清石灰水中加入紫色石蕊试液,试液由紫色变为蓝色
7.港珠澳大桥的桥、岛、隧以及“雪龙2号”的船身等主要由金属材料制成。下列金属防护措施不正确的是
A.在金属制品表面镀保护层
B.改变金属结构制成合金使用
C.在金属制品表面涂油漆
D.用稀盐酸定期清洗金属制品
8.下图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。下列说法不正确的是
A.①中甲、乙、丙三处比较,生锈最明显的地方是甲
B.①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水
C.③中附着在棉花上的氯化钙的作用是作干燥剂
D.四个实验中,生锈最快的是④中的铁钉
9.草木灰是一种农家肥,其主要成分是K2CO3,它属于( )
A.钾肥 B.磷肥 C.氮肥 D.复合肥
10.将一定质量的铁粉加入到Mg(NO3)2、AgNO3的混合溶液中,充分反应后过滤,得到滤液和滤渣。向滤液中加入稀盐酸,无明显现象。下列叙述正确的是( )
A.滤液中一定含有Mg2+和Fe3+
B.滤液中含有Mg2+和Ag+
C.滤渣中一定含有Ag
D.滤渣中可能含有Mg
11.下列关于金属的说法中,不正确的是
A.铜有良好的导电性,常用于制作导线
B.所有的金属都能与稀盐酸反应
C.铁制品在干燥的空气中不易生锈
D.不锈钢具有较强的耐腐蚀性,可用于制作医疗器械
二、简答题
12.化学与人类的生产生活密切相关,人类的衣食住行都与化学有关,请回答下列问题:
(1)中国古代的丝绸享誉世界,鉴别某面料是真丝而非全棉的方法是_____,洗涤衣物上的油污通常可用洗衣液,主要是利用了洗衣液的_____作用;有膳食专家说青少年的饮食只要“一把蔬菜一把豆,一个鸡蛋加点肉”就行,其中蔬菜给人提供的主要营养素是_____,从营养全面的角度,你发现该说法中除水、无机盐外,还缺少的一种主要的营养素是_____。厨房中最常用的调味品中含有的阴离子是_____(填符号)
(2)化学使人类出行更便利,住宅跟安全,现代建筑大量使用的钢筋混凝土是_____(填“金属材料”“合成材料”或“复合材料”),汽车通常表面进行刷漆处理,除了美观外,其主要作用是_____,现在汽车汽油中常加入乙醇以减少污染,节约石油,乙醇是由_____构成的。
13.下图为我国发行的人民币硬币,主要材料含有铁、铝、铜等。
(1)工业上用赤铁矿(主要成分Fe2O3)炼铁的化学方程式为 _____ 。
(2)选择铸造硬币的材料,需要考虑的因素是 _____ (填序号)。
A 金属的硬度 B 金属的导电性 C 金属的耐腐蚀性
三、推断题
14.有A,B,C,D四种可溶性的物质,每种由以下两组中的离子构成。(每种离子只能选用一次)
阳离子
阴离子
四种物质之间的反应有如下现象:
(1)A+B→白色沉淀,不溶于稀硝酸。
(2)B+D→蓝色沉淀。
(3)C+B→白色沉淀,再加稀硝酸沉淀溶解并生成C。
由此可推知:A为_____,B为_____,C为_____,D为_____。(写化学式)
15.下列字母A-H表示初中化学常见的物质,它们由氢、碳、氧、钠、氯、钙中的2-3种元素组成。
(1)A俗称生石灰,则A是_____。A与B(胃液中含有的酸)反应放出大量的热,该反应的化学方程式是_____。
(2)B与C在溶液中发生的中和反应可表示为:B+C→D+E,其中D是食盐的主要成分,E是水。能证明B、C恰好完全反应,可选用的试剂是_____(填字母序号)。
A.石蕊溶液 B.酚酞溶液 C.酚酞溶液和锌粒 D.pH试纸
(3)F能与B反应,G能与C反应生成H,且F与G反应生成白色沉淀。写出F与H反应的化学方程式_____。
四、实验题
16.如图,利用井穴板、打孔透明盖子、滴管和导管进行微型实验。
(1)井穴1中能证明石灰水和盐酸发生反应的现象是 ______ 。
(2)井穴2发生反应的化学方程式为 ______ 。
(3)欲证明未知粉末X中含有碳酸盐,实验操作为 ______ 。
17.用下图所示装置(气密性良好)验证氢氧化钠的性质。已知:碳酸钠溶液显碱性。
(1)实验时,关闭K1、K2和K3,先将注射器中少量(约2mL)20%的NaOH溶液缓慢推入A中后停止推动活塞,剩余的NaOH溶液能够自动吸入A中,产生该现象的原因是_____。
(2)打开K1、K3,能观察到C中溶液进入A中,C中导管下端露出液面。
(3)再打开K2,B中溶液进入A和C。能证明A中二氧化碳与氢氧化钠反应生成新物质的现象____;能证明氢氧化钠与盐酸反应的现象是____,反应的化学方程式为____。
18.用下图所示装置研究铝和铜的化学性质。
实验装置 实验步骤
I 检查装置的气密性; II 打开K1,关闭K2,用注射器向A中注入过量稀硫酸,直至液面浸没A中右侧导管口; III 打开K2,关闭K1
(1)用砂纸打磨铝片的目的是_____。
(2)检查装置气密性的操作;向B中加入蒸馏水至浸没导管口,关闭K1,打开K2,_____。
(3)步骤II,A中可以观察到的现象有_____。
(4)步骤III,A中液体进入B后,未观察到明显现象,原因是_____。
五、计算题
19.早在西汉时期的《淮南万毕术》中就记载“曾青得铁则化为铜”,成为现代湿法冶金的先驱。现有含16kg硫酸铜的工业废液,加入铁粉回收铜,请计算:
(1)硫酸铜中铜元素质量分数_____。
(2)理论上与硫酸铜反应消耗铁粉的质量_____。
20.黄铜是铜和锌的合金,常用来制造机械零件、仪表等。化学小组想测定黄铜中锌的含量,将10g黄铜粉末放入烧杯中,加入93.7g稀硫酸恰好完全反应,烧杯中剩余物质总质量变为103.5g。请计算:
(1)反应生成氢气的质量为______g。
(2)求黄铜样品中锌的质量分数。(写出计算过程)
21.家庭中常用洁厕剂的有效成分是盐酸。小明同学想测定某品牌洁厕剂中氯化氢的质量分数,他将足量的石灰石加入洁厕剂样品中(石灰石中的杂质既不与酸反应,也不溶于水),有关实验数据如下表:
反应前 反应后
实验数据 洁厕剂样 品的质量 加入石灰 石的质量 剩余物的总质量
36.5 g 25 g 57.1 g
请计算:
(1)反应后生成二氧化碳的质量为________。
(2)该洁厕剂中氯化氢的质量分数为________。
22.《天工开物》中记载“凡铁分生、熟,出中未炒则生,既炒则熟。生熟相和,炼成则钢”为测定某生铁样品中铁的质量分数,实验小组称取8.75g该生铁样品于烧杯中,然后向其中加入100g稀硫酸,恰好完全反应(假设杂质不参与反应),称得反应前后烧杯内物质的总质量随时间的变化关系如图所示。
(1)生成氢气的质量为______g。
(2)计算该生铁样品中铁的质量分数。(写出计算过程)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.A
3.C
4.B
5.C
6.A
7.D
8.A
9.A
10.C
11.B
12. 取样在火中灼烧,灼烧时会产生烧焦羽毛气味的是真丝,有烧纸气味的是棉花 乳化 维生素 糖类 Cl- 复合材料 防止生锈 乙醇分子
13. 3CO + Fe2O3 3CO2 + 2Fe AC
14. Na2SO4 Ba(OH)2 Mg(NO3)2 CuCl2
15. CaO CaO+2HCl=CaCl2+H2O ACD Na2CO3+Ca(OH)2=2NaOH+CaCO3↓
16. 红色溶液变成无色 6HCl+Fe2O3=2FeCl3 +3H2O 在孔穴6中加入澄清石灰水,将稀盐酸挤入孔穴3
17. CO2与NaOH溶液反应而消耗,使A中压强低于外界大气压,NaOH溶液被压入 A中有气泡产生 C中红色溶液褪为无色 NaOH+HCl=NaCl+H2O
18. 除去铝片表面的氧化物 向B中加入蒸馏水至浸没导管口,关闭K1,打开K2,双手紧握A装置外壁,若B装置的导管口有气泡冒出,则装置气密性良好 有气泡生成,且A中的的溶液会流入烧杯B中 硫酸与铜不反应,且硫酸与铝反应生成的硫酸铝与铜也不反应
19.(1)40%
硫酸铜中铜元素质量分数为;
(2)5.6kg
解:设消耗铁粉的质量为
答:消耗铁粉5.6kg。
20.(1)0.2g
(2)设样品中锌的质量为x,
锌的质量分数为:=65%
答:黄铜样品中锌的质量分数为65%。
21.(1)4.4 g(2)20%
22.(1)0.3
(2)解:设该生铁样品中铁的质量为x
该生铁样品中铁的质量分数为
答:该生铁样品中铁的质量分数为96%。
答案第1页,共2页
答案第1页,共2页
