化学人教版(2019)选择性必修3 2.3芳香烃(共46张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 2.3芳香烃(共46张ppt) |  | |
| 格式 | zip | ||
| 文件大小 | 3.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-11 11:12:59 | ||
图片预览






文档简介
(共46张PPT)
第三节 芳香烃
第二章 烃
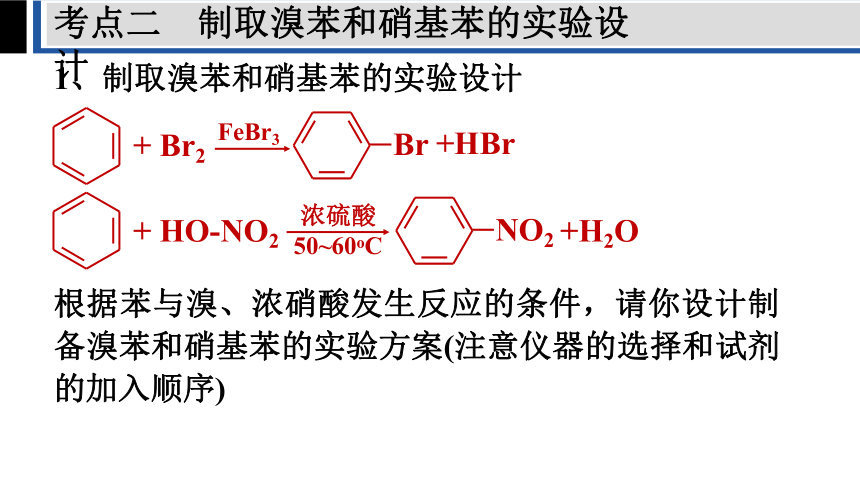
考点二 制取溴苯和硝基苯的实验设计
考点三 苯的同系物
内容索引
考点四 芳香烃的来源及其应用
考点五 有机分子里的共线、共面问题
考点一 苯的结构与性质
颜色:
无色
气味:
特殊气味
状态:
液态
熔点:
5.5℃
沸点:
80.1℃
密度:
比水小
毒性:
有毒
溶解性:
不溶于水,易溶于有机溶剂,也是良好的有机溶剂
其他:
易挥发
1、苯的物理性质
考点一 苯的结构与性质
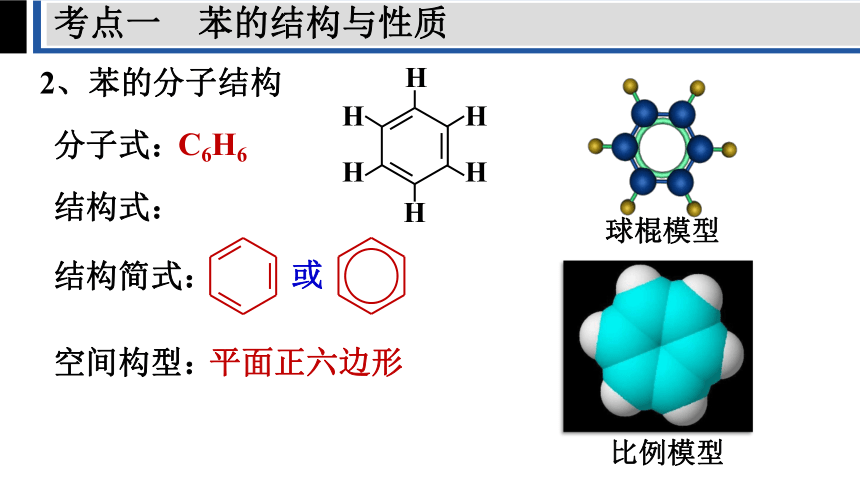
2、苯的分子结构
球棍模型
比例模型
分子式:
结构式:
结构简式:
空间构型:
C6H6
H
H
H
H
H
H
或
平面正六边形
考点一 苯的结构与性质
2、苯的分子结构
空间构型:
平面正六边形
(1)分子中12个原子共平面,分子中六个碳原子等效,六个氢原子等效
(2)6个碳碳键完全相同,是一种介于碳碳单键和碳碳双键之间的独特的键。
(3)邻二取代物没有同分异构体,只有一种结构
考点一 苯的结构与性质
3、苯的化学性质
性质
苯的特殊结构
苯的特殊性质
饱和烃
不饱和烃
取代反应
加成反应
结构
(1)从分子组成上看,苯属于不饱和烃,但分子中没有典型的不饱和键,不能像乙烯那样与溴水(溴的四氯化碳溶液)发生加成反应。
(2)从化学键上看,苯分子中的碳碳键是介于碳碳单键和碳碳双键之间的特殊键,能氧化,难加成,易取代。
考点一 苯的结构与性质
3、苯的化学性质
在通常情况下比较稳定,在一定条件下能发生氧化、加成、取代等反应。
(1)氧化反应—— 燃烧
现象:
火焰明亮,伴有浓烈的黑烟
方程式:
2C6H6 + 15O2 12CO2 + 6H2O
点燃
注: 不能使酸性KMnO4溶液褪色
考点一 苯的结构与性质
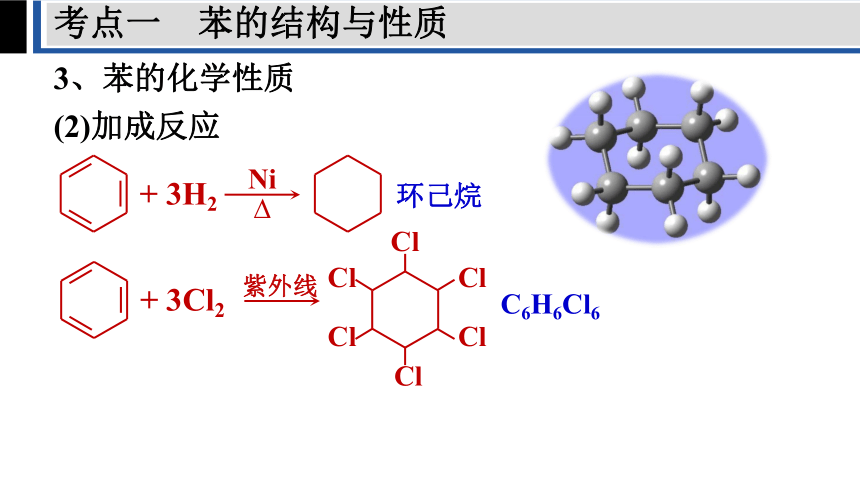
3、苯的化学性质
(2)加成反应
+ 3H2
Ni
环己烷
+ 3Cl2
紫外线
Cl
Cl
Cl
Cl
Cl
Cl
C6H6Cl6
考点一 苯的结构与性质
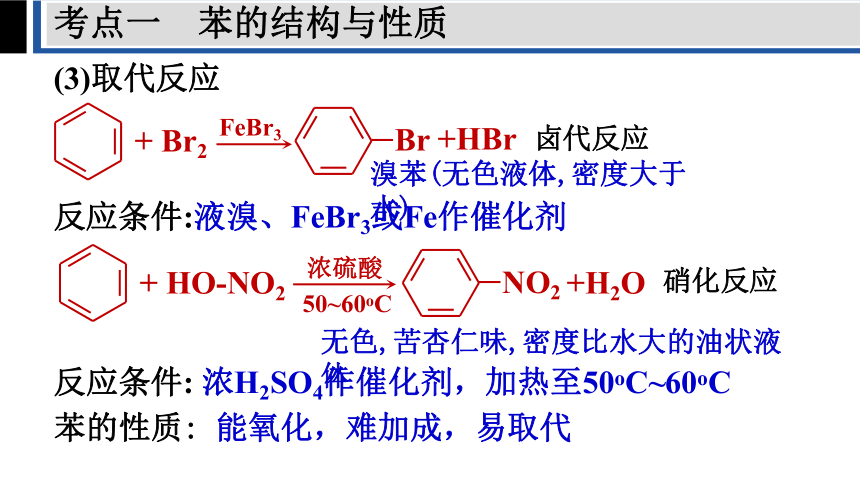
(3)取代反应
卤代反应
溴苯(无色液体,密度大于水)
+ Br2
FeBr3
+HBr
Br
反应条件:液溴、FeBr3或Fe作催化剂
+ HO-NO2
+H2O
NO2
浓硫酸
50~60oC
反应条件: 浓H2SO4作催化剂,加热至50oC~60oC
无色,苦杏仁味,密度比水大的油状液体
硝化反应
苯的性质: 能氧化,难加成,易取代
考点一 苯的结构与性质
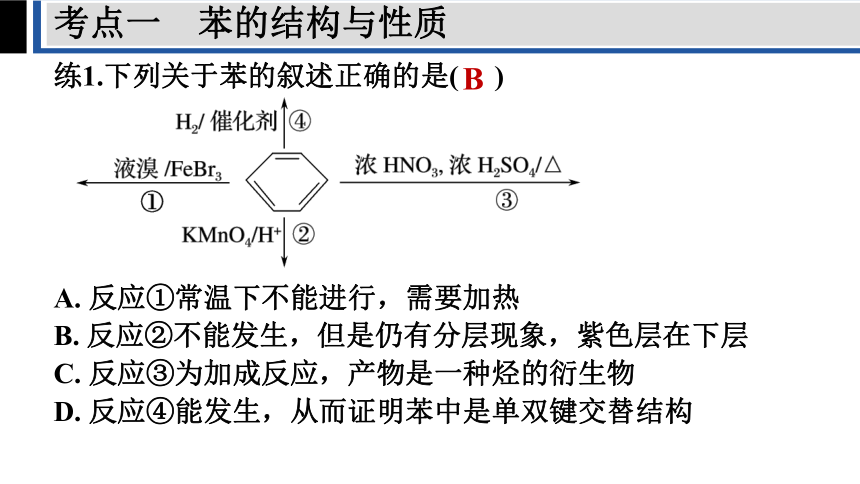
练1.下列关于苯的叙述正确的是( )
A. 反应①常温下不能进行,需要加热
B. 反应②不能发生,但是仍有分层现象,紫色层在下层
C. 反应③为加成反应,产物是一种烃的衍生物
D. 反应④能发生,从而证明苯中是单双键交替结构
B
考点一 苯的结构与性质
1、制取溴苯和硝基苯的实验设计
+ Br2
FeBr3
+HBr
Br
+ HO-NO2
+H2O
NO2
浓硫酸
50~60oC
根据苯与溴、浓硝酸发生反应的条件,请你设计制备溴苯和硝基苯的实验方案(注意仪器的选择和试剂的加入顺序)
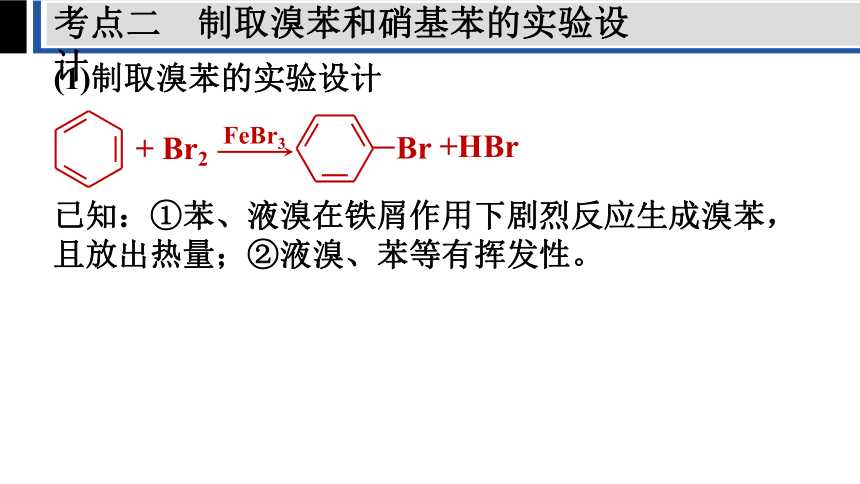
考点二 制取溴苯和硝基苯的实验设计
(1)制取溴苯的实验设计
+ Br2
FeBr3
+HBr
Br
已知:①苯、液溴在铁屑作用下剧烈反应生成溴苯,且放出热量;②液溴、苯等有挥发性。
考点二 制取溴苯和硝基苯的实验设计
(1)制取溴苯的实验设计
请选择最合适的装置制溴苯
图一 图二 图三
如何证明该反应是取代反应而不是加成反应
AgNO3
溶液
考点二 制取溴苯和硝基苯的实验设计
(1)制取溴苯的实验设计
①反应装置如图所示:
②长直导管的作用:
导气兼起冷凝回流作用
③导管末端不能伸入液面中的原因是防止倒吸
④催化剂是FeBr3,而反应时只需加Fe
考点二 制取溴苯和硝基苯的实验设计
(1)制取溴苯的实验设计
⑤实验现象:
混合液呈现微沸状态
反应器内充满红棕色气体,导管口有白雾
锥形瓶中出现浅黄色沉淀
反应结束后烧瓶中液体倒入盛有水的烧杯中,烧杯底部有油状的褐色液体
反应放热
生成的HBr遇水蒸气
产生AgBr沉淀
溴苯中混有溴
考点二 制取溴苯和硝基苯的实验设计
(1)制取溴苯的实验设计
思考:如何获得纯净的溴苯?
可能含有的杂质: Br2、HBr、苯、FeBr3
水洗→碱洗→水洗→干燥→蒸馏
除溶于水的杂质(如溴化铁)
除溴
除氢氧化钠及与其反应生成的盐
除水
除苯
考点二 制取溴苯和硝基苯的实验设计
(1)制取溴苯的实验设计
思考:如何改进?
冷凝回流导气
吸收HBr防止污染
防倒吸
除溴苯中溶解的溴
考点二 制取溴苯和硝基苯的实验设计
(2)制取硝基苯的实验设计
④将反应后的液体倒入盛冷水的烧杯中,可以看到烧杯底部有黄色油状物生成,经过分离得到粗硝基苯。
实验步骤:
①先将1.5mL浓硝酸注入大试管中,再慢慢注入2mL浓硫酸,并及时摇匀和冷却
②向冷却后的酸中逐滴加入1mL苯,充分振荡,混和均匀
③将混合物控制在50-60℃的条件下水浴加热约10min
考点二 制取溴苯和硝基苯的实验设计
(2)制取硝基苯的实验设计
④不纯的硝基苯显黄色
注意事项:
①为何要严格控制温度?
②水浴
③长导管的作用
100℃以下可采用水浴加热;超过100 ℃可采用油浴、沙浴
反应放热,温度过高,苯易挥发、硝酸、会分解,同时苯和浓硫酸在70~80℃时会发生副反应
冷凝回流
溶有NO2
考点二 制取溴苯和硝基苯的实验设计
(2)制取硝基苯的实验设计
思考:如何获得纯净的硝基苯?
水洗→碱洗(5%NaOH)→水洗→干燥→蒸馏
除硝酸和硫酸
除氢氧化钠及与其反应生成的盐
用无水CaCl2干燥
补: 苯的磺化反应(取代反应)
+ HO-SO3H
+H2O
SO3H
70~80oC
考点二 制取溴苯和硝基苯的实验设计
练2.已知苯与液溴的反应是放热反应,某校学生为探究苯与溴发生的反应,用如图装置进行实验,回答下列问题:
(1)实验开始时,关闭K2,打开K1和漏斗活塞,滴加苯和液溴的混合液,反应开始。一段时间后,在装置Ⅲ中可能观察到的现象是_______________________________________
__________________________________________。
小试管中有气泡,液体变为橙红色;有白雾出现;广口瓶内液体中有浅黄色沉淀生成。
考点二 制取溴苯和硝基苯的实验设计
练2.已知苯与液溴的反应是放热反应,某校学生为探究苯与溴发生的反应,用如图装置进行实验,回答下列问题:
(2)实验中能防止倒吸的装置有________(填装置序号)。
Ⅲ和Ⅳ
考点二 制取溴苯和硝基苯的实验设计
练2.已知苯与液溴的反应是放热反应,某校学生为探究苯与溴发生的反应,用如图装置进行实验,回答下列问题:
(3)反应结束后要使装置Ⅰ中的水倒吸入装置Ⅱ中。这样操作目的是_____________________________________________
简述这一操作:__________________________。
除去装置Ⅱ中的溴化氢气体,避免HBr逸出污染空气
打开K2,关闭K1和漏斗活塞
考点二 制取溴苯和硝基苯的实验设计
练2.已知苯与液溴的反应是放热反应,某校学生为探究苯与溴发生的反应,用如图装置进行实验,回答下列问题:
(3)通过该实验,可知苯与溴的反应是_____反应。
取代
考点二 制取溴苯和硝基苯的实验设计
1、苯的同系物的组成和结构特点
(1)定义:
苯环上的氢原子被烷基取代的产物
(2)通式:
CnH2n-6 (n≥7)
(3)结构特点:
只含有一个苯环,苯环上连接烷基
CH3
CH2CH3
CH=CH2
CH3—CH—CH—CH3
OH
考点三 苯的同系物
拓展: 多环芳香烃
CH2
二苯甲烷
联苯
萘
蒽
菲
C10H8
C14H10
C14H10
考点三 苯的同系物
1、苯的同系物的组成和结构特点
(4)苯的同系物的同分异构体
思考:分子式为C9H12属于苯的同系物的同分异构体有多少种?
分析:一个丙基:_______
一个甲基+一个乙基:_______
三个甲基:_______
一种
三种
三种
考点三 苯的同系物
2、苯的同系物化学性质
(1)氧化反应
②可使酸性高锰酸钾溶液褪色
反应机理:
C
H
酸性高锰酸钾溶液
COOH
与苯环直接相连的碳上要有H
①可燃性:
均能燃烧,火焰明亮伴有浓烟
考点三 苯的同系物
2、苯的同系物化学性质
②可使酸性高锰酸钾溶液褪色
反应机理:
C
H
酸性高锰酸钾溶液
COOH
应用:鉴别苯和部分苯的同系物
通过这个反应,可以说明:
苯环对侧链影响:苯环活化侧链,使侧链易于氧化
考点三 苯的同系物
迁移:甲基对苯环有影响吗?
2、苯的同系物化学性质
阅读课本P38实验完成下面的表格
温度 生成物
苯
甲苯
50℃-60℃
30℃
硝基苯
邻、对位硝基甲苯
侧链对苯环的影响:甲基活化了苯环的邻位和对位
考点三 苯的同系物
2、苯的同系物化学性质
(2)取代反应
+ 3HNO3
浓硫酸
△
+ 3H2O
CH3
CH3
NO2
NO2
O2N
烈性炸药
三硝基甲苯又叫TNT,是一种淡黄色晶体,不溶于水
它是一种烈性炸药,广泛用于国防、开矿、建筑等。
考点三 苯的同系物
归纳总结:苯环与侧链相互影响
(1)苯环影响侧链:
(2)侧链对苯环的影响:
使侧链烃基性质活泼而被氧化。苯的同系物被氧化时,不论它的侧链长短如何,如果侧链烃基中与苯环直接相连的碳原子上有氢原子,则该侧链烃基通常被氧化为羧基。
使苯环上侧链邻、对位上的H原子变得活泼。甲苯与硝酸反应时,生成三硝基甲苯,而苯与硝酸反应只生成硝基苯。
考点三 苯的同系物
2、苯的同系物化学性质
拓展:苯的同系物的卤代反应
CH3
CH3
+ Cl2
+ Cl2
CH2Cl
+HCl
CH3
Cl
CH3
Cl
+HCl
条件Ⅰ
条件Ⅱ
条件Ⅰ:_____、条件Ⅱ:_____
光照
FeCl3
考点三 苯的同系物
2、苯的同系物化学性质
(3)加成反应
+ 3H2
催化剂
△
CH3
CH3
小结与H2加成规律:
碳碳双键:__________
碳碳三键:__________
苯环:______________
1 : 1
1 : 2
1 : 3
考点三 苯的同系物
练3.芳香化合物A是一种基本化工原料,可以从煤和石油中得到。A、B、C、D、E转化关系如图所示:
回答下列问题:
(1)A的化学名称是________
E属于________(填“饱和烃”或“不饱和烃”)。
(2)A→B的反应类型是____________在该反应的副产物中,与B互为同分异构体的副产物的结构简式为______
邻二甲苯(1,2 二甲基苯)
饱和烃
取代反应
CBr3
CH2Br
考点三 苯的同系物
练3.芳香化合物A是一种基本化工原料,可以从煤和石油中得到。A、B、C、D、E转化关系如图所示:
(3)A→C的化学方程式为
____________________。
(4)A与酸性KMnO4溶液反
应可得到D,写出D的结构
简式:_________。
考点三 苯的同系物
CH3
CH3
+ Br2
FeBr3
+HBr
CH3
CH3
Br
CH3
CH3
Br
A→C:
D的结构简式:
COOH
COOH
考点三 苯的同系物
1、来源
(1)1845年至20世纪40年代通过煤的干馏是芳香烃的主要来源。
(2)20世纪40年代以后,通过石油化学工业中的催化重整等工艺获得
如苯、甲苯、二甲苯、乙苯等是基本的有机原料,可用于合成炸药、染料、药品、农药、合成材料等
2、应用
考点四 芳香烃的来源及其应用
甲烷 乙烯 乙炔 苯
比例
模型
空间
构型
109 28'
120
正四面体形
平面形
直线形
180
键角
平面正六边形
120
考点五 有机分子里的共线、共面问题
1、简单小分子的空间构型
①CH4分子为正四面体结构,其分子最多有3个原子共处同一平面
②乙烯分子中所有原子共平面
③乙炔分子中所有原子共直线
④苯分子中所有原子共平面
考点五 有机分子里的共线、共面问题
2、类比迁移规律
(1)CH4型:四面体结构
凡是C原子与其他四个原子形成共价单键时,空间结构为四面体结构
结论1: 结构中每出现一个饱和碳原子,则整个分子不再共面
考点五 有机分子里的共线、共面问题
2、类比迁移规律
(2)乙烯型:平面结构
当乙烯分子中某氢原子被其他原子或原子团取代时,则代替该氢原子的原子一定在乙烯的平面内
结论2:结构中每出现一个碳碳双键,至少有6个原子共面
考点五 有机分子里的共线、共面问题
2、类比迁移规律
(3)乙炔型:直线结构
当乙炔分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定和乙炔分子的其他原子共线
结论3:结构中每出现一个碳碳三键,至少有4个原子共线
考点五 有机分子里的共线、共面问题
2、类比迁移规律
(4)苯型:平面型结构
当苯分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定在苯分子所在平面内。
结论3:结构中每出现一个苯环,至少有12个原子共面
考点五 有机分子里的共线、共面问题
解决该类问题时还应注意:
1、认真审题:如分子中最多有多少个原子共面?可能共面的原子有多少个?一定共面的原子有多少个?最多有多少个碳原子共面?
2、单键可以旋转,而双、三键不能旋转。
考点五 有机分子里的共线、共面问题
练4.某有机物分子结构如下
关于该分子结构的说法正确的是( )
A. 除苯环外的其余碳原子有可能都在一条直线上
B. 除苯环外的其余碳原子不可能都在一条直线上
C. 12个碳原子不可能都在同一平面上
D. 12个碳原子一定都在同一平面上
B
C≡C
CI3
HC═CH
CHClF
考点五 有机分子里的共线、共面问题
第三节 芳香烃
第二章 烃
考点二 制取溴苯和硝基苯的实验设计
考点三 苯的同系物
内容索引
考点四 芳香烃的来源及其应用
考点五 有机分子里的共线、共面问题
考点一 苯的结构与性质
颜色:
无色
气味:
特殊气味
状态:
液态
熔点:
5.5℃
沸点:
80.1℃
密度:
比水小
毒性:
有毒
溶解性:
不溶于水,易溶于有机溶剂,也是良好的有机溶剂
其他:
易挥发
1、苯的物理性质
考点一 苯的结构与性质
2、苯的分子结构
球棍模型
比例模型
分子式:
结构式:
结构简式:
空间构型:
C6H6
H
H
H
H
H
H
或
平面正六边形
考点一 苯的结构与性质
2、苯的分子结构
空间构型:
平面正六边形
(1)分子中12个原子共平面,分子中六个碳原子等效,六个氢原子等效
(2)6个碳碳键完全相同,是一种介于碳碳单键和碳碳双键之间的独特的键。
(3)邻二取代物没有同分异构体,只有一种结构
考点一 苯的结构与性质
3、苯的化学性质
性质
苯的特殊结构
苯的特殊性质
饱和烃
不饱和烃
取代反应
加成反应
结构
(1)从分子组成上看,苯属于不饱和烃,但分子中没有典型的不饱和键,不能像乙烯那样与溴水(溴的四氯化碳溶液)发生加成反应。
(2)从化学键上看,苯分子中的碳碳键是介于碳碳单键和碳碳双键之间的特殊键,能氧化,难加成,易取代。
考点一 苯的结构与性质
3、苯的化学性质
在通常情况下比较稳定,在一定条件下能发生氧化、加成、取代等反应。
(1)氧化反应—— 燃烧
现象:
火焰明亮,伴有浓烈的黑烟
方程式:
2C6H6 + 15O2 12CO2 + 6H2O
点燃
注: 不能使酸性KMnO4溶液褪色
考点一 苯的结构与性质
3、苯的化学性质
(2)加成反应
+ 3H2
Ni
环己烷
+ 3Cl2
紫外线
Cl
Cl
Cl
Cl
Cl
Cl
C6H6Cl6
考点一 苯的结构与性质
(3)取代反应
卤代反应
溴苯(无色液体,密度大于水)
+ Br2
FeBr3
+HBr
Br
反应条件:液溴、FeBr3或Fe作催化剂
+ HO-NO2
+H2O
NO2
浓硫酸
50~60oC
反应条件: 浓H2SO4作催化剂,加热至50oC~60oC
无色,苦杏仁味,密度比水大的油状液体
硝化反应
苯的性质: 能氧化,难加成,易取代
考点一 苯的结构与性质
练1.下列关于苯的叙述正确的是( )
A. 反应①常温下不能进行,需要加热
B. 反应②不能发生,但是仍有分层现象,紫色层在下层
C. 反应③为加成反应,产物是一种烃的衍生物
D. 反应④能发生,从而证明苯中是单双键交替结构
B
考点一 苯的结构与性质
1、制取溴苯和硝基苯的实验设计
+ Br2
FeBr3
+HBr
Br
+ HO-NO2
+H2O
NO2
浓硫酸
50~60oC
根据苯与溴、浓硝酸发生反应的条件,请你设计制备溴苯和硝基苯的实验方案(注意仪器的选择和试剂的加入顺序)
考点二 制取溴苯和硝基苯的实验设计
(1)制取溴苯的实验设计
+ Br2
FeBr3
+HBr
Br
已知:①苯、液溴在铁屑作用下剧烈反应生成溴苯,且放出热量;②液溴、苯等有挥发性。
考点二 制取溴苯和硝基苯的实验设计
(1)制取溴苯的实验设计
请选择最合适的装置制溴苯
图一 图二 图三
如何证明该反应是取代反应而不是加成反应
AgNO3
溶液
考点二 制取溴苯和硝基苯的实验设计
(1)制取溴苯的实验设计
①反应装置如图所示:
②长直导管的作用:
导气兼起冷凝回流作用
③导管末端不能伸入液面中的原因是防止倒吸
④催化剂是FeBr3,而反应时只需加Fe
考点二 制取溴苯和硝基苯的实验设计
(1)制取溴苯的实验设计
⑤实验现象:
混合液呈现微沸状态
反应器内充满红棕色气体,导管口有白雾
锥形瓶中出现浅黄色沉淀
反应结束后烧瓶中液体倒入盛有水的烧杯中,烧杯底部有油状的褐色液体
反应放热
生成的HBr遇水蒸气
产生AgBr沉淀
溴苯中混有溴
考点二 制取溴苯和硝基苯的实验设计
(1)制取溴苯的实验设计
思考:如何获得纯净的溴苯?
可能含有的杂质: Br2、HBr、苯、FeBr3
水洗→碱洗→水洗→干燥→蒸馏
除溶于水的杂质(如溴化铁)
除溴
除氢氧化钠及与其反应生成的盐
除水
除苯
考点二 制取溴苯和硝基苯的实验设计
(1)制取溴苯的实验设计
思考:如何改进?
冷凝回流导气
吸收HBr防止污染
防倒吸
除溴苯中溶解的溴
考点二 制取溴苯和硝基苯的实验设计
(2)制取硝基苯的实验设计
④将反应后的液体倒入盛冷水的烧杯中,可以看到烧杯底部有黄色油状物生成,经过分离得到粗硝基苯。
实验步骤:
①先将1.5mL浓硝酸注入大试管中,再慢慢注入2mL浓硫酸,并及时摇匀和冷却
②向冷却后的酸中逐滴加入1mL苯,充分振荡,混和均匀
③将混合物控制在50-60℃的条件下水浴加热约10min
考点二 制取溴苯和硝基苯的实验设计
(2)制取硝基苯的实验设计
④不纯的硝基苯显黄色
注意事项:
①为何要严格控制温度?
②水浴
③长导管的作用
100℃以下可采用水浴加热;超过100 ℃可采用油浴、沙浴
反应放热,温度过高,苯易挥发、硝酸、会分解,同时苯和浓硫酸在70~80℃时会发生副反应
冷凝回流
溶有NO2
考点二 制取溴苯和硝基苯的实验设计
(2)制取硝基苯的实验设计
思考:如何获得纯净的硝基苯?
水洗→碱洗(5%NaOH)→水洗→干燥→蒸馏
除硝酸和硫酸
除氢氧化钠及与其反应生成的盐
用无水CaCl2干燥
补: 苯的磺化反应(取代反应)
+ HO-SO3H
+H2O
SO3H
70~80oC
考点二 制取溴苯和硝基苯的实验设计
练2.已知苯与液溴的反应是放热反应,某校学生为探究苯与溴发生的反应,用如图装置进行实验,回答下列问题:
(1)实验开始时,关闭K2,打开K1和漏斗活塞,滴加苯和液溴的混合液,反应开始。一段时间后,在装置Ⅲ中可能观察到的现象是_______________________________________
__________________________________________。
小试管中有气泡,液体变为橙红色;有白雾出现;广口瓶内液体中有浅黄色沉淀生成。
考点二 制取溴苯和硝基苯的实验设计
练2.已知苯与液溴的反应是放热反应,某校学生为探究苯与溴发生的反应,用如图装置进行实验,回答下列问题:
(2)实验中能防止倒吸的装置有________(填装置序号)。
Ⅲ和Ⅳ
考点二 制取溴苯和硝基苯的实验设计
练2.已知苯与液溴的反应是放热反应,某校学生为探究苯与溴发生的反应,用如图装置进行实验,回答下列问题:
(3)反应结束后要使装置Ⅰ中的水倒吸入装置Ⅱ中。这样操作目的是_____________________________________________
简述这一操作:__________________________。
除去装置Ⅱ中的溴化氢气体,避免HBr逸出污染空气
打开K2,关闭K1和漏斗活塞
考点二 制取溴苯和硝基苯的实验设计
练2.已知苯与液溴的反应是放热反应,某校学生为探究苯与溴发生的反应,用如图装置进行实验,回答下列问题:
(3)通过该实验,可知苯与溴的反应是_____反应。
取代
考点二 制取溴苯和硝基苯的实验设计
1、苯的同系物的组成和结构特点
(1)定义:
苯环上的氢原子被烷基取代的产物
(2)通式:
CnH2n-6 (n≥7)
(3)结构特点:
只含有一个苯环,苯环上连接烷基
CH3
CH2CH3
CH=CH2
CH3—CH—CH—CH3
OH
考点三 苯的同系物
拓展: 多环芳香烃
CH2
二苯甲烷
联苯
萘
蒽
菲
C10H8
C14H10
C14H10
考点三 苯的同系物
1、苯的同系物的组成和结构特点
(4)苯的同系物的同分异构体
思考:分子式为C9H12属于苯的同系物的同分异构体有多少种?
分析:一个丙基:_______
一个甲基+一个乙基:_______
三个甲基:_______
一种
三种
三种
考点三 苯的同系物
2、苯的同系物化学性质
(1)氧化反应
②可使酸性高锰酸钾溶液褪色
反应机理:
C
H
酸性高锰酸钾溶液
COOH
与苯环直接相连的碳上要有H
①可燃性:
均能燃烧,火焰明亮伴有浓烟
考点三 苯的同系物
2、苯的同系物化学性质
②可使酸性高锰酸钾溶液褪色
反应机理:
C
H
酸性高锰酸钾溶液
COOH
应用:鉴别苯和部分苯的同系物
通过这个反应,可以说明:
苯环对侧链影响:苯环活化侧链,使侧链易于氧化
考点三 苯的同系物
迁移:甲基对苯环有影响吗?
2、苯的同系物化学性质
阅读课本P38实验完成下面的表格
温度 生成物
苯
甲苯
50℃-60℃
30℃
硝基苯
邻、对位硝基甲苯
侧链对苯环的影响:甲基活化了苯环的邻位和对位
考点三 苯的同系物
2、苯的同系物化学性质
(2)取代反应
+ 3HNO3
浓硫酸
△
+ 3H2O
CH3
CH3
NO2
NO2
O2N
烈性炸药
三硝基甲苯又叫TNT,是一种淡黄色晶体,不溶于水
它是一种烈性炸药,广泛用于国防、开矿、建筑等。
考点三 苯的同系物
归纳总结:苯环与侧链相互影响
(1)苯环影响侧链:
(2)侧链对苯环的影响:
使侧链烃基性质活泼而被氧化。苯的同系物被氧化时,不论它的侧链长短如何,如果侧链烃基中与苯环直接相连的碳原子上有氢原子,则该侧链烃基通常被氧化为羧基。
使苯环上侧链邻、对位上的H原子变得活泼。甲苯与硝酸反应时,生成三硝基甲苯,而苯与硝酸反应只生成硝基苯。
考点三 苯的同系物
2、苯的同系物化学性质
拓展:苯的同系物的卤代反应
CH3
CH3
+ Cl2
+ Cl2
CH2Cl
+HCl
CH3
Cl
CH3
Cl
+HCl
条件Ⅰ
条件Ⅱ
条件Ⅰ:_____、条件Ⅱ:_____
光照
FeCl3
考点三 苯的同系物
2、苯的同系物化学性质
(3)加成反应
+ 3H2
催化剂
△
CH3
CH3
小结与H2加成规律:
碳碳双键:__________
碳碳三键:__________
苯环:______________
1 : 1
1 : 2
1 : 3
考点三 苯的同系物
练3.芳香化合物A是一种基本化工原料,可以从煤和石油中得到。A、B、C、D、E转化关系如图所示:
回答下列问题:
(1)A的化学名称是________
E属于________(填“饱和烃”或“不饱和烃”)。
(2)A→B的反应类型是____________在该反应的副产物中,与B互为同分异构体的副产物的结构简式为______
邻二甲苯(1,2 二甲基苯)
饱和烃
取代反应
CBr3
CH2Br
考点三 苯的同系物
练3.芳香化合物A是一种基本化工原料,可以从煤和石油中得到。A、B、C、D、E转化关系如图所示:
(3)A→C的化学方程式为
____________________。
(4)A与酸性KMnO4溶液反
应可得到D,写出D的结构
简式:_________。
考点三 苯的同系物
CH3
CH3
+ Br2
FeBr3
+HBr
CH3
CH3
Br
CH3
CH3
Br
A→C:
D的结构简式:
COOH
COOH
考点三 苯的同系物
1、来源
(1)1845年至20世纪40年代通过煤的干馏是芳香烃的主要来源。
(2)20世纪40年代以后,通过石油化学工业中的催化重整等工艺获得
如苯、甲苯、二甲苯、乙苯等是基本的有机原料,可用于合成炸药、染料、药品、农药、合成材料等
2、应用
考点四 芳香烃的来源及其应用
甲烷 乙烯 乙炔 苯
比例
模型
空间
构型
109 28'
120
正四面体形
平面形
直线形
180
键角
平面正六边形
120
考点五 有机分子里的共线、共面问题
1、简单小分子的空间构型
①CH4分子为正四面体结构,其分子最多有3个原子共处同一平面
②乙烯分子中所有原子共平面
③乙炔分子中所有原子共直线
④苯分子中所有原子共平面
考点五 有机分子里的共线、共面问题
2、类比迁移规律
(1)CH4型:四面体结构
凡是C原子与其他四个原子形成共价单键时,空间结构为四面体结构
结论1: 结构中每出现一个饱和碳原子,则整个分子不再共面
考点五 有机分子里的共线、共面问题
2、类比迁移规律
(2)乙烯型:平面结构
当乙烯分子中某氢原子被其他原子或原子团取代时,则代替该氢原子的原子一定在乙烯的平面内
结论2:结构中每出现一个碳碳双键,至少有6个原子共面
考点五 有机分子里的共线、共面问题
2、类比迁移规律
(3)乙炔型:直线结构
当乙炔分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定和乙炔分子的其他原子共线
结论3:结构中每出现一个碳碳三键,至少有4个原子共线
考点五 有机分子里的共线、共面问题
2、类比迁移规律
(4)苯型:平面型结构
当苯分子中的一个氢原子被其他原子或原子团取代时,代替该氢原子的原子一定在苯分子所在平面内。
结论3:结构中每出现一个苯环,至少有12个原子共面
考点五 有机分子里的共线、共面问题
解决该类问题时还应注意:
1、认真审题:如分子中最多有多少个原子共面?可能共面的原子有多少个?一定共面的原子有多少个?最多有多少个碳原子共面?
2、单键可以旋转,而双、三键不能旋转。
考点五 有机分子里的共线、共面问题
练4.某有机物分子结构如下
关于该分子结构的说法正确的是( )
A. 除苯环外的其余碳原子有可能都在一条直线上
B. 除苯环外的其余碳原子不可能都在一条直线上
C. 12个碳原子不可能都在同一平面上
D. 12个碳原子一定都在同一平面上
B
C≡C
CI3
HC═CH
CHClF
考点五 有机分子里的共线、共面问题
