化学人教版(2019)选择性必修3 3.3醛酮 (共38张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 3.3醛酮 (共38张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 4.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-11 00:00:00 | ||
图片预览








文档简介
(共38张PPT)
第三节 醛 酮
第三章 烃的衍生物
考点二 乙醛的结构
考点三 乙醛的化学性质
内容索引
考点一 乙醛的物理性质
考点四 醛类
考点五 特殊的醛—甲醛
考点六 酮类简介(丙酮)
实现下列转化需加何种试剂?写出反应方程式,标明条件和反应类型。
CH3CH2OH → CH3CHO
温故知新
1、乙醛的物理性质
颜色:
气味:
状态:
密度:
挥发性:
溶解性:
无色透明
刺激性气味
液体
比水小
易挥发,沸点20.8℃
能与水、乙醇、乙醚、氯仿等互溶
考点一 乙醛的物理性质
1、乙醛的结构
H
H
H
H
C
C
O
结
构
式
球
棍
模
型
官能团:
醛基 —CHO
结构简式:
CH3CHO或 OHCCH3
考点二 乙醛的结构
吸
收
强
度
10 8 6 4 2 0
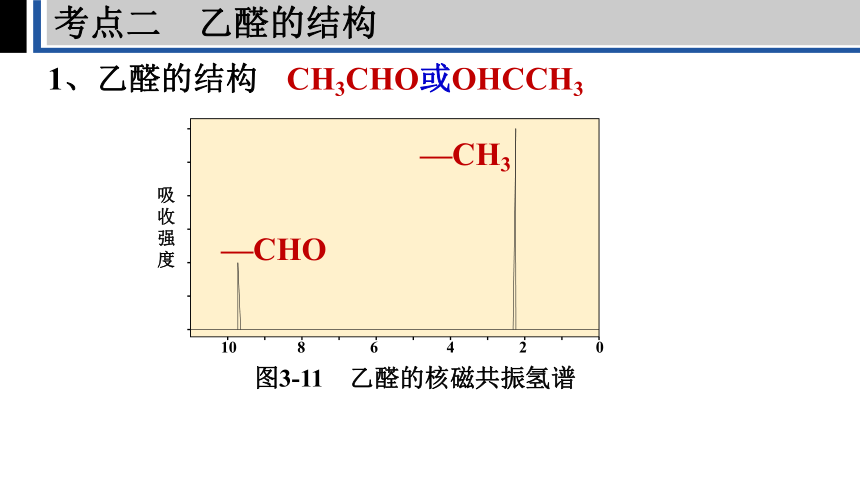
图3-11 乙醛的核磁共振氢谱
1、乙醛的结构
CH3CHO或OHCCH3
—CH3
—CHO
考点二 乙醛的结构
H
H
H
H
C
C
O
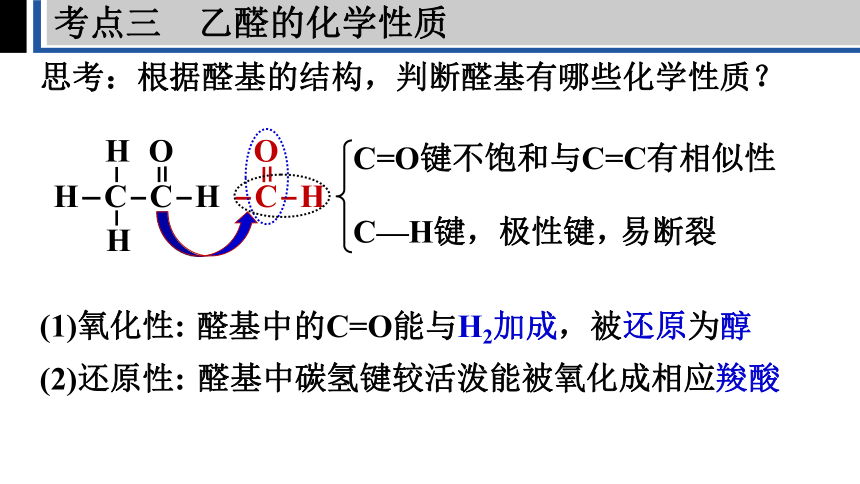
思考:根据醛基的结构,判断醛基有哪些化学性质?
H
C
O
C=O键不饱和与C=C有相似性
C—H键,极性键,
易断裂
(1)氧化性:
(2)还原性:
醛基中的C=O能与H2加成,被还原为醇
醛基中碳氢键较活泼能被氧化成相应羧酸
考点三 乙醛的化学性质
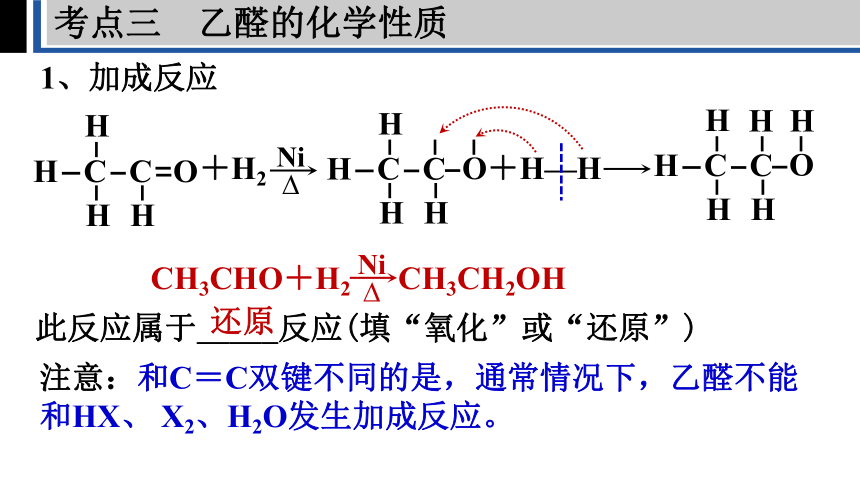
1、加成反应
+H2
Ni
H
H
H
C
C
O
H
H
H
H
C
C
O
H
+H—H
H
H
H
C
C
O
H
H H
Ni
CH3CHO+H2 CH3CH2OH
此反应属于_____反应(填“氧化”或“还原”)
还原
注意:和C=C双键不同的是,通常情况下,乙醛不能和HX、 X2、H2O发生加成反应。
考点三 乙醛的化学性质
2、氧化反应
(1)燃烧:
2CH3CHO+5O2 4CO2+4H2O
点燃
(2)催化氧化:
2CH3CHO+O2 2CH3COOH
催化剂
乙醇 乙醛 乙酸
[H]
[O]
[O]
[O]?
(3)与强氧化剂:
能使酸性KMnO4溶液、Br2水褪色
酸性KMnO4/K2Cr2O7溶液
注意: 乙醇不能被溴水氧化
考点三 乙醛的化学性质
2、氧化反应
(4)被弱氧化剂氧化
银镜反应
与新制的氢氧化铜反应
①银镜反应
考点三 乙醛的化学性质
2、氧化反应
(4)被弱氧化剂氧化
银镜反应
与新制的氢氧化铜反应
①银镜反应
2%AgNO3
2%
氨水
乙醛
水浴加热
银镜
考点三 乙醛的化学性质
①银镜反应
2%AgNO3
2%
氨水
乙醛
水浴加热
银镜
Ⅰ、配制银氨溶液:
AgNO3+NH3·H2O = AgOH↓+NH4NO3
AgOH+NH3·H2O =[Ag(NH3)2]OH +2H2O
氢氧化二氨合银
AgOH+2NH3.H2O=[Ag(NH3)2]++OH +2H2O
考点三 乙醛的化学性质
①银镜反应
2%AgNO3
2%
氨水
乙醛
水浴加热
银镜
Ⅱ、水浴加热生成银镜
CH3CHO+2Ag(NH3)2OH
水浴
H2O+2Ag↓+3NH3+CH3COONH4
1、2、3-水、银、氨
考点三 乙醛的化学性质
①银镜反应
实验注意事项:
5、可用稀HNO3清洗试管内壁的银镜
1、试管内壁应洁净,必须用水浴加热,不能用酒精灯加热
2、加热时不能振荡试管和摇动试管
3、银氨溶液必须随配随用,久置会产生易爆炸的物质
4、碱性环境下,乙醛被氧化成乙酸后与NH3反应生成乙酸铵
考点三 乙醛的化学性质
①银镜反应
银镜反应的应用及工业价值
(1)检验醛基的存在、测定醛基的数目
(2)工业上用来制瓶胆和镜子
考点三 乙醛的化学性质
(4)被弱氧化剂氧化
②与新制的氢氧化铜反应
考点三 乙醛的化学性质
②与新制的氢氧化铜反应
实验步骤:
Ⅰ、配制新制的Cu(OH)2悬浊液
①在试管里加入10%的NaOH溶液2mL(过量)
②滴入2%的CuSO4溶液 4~6滴,振荡
Ⅱ、乙醛的氧化
③加入乙醛溶液0.5mL,加热至沸腾
Cu2+ + 2OH =Cu(OH)2↓
CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O
砖红色
考点三 乙醛的化学性质
②与新制的氢氧化铜反应
实验注意事项:
(1)氢氧化铜溶液一定要新制
(2)碱一定要过量
应用:
(1)检验醛基的存在
(2)医学上检验病人是否患糖尿病
检验葡萄糖中的醛基
考点三 乙醛的化学性质
②与新制的氢氧化铜反应
①银镜反应
CH3CHO+2Ag(NH3)2OH
水浴
H2O+2Ag↓+3NH3+CH3COONH4
CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O
与新制的银氨溶液反应有光亮的银镜生成
与新制的氢氧化铜共热煮沸有红色沉淀生成
现象:
1mol CHO ~ 2mol Ag ~ 1mol Cu2O
考点三 乙醛的化学性质
H
H
H
H
C
C
O
加 H2
发生加成反应,被H2还原为醇
CH3 CH2OH
加 O2
H
H
H
OH
C
C
O
较活泼,能被氧化成相应羧酸
氧化性
还原性
氧
化
反
应
燃烧
催化氧化
能使酸性高锰酸钾、溴水褪色
被弱氧化剂氧化
银氨溶液
新制的Cu(OH)2
考点三 乙醛的化学性质
练、某醛的结构简式为(CH3)2C═CHCH2CH2CHO,
如何检验该有机物中的官能团?
简述实验设计方案:
相关反应的化学方程式:
先用银氨溶液检验醛基,酸化后再加溴水检验碳碳双键
(CH3)2C=CHCH2CH2CHO+2Ag(NH3)2OH →
(CH3)2C=CHCH2CH2COONH4+2Ag↓+3NH3+H2O
(CH3)2C=CHCH2CH2COOH+Br2 →
(CH3)2CBrCHBrCH2CH2COOH
当堂反馈
1、概念:
由烃基和醛基相连而构成的化合物
2、通式:
H
R
C
O
或 RCHO
饱和一元醛:
CnH2nO
考点四 醛类
3、醛的命名:
命名同卤代烃的相似,醛基不存在位置异构,都要从醛基碳开始编号。书写时先写烃基部分后写醛
CH3CHCH2CH2CH2CH=CHCHO
CH3
7-甲基-2-辛烯醛
4、饱和一元醛同分异构体的确定(碳链异构)
练、写出C5H10O表示醛的同分异构体
C5H10O→C4H9CHO
取代法
考点四 醛类
5、醛类的化学通性
(与乙醛相似)
(1)与氢气发生被还原成醇
(2)氧化反应
①燃烧
②催化氧化成羧酸
③被弱氧化剂氧化
④使酸性KMnO4溶液和溴水褪色
Ⅰ、银镜反应
Ⅱ、与新制的氢氧化铜反应
CHO
CHO
考点四 醛类
1、甲醛的物理性质、用途及危害
(1)物理性质:
(2)用途:
无色、有强烈刺激性气味气体,易溶于水,35%~40%的甲醛溶液叫福尔马林,具有杀菌和防腐性能
重要的有机合成原料,主要用于制酚醛树脂还可用于制作农药、肥料、浸制生物标本等
室内污染的罪魁祸首
(3)危害:
考点五 特殊的醛—甲醛(蚁醛)
室内去除甲醛植物高手
吊兰
绿萝
白掌
袖珍椰子
1、甲醛的物理性质、用途及危害
考点五 特殊的醛—甲醛(蚁醛)
2、甲醛的结构
球棍模型:平面三角形
结构简式:
结构式:
H
H
C
O
HCHO
结构特点:
H
H
C
O
甲醛分子中相当于含有两个醛基
即:甲醛中有2个活泼氢可被氧化
提醒: 甲醛是唯一的气态烃的含氧衍生物
考点五 特殊的醛—甲醛(蚁醛)
2、甲醛的结构
结构特点:
H
H
C
O
思考:甲醛催化氧化产物???
O
O
C
O
H
H
H2CO3
考点五 特殊的醛—甲醛(蚁醛)
3、甲醛的化学性质
(1)加成反应(还原反应)
HCHO+H2 CH3OH
Ni
(2)氧化反应
HCHO+O2 CO2+H2O
点燃
①燃烧
②催化氧化
2HCHO+O2 2HCOOH
催化剂
或HCHO+O2 HOCOOH
催化剂
即:H2CO3
考点五 特殊的醛—甲醛(蚁醛)
(2)氧化反应
③被弱氧化剂氧化
Ⅰ、银镜反应
HCHO+ 4[Ag(NH3)2]OH
2H2O+4Ag↓+6NH3+(NH4)2CO3↑
水浴
Ⅱ、与碱性的新制氢氧化铜反应
CO2↑+ 2Cu2O↓+5H2O
HCHO+4Cu(OH)2
1molHCHO ~ 4molAg ~ 2molCu2O
考点五 特殊的醛—甲醛(蚁醛)
(3)酚醛树脂的制取
OH
H
+ H
C
O
H+
OH
CH2OH
n
OH
CH2OH
H+
OH
CH2 OH
H
n
+(n-1)H2O
酚醛树脂
考点五 特殊的醛—甲醛(蚁醛)
(3)酚醛树脂的制取
nHCHO+n
OH
H+
OH
CH2 OH
H
n
+(n-1)H2O
缩聚反应:
有机物分子之间脱去小分子(H2O、NH3等)而形成高分子化合物的反应。
考点五 特殊的醛—甲醛(蚁醛)
(3)酚醛树脂的制取
酚醛树脂是人类合成的第一种高分子材料,其重要特征是耐高温性,即使在非常高的温度下,也能保持其结构的整体性和尺寸的稳定性。因此,酚醛树脂被广泛应用于高温领域,如耐火材料,摩擦材料,粘结剂和铸造行业。
考点五 特殊的醛—甲醛(蚁醛)
1、丙酮组成与结构
(1)分子式:
C3H6O
(2)结构简式:
或CH3COCH3
CH3CCH3
O
(3)管能团:
C
O
(4)酮: 羰基碳原子与两个烃基相连的化合物
(5)通式:
C
O
R'
R
考点六 酮类简介(丙酮)
2、丙酮的化学性质
不能被银氨溶液、新制氢氧化铜等弱氧化剂氧化,可催化加氢成醇。
CH3COCH3+H2 CH3CHOHCH3
Ni
考点六 酮类简介(丙酮)
拓展:醛与酮、烯醇、环醇的同分异构现象
如:C3H6O
CH3CH2CHO
CH3COCH3
CH2=CHCH2OH
OH
丙醛
丙酮
丙烯醇
环丙醇
考点六 酮类简介(丙酮)
练、A能发生一系列反应,最终产物为草酸
光
溴
A
B
NaOH、醇
C
D
溴水
NaOH、水
O2、催化剂
E
F
O2、催化剂
COOH
COOH
已知:B的相对分子质量比A大79,MBr=80
当堂反馈
练、信息迁移
已知:
RC=O +H CH2CHO
H
OH
→ R-CH-CH2-CHO
根据上述信息,用乙醛合成1-丁醇。
当堂反馈
第三节 醛 酮
第三章 烃的衍生物
考点二 乙醛的结构
考点三 乙醛的化学性质
内容索引
考点一 乙醛的物理性质
考点四 醛类
考点五 特殊的醛—甲醛
考点六 酮类简介(丙酮)
实现下列转化需加何种试剂?写出反应方程式,标明条件和反应类型。
CH3CH2OH → CH3CHO
温故知新
1、乙醛的物理性质
颜色:
气味:
状态:
密度:
挥发性:
溶解性:
无色透明
刺激性气味
液体
比水小
易挥发,沸点20.8℃
能与水、乙醇、乙醚、氯仿等互溶
考点一 乙醛的物理性质
1、乙醛的结构
H
H
H
H
C
C
O
结
构
式
球
棍
模
型
官能团:
醛基 —CHO
结构简式:
CH3CHO或 OHCCH3
考点二 乙醛的结构
吸
收
强
度
10 8 6 4 2 0
图3-11 乙醛的核磁共振氢谱
1、乙醛的结构
CH3CHO或OHCCH3
—CH3
—CHO
考点二 乙醛的结构
H
H
H
H
C
C
O
思考:根据醛基的结构,判断醛基有哪些化学性质?
H
C
O
C=O键不饱和与C=C有相似性
C—H键,极性键,
易断裂
(1)氧化性:
(2)还原性:
醛基中的C=O能与H2加成,被还原为醇
醛基中碳氢键较活泼能被氧化成相应羧酸
考点三 乙醛的化学性质
1、加成反应
+H2
Ni
H
H
H
C
C
O
H
H
H
H
C
C
O
H
+H—H
H
H
H
C
C
O
H
H H
Ni
CH3CHO+H2 CH3CH2OH
此反应属于_____反应(填“氧化”或“还原”)
还原
注意:和C=C双键不同的是,通常情况下,乙醛不能和HX、 X2、H2O发生加成反应。
考点三 乙醛的化学性质
2、氧化反应
(1)燃烧:
2CH3CHO+5O2 4CO2+4H2O
点燃
(2)催化氧化:
2CH3CHO+O2 2CH3COOH
催化剂
乙醇 乙醛 乙酸
[H]
[O]
[O]
[O]?
(3)与强氧化剂:
能使酸性KMnO4溶液、Br2水褪色
酸性KMnO4/K2Cr2O7溶液
注意: 乙醇不能被溴水氧化
考点三 乙醛的化学性质
2、氧化反应
(4)被弱氧化剂氧化
银镜反应
与新制的氢氧化铜反应
①银镜反应
考点三 乙醛的化学性质
2、氧化反应
(4)被弱氧化剂氧化
银镜反应
与新制的氢氧化铜反应
①银镜反应
2%AgNO3
2%
氨水
乙醛
水浴加热
银镜
考点三 乙醛的化学性质
①银镜反应
2%AgNO3
2%
氨水
乙醛
水浴加热
银镜
Ⅰ、配制银氨溶液:
AgNO3+NH3·H2O = AgOH↓+NH4NO3
AgOH+NH3·H2O =[Ag(NH3)2]OH +2H2O
氢氧化二氨合银
AgOH+2NH3.H2O=[Ag(NH3)2]++OH +2H2O
考点三 乙醛的化学性质
①银镜反应
2%AgNO3
2%
氨水
乙醛
水浴加热
银镜
Ⅱ、水浴加热生成银镜
CH3CHO+2Ag(NH3)2OH
水浴
H2O+2Ag↓+3NH3+CH3COONH4
1、2、3-水、银、氨
考点三 乙醛的化学性质
①银镜反应
实验注意事项:
5、可用稀HNO3清洗试管内壁的银镜
1、试管内壁应洁净,必须用水浴加热,不能用酒精灯加热
2、加热时不能振荡试管和摇动试管
3、银氨溶液必须随配随用,久置会产生易爆炸的物质
4、碱性环境下,乙醛被氧化成乙酸后与NH3反应生成乙酸铵
考点三 乙醛的化学性质
①银镜反应
银镜反应的应用及工业价值
(1)检验醛基的存在、测定醛基的数目
(2)工业上用来制瓶胆和镜子
考点三 乙醛的化学性质
(4)被弱氧化剂氧化
②与新制的氢氧化铜反应
考点三 乙醛的化学性质
②与新制的氢氧化铜反应
实验步骤:
Ⅰ、配制新制的Cu(OH)2悬浊液
①在试管里加入10%的NaOH溶液2mL(过量)
②滴入2%的CuSO4溶液 4~6滴,振荡
Ⅱ、乙醛的氧化
③加入乙醛溶液0.5mL,加热至沸腾
Cu2+ + 2OH =Cu(OH)2↓
CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O
砖红色
考点三 乙醛的化学性质
②与新制的氢氧化铜反应
实验注意事项:
(1)氢氧化铜溶液一定要新制
(2)碱一定要过量
应用:
(1)检验醛基的存在
(2)医学上检验病人是否患糖尿病
检验葡萄糖中的醛基
考点三 乙醛的化学性质
②与新制的氢氧化铜反应
①银镜反应
CH3CHO+2Ag(NH3)2OH
水浴
H2O+2Ag↓+3NH3+CH3COONH4
CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O
与新制的银氨溶液反应有光亮的银镜生成
与新制的氢氧化铜共热煮沸有红色沉淀生成
现象:
1mol CHO ~ 2mol Ag ~ 1mol Cu2O
考点三 乙醛的化学性质
H
H
H
H
C
C
O
加 H2
发生加成反应,被H2还原为醇
CH3 CH2OH
加 O2
H
H
H
OH
C
C
O
较活泼,能被氧化成相应羧酸
氧化性
还原性
氧
化
反
应
燃烧
催化氧化
能使酸性高锰酸钾、溴水褪色
被弱氧化剂氧化
银氨溶液
新制的Cu(OH)2
考点三 乙醛的化学性质
练、某醛的结构简式为(CH3)2C═CHCH2CH2CHO,
如何检验该有机物中的官能团?
简述实验设计方案:
相关反应的化学方程式:
先用银氨溶液检验醛基,酸化后再加溴水检验碳碳双键
(CH3)2C=CHCH2CH2CHO+2Ag(NH3)2OH →
(CH3)2C=CHCH2CH2COONH4+2Ag↓+3NH3+H2O
(CH3)2C=CHCH2CH2COOH+Br2 →
(CH3)2CBrCHBrCH2CH2COOH
当堂反馈
1、概念:
由烃基和醛基相连而构成的化合物
2、通式:
H
R
C
O
或 RCHO
饱和一元醛:
CnH2nO
考点四 醛类
3、醛的命名:
命名同卤代烃的相似,醛基不存在位置异构,都要从醛基碳开始编号。书写时先写烃基部分后写醛
CH3CHCH2CH2CH2CH=CHCHO
CH3
7-甲基-2-辛烯醛
4、饱和一元醛同分异构体的确定(碳链异构)
练、写出C5H10O表示醛的同分异构体
C5H10O→C4H9CHO
取代法
考点四 醛类
5、醛类的化学通性
(与乙醛相似)
(1)与氢气发生被还原成醇
(2)氧化反应
①燃烧
②催化氧化成羧酸
③被弱氧化剂氧化
④使酸性KMnO4溶液和溴水褪色
Ⅰ、银镜反应
Ⅱ、与新制的氢氧化铜反应
CHO
CHO
考点四 醛类
1、甲醛的物理性质、用途及危害
(1)物理性质:
(2)用途:
无色、有强烈刺激性气味气体,易溶于水,35%~40%的甲醛溶液叫福尔马林,具有杀菌和防腐性能
重要的有机合成原料,主要用于制酚醛树脂还可用于制作农药、肥料、浸制生物标本等
室内污染的罪魁祸首
(3)危害:
考点五 特殊的醛—甲醛(蚁醛)
室内去除甲醛植物高手
吊兰
绿萝
白掌
袖珍椰子
1、甲醛的物理性质、用途及危害
考点五 特殊的醛—甲醛(蚁醛)
2、甲醛的结构
球棍模型:平面三角形
结构简式:
结构式:
H
H
C
O
HCHO
结构特点:
H
H
C
O
甲醛分子中相当于含有两个醛基
即:甲醛中有2个活泼氢可被氧化
提醒: 甲醛是唯一的气态烃的含氧衍生物
考点五 特殊的醛—甲醛(蚁醛)
2、甲醛的结构
结构特点:
H
H
C
O
思考:甲醛催化氧化产物???
O
O
C
O
H
H
H2CO3
考点五 特殊的醛—甲醛(蚁醛)
3、甲醛的化学性质
(1)加成反应(还原反应)
HCHO+H2 CH3OH
Ni
(2)氧化反应
HCHO+O2 CO2+H2O
点燃
①燃烧
②催化氧化
2HCHO+O2 2HCOOH
催化剂
或HCHO+O2 HOCOOH
催化剂
即:H2CO3
考点五 特殊的醛—甲醛(蚁醛)
(2)氧化反应
③被弱氧化剂氧化
Ⅰ、银镜反应
HCHO+ 4[Ag(NH3)2]OH
2H2O+4Ag↓+6NH3+(NH4)2CO3↑
水浴
Ⅱ、与碱性的新制氢氧化铜反应
CO2↑+ 2Cu2O↓+5H2O
HCHO+4Cu(OH)2
1molHCHO ~ 4molAg ~ 2molCu2O
考点五 特殊的醛—甲醛(蚁醛)
(3)酚醛树脂的制取
OH
H
+ H
C
O
H+
OH
CH2OH
n
OH
CH2OH
H+
OH
CH2 OH
H
n
+(n-1)H2O
酚醛树脂
考点五 特殊的醛—甲醛(蚁醛)
(3)酚醛树脂的制取
nHCHO+n
OH
H+
OH
CH2 OH
H
n
+(n-1)H2O
缩聚反应:
有机物分子之间脱去小分子(H2O、NH3等)而形成高分子化合物的反应。
考点五 特殊的醛—甲醛(蚁醛)
(3)酚醛树脂的制取
酚醛树脂是人类合成的第一种高分子材料,其重要特征是耐高温性,即使在非常高的温度下,也能保持其结构的整体性和尺寸的稳定性。因此,酚醛树脂被广泛应用于高温领域,如耐火材料,摩擦材料,粘结剂和铸造行业。
考点五 特殊的醛—甲醛(蚁醛)
1、丙酮组成与结构
(1)分子式:
C3H6O
(2)结构简式:
或CH3COCH3
CH3CCH3
O
(3)管能团:
C
O
(4)酮: 羰基碳原子与两个烃基相连的化合物
(5)通式:
C
O
R'
R
考点六 酮类简介(丙酮)
2、丙酮的化学性质
不能被银氨溶液、新制氢氧化铜等弱氧化剂氧化,可催化加氢成醇。
CH3COCH3+H2 CH3CHOHCH3
Ni
考点六 酮类简介(丙酮)
拓展:醛与酮、烯醇、环醇的同分异构现象
如:C3H6O
CH3CH2CHO
CH3COCH3
CH2=CHCH2OH
OH
丙醛
丙酮
丙烯醇
环丙醇
考点六 酮类简介(丙酮)
练、A能发生一系列反应,最终产物为草酸
光
溴
A
B
NaOH、醇
C
D
溴水
NaOH、水
O2、催化剂
E
F
O2、催化剂
COOH
COOH
已知:B的相对分子质量比A大79,MBr=80
当堂反馈
练、信息迁移
已知:
RC=O +H CH2CHO
H
OH
→ R-CH-CH2-CHO
根据上述信息,用乙醛合成1-丁醇。
当堂反馈
