黑龙江省鸡西市第四中学2022-2023学年九年级(五四学制)上学期期中考试化学试题(含答案)
文档属性
| 名称 | 黑龙江省鸡西市第四中学2022-2023学年九年级(五四学制)上学期期中考试化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-12 00:00:00 | ||
图片预览




文档简介
鸡西四中2022-2023年度上学期期中考试 2022.11
九年级化学试题
可能用到的相对原子质量 H:1 O:16 Na:23 S:32 C:12 N:14 Zn:65
总分:100分 时间:60分钟 班级: 姓名:
一、选择题(每题只有一个正确答案,每题2分共30分)
1.下列变化中,属于化学变化的是( )
A.比较硬度 B. 探究铁生锈的条件 C. 洗涤剂除油污 D.自制汽水
2.下列实验操作正确的是( )
3.物质的性质决定其用途。下列物质的用途与性质对应关系错误的是 ( )
A稀盐酸可除铁锈-稀盐酸可与铁锈的主要成分Fe2O3反应
B氮气可用做保护气-氮气化学性质稳定
C液氧可用于火箭发射-液氧具有可燃性
D氧化钙可用做食品干燥剂-氧化钙能与水反应
下列金属中导电性最好的是( )
A. Cu B. Al C. Fe D. Ag
5.冶铁的原料中,除铁矿石、焦炭、空气,还应添加的是( )
A.一氧化碳 B.石灰石 C.二氧化锰 D.氧化铁
6.下列关于溶液的叙述正确的是( )
A.凡是均一、稳定的液体都是溶液 B.溶液都是无色透明的
C.溶液是均一、稳定的混合物 D.稀溶液一定是不饱和溶液
7.下列实验现象的描述正确的是 ( )
A.一氧化碳燃烧:无色气体燃烧,产生蓝色火焰,放热,生成二氧化碳气体
B.向稀盐酸中滴加石蕊溶液:溶液变成蓝色
C.紫色石蕊试液滴加到生石灰上:紫色石蕊溶液无明显变化
D.铝丝放在硫酸铜溶液中:银白色固体表面覆盖紅色固体,溶液由蓝色变为无色
8.下列物质能与稀硫酸反应,且反应后溶液为浅绿色的是( )
A.铜 B.锌 C.铁 D.铝
9. 医用降温冰袋中可能盛有以下物质中的( )
A. 氢氧化钠 B.氯化钠 C.浓硫酸 D.硝酸铵
10. 20℃时,氯化钠的溶解度为36g。对这句话理解错误的是 ( )
A.20℃时,100g水最多能溶解氯化钠36g
B.20℃时,100g氯化钠饱和溶液中含氯化钠36g
C.20℃时,氯化钠饱和溶液中水与氯化钠的质量比为100:36
D.20℃时,将36g氯化钠溶解于100g水中,所得溶液为该温度下氯化钠饱和溶液
11.浓硫酸和浓盐酸敞口放置在空气中一段时间后,溶液中( )
A.溶质的质量分数都变小[ B.溶液的质量都增大
C.溶质的质量分数都变大 D.溶质的质量分数前者变大,后者变小
12.下列叙述正确的是( )
A.降低温度能使任何饱和溶液都析出晶体 B.凡是易溶物质的溶液必是浓溶液
C.气体溶解度只受温度的影响 D.所有固体溶解度都随温度升高而增大
13.下列溶液中的溶剂不是水的是( )
A.碘酒 B.生理盐水 C.稀硫酸 D.稀盐酸
14.将下列厨房里常用的物质分别放入水中,不能形成溶液的是( )
A.食盐 B.食用油 C.白醋 D.蔗糖
15.下列应用的原理(用化学方程式表示)及基本反应类型均正确的是 ( )
A.用生石灰中和硫酸厂的废水 化合反应
B.用稀硫酸洗去试管上附着的铜 置换反应
C.实验室制取氢气Zn+H2SO4=ZnSO4+H2 置换反应
D.验证铁和银的活动性 置换反应
二、不定项选择(每题有1或2个正确答案,每题2分共10分)
16.在金属表面覆盖保护膜是普遍采用的金属防锈措施之一。下列自行车的防锈措施中,正确的的是 ( )
A.用已生锈的铁锈做保护膜 B.链条上油 C.轮圈镀铬 D.漏天放置
17.推理是化学学习中常用的思维方法,下列推理正确的是 ( )
A.碱溶液能跟某些非金属氧化物反应,所以碱溶液能吸收CO气体
B.置换反应生成单质和化合物,但是有单质和化合物生成的反应不一定是置换反应
C.铝的化学性质比较活泼,所以在空气中铝比铁更容易被锈浊
D.酸溶液能使紫色石蕊试液变红,所以能使紫色石蕊试液变红的一定是酸性溶液
18.将80 g质量分数为36%的浓盐酸稀释成6%的稀盐酸,需加水的质量为( )
A.480 g B.400 g C.320 g D.80 g
19.NaCl和KNO3的溶解度曲线如图所示,下列说法正确的( )
A.KNO3的溶解度一定大于NaCl
B.NaCl的溶解度受温度影响的程度比KNO3大
C.40 ℃时,KNO3饱和溶液的溶质质量分数为63.9%
D.将60 ℃时的210 g KNO3饱和溶液稀释到20%需加水340 g
20.等质量的镁、铁、锌三种金属分别与足量稀硫酸反应,下列图像能正确表示产生氢气的质量与反应时间关系的是 ( )
三、填空(每空一分,共25分)
用化学用语填空
铁锈的主要成分 ;(2)硫酸铜溶液中的溶质 ;
(3)盐酸中氯元素的化合价 ;(4)医用酒精中的溶剂 ;
22.现有氢氧化钙、氢氧化铝、硫酸等物质,选择合适的物质填空:
(1)汽车用铅蓄电池中含有的是 ;
(2)改良酸性土壤的是 :
(3)可用于治疗胃酸过多的碱是 。
23.用化学知识回答下列问题:
(1)打开汽水瓶盖,汽水会自动喷出的原因是 ;
(2)用洗涤剂去除油污是因为洗涤剂具有 功能;
(3)回收废旧金属的好处 :
(4)铝可制成电线,主要是利用其有 性,用铝箔包装糖果是利用其具有 性。铝制品具有很好的抗腐蚀性能,其原因是 。(用化学方程式表示)
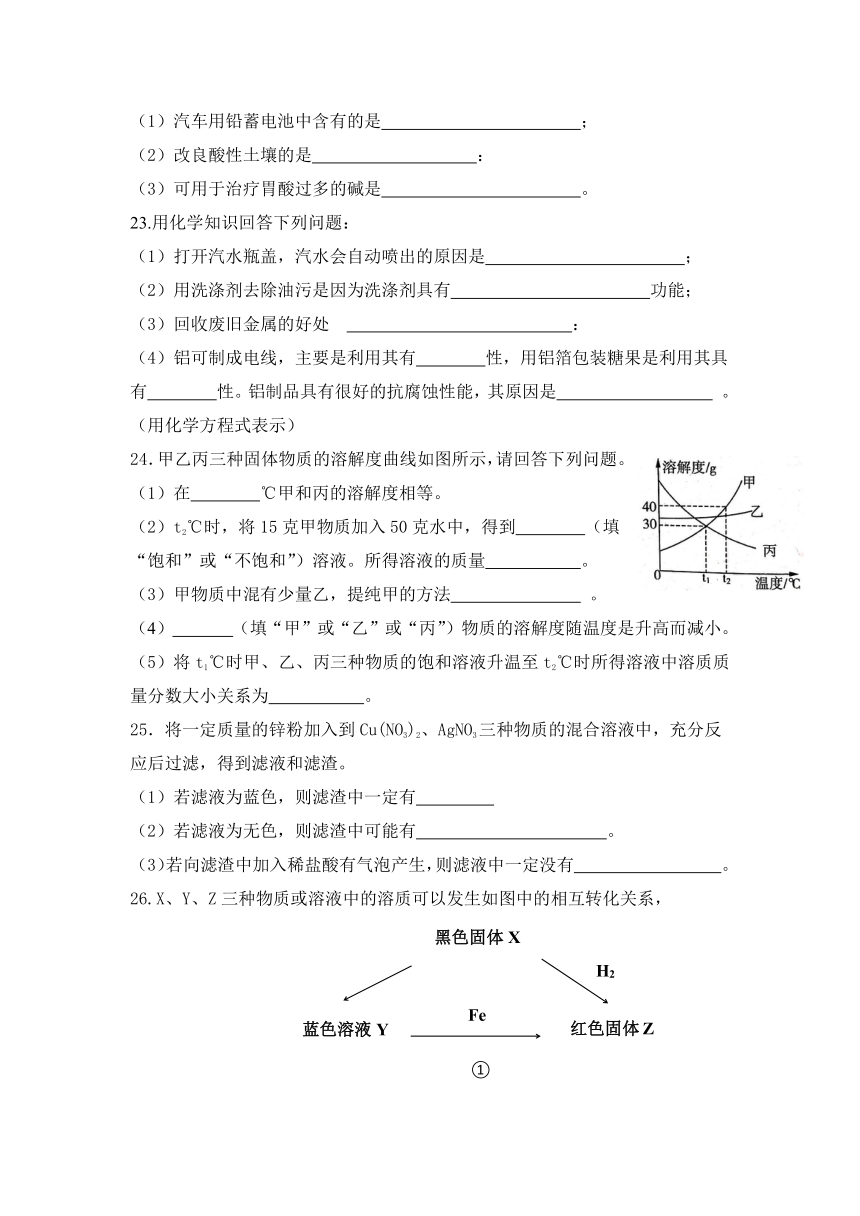
24.甲乙丙三种固体物质的溶解度曲线如图所示,请回答下列问题。
(1)在 ℃甲和丙的溶解度相等。
(2)t2℃时,将15克甲物质加入50克水中,得到 (填
“饱和”或“不饱和”)溶液。所得溶液的质量 。
甲物质中混有少量乙,提纯甲的方法 。
(4) (填“甲”或“乙”或“丙”)物质的溶解度随温度是升高而减小。
(5)将t1℃时甲、乙、丙三种物质的饱和溶液升温至t2℃时所得溶液中溶质质量分数大小关系为 。
25.将一定质量的锌粉加入到Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。
(1)若滤液为蓝色,则滤渣中一定有
(2)若滤液为无色,则滤渣中可能有 。
(3)若向滤渣中加入稀盐酸有气泡产生,则滤液中一定没有 。
26.X、Y、Z三种物质或溶液中的溶质可以发生如图中的相互转化关系,
(
黑色固体
X
)
(
H
2
)
(
Fe
) (
红色固体
Z
) (
蓝色溶液
Y
)
(
①
)
物质X化学式 ,物质Z化学式
①反应化学方程式
四、实验题(每空一分,共25分)
27.根据下列实验装置图,按要求回答下列问题:
(
A B C D E
)
(1)写出标有序号的仪器名称:①______________;②______________。
(2)实验室制取CO2的化学反应方程式为________________________________;制取并收集该气体应选择的装置是______________(填序号);若想控制反应速率,可以将仪器②用______________代替;
(3)如果选择与制取CO2相同的发生装置来制取O2,则发生反应的化学方程式为_____________________________,其基本反应类型是____________。
28.配制100克溶质质量分数为5%的氯化钠溶液常按以下操作顺序进行。
(1)正确配制该溶液的操作顺序为 、 、 、 。
(2)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向右盘,应 。应称量 克氯化钠,需要水 ml,应选用 (10ml、50ml、100ml)量筒。
(
a
b
)(3)将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌,其目的是 。配置过程用到的玻璃仪器有 。
(4)实验室用98%的浓硫酸配制100g溶质质量分数为20%的稀硫酸。
浓硫酸稀释过程如图所示,b中盛放的物质是 ,
a仪器的名称 ,其作用是 。
29.为了研究炼铁原理,按如图所示,用一氧化碳与氧化铁反应进行实验,回答问题。
(1)该实验开始时,要先通一会儿一氧化碳再点燃酒精灯,其目的是 。
(2)硬质玻璃管内发生反应的化学方程式是 ;现象是 。
(3)将尾气点燃的好处是 。实验结束应先 (填熄灭酒精灯或停止通入一氧化碳)
五、计算(共10分)
30.专家提醒:烧烤摊里会吃出“癌症风险”。腌制的肉串会产生一种叫做二甲基亚硝胺(C2H6N2O)的强致癌物质。请回答下列问题:
(1)该物质的相对分子质量 。
(2)该物质中碳元素和氮元素的质量比 (答最简整数比)。
(3)3.7g该物质中氮元素的质量 。
31. 6.5g的锌和100g的稀硫酸恰好完全反应,试回答下列问题
(1)求生成氢气的质量
(2)求硫酸溶液的溶质质量分数
考号 班级 姓名
答题卡
选择题:
1 2 3 4 5 6 7 8 9 10
11 12 13 14 15 16 17 18 19 20
三、填空(每空一分,共25分)
21.用化学用语填空
(1) ;(2) ;
(3) ;(4) ;
22.(1) ;
(2) :
(3) 。
23.(1) ;
(2) 功能;
(3) :
(4) 性, 性。 。
24.(1) ℃
(2) 。 。
(3) 。
(4) (填“甲”或“乙”或“丙”)。
(5) 。
25.(1)
(2) 。
(3) 。
26.(1) ,
(2)
四、实验题(每空一分,共25分)
27.
(1)①______________;②______________。
(2)________________________________;______________(填序号);______________代替;
(3)_____________________________,____________。
28.
(1) 、 、 、 。
(2) 。 克, ml, 。
(3) 。 。
(4) , , 。
29.
(1) 。
(2) ;
现象是 。
(3) 。 .
五、计算(共10分)
30.(1) 。
(2) (答最简整数比)。
(3) 。
31.
鸡西四中2022-2023年度上学期期中考试 2022.11
九年级化学试题
答案;选择题:
1 2 3 4 5 6 7 8 9 10
D A C D B C D C D B
11 12 13 14 15 16 17 18 19 20
A B A B C BC BD B D A
三、填空(每空一分,共25分)
21.用化学用语填空
(1) Fe2O3 ;(2) CuSO4 ;
(3) ;(4) H2O ;
22.(1) 硫酸 ;
(2) 氢氧化钙 :
(3) 氢氧化铝 。
23.(1) 压强减小气体溶解度减小 ;
(2) 乳化 功能;
(3) 节约资源(合理即可) :
(4) 导电 性, 延展 性4Al+3O2=2Al2O3 。
24.(1) t1 ℃
(2) 不饱和 。 65g 。
(3) 降温结晶 。
(4) 丙 (填“甲”或“乙”或“丙”)。
(5) 乙》甲》丙 。
25.(1) 银
(2) 锌 。
(3) 硝酸银 、硝酸铜 。
26.(1) CuO , Cu
(2) CuSO4+Fe=Cu+FeSO4
四、实验题(每空一分,共25分)
27.
(1)①____试管__________;②___长颈漏斗___________。
(2)_____CaCO3+2HCl=CaCl2+H2O+CO2↑_;__BE______(填序号);___分液漏斗_______代替;
(3)_____2H2O22H2O+O2↑___,_____分解_______。
28.
(1) 计算 、 称量 、 量取 、 溶解 。
(2) 添加药品至天平平衡 。 5 克, 95 ml, 100ml 。
(3) 搅拌,加速溶解 。 玻璃棒、烧杯、量筒、胶头滴管 。
(4) 浓硫酸 , 玻璃棒 , 搅拌,散热 。
29.
(1) 排尽试管内的空气,防止爆炸。 。
(2) 3CO+Fe2O32Fe+3CO2 ;
现象是 红色粉末变黑 。
(3) 防止空气污染 。 熄灭酒精灯 .
五、计算(共10分)
30.(1) 74 。
(2) 6:7 (答最简整数比)。
(3) 1.4g 。
解:设生成氢气的质量为x,硫酸中溶质质量为Y
硫酸溶质质量分数=×100%=9.8%
答:生成氢气的质量0.2g 硫酸溶质质量分数9.8%
九年级化学试题
可能用到的相对原子质量 H:1 O:16 Na:23 S:32 C:12 N:14 Zn:65
总分:100分 时间:60分钟 班级: 姓名:
一、选择题(每题只有一个正确答案,每题2分共30分)
1.下列变化中,属于化学变化的是( )
A.比较硬度 B. 探究铁生锈的条件 C. 洗涤剂除油污 D.自制汽水
2.下列实验操作正确的是( )
3.物质的性质决定其用途。下列物质的用途与性质对应关系错误的是 ( )
A稀盐酸可除铁锈-稀盐酸可与铁锈的主要成分Fe2O3反应
B氮气可用做保护气-氮气化学性质稳定
C液氧可用于火箭发射-液氧具有可燃性
D氧化钙可用做食品干燥剂-氧化钙能与水反应
下列金属中导电性最好的是( )
A. Cu B. Al C. Fe D. Ag
5.冶铁的原料中,除铁矿石、焦炭、空气,还应添加的是( )
A.一氧化碳 B.石灰石 C.二氧化锰 D.氧化铁
6.下列关于溶液的叙述正确的是( )
A.凡是均一、稳定的液体都是溶液 B.溶液都是无色透明的
C.溶液是均一、稳定的混合物 D.稀溶液一定是不饱和溶液
7.下列实验现象的描述正确的是 ( )
A.一氧化碳燃烧:无色气体燃烧,产生蓝色火焰,放热,生成二氧化碳气体
B.向稀盐酸中滴加石蕊溶液:溶液变成蓝色
C.紫色石蕊试液滴加到生石灰上:紫色石蕊溶液无明显变化
D.铝丝放在硫酸铜溶液中:银白色固体表面覆盖紅色固体,溶液由蓝色变为无色
8.下列物质能与稀硫酸反应,且反应后溶液为浅绿色的是( )
A.铜 B.锌 C.铁 D.铝
9. 医用降温冰袋中可能盛有以下物质中的( )
A. 氢氧化钠 B.氯化钠 C.浓硫酸 D.硝酸铵
10. 20℃时,氯化钠的溶解度为36g。对这句话理解错误的是 ( )
A.20℃时,100g水最多能溶解氯化钠36g
B.20℃时,100g氯化钠饱和溶液中含氯化钠36g
C.20℃时,氯化钠饱和溶液中水与氯化钠的质量比为100:36
D.20℃时,将36g氯化钠溶解于100g水中,所得溶液为该温度下氯化钠饱和溶液
11.浓硫酸和浓盐酸敞口放置在空气中一段时间后,溶液中( )
A.溶质的质量分数都变小[ B.溶液的质量都增大
C.溶质的质量分数都变大 D.溶质的质量分数前者变大,后者变小
12.下列叙述正确的是( )
A.降低温度能使任何饱和溶液都析出晶体 B.凡是易溶物质的溶液必是浓溶液
C.气体溶解度只受温度的影响 D.所有固体溶解度都随温度升高而增大
13.下列溶液中的溶剂不是水的是( )
A.碘酒 B.生理盐水 C.稀硫酸 D.稀盐酸
14.将下列厨房里常用的物质分别放入水中,不能形成溶液的是( )
A.食盐 B.食用油 C.白醋 D.蔗糖
15.下列应用的原理(用化学方程式表示)及基本反应类型均正确的是 ( )
A.用生石灰中和硫酸厂的废水 化合反应
B.用稀硫酸洗去试管上附着的铜 置换反应
C.实验室制取氢气Zn+H2SO4=ZnSO4+H2 置换反应
D.验证铁和银的活动性 置换反应
二、不定项选择(每题有1或2个正确答案,每题2分共10分)
16.在金属表面覆盖保护膜是普遍采用的金属防锈措施之一。下列自行车的防锈措施中,正确的的是 ( )
A.用已生锈的铁锈做保护膜 B.链条上油 C.轮圈镀铬 D.漏天放置
17.推理是化学学习中常用的思维方法,下列推理正确的是 ( )
A.碱溶液能跟某些非金属氧化物反应,所以碱溶液能吸收CO气体
B.置换反应生成单质和化合物,但是有单质和化合物生成的反应不一定是置换反应
C.铝的化学性质比较活泼,所以在空气中铝比铁更容易被锈浊
D.酸溶液能使紫色石蕊试液变红,所以能使紫色石蕊试液变红的一定是酸性溶液
18.将80 g质量分数为36%的浓盐酸稀释成6%的稀盐酸,需加水的质量为( )
A.480 g B.400 g C.320 g D.80 g
19.NaCl和KNO3的溶解度曲线如图所示,下列说法正确的( )
A.KNO3的溶解度一定大于NaCl
B.NaCl的溶解度受温度影响的程度比KNO3大
C.40 ℃时,KNO3饱和溶液的溶质质量分数为63.9%
D.将60 ℃时的210 g KNO3饱和溶液稀释到20%需加水340 g
20.等质量的镁、铁、锌三种金属分别与足量稀硫酸反应,下列图像能正确表示产生氢气的质量与反应时间关系的是 ( )
三、填空(每空一分,共25分)
用化学用语填空
铁锈的主要成分 ;(2)硫酸铜溶液中的溶质 ;
(3)盐酸中氯元素的化合价 ;(4)医用酒精中的溶剂 ;
22.现有氢氧化钙、氢氧化铝、硫酸等物质,选择合适的物质填空:
(1)汽车用铅蓄电池中含有的是 ;
(2)改良酸性土壤的是 :
(3)可用于治疗胃酸过多的碱是 。
23.用化学知识回答下列问题:
(1)打开汽水瓶盖,汽水会自动喷出的原因是 ;
(2)用洗涤剂去除油污是因为洗涤剂具有 功能;
(3)回收废旧金属的好处 :
(4)铝可制成电线,主要是利用其有 性,用铝箔包装糖果是利用其具有 性。铝制品具有很好的抗腐蚀性能,其原因是 。(用化学方程式表示)
24.甲乙丙三种固体物质的溶解度曲线如图所示,请回答下列问题。
(1)在 ℃甲和丙的溶解度相等。
(2)t2℃时,将15克甲物质加入50克水中,得到 (填
“饱和”或“不饱和”)溶液。所得溶液的质量 。
甲物质中混有少量乙,提纯甲的方法 。
(4) (填“甲”或“乙”或“丙”)物质的溶解度随温度是升高而减小。
(5)将t1℃时甲、乙、丙三种物质的饱和溶液升温至t2℃时所得溶液中溶质质量分数大小关系为 。
25.将一定质量的锌粉加入到Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。
(1)若滤液为蓝色,则滤渣中一定有
(2)若滤液为无色,则滤渣中可能有 。
(3)若向滤渣中加入稀盐酸有气泡产生,则滤液中一定没有 。
26.X、Y、Z三种物质或溶液中的溶质可以发生如图中的相互转化关系,
(
黑色固体
X
)
(
H
2
)
(
Fe
) (
红色固体
Z
) (
蓝色溶液
Y
)
(
①
)
物质X化学式 ,物质Z化学式
①反应化学方程式
四、实验题(每空一分,共25分)
27.根据下列实验装置图,按要求回答下列问题:
(
A B C D E
)
(1)写出标有序号的仪器名称:①______________;②______________。
(2)实验室制取CO2的化学反应方程式为________________________________;制取并收集该气体应选择的装置是______________(填序号);若想控制反应速率,可以将仪器②用______________代替;
(3)如果选择与制取CO2相同的发生装置来制取O2,则发生反应的化学方程式为_____________________________,其基本反应类型是____________。
28.配制100克溶质质量分数为5%的氯化钠溶液常按以下操作顺序进行。
(1)正确配制该溶液的操作顺序为 、 、 、 。
(2)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向右盘,应 。应称量 克氯化钠,需要水 ml,应选用 (10ml、50ml、100ml)量筒。
(
a
b
)(3)将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌,其目的是 。配置过程用到的玻璃仪器有 。
(4)实验室用98%的浓硫酸配制100g溶质质量分数为20%的稀硫酸。
浓硫酸稀释过程如图所示,b中盛放的物质是 ,
a仪器的名称 ,其作用是 。
29.为了研究炼铁原理,按如图所示,用一氧化碳与氧化铁反应进行实验,回答问题。
(1)该实验开始时,要先通一会儿一氧化碳再点燃酒精灯,其目的是 。
(2)硬质玻璃管内发生反应的化学方程式是 ;现象是 。
(3)将尾气点燃的好处是 。实验结束应先 (填熄灭酒精灯或停止通入一氧化碳)
五、计算(共10分)
30.专家提醒:烧烤摊里会吃出“癌症风险”。腌制的肉串会产生一种叫做二甲基亚硝胺(C2H6N2O)的强致癌物质。请回答下列问题:
(1)该物质的相对分子质量 。
(2)该物质中碳元素和氮元素的质量比 (答最简整数比)。
(3)3.7g该物质中氮元素的质量 。
31. 6.5g的锌和100g的稀硫酸恰好完全反应,试回答下列问题
(1)求生成氢气的质量
(2)求硫酸溶液的溶质质量分数
考号 班级 姓名
答题卡
选择题:
1 2 3 4 5 6 7 8 9 10
11 12 13 14 15 16 17 18 19 20
三、填空(每空一分,共25分)
21.用化学用语填空
(1) ;(2) ;
(3) ;(4) ;
22.(1) ;
(2) :
(3) 。
23.(1) ;
(2) 功能;
(3) :
(4) 性, 性。 。
24.(1) ℃
(2) 。 。
(3) 。
(4) (填“甲”或“乙”或“丙”)。
(5) 。
25.(1)
(2) 。
(3) 。
26.(1) ,
(2)
四、实验题(每空一分,共25分)
27.
(1)①______________;②______________。
(2)________________________________;______________(填序号);______________代替;
(3)_____________________________,____________。
28.
(1) 、 、 、 。
(2) 。 克, ml, 。
(3) 。 。
(4) , , 。
29.
(1) 。
(2) ;
现象是 。
(3) 。 .
五、计算(共10分)
30.(1) 。
(2) (答最简整数比)。
(3) 。
31.
鸡西四中2022-2023年度上学期期中考试 2022.11
九年级化学试题
答案;选择题:
1 2 3 4 5 6 7 8 9 10
D A C D B C D C D B
11 12 13 14 15 16 17 18 19 20
A B A B C BC BD B D A
三、填空(每空一分,共25分)
21.用化学用语填空
(1) Fe2O3 ;(2) CuSO4 ;
(3) ;(4) H2O ;
22.(1) 硫酸 ;
(2) 氢氧化钙 :
(3) 氢氧化铝 。
23.(1) 压强减小气体溶解度减小 ;
(2) 乳化 功能;
(3) 节约资源(合理即可) :
(4) 导电 性, 延展 性4Al+3O2=2Al2O3 。
24.(1) t1 ℃
(2) 不饱和 。 65g 。
(3) 降温结晶 。
(4) 丙 (填“甲”或“乙”或“丙”)。
(5) 乙》甲》丙 。
25.(1) 银
(2) 锌 。
(3) 硝酸银 、硝酸铜 。
26.(1) CuO , Cu
(2) CuSO4+Fe=Cu+FeSO4
四、实验题(每空一分,共25分)
27.
(1)①____试管__________;②___长颈漏斗___________。
(2)_____CaCO3+2HCl=CaCl2+H2O+CO2↑_;__BE______(填序号);___分液漏斗_______代替;
(3)_____2H2O22H2O+O2↑___,_____分解_______。
28.
(1) 计算 、 称量 、 量取 、 溶解 。
(2) 添加药品至天平平衡 。 5 克, 95 ml, 100ml 。
(3) 搅拌,加速溶解 。 玻璃棒、烧杯、量筒、胶头滴管 。
(4) 浓硫酸 , 玻璃棒 , 搅拌,散热 。
29.
(1) 排尽试管内的空气,防止爆炸。 。
(2) 3CO+Fe2O32Fe+3CO2 ;
现象是 红色粉末变黑 。
(3) 防止空气污染 。 熄灭酒精灯 .
五、计算(共10分)
30.(1) 74 。
(2) 6:7 (答最简整数比)。
(3) 1.4g 。
解:设生成氢气的质量为x,硫酸中溶质质量为Y
硫酸溶质质量分数=×100%=9.8%
答:生成氢气的质量0.2g 硫酸溶质质量分数9.8%
同课章节目录
