第2章 官能团与有机化学反应 烃的衍生物 单元测试卷 2022-2023学年高二下学期化学鲁科版(2019)选择性必修3(Word含答案)
文档属性
| 名称 | 第2章 官能团与有机化学反应 烃的衍生物 单元测试卷 2022-2023学年高二下学期化学鲁科版(2019)选择性必修3(Word含答案) |
|
|
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-13 00:00:00 | ||
图片预览




文档简介
第2章 官能团与有机化学反应 烃的衍生物 单元测试卷
一、选择题
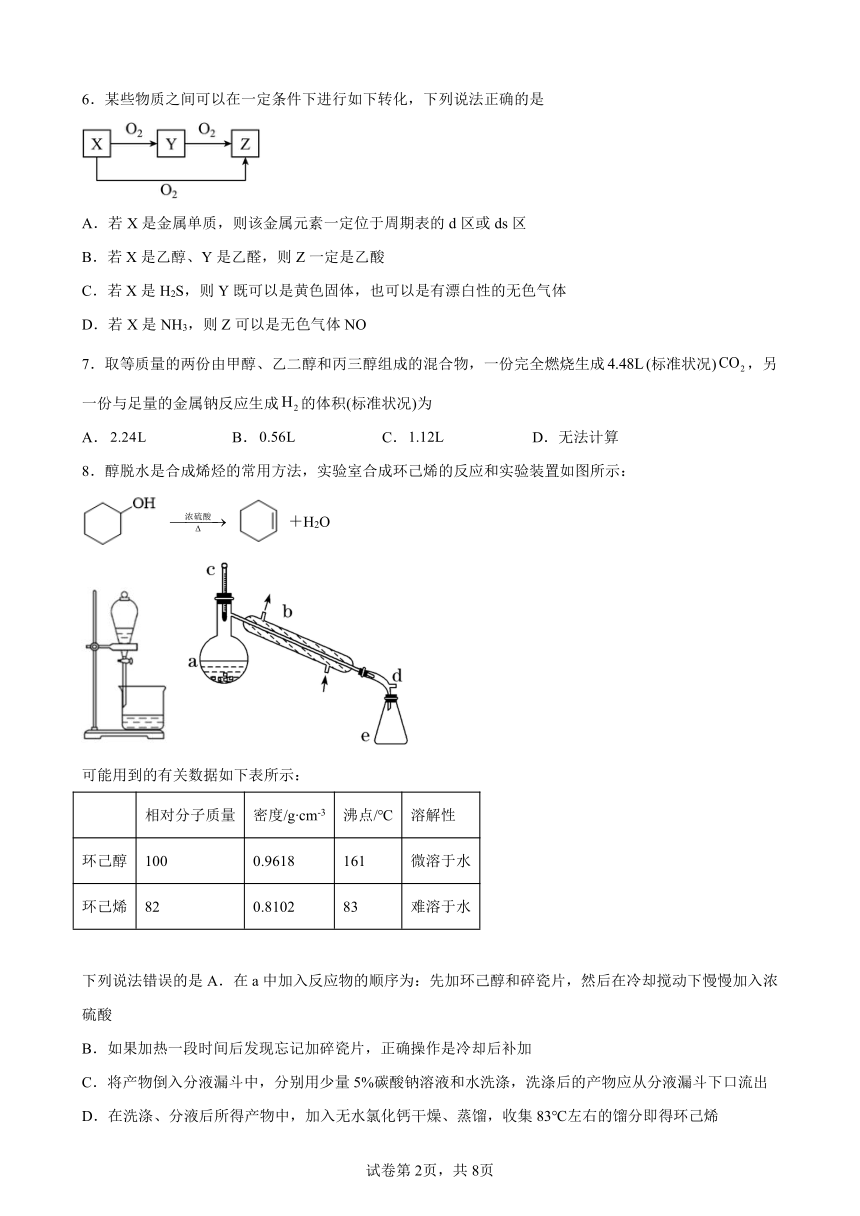
1.莲藕中某多酚类物质的结构简式如图所示(R为烃基)。下列说法不正确的是
A.置于空气中易被氧化 B.能与FeCl3溶液发生显色反应
C.能与饱和溴水发生加成反应 D.与苯环直接相连的原子共平面
2.下列化合物的分子中,所有原子可能共平面且共平面原子数最多的是
A.乙烯基环己烷 B.苯乙炔 C.苯甲酸 D.丙烯醇
3.1mol有机羧酸酯A在酸性条件下完全水解能得到相对分子质量相同的两种物质,则A是
A.甲酸甲酯 B.甲酸乙酯 C.乙酸甲酯 D.乙酸乙酯
4.化学与生活密切相关。下列叙述错误的是
A.纯碱溶液可以用于清洗餐具油污
B.玉米淀粉和废弃秸秆可生产乙醇
C.珠江三角洲的形成与胶体聚沉有关
D.“84消毒液”可以喷洒于衣物上进行杀菌消毒
5.目前工业上多采用甲醇和一氧化碳反应制备醋酸:,反应过程如图所示,下列有关说法中错误的是
A.为催化剂 B.⑤与水的反应为取代反应
C.该反应过程中不存在非极性键的形成 D.在反应过程中Rh的配位数发生改变
6.某些物质之间可以在一定条件下进行如下转化,下列说法正确的是
A.若X是金属单质,则该金属元素一定位于周期表的d区或ds区
B.若X是乙醇、Y是乙醛,则Z一定是乙酸
C.若X是H2S,则Y既可以是黄色固体,也可以是有漂白性的无色气体
D.若X是NH3,则Z可以是无色气体NO
7.取等质量的两份由甲醇、乙二醇和丙三醇组成的混合物,一份完全燃烧生成(标准状况),另一份与足量的金属钠反应生成的体积(标准状况)为
A. B. C. D.无法计算
8.醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图所示:
+H2O
可能用到的有关数据如下表所示:
相对分子质量 密度/g cm-3 沸点/℃ 溶解性
环己醇 100 0.9618 161 微溶于水
环己烯 82 0.8102 83 难溶于水
下列说法错误的是A.在a中加入反应物的顺序为:先加环己醇和碎瓷片,然后在冷却搅动下慢慢加入浓硫酸
B.如果加热一段时间后发现忘记加碎瓷片,正确操作是冷却后补加
C.将产物倒入分液漏斗中,分别用少量5%碳酸钠溶液和水洗涤,洗涤后的产物应从分液漏斗下口流出
D.在洗涤、分液后所得产物中,加入无水氯化钙干燥、蒸馏,收集83℃左右的馏分即得环己烯
9.生活中处处有化学,下列叙述不正确的是
A.漂粉精可用于游泳池的消毒 B.碳酸氢钠可做食品膨松剂
C.青铜和黄铜是不同结构的单质铜 D.金属氧化物可使玻璃呈现不同颜色
10.设为阿伏伽德罗常数的值,下列有关叙述正确的是
A.1mol与足量的充分反应,得到
B.100g46%乙醇溶液中所含O—H键的数目为
C.标准状况下,11.2LNO和11.2L混合气体充入密闭容器,所含氧原子数等于1.5
D.12g固体中含离子数为0.3
11.已知苯并唑酮()可转化为X(),下列说法正确的是
A.1molX与足量NaOH溶液充分反应,最多可消耗4molNaOH
B.X能使酸性高锰酸钾溶液褪色,但不能使溴水褪色
C.X与足量加成后所得有机物分子中手性碳原子数目为3个
D.1mol苯并唑酮完全燃烧需要消耗6.25mol氧气
12.2020年,“新冠”席卷全球,给各个国家造成了极大的危害。阿比朵尔是治疗“新冠”疾病的一种药物,其结构简式如图所示。下列有关说法正确的是
A.1mol阿比朵尔最多可与3mol NaOH发生反应
B.1mol阿比朵尔最多可与8 mol H2发生加成反应
C.阿比朵尔不是手性分子
D.阿比朵尔分子O原子的杂化方式只有一种
13.新冠病毒是一种具有包膜的RNA病毒,包膜的主要成分是蛋白质和脂质。核酸检测就是检测新冠病毒的RNA。下列说法不正确的是
A.核酸和蛋白质都是生物大分子
B.蛋白质能发生水解反应,而核酸不能发生水解反应
C.核酸中核苷酸之间通过磷酯键连接
D.一定浓度的含氯消毒液可使新冠病毒中的蛋白质变性
14.下列表示正确的是
A.乙烯的实验式:C2H4 B.乙酸甲酯的结构简式:HCOOCH2CH3
C.2-甲基丁烷的键线式: D.羟基的电子式:
二、填空题
15.现有以下几种有机物:
①CH4②CH3CH2OH ③ ④癸烷 ⑤CH3COOH ⑥⑦ ⑧ ⑨丙烷
请利用上述给出的物质按要求回答下列问题:
(1)相对分子质量为44的烷烃结构简式为_____。
(2)分子中含有14个氢原子的烷烃的分子式是____。
(3)与③互为同分异构体的是_____(填序号)。
(4)⑦的所有同分异构体(不考虑空间异构)中一氯代物有3种的有_____种。
(5)具有特殊气味,常作萃取剂的有机物在铁作催化剂的条件下与液溴发生一溴代反应的化学方程式为_____。
(6)有机物②在Cu作催化剂,加热条件下与O2反应的化学方程式为____。
(7)在120℃,1.01×105Pa条件下,某种气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃是____(填序号)。
(8)有机物⑤和②在一定条件下发生反应的化学方程式是_____。
16.I.已知乳酸的结构简式为,试回答下列问题:
(1)乳酸分子中含有_______和_______(写名称)两种官能团
(2)乳酸与足量金属钠反应的化学方程式为_______;
(3)足量乳酸与Na2CO3反应的化学方程式为_______
(4)乳酸的某些化学性质与乙醇相似,如在催化剂、加热的条件下可被氧气氧化,该反应的化学方程式为_______。
(5)在一定条件下,两分子乳酸之间可以反应生成含三种不同官能团的有机化合物A(C6H10O5),该反应的反应类型是_______,A的结构简式为_______。
Ⅱ.0.2mol某烃A在氧气中充分燃烧后,生成化合物B、C各1.2mol。请回答下列问题:
(6)烃A的分子式为_______。
(7)若烃A不能使溴水褪色,但在一定条件下,能与氯气发生取代反应,其一氯代物只有一种,则烃A的结构简式为_______。
(8)若烃A可与HBr加成,与HBr加成后只能得到一种产物,且烃A的一氯代物只有一种。A的结构简式为_______。
17.I.写出下列物质的分子式:
(1)_______;
(2)_______;
(3)_______;
II.某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%。
(4)A的分子式为_______。
(5)A与溴的四氯化碳溶液反应的化学方程式为_______,反应类型是_______。
18.按要求回答下列问题:
(1)有机物 的系统命名法名称为_______。
(2)实验室制乙炔的化学方程式为_______,反应产生的气体需先通过溶液,目的是为了除去气体中的等杂质,写出与溶液反应的离子方程式_______。制乙炔需用到电石,其主要成分是一种离子化合物,各原子均满足8电子稳定结构。写出的电子式_______。
(3)某链状烷烃的相对分子质量为114,其一氯代物只有一种,该烷烃的结构简式为_______。
(4) 中含氧官能团的名称为_______。
(5)_______(填“是”或“否”)存在顺反异构,1mol该有机物最多能与_______molH2加成。
19.按照要求回答下列问题:
(1)有机物命名_______(系统命名法)
(2)下列几组物质中,互为同分异构体的是_______(填字母,下同);互为同系物的是_______;
A.甲烷与新戊烷 B.氧气和臭氧 C.和 D.和 E.CH3CH2OH和CH3OCH3
(3)乙炔的实验室制法的化学方程式为_______。
(4)乙醇发生催化氧化反应的化学方程式为_______。
(5)2-氯丙烷发生消去反应的化学方程式为_______。
(6)甲醛发生银镜反应的化学方程式为_______。
三、有机推断题
20.某芳香烃A(相对分子质量为78)是一种重要的有机化工原料,以它为初始原料经过如下转化关系图(部分产物和反应条件略去)可以合成阿司匹林(乙酰水杨酸)。
已知:Ⅰ.
Ⅱ.
回答下列问题:
(1)条件X是_______;反应⑤的反应类型是_______。
(2)水杨酸中官能团的名称是_______。
(3)阿司匹林与足量溶液反应的化学方程式为_______。
(4)阿司匹林有多种同分异构体,满足下列条件的同分异构体有_______种;其中核磁共振氢谱有四组峰,且峰面积之比为的结构简式为_______。
①含有苯环;
②既不能发生水解反应,也不能发生银镜反应;
③该有机物能与完全反应。
21.是一种重要的化工原料,可以合成各种有机化工产品。苯在一定条件下有如图转化关系,请按要求回答下列问题。
(1)E中官能团的名称是_______,高聚物D的结构简式为_______。
(2)C→E的反应条件是_______,F→G反应的类型是_______。
(3)E物质苯环上的一氯代物共有_______种。
(4)B物质分子中最多有_______个原子共平面。
(5)写出F→G的化学方程式_______。
22.以甲苯为主要原料,采取以下路线合成某药物中间体。
已知:
回答下列问题:
(1)生成A的化学方程式为:___________。
(2)C的化学式为:___________;的反应类型是___________。
(3)B的学名为氯硝基甲苯,反应过程中会产生一种学名为氯硝基甲苯的副产物,其结构简式为:___________。
(4)物质D中含氧官能团有___________;D在水中的溶解度大于B的原因是___________。
(5)E既可以和溶液反应又可以和盐酸反应,写出E与盐酸反应的化学方程式为:___________。
试卷第1页,共3页
参考答案:
1.C
【详解】A.分子中含有酚羟基,置于空气中易被氧化,A正确;
B.分子中含有酚羟基,与FeCl3溶液发生显色反应,B正确;
C.分子含有苯环和羟基、酯基,均不能与饱和溴水发生加成反应,C错误;
D.苯环为平面结构,与苯环直接相连的原子共平面,D正确;
故选C。
2.C
【详解】A.乙烯基环己烷中含有饱和碳原子,与饱和碳原子直接相连的四个原子形成四面体结构,故乙烯基环己烷中所有原子不能共平面,A项不符合题意;
B.苯环为平面结构,乙炔为直线形结构,苯乙炔可看作是苯环取代乙炔上的一个氢,故所有原子(14个)共平面;
C.苯环和羧基均为平面结构,单键可以旋转,故苯甲酸分子中所有原子(15个)可能共平面;
D.丙烯醇()分子中含有饱和碳原子,所有原子不可能共平面,D项不符合题意;
综上, C项符合题意;选C。
3.B
【详解】A. 甲酸甲酯水解得到甲酸和甲醇,相对分子质量前者为46、后者为32,A不符合;
B. 甲酸乙酯水解得到甲酸和乙醇,相对分子质量前者为46、后者为46,B符合;
C. 乙酸甲酯水解得到乙酸和甲醇,相对分子质量前者为60、后者为32,C不符合;
D. 乙酸乙酯水解得到甲酸和乙醇,相对分子质量前者为60、后者为46,D不符合;
答案选B。
4.D
【详解】A.纯碱是碳酸钠,水解成碱性,油脂为酯类,碱性条件下会水解成溶于水的甘油和脂肪酸钠,所以碳酸钠可以用于清洗餐具油污,A正确;
B.玉米淀粉和废弃秸秆均可水解产生葡萄糖,在微生物发酵作用下可产生乙醇,B正确;
C.珠江三角洲的形成与胶体的聚沉有关,C正确;
D.84消毒液具有漂白性,会使衣物漂白,D错误;
答案选D。
5.C
【详解】A.题干给出了主要反应,[Rh(CO)2I2]-为催化剂,A正确;
B.根据图示反应可知,⑤为,与水的反应为取代反应,B正确;
C.该反应过程中在②转化为③中形成了碳碳键,存在非极性键的形成,C错误;
D.从图中可看出在反应过程中Rh的配位数有4,有6,D正确;
故选C。
6.D
【详解】A.若X是金属单质,则该金属元素不一定位于周期表的d区或ds区,可以是Na,4Na+O2=2Na2O,2Na2O+O22Na2O2,2Na+O22Na2O2,Na是s区元素,A不合题意;
B.若X是乙醇、Y是乙醛,2CH3CH2OH+O22CH3CHO+2H2O,但Z不一定是乙酸CO2,B不合题意;
C.已知2H2S+O22H2O+S,S+O2SO2,2SO2+O22SO3,但H2S与O2不能直接反应得到SO3,即Y不可能是有漂白性的无色气体SO2,H2S可以直接燃烧生成SO2,则若X是H2S,则Y是黄色固体S,Z是有漂白性的无色气体SO2,C不合题意;
D.若X是NH3,则Z可以是无色气体NO,转化过程为:4NH3+3O22N2+6H2O,N2+O22NO,4NH3+5O24NO+6H2O,D符合题意;
故答案为:D。
7.A
【详解】标准状况下4.48LCO2的物质的量为=0.2mol,根据甲醇、乙二醇和丙三醇的分子式可知,含有的碳原子与羟基的个数相等,因此取等质量的两份由甲醇、乙二醇中含有羟基0.2mol,已知:2-OH~H2,则生成氢气0.1 mol,标准状况下的体积为2.24L。
故选A。
8.C
【分析】实验室用环己醇和浓硫酸加热反应生成环己烯,a中为环己醇和浓硫酸的混合液,通过c处的温度计控制馏出物的温度不超过90℃,b中通入冷却水起到冷凝作用,最后产物收集在锥形瓶中。
【详解】A.由于浓硫酸稀释放热,因此反应物加入顺序:先加入环己醇和碎瓷片,然后在冷却搅动下缓慢加入浓硫酸,A正确;
B.加入碎瓷片的作用是防止有机物在加热时发生暴沸,如果在加热时发现忘记加碎瓷片,这时必须停止加热,待冷却后补加碎瓷片,B正确;
C.环己烯密度比水小,位于上层,应从分液漏斗上口倒出,C错误;
D.粗产物干燥后,环己烯中溶有环己醇,用蒸馏进行分离,根据沸点差别,可知在收集83℃左右的馏分,D正确;
故选C。
9.C
【详解】A.漂粉精中含有的Ca(ClO)2具有强氧化性,能杀菌消毒,可用于游泳池的消毒,A正确;
B.碳酸氢钠受热分解放出的二氧化碳气体包在面团中,能使面团体积膨胀,可做食品膨松剂,B正确;
C.青铜是铜锡等的合金,黄铜是铜锌等的合金,它们都是铜的混合物,C不正确;
D.金属氧化物可使玻璃呈现不同颜色,如Cu2O使玻璃显红色,Co2O3使玻璃显蓝色,D正确;
故选C。
10.C
【详解】A.1mol与足量的充分反应是过氧化钠自身的歧化,氧气中的氧元素来自过氧化钠,未标记,A错误;
B.100g46%乙醇溶液中乙醇有=1mol,水有=3mol, 1mol乙醇含有1mol O—H键,3mol水含有6mol的O—H键,故总的含有O—H键的数目为7,B错误;
C.氧元素守恒,故标准状况下,11.2LNO和11.2L混合气体充入密闭容器,所含氧原子数等于=1.5mol,C正确;
D.固体中一个硫酸氢钠有一个钠离子和一个硫酸氢根离子,故12g固体即0.1mol硫酸氢钠中含离子数为0.2NA,D错误;
故选C。
11.A
【详解】A.X水解生成的碳酸、酚羟基、HBr都能与NaOH反应,碳酸和NaOH最多以1:2反应、HBr和NaOH以1:1反应、酚羟基和NaOH以1:1反应,则1molX与足量NaOH溶液充分反应,最多可消耗4molNaOH,A正确;
B.X中醛基能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色、能被溴水氧化而使溴水褪色,B错误;
C.X与足量加成后所得有机物分子中手性碳原子如图,手性碳原子有4个,C错误;
D.苯并唑酮C7H5O2N,C元素被氧化生成CO2、H元素被氧化生成H2O,如果N元素转化为N2,需氧量最少,可以改写为,则1mol苯并唑酮完全燃烧需要消耗氧气最少为,D错误;
故选A。
12.C
【详解】A.分析阿比朵尔的结构简式可知,其能与NaOH反应的官能团有酚羟基、酯基和碳溴键,但碳溴键水解后生成的是酚羟基,所以1mol阿比朵尔最多可与4mol NaOH发生反应,选项A错误;
B.1mol阿比朵尔最多可与7 mol H2发生加成反应,酯基不与H2发生加成反应,选项B错误;
C.阿比朵尔分子中不存在手性碳原子,不是手性分子,选项C正确;
D.阿比朵尔分子O原子存在单键和双键,杂化方式有两种,选项D错误;
答案选C。
13.B
【详解】A.核酸和蛋白质都是生物大分子,A正确;
B.蛋白质能水解为氨基酸,核酸可在稀盐酸中逐步水解为磷酸、戊糖和碱基,B错误;
C.核酸是由核苷酸之间通过磷酯键连接,C正确;
D.含氯消毒液的强氧化性可使蛋白质变性,D错误;
故答案选B。
14.CD
【详解】A. 乙烯分子式C2H4,各原子的最简单的整数比为实验式,其实验式为CH2,故A错误;
B. 乙酸甲酯由乙酸和甲醇发生酯化反应得到,结构简式为:CH3COOCH3,故B错误;
C. 2-甲基丁烷的结构简式为:(CH3)2CHCH2-CH3,去掉C原子和氢原子得出键线式为:,故C正确;
D. 羟基不带电,O原子与H原子形成一对共用电子对,O原子周围共7个电子,电子式:,故D正确;
故选CD。
15.(1)CH3CH2CH3
(2)C6H14
(3)⑦
(4)2
(5)+Br2+HBr
(6)2CH3CH2OH+O22CH3CHO+2H2O
(7)①
(8)CH3COOH+HOC2H5CH3COOC2H5+H2O
【详解】(1)依据烷烃的通式CnH2n+2,12n+2n+2=44,解得n=3,即此烷烃为C3H8,结构简式为CH3CH2CH3。
(2)烷烃分子中含有14个氢原子,依据烷烃的通式CnH2n+2,因此有2n+2=14,即n=6,此的分子式是C6H14。
(3)③为2,2-二甲基丁烷、含有6个碳原子,14氢原子,根据同分异构体的定义,与③互为同分异构体的是⑦。
(4)⑦的同分异构体(包括⑦)有CH3CH2CH2CH2CH2CH3(有3种不同的氢原子,一氯代物有3种);(CH3)2CHCH2CH2CH3有5种不同的氢原子,一氯代物有5种;CH3CH2CH(CH3)CH2CH3有4种不同的氢原子,一氯代物有4种;(CH3)2CHCH(CH3)2有2种不同的氢原子,一氯代物有2种;(CH3)3CCH2CH3有3种不同的氢原子,一氯代物有3种,符合题意的有2种。
(5)具有特殊气味,常作萃取剂的有机物在铁作催化剂的条件下与液溴发生一溴代反应,此有机物是苯,化学方程式为+Br2 +HBr。
(6)有机物②在Cu作催化剂,加热条件下与O2反应,即乙醇被氧气催化氧化生成乙醛和水,其化学方程式为2CH3CH2OH+O22CH3CHO+2H2O。
(7)120℃时,某烃为CxHy,燃烧的方程式为CxHy(g)+(x+)O2(g)→xCO2(g)+H2O(g),反应前后气体的体积没有发生改变,则1+x+=x+,解得y=4,根据给定的物质,甲烷符合,则该烃是①。
(8)有机物⑤和②为乙酸与乙醇,其在浓硫酸加热的条件下发生取代反应生成乙酸乙酯和水,化学方程式是CH3COOH+HOC2H5CH3COOC2H5+H2O。
16.(1) 羟基 羧基
(2)+2Na→+H2↑
(3)2+Na2CO3→2+H2O+CO2↑
(4)2+O22CH3COCOOH+2H2O
(5) 酯化(取代)反应
(6)C6H12
(7)
(8)(CH3)2C=C(CH3)2
【解析】(1)
根据乳酸分子的结构简式可知,其中含有的官能团为:羟基和羧基;
(2)
乳酸分子中的羟基和羧基都可以和金属钠反应生成氢气,方程式为:+2Na→+H2↑;
(3)
乳酸中含有羧基,可与Na2CO3反应生成水和二氧化碳,反应的方程式为2+Na2CO3→2+H2O+CO2↑;
(4)
乳酸分子中羟基连接的C原子上有H原子,因此能够发生催化氧化反应,羟基被氧化变为羰基,反应化学方程式为:2+O22CH3COCOOH+2H2O;
(5)
乳酸分子中既含有羟基又含有羧基,两分子乳酸通过酯化(取代)反应生成乳酸酯,消耗了一个羧基和醇羟基,多了1个酯基官能团,脱水时羧基脱去羟基,醇羟基脱去l个H原子形成酯基,脱去的H原子与—OH结合形成H2O,反应的化学方程式为:CH3CHOHCOOH+CH3CHOHCOOH+H2O,故答案为:酯化(取代)反应;;
(6)
烃为只含有C、H两种元素的有机物,0.2mol烃A在氧气中完全燃烧生成的产物为水和二氧化碳,且物质的量均为1.2mol,则1mol烃A生成6mol二氧化碳和6mol水,故A的化学式为C6H12;
(7)
烃A不能使溴水褪色,其不饱和度为1,则含有1个环,且一氯代物只有一种,则烃A为环己烷,结构简式为;
(8)
烃A可与HBr加成,则A含有碳碳双键,其与HBr加成后只能得到一种产物,且烃A的一氯代物只有一种,其为对称结构,含有4个等效的甲基,结构简式为(CH3)2C=C(CH3)2。
17.(1)
(2)
(3)
(4)
(5) 加成反应
【解析】(1)
根据键线式可得,分子式为;
(2)
根据键线式可得,分子式为;
(3)
根据键线式可得,分子式为;
(4)
化合物A含苯环,其相对分子质量为104,其中碳的质量分数为92.3%,碳原子个数:,C原子为8个,氢原子个数:
所以化合物A的分子式为;
(5)
A含有苯环,且能与溴的四氯化碳溶液反应,说明A为苯乙烯,与溴的四氯化碳溶液发生加成反应:。
18.(1)4—甲基—3—乙基—2,5—庚二烯
(2)
(3)
(4)羟基、酯基、醛基
(5) 是 6
【解析】(1)由结构简式可知, 属于二烯烃,分子中含有碳碳双键的最长碳链含有7个碳原子,侧链为甲基和乙基,名称为4—甲基—3—乙基—2,5—庚二烯,故答案为:4—甲基—3—乙基—2,5—庚二烯;
(2)实验室制乙炔的反应为碳化钙与水反应生成氢氧化钙和乙炔,反应的化学方程式为;乙炔气体中混有的硫化氢与硫酸铜溶液反应生成硫化铜沉淀和稀硫酸,反应的离子方程式为;碳化钙是离子化合物,电子式为 ,故答案为:;; ;
(3)设烷烃的分子式为CnH2n+2,由烷烃的相对分子质量为114可得:14n+2=114,解得n=8,一氯代物只有一种辛烷的结构简式为 ,故答案为: ;
(4)由结构简式可知, 分子含有的官能团为羟基、酯基、醛基,故答案为:羟基、酯基、醛基;
(5)由结构简式可知, 分子中碳碳双键的两个碳原子上连有两个不同的原子或原子团,存在顺反异构,分子中含有的苯环、碳碳双键、碳碳三键一定条件下能与氢气发生加成反应,则1mol最多能与6mol氢气发生加成反应,故答案为:6。
19.(1)2,3-二甲基戊烷
(2) E A
(3)CaC2+2H2O→Ca(OH)2+CH≡CH↑
(4)2CH3CH2OH+O22CH3CHO+2H2O
(5)
(6)
【解析】(1)
分子中最长碳链上含有5个C原子,从离支链较近的右端为起点,给主链上的C原子编号,以确定支链连接在主链上的位置,该物质名称为2,3-二甲基戊烷;
(2)
E.CH3CH2OH和CH3OCH3分子式都是C2H6O,结构不同,因此二者属于同分异构体,故属于同分异构体的物质序号是E;
A.甲烷与新戊烷分子式都符合通式CnH2n+2,结构相似,在分子组成上相差4个CH2原子团,二者互为同系物,故属于同系物的物质序号是A;
(3)
在实验室中是用电石与水反应制取乙炔气体,反应方程式为:CaC2+2H2O→Ca(OH)2+CH≡CH↑;
(4)
乙醇与O2在Cu作催化剂存在条件下加热,发生氧化反应产生乙醛CH3CHO和H2O,该反应的化学方程式为:2CH3CH2OH+O22CH3CHO+2H2O;
(5)
2-氯丙烷与NaOH的乙醇溶液共热,发生消去反应产生丙烯、NaCl、H2O,该反应的化学方程式为:;
(6)
甲醛分子中含有2个-CHO,能够与银氨溶液水浴加热发生银镜反应产生(NH4)2CO3、Ag、NH3、H2O,该反应的化学方程式为。
20.(1) (或) 取代反应(或酯化反应)
(2)羧基、(酚)羟基
(3)
(4) 10 、
【分析】芳香烃A(相对分子质量为78)说明含有苯环,由,分子式为C6H6,A为,苯和氯气在铁或氯化铁做催化剂下反应生成B为,其中一个-Cl发生已知反应I生成-ONa,另一个发生水解反应生成-OH,则C为, 酸化后得到水杨酸即,再发生已知信息II反应生成;
【详解】(1)由分析可知,A为,苯和氯气在铁或氯化铁做催化剂下反应生成B为,条件X是(或);水杨酸即,与乙酸发生酯化反应生成阿司匹林,则反应⑤的反应类型是取代反应(或酯化反应);
(2)水杨酸即,水杨酸中官能团的名称是羧基、(酚)羟基;
(3)阿司匹林中酯基与足量溶液发生水解反应,反应的化学方程式为;
(4)阿司匹林满足条件:①含有苯环;②既不能发生水解反应,也不能发生银镜反应,说明不能含有酯基和醛基;③该有机物能与完全反应,说明含有2个羧基,同分异构体有、、、、共10种;其中核磁共振氢谱有四组峰,且峰面积之比为的结构简式为、。
21.(1) 硝基
(2) 浓硝酸、浓硫酸、加热 氧化反应
(3)4
(4)16
(5)
【分析】苯与乙炔发生加成反应得到B:苯乙烯,苯乙烯发生加聚反应得到高聚物D:聚苯乙烯,B与氢气发生加成反应得到C:苯乙烷,苯乙烷发生硝化反应得到E;根据G可知苯乙烯与水发生加成反应得到F:。
【详解】(1)E中的官能团为:硝基;高聚物D为聚苯乙烯,结构简式为:;
(2)苯乙烷发生硝化反应得到E,反应条件为:浓硝酸、浓硫酸、加热;F为,F到G羟基被氧化为醛基,反应类型为:氧化反应;
(3)E中苯环上的氢原子化学环境均不同,有4种不同化学环境的氢原子,故E苯环上的一氯代物有4种;
(4)苯环和双键均为平面构型,两者之间通过单键相连,所有的原子均可能共平面,故B最多有16个原子共平面;
(5)F到G羟基被氧化为醛基,化学方程式为:。
22.(1)+HCl
(2) 还原反应
(3)
(4) D中含有羟基,容易与水形成氢键
(5)+HCl→
【分析】甲苯与氯气在氯化铁做催化剂的条件下生成A,在浓硫酸与浓硝酸的条件下生成B:;水解生成,与HCl反应生成,发生还原反应生成,据此分析解题。
(1)
生成A的化学方程式为:+HCl;
(2)
C的化学式为:;的反应类型是还原反应;
(3)
氯硝基甲苯结构简式为:;
(4)
物质D的结构简式为:,含氧官能团有羟基、硝基;D在水中的溶解度大于B的原因是因为D中含有羟基,容易与水形成氢键;
(5)
E与盐酸反应的化学方程式为:+HCl→;
答案第1页,共2页
答案第1页,共2页
一、选择题
1.莲藕中某多酚类物质的结构简式如图所示(R为烃基)。下列说法不正确的是
A.置于空气中易被氧化 B.能与FeCl3溶液发生显色反应
C.能与饱和溴水发生加成反应 D.与苯环直接相连的原子共平面
2.下列化合物的分子中,所有原子可能共平面且共平面原子数最多的是
A.乙烯基环己烷 B.苯乙炔 C.苯甲酸 D.丙烯醇
3.1mol有机羧酸酯A在酸性条件下完全水解能得到相对分子质量相同的两种物质,则A是
A.甲酸甲酯 B.甲酸乙酯 C.乙酸甲酯 D.乙酸乙酯
4.化学与生活密切相关。下列叙述错误的是
A.纯碱溶液可以用于清洗餐具油污
B.玉米淀粉和废弃秸秆可生产乙醇
C.珠江三角洲的形成与胶体聚沉有关
D.“84消毒液”可以喷洒于衣物上进行杀菌消毒
5.目前工业上多采用甲醇和一氧化碳反应制备醋酸:,反应过程如图所示,下列有关说法中错误的是
A.为催化剂 B.⑤与水的反应为取代反应
C.该反应过程中不存在非极性键的形成 D.在反应过程中Rh的配位数发生改变
6.某些物质之间可以在一定条件下进行如下转化,下列说法正确的是
A.若X是金属单质,则该金属元素一定位于周期表的d区或ds区
B.若X是乙醇、Y是乙醛,则Z一定是乙酸
C.若X是H2S,则Y既可以是黄色固体,也可以是有漂白性的无色气体
D.若X是NH3,则Z可以是无色气体NO
7.取等质量的两份由甲醇、乙二醇和丙三醇组成的混合物,一份完全燃烧生成(标准状况),另一份与足量的金属钠反应生成的体积(标准状况)为
A. B. C. D.无法计算
8.醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图所示:
+H2O
可能用到的有关数据如下表所示:
相对分子质量 密度/g cm-3 沸点/℃ 溶解性
环己醇 100 0.9618 161 微溶于水
环己烯 82 0.8102 83 难溶于水
下列说法错误的是A.在a中加入反应物的顺序为:先加环己醇和碎瓷片,然后在冷却搅动下慢慢加入浓硫酸
B.如果加热一段时间后发现忘记加碎瓷片,正确操作是冷却后补加
C.将产物倒入分液漏斗中,分别用少量5%碳酸钠溶液和水洗涤,洗涤后的产物应从分液漏斗下口流出
D.在洗涤、分液后所得产物中,加入无水氯化钙干燥、蒸馏,收集83℃左右的馏分即得环己烯
9.生活中处处有化学,下列叙述不正确的是
A.漂粉精可用于游泳池的消毒 B.碳酸氢钠可做食品膨松剂
C.青铜和黄铜是不同结构的单质铜 D.金属氧化物可使玻璃呈现不同颜色
10.设为阿伏伽德罗常数的值,下列有关叙述正确的是
A.1mol与足量的充分反应,得到
B.100g46%乙醇溶液中所含O—H键的数目为
C.标准状况下,11.2LNO和11.2L混合气体充入密闭容器,所含氧原子数等于1.5
D.12g固体中含离子数为0.3
11.已知苯并唑酮()可转化为X(),下列说法正确的是
A.1molX与足量NaOH溶液充分反应,最多可消耗4molNaOH
B.X能使酸性高锰酸钾溶液褪色,但不能使溴水褪色
C.X与足量加成后所得有机物分子中手性碳原子数目为3个
D.1mol苯并唑酮完全燃烧需要消耗6.25mol氧气
12.2020年,“新冠”席卷全球,给各个国家造成了极大的危害。阿比朵尔是治疗“新冠”疾病的一种药物,其结构简式如图所示。下列有关说法正确的是
A.1mol阿比朵尔最多可与3mol NaOH发生反应
B.1mol阿比朵尔最多可与8 mol H2发生加成反应
C.阿比朵尔不是手性分子
D.阿比朵尔分子O原子的杂化方式只有一种
13.新冠病毒是一种具有包膜的RNA病毒,包膜的主要成分是蛋白质和脂质。核酸检测就是检测新冠病毒的RNA。下列说法不正确的是
A.核酸和蛋白质都是生物大分子
B.蛋白质能发生水解反应,而核酸不能发生水解反应
C.核酸中核苷酸之间通过磷酯键连接
D.一定浓度的含氯消毒液可使新冠病毒中的蛋白质变性
14.下列表示正确的是
A.乙烯的实验式:C2H4 B.乙酸甲酯的结构简式:HCOOCH2CH3
C.2-甲基丁烷的键线式: D.羟基的电子式:
二、填空题
15.现有以下几种有机物:
①CH4②CH3CH2OH ③ ④癸烷 ⑤CH3COOH ⑥⑦ ⑧ ⑨丙烷
请利用上述给出的物质按要求回答下列问题:
(1)相对分子质量为44的烷烃结构简式为_____。
(2)分子中含有14个氢原子的烷烃的分子式是____。
(3)与③互为同分异构体的是_____(填序号)。
(4)⑦的所有同分异构体(不考虑空间异构)中一氯代物有3种的有_____种。
(5)具有特殊气味,常作萃取剂的有机物在铁作催化剂的条件下与液溴发生一溴代反应的化学方程式为_____。
(6)有机物②在Cu作催化剂,加热条件下与O2反应的化学方程式为____。
(7)在120℃,1.01×105Pa条件下,某种气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃是____(填序号)。
(8)有机物⑤和②在一定条件下发生反应的化学方程式是_____。
16.I.已知乳酸的结构简式为,试回答下列问题:
(1)乳酸分子中含有_______和_______(写名称)两种官能团
(2)乳酸与足量金属钠反应的化学方程式为_______;
(3)足量乳酸与Na2CO3反应的化学方程式为_______
(4)乳酸的某些化学性质与乙醇相似,如在催化剂、加热的条件下可被氧气氧化,该反应的化学方程式为_______。
(5)在一定条件下,两分子乳酸之间可以反应生成含三种不同官能团的有机化合物A(C6H10O5),该反应的反应类型是_______,A的结构简式为_______。
Ⅱ.0.2mol某烃A在氧气中充分燃烧后,生成化合物B、C各1.2mol。请回答下列问题:
(6)烃A的分子式为_______。
(7)若烃A不能使溴水褪色,但在一定条件下,能与氯气发生取代反应,其一氯代物只有一种,则烃A的结构简式为_______。
(8)若烃A可与HBr加成,与HBr加成后只能得到一种产物,且烃A的一氯代物只有一种。A的结构简式为_______。
17.I.写出下列物质的分子式:
(1)_______;
(2)_______;
(3)_______;
II.某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%。
(4)A的分子式为_______。
(5)A与溴的四氯化碳溶液反应的化学方程式为_______,反应类型是_______。
18.按要求回答下列问题:
(1)有机物 的系统命名法名称为_______。
(2)实验室制乙炔的化学方程式为_______,反应产生的气体需先通过溶液,目的是为了除去气体中的等杂质,写出与溶液反应的离子方程式_______。制乙炔需用到电石,其主要成分是一种离子化合物,各原子均满足8电子稳定结构。写出的电子式_______。
(3)某链状烷烃的相对分子质量为114,其一氯代物只有一种,该烷烃的结构简式为_______。
(4) 中含氧官能团的名称为_______。
(5)_______(填“是”或“否”)存在顺反异构,1mol该有机物最多能与_______molH2加成。
19.按照要求回答下列问题:
(1)有机物命名_______(系统命名法)
(2)下列几组物质中,互为同分异构体的是_______(填字母,下同);互为同系物的是_______;
A.甲烷与新戊烷 B.氧气和臭氧 C.和 D.和 E.CH3CH2OH和CH3OCH3
(3)乙炔的实验室制法的化学方程式为_______。
(4)乙醇发生催化氧化反应的化学方程式为_______。
(5)2-氯丙烷发生消去反应的化学方程式为_______。
(6)甲醛发生银镜反应的化学方程式为_______。
三、有机推断题
20.某芳香烃A(相对分子质量为78)是一种重要的有机化工原料,以它为初始原料经过如下转化关系图(部分产物和反应条件略去)可以合成阿司匹林(乙酰水杨酸)。
已知:Ⅰ.
Ⅱ.
回答下列问题:
(1)条件X是_______;反应⑤的反应类型是_______。
(2)水杨酸中官能团的名称是_______。
(3)阿司匹林与足量溶液反应的化学方程式为_______。
(4)阿司匹林有多种同分异构体,满足下列条件的同分异构体有_______种;其中核磁共振氢谱有四组峰,且峰面积之比为的结构简式为_______。
①含有苯环;
②既不能发生水解反应,也不能发生银镜反应;
③该有机物能与完全反应。
21.是一种重要的化工原料,可以合成各种有机化工产品。苯在一定条件下有如图转化关系,请按要求回答下列问题。
(1)E中官能团的名称是_______,高聚物D的结构简式为_______。
(2)C→E的反应条件是_______,F→G反应的类型是_______。
(3)E物质苯环上的一氯代物共有_______种。
(4)B物质分子中最多有_______个原子共平面。
(5)写出F→G的化学方程式_______。
22.以甲苯为主要原料,采取以下路线合成某药物中间体。
已知:
回答下列问题:
(1)生成A的化学方程式为:___________。
(2)C的化学式为:___________;的反应类型是___________。
(3)B的学名为氯硝基甲苯,反应过程中会产生一种学名为氯硝基甲苯的副产物,其结构简式为:___________。
(4)物质D中含氧官能团有___________;D在水中的溶解度大于B的原因是___________。
(5)E既可以和溶液反应又可以和盐酸反应,写出E与盐酸反应的化学方程式为:___________。
试卷第1页,共3页
参考答案:
1.C
【详解】A.分子中含有酚羟基,置于空气中易被氧化,A正确;
B.分子中含有酚羟基,与FeCl3溶液发生显色反应,B正确;
C.分子含有苯环和羟基、酯基,均不能与饱和溴水发生加成反应,C错误;
D.苯环为平面结构,与苯环直接相连的原子共平面,D正确;
故选C。
2.C
【详解】A.乙烯基环己烷中含有饱和碳原子,与饱和碳原子直接相连的四个原子形成四面体结构,故乙烯基环己烷中所有原子不能共平面,A项不符合题意;
B.苯环为平面结构,乙炔为直线形结构,苯乙炔可看作是苯环取代乙炔上的一个氢,故所有原子(14个)共平面;
C.苯环和羧基均为平面结构,单键可以旋转,故苯甲酸分子中所有原子(15个)可能共平面;
D.丙烯醇()分子中含有饱和碳原子,所有原子不可能共平面,D项不符合题意;
综上, C项符合题意;选C。
3.B
【详解】A. 甲酸甲酯水解得到甲酸和甲醇,相对分子质量前者为46、后者为32,A不符合;
B. 甲酸乙酯水解得到甲酸和乙醇,相对分子质量前者为46、后者为46,B符合;
C. 乙酸甲酯水解得到乙酸和甲醇,相对分子质量前者为60、后者为32,C不符合;
D. 乙酸乙酯水解得到甲酸和乙醇,相对分子质量前者为60、后者为46,D不符合;
答案选B。
4.D
【详解】A.纯碱是碳酸钠,水解成碱性,油脂为酯类,碱性条件下会水解成溶于水的甘油和脂肪酸钠,所以碳酸钠可以用于清洗餐具油污,A正确;
B.玉米淀粉和废弃秸秆均可水解产生葡萄糖,在微生物发酵作用下可产生乙醇,B正确;
C.珠江三角洲的形成与胶体的聚沉有关,C正确;
D.84消毒液具有漂白性,会使衣物漂白,D错误;
答案选D。
5.C
【详解】A.题干给出了主要反应,[Rh(CO)2I2]-为催化剂,A正确;
B.根据图示反应可知,⑤为,与水的反应为取代反应,B正确;
C.该反应过程中在②转化为③中形成了碳碳键,存在非极性键的形成,C错误;
D.从图中可看出在反应过程中Rh的配位数有4,有6,D正确;
故选C。
6.D
【详解】A.若X是金属单质,则该金属元素不一定位于周期表的d区或ds区,可以是Na,4Na+O2=2Na2O,2Na2O+O22Na2O2,2Na+O22Na2O2,Na是s区元素,A不合题意;
B.若X是乙醇、Y是乙醛,2CH3CH2OH+O22CH3CHO+2H2O,但Z不一定是乙酸CO2,B不合题意;
C.已知2H2S+O22H2O+S,S+O2SO2,2SO2+O22SO3,但H2S与O2不能直接反应得到SO3,即Y不可能是有漂白性的无色气体SO2,H2S可以直接燃烧生成SO2,则若X是H2S,则Y是黄色固体S,Z是有漂白性的无色气体SO2,C不合题意;
D.若X是NH3,则Z可以是无色气体NO,转化过程为:4NH3+3O22N2+6H2O,N2+O22NO,4NH3+5O24NO+6H2O,D符合题意;
故答案为:D。
7.A
【详解】标准状况下4.48LCO2的物质的量为=0.2mol,根据甲醇、乙二醇和丙三醇的分子式可知,含有的碳原子与羟基的个数相等,因此取等质量的两份由甲醇、乙二醇中含有羟基0.2mol,已知:2-OH~H2,则生成氢气0.1 mol,标准状况下的体积为2.24L。
故选A。
8.C
【分析】实验室用环己醇和浓硫酸加热反应生成环己烯,a中为环己醇和浓硫酸的混合液,通过c处的温度计控制馏出物的温度不超过90℃,b中通入冷却水起到冷凝作用,最后产物收集在锥形瓶中。
【详解】A.由于浓硫酸稀释放热,因此反应物加入顺序:先加入环己醇和碎瓷片,然后在冷却搅动下缓慢加入浓硫酸,A正确;
B.加入碎瓷片的作用是防止有机物在加热时发生暴沸,如果在加热时发现忘记加碎瓷片,这时必须停止加热,待冷却后补加碎瓷片,B正确;
C.环己烯密度比水小,位于上层,应从分液漏斗上口倒出,C错误;
D.粗产物干燥后,环己烯中溶有环己醇,用蒸馏进行分离,根据沸点差别,可知在收集83℃左右的馏分,D正确;
故选C。
9.C
【详解】A.漂粉精中含有的Ca(ClO)2具有强氧化性,能杀菌消毒,可用于游泳池的消毒,A正确;
B.碳酸氢钠受热分解放出的二氧化碳气体包在面团中,能使面团体积膨胀,可做食品膨松剂,B正确;
C.青铜是铜锡等的合金,黄铜是铜锌等的合金,它们都是铜的混合物,C不正确;
D.金属氧化物可使玻璃呈现不同颜色,如Cu2O使玻璃显红色,Co2O3使玻璃显蓝色,D正确;
故选C。
10.C
【详解】A.1mol与足量的充分反应是过氧化钠自身的歧化,氧气中的氧元素来自过氧化钠,未标记,A错误;
B.100g46%乙醇溶液中乙醇有=1mol,水有=3mol, 1mol乙醇含有1mol O—H键,3mol水含有6mol的O—H键,故总的含有O—H键的数目为7,B错误;
C.氧元素守恒,故标准状况下,11.2LNO和11.2L混合气体充入密闭容器,所含氧原子数等于=1.5mol,C正确;
D.固体中一个硫酸氢钠有一个钠离子和一个硫酸氢根离子,故12g固体即0.1mol硫酸氢钠中含离子数为0.2NA,D错误;
故选C。
11.A
【详解】A.X水解生成的碳酸、酚羟基、HBr都能与NaOH反应,碳酸和NaOH最多以1:2反应、HBr和NaOH以1:1反应、酚羟基和NaOH以1:1反应,则1molX与足量NaOH溶液充分反应,最多可消耗4molNaOH,A正确;
B.X中醛基能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色、能被溴水氧化而使溴水褪色,B错误;
C.X与足量加成后所得有机物分子中手性碳原子如图,手性碳原子有4个,C错误;
D.苯并唑酮C7H5O2N,C元素被氧化生成CO2、H元素被氧化生成H2O,如果N元素转化为N2,需氧量最少,可以改写为,则1mol苯并唑酮完全燃烧需要消耗氧气最少为,D错误;
故选A。
12.C
【详解】A.分析阿比朵尔的结构简式可知,其能与NaOH反应的官能团有酚羟基、酯基和碳溴键,但碳溴键水解后生成的是酚羟基,所以1mol阿比朵尔最多可与4mol NaOH发生反应,选项A错误;
B.1mol阿比朵尔最多可与7 mol H2发生加成反应,酯基不与H2发生加成反应,选项B错误;
C.阿比朵尔分子中不存在手性碳原子,不是手性分子,选项C正确;
D.阿比朵尔分子O原子存在单键和双键,杂化方式有两种,选项D错误;
答案选C。
13.B
【详解】A.核酸和蛋白质都是生物大分子,A正确;
B.蛋白质能水解为氨基酸,核酸可在稀盐酸中逐步水解为磷酸、戊糖和碱基,B错误;
C.核酸是由核苷酸之间通过磷酯键连接,C正确;
D.含氯消毒液的强氧化性可使蛋白质变性,D错误;
故答案选B。
14.CD
【详解】A. 乙烯分子式C2H4,各原子的最简单的整数比为实验式,其实验式为CH2,故A错误;
B. 乙酸甲酯由乙酸和甲醇发生酯化反应得到,结构简式为:CH3COOCH3,故B错误;
C. 2-甲基丁烷的结构简式为:(CH3)2CHCH2-CH3,去掉C原子和氢原子得出键线式为:,故C正确;
D. 羟基不带电,O原子与H原子形成一对共用电子对,O原子周围共7个电子,电子式:,故D正确;
故选CD。
15.(1)CH3CH2CH3
(2)C6H14
(3)⑦
(4)2
(5)+Br2+HBr
(6)2CH3CH2OH+O22CH3CHO+2H2O
(7)①
(8)CH3COOH+HOC2H5CH3COOC2H5+H2O
【详解】(1)依据烷烃的通式CnH2n+2,12n+2n+2=44,解得n=3,即此烷烃为C3H8,结构简式为CH3CH2CH3。
(2)烷烃分子中含有14个氢原子,依据烷烃的通式CnH2n+2,因此有2n+2=14,即n=6,此的分子式是C6H14。
(3)③为2,2-二甲基丁烷、含有6个碳原子,14氢原子,根据同分异构体的定义,与③互为同分异构体的是⑦。
(4)⑦的同分异构体(包括⑦)有CH3CH2CH2CH2CH2CH3(有3种不同的氢原子,一氯代物有3种);(CH3)2CHCH2CH2CH3有5种不同的氢原子,一氯代物有5种;CH3CH2CH(CH3)CH2CH3有4种不同的氢原子,一氯代物有4种;(CH3)2CHCH(CH3)2有2种不同的氢原子,一氯代物有2种;(CH3)3CCH2CH3有3种不同的氢原子,一氯代物有3种,符合题意的有2种。
(5)具有特殊气味,常作萃取剂的有机物在铁作催化剂的条件下与液溴发生一溴代反应,此有机物是苯,化学方程式为+Br2 +HBr。
(6)有机物②在Cu作催化剂,加热条件下与O2反应,即乙醇被氧气催化氧化生成乙醛和水,其化学方程式为2CH3CH2OH+O22CH3CHO+2H2O。
(7)120℃时,某烃为CxHy,燃烧的方程式为CxHy(g)+(x+)O2(g)→xCO2(g)+H2O(g),反应前后气体的体积没有发生改变,则1+x+=x+,解得y=4,根据给定的物质,甲烷符合,则该烃是①。
(8)有机物⑤和②为乙酸与乙醇,其在浓硫酸加热的条件下发生取代反应生成乙酸乙酯和水,化学方程式是CH3COOH+HOC2H5CH3COOC2H5+H2O。
16.(1) 羟基 羧基
(2)+2Na→+H2↑
(3)2+Na2CO3→2+H2O+CO2↑
(4)2+O22CH3COCOOH+2H2O
(5) 酯化(取代)反应
(6)C6H12
(7)
(8)(CH3)2C=C(CH3)2
【解析】(1)
根据乳酸分子的结构简式可知,其中含有的官能团为:羟基和羧基;
(2)
乳酸分子中的羟基和羧基都可以和金属钠反应生成氢气,方程式为:+2Na→+H2↑;
(3)
乳酸中含有羧基,可与Na2CO3反应生成水和二氧化碳,反应的方程式为2+Na2CO3→2+H2O+CO2↑;
(4)
乳酸分子中羟基连接的C原子上有H原子,因此能够发生催化氧化反应,羟基被氧化变为羰基,反应化学方程式为:2+O22CH3COCOOH+2H2O;
(5)
乳酸分子中既含有羟基又含有羧基,两分子乳酸通过酯化(取代)反应生成乳酸酯,消耗了一个羧基和醇羟基,多了1个酯基官能团,脱水时羧基脱去羟基,醇羟基脱去l个H原子形成酯基,脱去的H原子与—OH结合形成H2O,反应的化学方程式为:CH3CHOHCOOH+CH3CHOHCOOH+H2O,故答案为:酯化(取代)反应;;
(6)
烃为只含有C、H两种元素的有机物,0.2mol烃A在氧气中完全燃烧生成的产物为水和二氧化碳,且物质的量均为1.2mol,则1mol烃A生成6mol二氧化碳和6mol水,故A的化学式为C6H12;
(7)
烃A不能使溴水褪色,其不饱和度为1,则含有1个环,且一氯代物只有一种,则烃A为环己烷,结构简式为;
(8)
烃A可与HBr加成,则A含有碳碳双键,其与HBr加成后只能得到一种产物,且烃A的一氯代物只有一种,其为对称结构,含有4个等效的甲基,结构简式为(CH3)2C=C(CH3)2。
17.(1)
(2)
(3)
(4)
(5) 加成反应
【解析】(1)
根据键线式可得,分子式为;
(2)
根据键线式可得,分子式为;
(3)
根据键线式可得,分子式为;
(4)
化合物A含苯环,其相对分子质量为104,其中碳的质量分数为92.3%,碳原子个数:,C原子为8个,氢原子个数:
所以化合物A的分子式为;
(5)
A含有苯环,且能与溴的四氯化碳溶液反应,说明A为苯乙烯,与溴的四氯化碳溶液发生加成反应:。
18.(1)4—甲基—3—乙基—2,5—庚二烯
(2)
(3)
(4)羟基、酯基、醛基
(5) 是 6
【解析】(1)由结构简式可知, 属于二烯烃,分子中含有碳碳双键的最长碳链含有7个碳原子,侧链为甲基和乙基,名称为4—甲基—3—乙基—2,5—庚二烯,故答案为:4—甲基—3—乙基—2,5—庚二烯;
(2)实验室制乙炔的反应为碳化钙与水反应生成氢氧化钙和乙炔,反应的化学方程式为;乙炔气体中混有的硫化氢与硫酸铜溶液反应生成硫化铜沉淀和稀硫酸,反应的离子方程式为;碳化钙是离子化合物,电子式为 ,故答案为:;; ;
(3)设烷烃的分子式为CnH2n+2,由烷烃的相对分子质量为114可得:14n+2=114,解得n=8,一氯代物只有一种辛烷的结构简式为 ,故答案为: ;
(4)由结构简式可知, 分子含有的官能团为羟基、酯基、醛基,故答案为:羟基、酯基、醛基;
(5)由结构简式可知, 分子中碳碳双键的两个碳原子上连有两个不同的原子或原子团,存在顺反异构,分子中含有的苯环、碳碳双键、碳碳三键一定条件下能与氢气发生加成反应,则1mol最多能与6mol氢气发生加成反应,故答案为:6。
19.(1)2,3-二甲基戊烷
(2) E A
(3)CaC2+2H2O→Ca(OH)2+CH≡CH↑
(4)2CH3CH2OH+O22CH3CHO+2H2O
(5)
(6)
【解析】(1)
分子中最长碳链上含有5个C原子,从离支链较近的右端为起点,给主链上的C原子编号,以确定支链连接在主链上的位置,该物质名称为2,3-二甲基戊烷;
(2)
E.CH3CH2OH和CH3OCH3分子式都是C2H6O,结构不同,因此二者属于同分异构体,故属于同分异构体的物质序号是E;
A.甲烷与新戊烷分子式都符合通式CnH2n+2,结构相似,在分子组成上相差4个CH2原子团,二者互为同系物,故属于同系物的物质序号是A;
(3)
在实验室中是用电石与水反应制取乙炔气体,反应方程式为:CaC2+2H2O→Ca(OH)2+CH≡CH↑;
(4)
乙醇与O2在Cu作催化剂存在条件下加热,发生氧化反应产生乙醛CH3CHO和H2O,该反应的化学方程式为:2CH3CH2OH+O22CH3CHO+2H2O;
(5)
2-氯丙烷与NaOH的乙醇溶液共热,发生消去反应产生丙烯、NaCl、H2O,该反应的化学方程式为:;
(6)
甲醛分子中含有2个-CHO,能够与银氨溶液水浴加热发生银镜反应产生(NH4)2CO3、Ag、NH3、H2O,该反应的化学方程式为。
20.(1) (或) 取代反应(或酯化反应)
(2)羧基、(酚)羟基
(3)
(4) 10 、
【分析】芳香烃A(相对分子质量为78)说明含有苯环,由,分子式为C6H6,A为,苯和氯气在铁或氯化铁做催化剂下反应生成B为,其中一个-Cl发生已知反应I生成-ONa,另一个发生水解反应生成-OH,则C为, 酸化后得到水杨酸即,再发生已知信息II反应生成;
【详解】(1)由分析可知,A为,苯和氯气在铁或氯化铁做催化剂下反应生成B为,条件X是(或);水杨酸即,与乙酸发生酯化反应生成阿司匹林,则反应⑤的反应类型是取代反应(或酯化反应);
(2)水杨酸即,水杨酸中官能团的名称是羧基、(酚)羟基;
(3)阿司匹林中酯基与足量溶液发生水解反应,反应的化学方程式为;
(4)阿司匹林满足条件:①含有苯环;②既不能发生水解反应,也不能发生银镜反应,说明不能含有酯基和醛基;③该有机物能与完全反应,说明含有2个羧基,同分异构体有、、、、共10种;其中核磁共振氢谱有四组峰,且峰面积之比为的结构简式为、。
21.(1) 硝基
(2) 浓硝酸、浓硫酸、加热 氧化反应
(3)4
(4)16
(5)
【分析】苯与乙炔发生加成反应得到B:苯乙烯,苯乙烯发生加聚反应得到高聚物D:聚苯乙烯,B与氢气发生加成反应得到C:苯乙烷,苯乙烷发生硝化反应得到E;根据G可知苯乙烯与水发生加成反应得到F:。
【详解】(1)E中的官能团为:硝基;高聚物D为聚苯乙烯,结构简式为:;
(2)苯乙烷发生硝化反应得到E,反应条件为:浓硝酸、浓硫酸、加热;F为,F到G羟基被氧化为醛基,反应类型为:氧化反应;
(3)E中苯环上的氢原子化学环境均不同,有4种不同化学环境的氢原子,故E苯环上的一氯代物有4种;
(4)苯环和双键均为平面构型,两者之间通过单键相连,所有的原子均可能共平面,故B最多有16个原子共平面;
(5)F到G羟基被氧化为醛基,化学方程式为:。
22.(1)+HCl
(2) 还原反应
(3)
(4) D中含有羟基,容易与水形成氢键
(5)+HCl→
【分析】甲苯与氯气在氯化铁做催化剂的条件下生成A,在浓硫酸与浓硝酸的条件下生成B:;水解生成,与HCl反应生成,发生还原反应生成,据此分析解题。
(1)
生成A的化学方程式为:+HCl;
(2)
C的化学式为:;的反应类型是还原反应;
(3)
氯硝基甲苯结构简式为:;
(4)
物质D的结构简式为:,含氧官能团有羟基、硝基;D在水中的溶解度大于B的原因是因为D中含有羟基,容易与水形成氢键;
(5)
E与盐酸反应的化学方程式为:+HCl→;
答案第1页,共2页
答案第1页,共2页
