第12章盐巩固 九年级化学京改版(2013)下册(有答案)
文档属性
| 名称 | 第12章盐巩固 九年级化学京改版(2013)下册(有答案) |
|
|
| 格式 | zip | ||
| 文件大小 | 111.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-14 00:00:00 | ||
图片预览




文档简介
第12章盐巩固 九年级化学京改版(2013)下册
一、单选题
1.小东同学家的西红柿植株生长不茂盛,叶色淡绿需要施加的肥料是
A.尿素
B.磷矿粉
C.碳酸钾
D.磷酸二氢钾
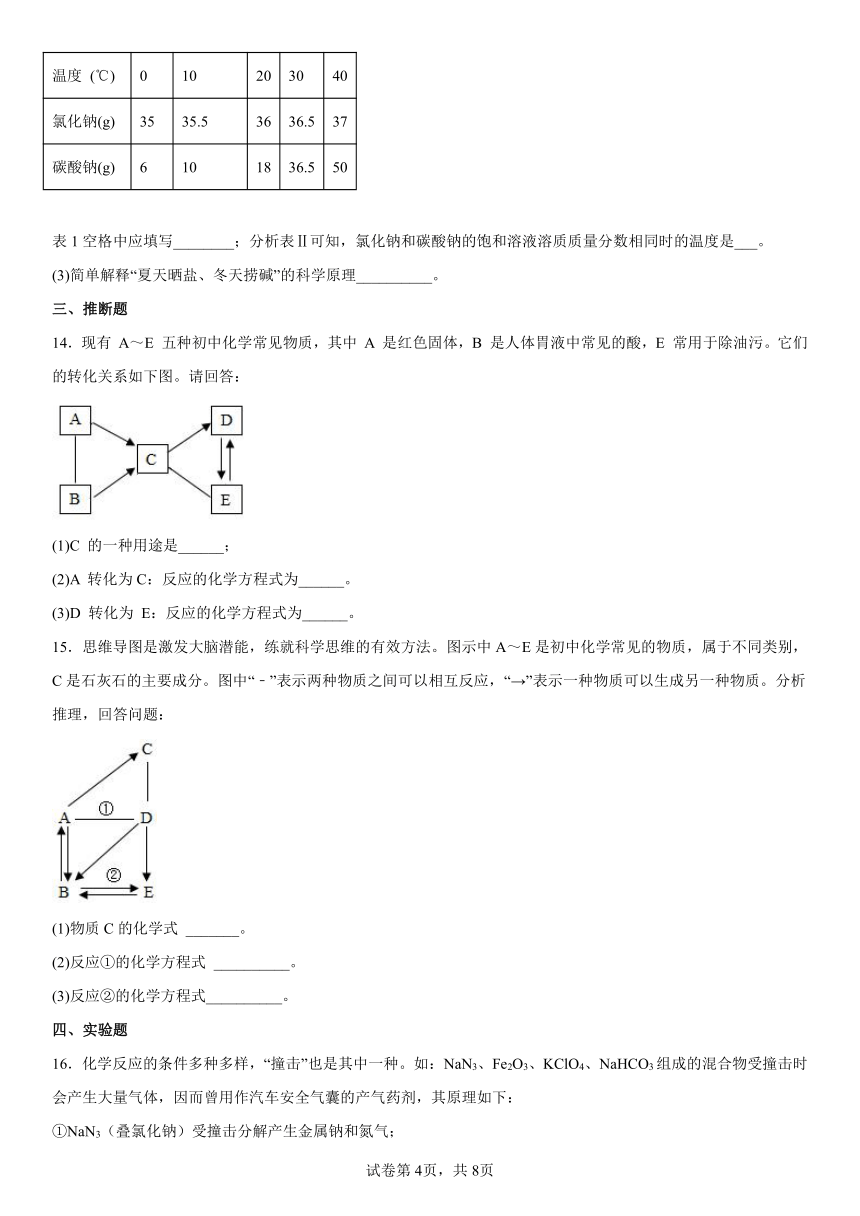
2.为鉴别失去标签的稀盐酸稀硫酸、NaOH和四种溶液,设计如下实验:
下面对试剂①、试剂②和试剂③的选择,合理的是( )
A.①酚酞 ②BaCl2 ③CuSO4
B.①酚酞 ②AgNO3 ③Na2CO3
C.①石蕊 ②BaCl2 ③Na2CO3
D.①石蕊 ②AgNO3 ③CuSO4
3.草木灰是一种碱性农家肥,下列肥料不能与草木灰混合使用的是
A.KNO3 B.NH4HCO3 C.KCl D.Ca3(PO4)2
4.物质的俗称和化学式对应正确的是
A.胆矾CuSO4 B.食盐NaCl C.水银Ag D.熟石灰CaCO3
5.如图给出了三种物质可能存在的转化关系,根据所学的物质性质及化学变化规律,下列选项判断正确的是
A.三种物质彼此间均能一步实现转化
B.实现①转化,可加入碳酸溶液
C.实现④转化,只能加稀盐酸
D.实现⑥转化,可加入熟石灰
6.下列各组物质用稀硫酸不能区分开的是( )
A.镁粉、氧化铜粉 B.NaOH溶液、KOH溶液
C.铁片、铜片 D.Na2CO3溶液、NaCl溶液
7.已知,常温下氯化钙、氯化钠的水溶液均呈中性,向含有盐酸和氯化钙的混合溶液中逐滴滴入过量的x,溶液pH与滴入x的量的关系如图所示,则x可能是下列物质中的( )
A.水 B.氢氧化钠溶液 C.纯碱溶液 D.硝酸银溶液
8.西汉时期,人们就会用石灰水或草木灰水(主要成分是K2CO2)等碱性溶液为丝麻脱胶来造纸。下列物质属于碱的是
A.生石灰 B.水 C.熟石灰 D.草木灰
9.下列物质的用途,利用了其物理性质的是
A.生石灰用作干燥剂 B.铁粉用作食品保鲜吸氧剂
C.氦气填充飞艇 D.小苏打用于治疗胃酸过多
10.向一定质量的FeCl3溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势如图所示。下列说法正确的是
A.a点时溶液中一定存在Fe3+
B.c点时所加试剂是NaOH溶液
C.加入试剂总体积为V1时,溶液中不存在NaOH
D.d点时溶液中的溶质不只是盐
11.向盛有硫酸和硫酸铜混合溶液的烧杯中滴入Ba(OH)2溶液,烧杯中溶质的质量与加入的Ba(OH)2溶液的质量关系如图所示。下列有关说法正确的是
A.a→b段溶液的质量一定减小
B.b→c段有水生成
C.b点溶液溶质为硫酸铜
D.d点沉淀质量与b点沉淀质量相等
二、简答题
12.碳酸钠广泛用于玻璃、造纸、纺织和洗涤剂的生产等。
(1)如何除去一瓶氢氧化钠溶液中混有的碳酸钠?用化学方程式表示除去杂质的原理_____。
(2)某趣味实验装置图,其气密性良好。打开分液漏斗的活塞后,可观察到气球胀大的现象。请用化学方程式解释产生此现象的原因_____。
13.溶液对于自然界中的生命活动和人类生产活动具有重要的意义,多角度认识溶液有助于指导我们的生活。
(1)关于溶液的说法,正确的是_________(填写标号)
A.溶液中各部分的性质相同B.均一、稳定的液体一定是溶液
C.浓溶液不一定是饱和溶液D.溶液加水稀释后溶质的质量变小
(2)表1是部分物质在20℃时的溶解性;表Ⅱ是氯化钠、碳酸钠在不同温度时的溶解度。
离子 OH- Cl- CO32- SO42-
K+ 溶 溶 溶 溶
Mg2+ 不 溶 微 溶
.Ba2+. 溶 溶 不
温度 (℃) 0 10 20 30 40
氯化钠(g) 35 35.5 36 36.5 37
碳酸钠(g) 6 10 18 36.5 50
表1空格中应填写________;分析表Ⅱ可知,氯化钠和碳酸钠的饱和溶液溶质质量分数相同时的温度是___。
(3)简单解释“夏天晒盐、冬天捞碱”的科学原理__________。
三、推断题
14.现有 A~E 五种初中化学常见物质,其中 A 是红色固体,B 是人体胃液中常见的酸,E 常用于除油污。它们的转化关系如下图。请回答:
(1)C 的一种用途是______;
(2)A 转化为C:反应的化学方程式为______。
(3)D 转化为 E:反应的化学方程式为______。
15.思维导图是激发大脑潜能,练就科学思维的有效方法。图示中A~E是初中化学常见的物质,属于不同类别,C是石灰石的主要成分。图中“﹣”表示两种物质之间可以相互反应,“→”表示一种物质可以生成另一种物质。分析推理,回答问题:
(1)物质C的化学式 _______。
(2)反应①的化学方程式 __________。
(3)反应②的化学方程式__________。
四、实验题
16.化学反应的条件多种多样,“撞击”也是其中一种。如:NaN3、Fe2O3、KClO4、NaHCO3组成的混合物受撞击时会产生大量气体,因而曾用作汽车安全气囊的产气药剂,其原理如下:
①NaN3(叠氯化钠)受撞击分解产生金属钠和氮气;
②金属钠将Fe2O3中的铁置换出来,同时钠与KClO4反应生成KCl及Na2O;
③NaHCO3受热分解生成碳酸钠及两种氧化物。
请回答下列问题:
(1)以上介绍的产气药剂中金属元素共有______种;写出KClO4(高氯酸钾)中阳离子的符号______。
(2)写出NaN3受撞击发生反应的化学方程式______;NaHCO3受热分解说明NaHCO3与碳酸钠中更稳定的是______(填化学式)
(3)若取100g上述产气药剂进行撞击反应实验(假设各物质均反应完全);
资料1:碱石灰能吸收水和二氧化碳;
资料2:标准状况下,气体的体积与质量有如下关系:
22.4L气体 水蒸气 氮气 氧气 二氧化碳
相应的质量(克) 18 28 32 44
①产气药剂撞击后产生的气体成分有氮气、______及水蒸气。
②将以上气体全部通过足量的碱石灰后体积为33.6L(标准状况),则产气药剂中NaN3的质量分数为______。
(4)已知相关物质的溶解度随温度变化的曲线如图。
①由此可知NaClO4属于______(选填“易溶”或“微溶”或“难溶”)物质。
②实验室称取一定质量的KCl、NaClO4溶解后加热反应、降温结晶、蒸馏水洗涤、真空干燥得到KClO4晶体。检验洗涤是否干净的方法是取最后一次洗涤液______,若观察到______证明还未洗净。
17.现有一瓶没有标签的白色固体,已知该白色固体是生石灰或大理石中的一种,为鉴定该物质,需要进行实验,请完成实验报告。
实验目的:_________
实验药品:白色固体、________
实验仪器:试管、镊子、胶头滴管
实验步骤 实验现象 实验结论
________ _______ 该白色固体是___
18.学完酸碱盐知识后,小美对妈妈焙制糕点用的小苏打很感兴趣,她把小苏打带到实验室与小刚一起进行探究.
(1)小美取少量小苏打溶于水,滴加酚酞试液后,溶液变红,说明小苏打的水溶液显___性;
(2)小刚在烧杯内放入少量小苏打,向其中滴加稀盐酸,立即有____产生,说明小苏打能与酸反应.在医疗上可以用小苏打治疗_______;
(3)小美想:糕点非常松软,是不是小苏打受热分解产生了CO2气体呢?于是她如图装置对小苏打进行加热,一段时间后,导管口的确有气泡冒出,澄清石灰水变浑浊,同时试管口有水珠生成.当导管口不再有气泡产生时,试管内仍有白色固体,她猜测剩余固体可能是:①NaOH;②Na2CO3;③NaCl.小刚认为猜想_____一定不正确,理由是_______.小刚从试管内取少量白色固体溶于水,滴加酚酞,溶液变红,他判断该固体为NaOH,小美认为他的实验设计不合理,因为_______________________
(4)小美和小刚继续探究固体成分,设计了如下实验:
操作步骤 实验现象 结论
取少量白色固体于试管中,加水溶解,向其中滴加____溶液 产生白色沉淀 试管内剩余的固体为Na2CO3
通过实验证明小苏打受热会分解,反应的化学方程式为:________________________.通过本次探究学习,小美对小苏打的性质有了全面的认识,她给妈妈提出保存小苏打的建议有:____(答出一点即可).
五、计算题
19.某化学兴趣活动小组用采集的石灰岩样品进行相关实验。将采集到的样品用水冲洗后晾干,称取20.00g样品平均分成两份,分别与足量相同的稀盐酸反应,测定释放出二氧化碳的质量与反应时间的关系如图所示。
(1)由图中曲线可以看出,固体物质与液体物质反应,当其他条件相同时,接触面积越 ,其反应速率越 。
(2)求样品中碳酸钙的质量分数(假设样品中其他杂质不参加反应,不考虑水、氯化氢逸出)。
20.菱铁矿(主要成分是碳酸亚铁)是炼铁的原料之一,现取20.0 g菱铁矿,向其中加入足量稀硫酸,充分反应(菱铁矿中的杂质不参加反应,且难溶于水),测得固体质量与所加稀硫酸的质量关系如图所示。
(1)20.0 g菱铁矿中FeCO3的质量分数为________%。
(2)列式计算,恰好完全反应时所得溶液的质量。
(3)向上述所得溶液中加入____________g水,能得到10%的硫酸亚铁溶液,用于缺铁花卉的营养液。
21.某课外活动小组为了测定一批石灰石碳酸钙的质量分数,将石灰石样品研成粉末,然后取一定量的石灰石粉末与过量稀盐酸充分反应(假设石灰石中的杂质既不和酸反应,也不溶于水),过滤、洗涤、干燥后称量滤渣质量的数据如下表:
实验序号 样品的质量/g 滤渣的质量/g
第一次 3.4 0.3
第二次 3.6 0.4
第三次 5.0 0.5
(1)该样品中碳酸钙质量分数的平均值为:_________。(结果精确到0.1%)
(2)引起三次实验数据差异的操作原因可能是:________________________。
(3)若利用题(1)的结果,煅烧100t这种石灰石,理论上最多能得到氧化钙______吨 (结果精确到0.1t)
22.硝酸溶解废旧CPU所得溶液中含有Cu2+和Ag+,用适当浓度的盐酸、氯化钠溶液、氨水和铁粉,按照如下方法回收Cu和Ag(图中标注的试剂均不同)。
(1)加入过量Fe粉发生的主要反应为______(写化学方程式)。
(2)试剂1和试剂3的名称依次是______。
(3)若向66g物质1中加入100g试剂2后,恰好完全反应,剩余固体质量为60.4g,求所得溶液中溶质的质量分数(写出计算过程,计算结果精确到0.1%)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.C
3.B
4.B
5.D
6.B
7.C
8.C
9.C
10.C
11.C
12.
13. A、C 不 30 “夏天晒盐”是因为食盐的溶解度受温度变化的影响不大,夏天气温高,水分蒸发快,食盐易结晶析出.“冬天捞碱”,是因为纯碱的溶解度受温度变化的影响较大,冬天气温低,纯碱易结晶析出
14.(1)灭火等
(2)等
(3)
15.(1)CaCO3
(2)(合理即可)
(3)
16. 三 K+ Na2CO3 二氧化碳 65% 易溶 加入硝酸银溶液 有白色沉淀
17. 确定白色固体的组成 稀盐酸 取少量白色固体与试管中,滴加适量稀盐酸 固体溶解,有气泡产生(或固体溶解,无气泡产生) 大理石(该白色固体是生石灰,与上一空对应)
18. 碱 气体 胃酸过多症 ③ 小苏打中不含氯元素 碳酸钠溶液也可以使酚酞变红 氯化钙 NaHCO3Na2CO3+H2O+CO2↑ 密封保存
19.(1) 大 快 (或 小 慢) (2)75%
20.(1)58(2)解:设生成FeSO4质量为x,CO2质量为y,
FeCO3+H2SO4=FeSO4+CO2+H2O
116 142 44
11.6g x y
,x=15.2g
,y=4.4g
恰好完全反应时,所得溶液的质量为20.0 g-8.4 g+50.0 g-4.4 g=57.2 g
答:恰好完全反应时,所得溶液的质量为57.2 g。
(3)94.8
21. 90.0% 石灰石中碳酸钙分布不均匀(或滤渣未清洗干净或称量样品不准确或石灰石颗粒未充分反应) 50.4t
22.(1)
(2)氯化钠溶液、氨水
(3)剩余固体的质量为铜的质量,故物质1中铁的质量为:66g-60.4g=5.6g
解:设反应生成氯化亚铁的质量为x,生成氢气的质量为y
x=12.7g
y=0.2g
故所得溶液中溶质的质量分数:
答:所得溶液中溶质的质量分数为12.0%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.小东同学家的西红柿植株生长不茂盛,叶色淡绿需要施加的肥料是
A.尿素
B.磷矿粉
C.碳酸钾
D.磷酸二氢钾
2.为鉴别失去标签的稀盐酸稀硫酸、NaOH和四种溶液,设计如下实验:
下面对试剂①、试剂②和试剂③的选择,合理的是( )
A.①酚酞 ②BaCl2 ③CuSO4
B.①酚酞 ②AgNO3 ③Na2CO3
C.①石蕊 ②BaCl2 ③Na2CO3
D.①石蕊 ②AgNO3 ③CuSO4
3.草木灰是一种碱性农家肥,下列肥料不能与草木灰混合使用的是
A.KNO3 B.NH4HCO3 C.KCl D.Ca3(PO4)2
4.物质的俗称和化学式对应正确的是
A.胆矾CuSO4 B.食盐NaCl C.水银Ag D.熟石灰CaCO3
5.如图给出了三种物质可能存在的转化关系,根据所学的物质性质及化学变化规律,下列选项判断正确的是
A.三种物质彼此间均能一步实现转化
B.实现①转化,可加入碳酸溶液
C.实现④转化,只能加稀盐酸
D.实现⑥转化,可加入熟石灰
6.下列各组物质用稀硫酸不能区分开的是( )
A.镁粉、氧化铜粉 B.NaOH溶液、KOH溶液
C.铁片、铜片 D.Na2CO3溶液、NaCl溶液
7.已知,常温下氯化钙、氯化钠的水溶液均呈中性,向含有盐酸和氯化钙的混合溶液中逐滴滴入过量的x,溶液pH与滴入x的量的关系如图所示,则x可能是下列物质中的( )
A.水 B.氢氧化钠溶液 C.纯碱溶液 D.硝酸银溶液
8.西汉时期,人们就会用石灰水或草木灰水(主要成分是K2CO2)等碱性溶液为丝麻脱胶来造纸。下列物质属于碱的是
A.生石灰 B.水 C.熟石灰 D.草木灰
9.下列物质的用途,利用了其物理性质的是
A.生石灰用作干燥剂 B.铁粉用作食品保鲜吸氧剂
C.氦气填充飞艇 D.小苏打用于治疗胃酸过多
10.向一定质量的FeCl3溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势如图所示。下列说法正确的是
A.a点时溶液中一定存在Fe3+
B.c点时所加试剂是NaOH溶液
C.加入试剂总体积为V1时,溶液中不存在NaOH
D.d点时溶液中的溶质不只是盐
11.向盛有硫酸和硫酸铜混合溶液的烧杯中滴入Ba(OH)2溶液,烧杯中溶质的质量与加入的Ba(OH)2溶液的质量关系如图所示。下列有关说法正确的是
A.a→b段溶液的质量一定减小
B.b→c段有水生成
C.b点溶液溶质为硫酸铜
D.d点沉淀质量与b点沉淀质量相等
二、简答题
12.碳酸钠广泛用于玻璃、造纸、纺织和洗涤剂的生产等。
(1)如何除去一瓶氢氧化钠溶液中混有的碳酸钠?用化学方程式表示除去杂质的原理_____。
(2)某趣味实验装置图,其气密性良好。打开分液漏斗的活塞后,可观察到气球胀大的现象。请用化学方程式解释产生此现象的原因_____。
13.溶液对于自然界中的生命活动和人类生产活动具有重要的意义,多角度认识溶液有助于指导我们的生活。
(1)关于溶液的说法,正确的是_________(填写标号)
A.溶液中各部分的性质相同B.均一、稳定的液体一定是溶液
C.浓溶液不一定是饱和溶液D.溶液加水稀释后溶质的质量变小
(2)表1是部分物质在20℃时的溶解性;表Ⅱ是氯化钠、碳酸钠在不同温度时的溶解度。
离子 OH- Cl- CO32- SO42-
K+ 溶 溶 溶 溶
Mg2+ 不 溶 微 溶
.Ba2+. 溶 溶 不
温度 (℃) 0 10 20 30 40
氯化钠(g) 35 35.5 36 36.5 37
碳酸钠(g) 6 10 18 36.5 50
表1空格中应填写________;分析表Ⅱ可知,氯化钠和碳酸钠的饱和溶液溶质质量分数相同时的温度是___。
(3)简单解释“夏天晒盐、冬天捞碱”的科学原理__________。
三、推断题
14.现有 A~E 五种初中化学常见物质,其中 A 是红色固体,B 是人体胃液中常见的酸,E 常用于除油污。它们的转化关系如下图。请回答:
(1)C 的一种用途是______;
(2)A 转化为C:反应的化学方程式为______。
(3)D 转化为 E:反应的化学方程式为______。
15.思维导图是激发大脑潜能,练就科学思维的有效方法。图示中A~E是初中化学常见的物质,属于不同类别,C是石灰石的主要成分。图中“﹣”表示两种物质之间可以相互反应,“→”表示一种物质可以生成另一种物质。分析推理,回答问题:
(1)物质C的化学式 _______。
(2)反应①的化学方程式 __________。
(3)反应②的化学方程式__________。
四、实验题
16.化学反应的条件多种多样,“撞击”也是其中一种。如:NaN3、Fe2O3、KClO4、NaHCO3组成的混合物受撞击时会产生大量气体,因而曾用作汽车安全气囊的产气药剂,其原理如下:
①NaN3(叠氯化钠)受撞击分解产生金属钠和氮气;
②金属钠将Fe2O3中的铁置换出来,同时钠与KClO4反应生成KCl及Na2O;
③NaHCO3受热分解生成碳酸钠及两种氧化物。
请回答下列问题:
(1)以上介绍的产气药剂中金属元素共有______种;写出KClO4(高氯酸钾)中阳离子的符号______。
(2)写出NaN3受撞击发生反应的化学方程式______;NaHCO3受热分解说明NaHCO3与碳酸钠中更稳定的是______(填化学式)
(3)若取100g上述产气药剂进行撞击反应实验(假设各物质均反应完全);
资料1:碱石灰能吸收水和二氧化碳;
资料2:标准状况下,气体的体积与质量有如下关系:
22.4L气体 水蒸气 氮气 氧气 二氧化碳
相应的质量(克) 18 28 32 44
①产气药剂撞击后产生的气体成分有氮气、______及水蒸气。
②将以上气体全部通过足量的碱石灰后体积为33.6L(标准状况),则产气药剂中NaN3的质量分数为______。
(4)已知相关物质的溶解度随温度变化的曲线如图。
①由此可知NaClO4属于______(选填“易溶”或“微溶”或“难溶”)物质。
②实验室称取一定质量的KCl、NaClO4溶解后加热反应、降温结晶、蒸馏水洗涤、真空干燥得到KClO4晶体。检验洗涤是否干净的方法是取最后一次洗涤液______,若观察到______证明还未洗净。
17.现有一瓶没有标签的白色固体,已知该白色固体是生石灰或大理石中的一种,为鉴定该物质,需要进行实验,请完成实验报告。
实验目的:_________
实验药品:白色固体、________
实验仪器:试管、镊子、胶头滴管
实验步骤 实验现象 实验结论
________ _______ 该白色固体是___
18.学完酸碱盐知识后,小美对妈妈焙制糕点用的小苏打很感兴趣,她把小苏打带到实验室与小刚一起进行探究.
(1)小美取少量小苏打溶于水,滴加酚酞试液后,溶液变红,说明小苏打的水溶液显___性;
(2)小刚在烧杯内放入少量小苏打,向其中滴加稀盐酸,立即有____产生,说明小苏打能与酸反应.在医疗上可以用小苏打治疗_______;
(3)小美想:糕点非常松软,是不是小苏打受热分解产生了CO2气体呢?于是她如图装置对小苏打进行加热,一段时间后,导管口的确有气泡冒出,澄清石灰水变浑浊,同时试管口有水珠生成.当导管口不再有气泡产生时,试管内仍有白色固体,她猜测剩余固体可能是:①NaOH;②Na2CO3;③NaCl.小刚认为猜想_____一定不正确,理由是_______.小刚从试管内取少量白色固体溶于水,滴加酚酞,溶液变红,他判断该固体为NaOH,小美认为他的实验设计不合理,因为_______________________
(4)小美和小刚继续探究固体成分,设计了如下实验:
操作步骤 实验现象 结论
取少量白色固体于试管中,加水溶解,向其中滴加____溶液 产生白色沉淀 试管内剩余的固体为Na2CO3
通过实验证明小苏打受热会分解,反应的化学方程式为:________________________.通过本次探究学习,小美对小苏打的性质有了全面的认识,她给妈妈提出保存小苏打的建议有:____(答出一点即可).
五、计算题
19.某化学兴趣活动小组用采集的石灰岩样品进行相关实验。将采集到的样品用水冲洗后晾干,称取20.00g样品平均分成两份,分别与足量相同的稀盐酸反应,测定释放出二氧化碳的质量与反应时间的关系如图所示。
(1)由图中曲线可以看出,固体物质与液体物质反应,当其他条件相同时,接触面积越 ,其反应速率越 。
(2)求样品中碳酸钙的质量分数(假设样品中其他杂质不参加反应,不考虑水、氯化氢逸出)。
20.菱铁矿(主要成分是碳酸亚铁)是炼铁的原料之一,现取20.0 g菱铁矿,向其中加入足量稀硫酸,充分反应(菱铁矿中的杂质不参加反应,且难溶于水),测得固体质量与所加稀硫酸的质量关系如图所示。
(1)20.0 g菱铁矿中FeCO3的质量分数为________%。
(2)列式计算,恰好完全反应时所得溶液的质量。
(3)向上述所得溶液中加入____________g水,能得到10%的硫酸亚铁溶液,用于缺铁花卉的营养液。
21.某课外活动小组为了测定一批石灰石碳酸钙的质量分数,将石灰石样品研成粉末,然后取一定量的石灰石粉末与过量稀盐酸充分反应(假设石灰石中的杂质既不和酸反应,也不溶于水),过滤、洗涤、干燥后称量滤渣质量的数据如下表:
实验序号 样品的质量/g 滤渣的质量/g
第一次 3.4 0.3
第二次 3.6 0.4
第三次 5.0 0.5
(1)该样品中碳酸钙质量分数的平均值为:_________。(结果精确到0.1%)
(2)引起三次实验数据差异的操作原因可能是:________________________。
(3)若利用题(1)的结果,煅烧100t这种石灰石,理论上最多能得到氧化钙______吨 (结果精确到0.1t)
22.硝酸溶解废旧CPU所得溶液中含有Cu2+和Ag+,用适当浓度的盐酸、氯化钠溶液、氨水和铁粉,按照如下方法回收Cu和Ag(图中标注的试剂均不同)。
(1)加入过量Fe粉发生的主要反应为______(写化学方程式)。
(2)试剂1和试剂3的名称依次是______。
(3)若向66g物质1中加入100g试剂2后,恰好完全反应,剩余固体质量为60.4g,求所得溶液中溶质的质量分数(写出计算过程,计算结果精确到0.1%)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.C
3.B
4.B
5.D
6.B
7.C
8.C
9.C
10.C
11.C
12.
13. A、C 不 30 “夏天晒盐”是因为食盐的溶解度受温度变化的影响不大,夏天气温高,水分蒸发快,食盐易结晶析出.“冬天捞碱”,是因为纯碱的溶解度受温度变化的影响较大,冬天气温低,纯碱易结晶析出
14.(1)灭火等
(2)等
(3)
15.(1)CaCO3
(2)(合理即可)
(3)
16. 三 K+ Na2CO3 二氧化碳 65% 易溶 加入硝酸银溶液 有白色沉淀
17. 确定白色固体的组成 稀盐酸 取少量白色固体与试管中,滴加适量稀盐酸 固体溶解,有气泡产生(或固体溶解,无气泡产生) 大理石(该白色固体是生石灰,与上一空对应)
18. 碱 气体 胃酸过多症 ③ 小苏打中不含氯元素 碳酸钠溶液也可以使酚酞变红 氯化钙 NaHCO3Na2CO3+H2O+CO2↑ 密封保存
19.(1) 大 快 (或 小 慢) (2)75%
20.(1)58(2)解:设生成FeSO4质量为x,CO2质量为y,
FeCO3+H2SO4=FeSO4+CO2+H2O
116 142 44
11.6g x y
,x=15.2g
,y=4.4g
恰好完全反应时,所得溶液的质量为20.0 g-8.4 g+50.0 g-4.4 g=57.2 g
答:恰好完全反应时,所得溶液的质量为57.2 g。
(3)94.8
21. 90.0% 石灰石中碳酸钙分布不均匀(或滤渣未清洗干净或称量样品不准确或石灰石颗粒未充分反应) 50.4t
22.(1)
(2)氯化钠溶液、氨水
(3)剩余固体的质量为铜的质量,故物质1中铁的质量为:66g-60.4g=5.6g
解:设反应生成氯化亚铁的质量为x,生成氢气的质量为y
x=12.7g
y=0.2g
故所得溶液中溶质的质量分数:
答:所得溶液中溶质的质量分数为12.0%。
答案第1页,共2页
答案第1页,共2页
