第四单元盐化肥练习题九年级化学人教版(五四学制)全一册(有答案)
文档属性
| 名称 | 第四单元盐化肥练习题九年级化学人教版(五四学制)全一册(有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 121.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-14 00:00:00 | ||
图片预览


文档简介
第四单元盐化肥练习题九年级化学人教版(五四学制)全一册
一、单选题
1.(2017·上海·中考真题)氢氧化钙俗称
A.烧碱 B.纯碱 C.熟石灰 D.石灰石
2.(2022·全国·九年级课前预习)某农用物资商店里的化肥有Ca3(PO4)2、K2SO4、CO(NH2)2,其中缺少的肥料品种是
A.氮肥 B.磷肥
C.钾肥 D.复合肥
3.(2020·湖南湘潭·中考真题)某pH=12的无色溶液中大量存在的离子有Na+、Ba2+、NO、X,则X可能是
A.Cu2+ B.Cl- C.H+ D.SO
4.(2019·天津河西·九年级学业考试)下列物质属于碱的是
A.NaHCO3 B.H2O C.NH3·H2O D.CH3COOH
5.(2021·四川自贡·一模)合理使用化肥,有利于农作物的生长和减少环境污染。下列有关化肥的说法不正确的是
A.为保证高产尽量多施用化肥
B.不能将氯化铵与碱性物质混合施用
C.KNO3是一种常用的复合肥料
D.提倡将农家肥与化肥综合使用
6.(2016·广西桂林·中考真题)下列有关NaCl的叙述,错误的是
A.不溶于水 B.溶液呈中性
C.是食盐的主要成分 D.可用于配制生理盐水
7.(2013·四川达州·中考真题)下列试剂中,能把稀硫酸、KOH溶液、CaCl2溶液一次性鉴别出来的是
A.KCl溶液 B.K2CO3溶液
C.稀盐酸 D.NaNO3溶液
8.(2018·宁夏中卫市第四中学一模)下列除去杂质的方法不正确的是( )
A.FeSO4溶液(CuSO4):过量的铁粉过滤 B.H2(H2O):浓硫酸
C.CO2(CO):通过灼热的氧化铜粉末 D.CaO(CaCO3):稀盐酸
9.(2017·河北·中考真题)下列对化肥的认识不正确的是
A.KNO3是一种复合肥 B.施用氮肥,能促进植物茎叶生长
C.铵态氮肥不能与碱性肥料混合使用 D.化肥能提高粮食产量,施用越多越好
10.(2014·山西·九年级专题练习)硝酸铵(NH4NO3)是一种高效化肥,它属于
A.氮肥 B.磷肥 C.钾肥 D.复合肥
11.(2019·四川泸州·中考真题)以下是Na2CO3、NaHCO3的溶解度表。下列说法中错误的是( )
0℃ 10℃ 20℃ 30℃ 40℃ 50℃ 60℃
Na2CO3的溶解度(g/100g水) 7.1 12.5 21.5 39.7 49.0 48.5 46.0
NaHCO3的溶解度(g/100g水) 6.9 8.1 9.6 11.1 12.7 14.5 16.4
A.40℃的饱和Na2CO3溶液升温到60℃,会析出晶体
B.60℃的NaHCO3溶液蒸干并充分灼烧,可得到NaHCO3晶体
C.30℃的溶质质量分数为25%的Na2CO3溶液降温到20℃,有晶体析出
D.20℃的饱和Na2CO3溶液中通足量CO2,生成的NaHCO3会部分析出
12.(2021·四川达州·中考真题)某水溶液中可能含有以下几种离子中的一种或几种:Na+、Cl﹣、Ca2+、Ba2+、SO、CO,现取两份等质量的溶液进行如下实验:
(1)第一份加入AgNO3溶液产生白色沉淀;
(2)第二份加足量的Ba(NO3)2溶液产生白色沉淀,继续加入过量的稀硝酸,沉淀部分溶解。
根据上述实验现象,下列推测合理的是
A.一定存在Na+
B.一定存在CO,可能存在Ba2+
C.一定存在Cl﹣
D.一定存在SO,可能存在Ca2+
二、简答题
13.(2021·河南商丘·九年级期中)请用所学的知识回答下列问题:
(1)铵态氮肥为什么不能和碱性物质混合施用?
(2)电解水实验时,为什么要向水中加入少量硫酸钠或氢氧化钠?
14.(2019·广东·中考模拟)现有失去标签的4种固体物质,分别是BaCl2、BaCO3、Na2CO3和NaHSO4。
(1)在仅提供蒸馏水和所需仪器的条件下,鉴别出上述4种固体物质。
①最先鉴别出来的固体物质是 _____ 。
②利用①中鉴别出来的物质又可直接鉴别出的固体物质是 _____ ,依据的实验现象是 _____ 。
③利用②中鉴别出来的物质即可鉴别出其它物质。
(2)用鉴别出来的物质进行实验:向Na2CO3溶液中滴入BaCl2溶液至恰好完全反应。
①观察到的实验现象是 _____ 。
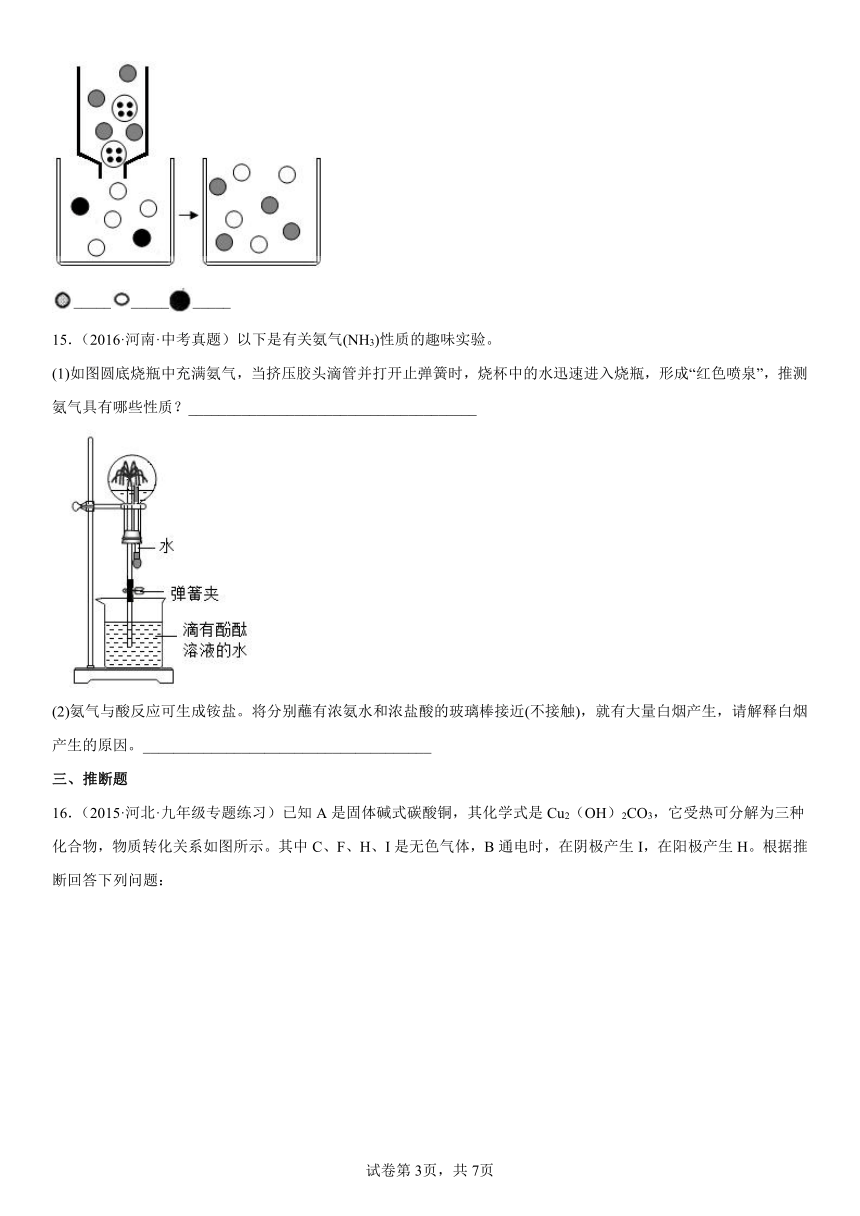
②下图表示该反应前后溶液中存在的主要离子,写出以下图形代表的离子(填离子符号):
_______________
15.(2016·河南·中考真题)以下是有关氨气(NH3)性质的趣味实验。
(1)如图圆底烧瓶中充满氨气,当挤压胶头滴管并打开止弹簧时,烧杯中的水迅速进入烧瓶,形成“红色喷泉”,推测氨气具有哪些性质?______________________________________
(2)氨气与酸反应可生成铵盐。将分别蘸有浓氨水和浓盐酸的玻璃棒接近(不接触),就有大量白烟产生,请解释白烟产生的原因。______________________________________
三、推断题
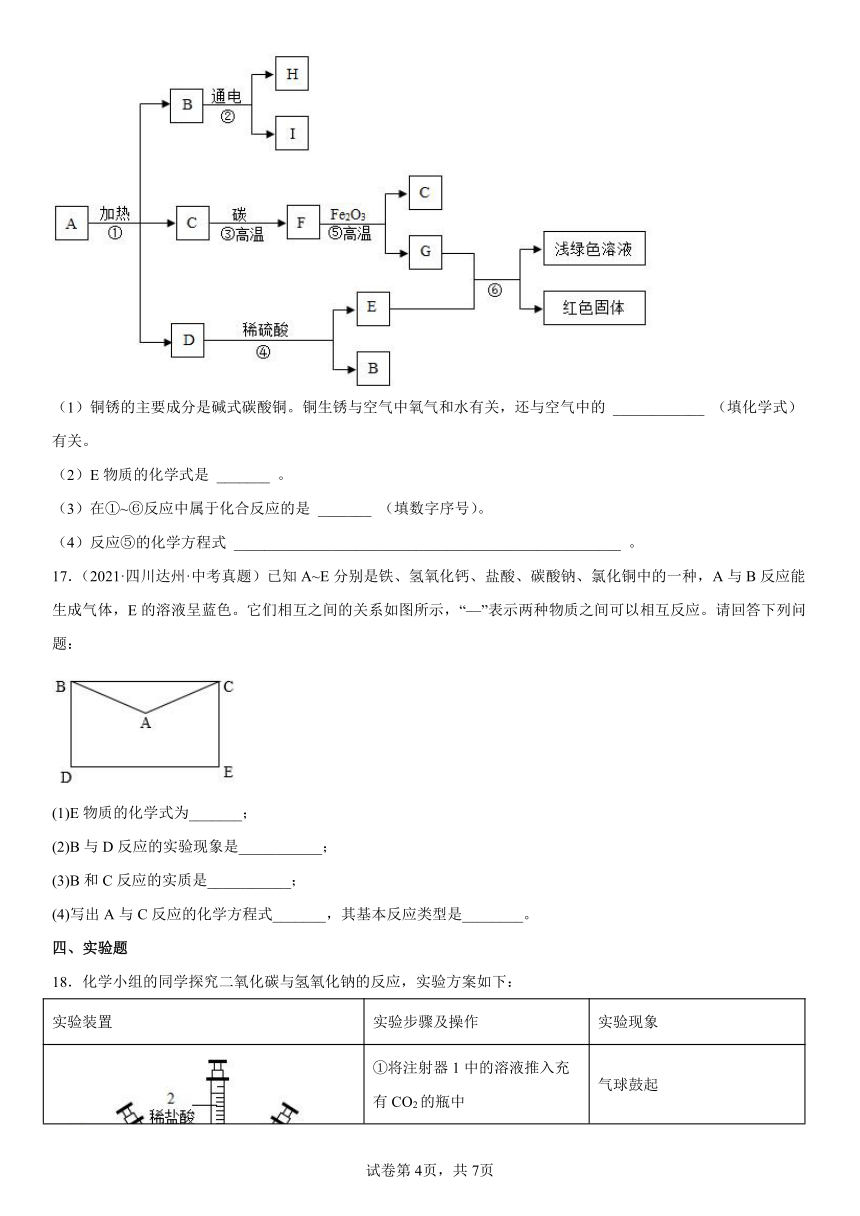
16.(2015·河北·九年级专题练习)已知A是固体碱式碳酸铜,其化学式是Cu2(OH)2CO3,它受热可分解为三种化合物,物质转化关系如图所示。其中C、F、H、I是无色气体,B通电时,在阴极产生I,在阳极产生H。根据推断回答下列问题:
(1)铜锈的主要成分是碱式碳酸铜。铜生锈与空气中氧气和水有关,还与空气中的 ____________ (填化学式)有关。
(2)E物质的化学式是 _______ 。
(3)在①~⑥反应中属于化合反应的是 _______ (填数字序号)。
(4)反应⑤的化学方程式 ___________________________________________________ 。
17.(2021·四川达州·中考真题)已知A~E分别是铁、氢氧化钙、盐酸、碳酸钠、氯化铜中的一种,A与B反应能生成气体,E的溶液呈蓝色。它们相互之间的关系如图所示,“—”表示两种物质之间可以相互反应。请回答下列问题:
(1)E物质的化学式为_______;
(2)B与D反应的实验现象是___________;
(3)B和C反应的实质是___________;
(4)写出A与C反应的化学方程式_______,其基本反应类型是________。
四、实验题
18.化学小组的同学探究二氧化碳与氢氧化钠的反应,实验方案如下:
实验装置 实验步骤及操作 实验现象
①将注射器1中的溶液推入充有CO2的瓶中 气球鼓起
②_____ 无明显现象
③将注射器2中的溶液推入瓶中 溶液中有气泡产生,气球变瘪
④向外拉注射器3 澄清石灰水变浑浊
(1)步骤①中气球鼓起的原因可能是_____.
(2)步骤②中的操作是_____,其目的是验证瓶内_____是否完全反应.
(3)本实验的结论是_____.
19.(2019·福建省泉州实验中学九年级阶段练习)小康同学在老师的指导下,设计如下装置验证碳酸钙的性质的同时,探究氧化钙与二氧化碳在加热的条件下是否也能发生反应生成碳酸钙。
(1)当B中出现 _________________ 的现象时,说明A中发生了反应,A中反应的化学方程式为 _______________________________________ 。
(2)实验后小弘同学对D中是否也发生了反应进行如下探究:
取一定量的D中固体于试管中,并加入一定量的水,振荡,有白色不溶物。小烨同学认为试管中的固体为碳酸钙,即D中确实发生了反应;小彭同学认为上述实验不足以证明D中发生了反应,其理由是 _________________________________________________ ;她又重新设计实验,她的实验步骤及现象为 ______________________________________________________________ 。
20.(2022·全国·九年级专题练习)工业烧碱具有较好的杀菌消毒作用且廉价易得,但工业烧碱中含有一种杂质碳酸钠。某科学学习小组同学围绕工业“烧碱”样品纯度测定问题,展开了讨论与探究。
【原理思路】利用Na2CO3与稀H2SO4反应产生CO2,通过CO2质量的测定,确定样品中碳酸钠的质量,从而计算工业“烧碱”样品纯度。
【实验方案】根据以上思路,小科设计的方案是:利用如图甲的装置(固定装置省略),通过测定反应前后整套装置和药品的总质量的减少量确定CO2质量。
(1)小科按该方案进行测定,加入足量稀硫酸充分反应后,发现最终测得碳酸钠的质量明显偏低。你认为导致测得的“碳酸钠”的质量明显偏低的原因是______;
【方案改进】为减少误差,小组同学经讨论,对小科方案进行改进,设计了如图乙的实验方案(固定装置省略)。通过测定反应前后D质量的变化。
(2)图乙B装置中样品在与足量稀硫酸反应前和停止反应后,都要鼓入足量的空气,在反应前通空气时,a、b、c三个弹簧夹的控制方法是______。
(3)若撤去图乙中的A和E装置,则测得工业“烧碱”的纯度将______(选填“偏高”“偏低”或“无影响”)。
(4)按改进后的图乙实验方案进行实验,发现测得的工业“烧碱”的纯度明显偏高,从实验操作上分析产生上述结果的原因是______(写出一种即可)。
五、计算题
21.(2020·湖北·罗田县万密斋初级中学九年级阶段练习)某中学化学课外实验兴趣小组欲测定一瓶混有氯化钠的苏打中碳酸钠的质量分数。从该瓶试剂中取出100克样品,放在锥形瓶中加水至全部溶解,再加入稀盐酸,实验相关数据如图。
(1)产生的二氧化碳气体是__________克;
(2)该瓶苏打中碳酸钠的质量分数是_________?(写出计算过程)
22.(2018·湖北咸宁·中考真题)为了测定一瓶硫酸铜溶液的溶质质量分数,取出50克该溶液,向其中逐滴加入溶质质量分数为16%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示:
请你仔细分析此关系图,并进行计算。
(1)当滴入氢氧化钠溶液_____克时,硫酸铜与氢氧化钠恰好完全反应。
(2)计算此硫酸铜溶液中溶质的质量分数为_________(写出计算过程)。
23.(2020·内蒙古·兴安盟教师发展中心中考真题)为测定某CuSO4溶液中溶质的质量分数,取150gCuSO4溶液,平均分为三份,每一份样品均按如图所示进行实验,实验数据见下表。请计算:
实验1 实验2 实验3
样品质量/g 50 50 50
NaOH溶液质量/g 20 40 60
m/g 44.9 49.8 49.8
(1)50gCuSO4溶液完全反应时,所得沉淀的质量为______________g。
(2)CuSO4溶液中溶质的质量分数。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.D
3.B
4.C
5.A
6.A
7.B
8.D
9.D
10.A
11.B
12.A
13.(1)铵态氮肥和碱性物质混合能生成氨气,从而降低肥效(2)增强水的导电性
14. BaCO3 NaHSO4 有气泡产生 产生白色沉淀 Cl- Na+ CO32-
15. 氨气易溶于水,溶液显碱性 浓盐酸易挥发出氯化氢气体,氯化氢气体能与氨气化合生成了氯化铵颗粒
16. CO2 CuSO4 ③
17. CuCl2 溶液变浅绿色,有气体生成 氢离子和氢氧根离子生成水 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH 复分解反应
18. 氢氧化钠与二氧化碳反应,消耗瓶内二氧化碳,气压减小 向外拉注射器 3 二氧化碳 二氧化碳能与氢氧化钠反应
19. 石灰水变浑浊 氧化钙和水反应生成的氢氧化钙是微溶物质,加入一定量的水后,有白色不溶物也可能是氢氧化钙; 取样品,加入足量的盐酸,有气体产生,证明有碳酸钙
20.(1)反应生成的二氧化碳部分留在装置中
(2)打开ab,关闭c
(3)偏低
(4)反应后没有鼓入足量的空气
21.(1)4.4(2)10.6%
22.(1)25(2)16%
23.(1)9.8g (2)32%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.(2017·上海·中考真题)氢氧化钙俗称
A.烧碱 B.纯碱 C.熟石灰 D.石灰石
2.(2022·全国·九年级课前预习)某农用物资商店里的化肥有Ca3(PO4)2、K2SO4、CO(NH2)2,其中缺少的肥料品种是
A.氮肥 B.磷肥
C.钾肥 D.复合肥
3.(2020·湖南湘潭·中考真题)某pH=12的无色溶液中大量存在的离子有Na+、Ba2+、NO、X,则X可能是
A.Cu2+ B.Cl- C.H+ D.SO
4.(2019·天津河西·九年级学业考试)下列物质属于碱的是
A.NaHCO3 B.H2O C.NH3·H2O D.CH3COOH
5.(2021·四川自贡·一模)合理使用化肥,有利于农作物的生长和减少环境污染。下列有关化肥的说法不正确的是
A.为保证高产尽量多施用化肥
B.不能将氯化铵与碱性物质混合施用
C.KNO3是一种常用的复合肥料
D.提倡将农家肥与化肥综合使用
6.(2016·广西桂林·中考真题)下列有关NaCl的叙述,错误的是
A.不溶于水 B.溶液呈中性
C.是食盐的主要成分 D.可用于配制生理盐水
7.(2013·四川达州·中考真题)下列试剂中,能把稀硫酸、KOH溶液、CaCl2溶液一次性鉴别出来的是
A.KCl溶液 B.K2CO3溶液
C.稀盐酸 D.NaNO3溶液
8.(2018·宁夏中卫市第四中学一模)下列除去杂质的方法不正确的是( )
A.FeSO4溶液(CuSO4):过量的铁粉过滤 B.H2(H2O):浓硫酸
C.CO2(CO):通过灼热的氧化铜粉末 D.CaO(CaCO3):稀盐酸
9.(2017·河北·中考真题)下列对化肥的认识不正确的是
A.KNO3是一种复合肥 B.施用氮肥,能促进植物茎叶生长
C.铵态氮肥不能与碱性肥料混合使用 D.化肥能提高粮食产量,施用越多越好
10.(2014·山西·九年级专题练习)硝酸铵(NH4NO3)是一种高效化肥,它属于
A.氮肥 B.磷肥 C.钾肥 D.复合肥
11.(2019·四川泸州·中考真题)以下是Na2CO3、NaHCO3的溶解度表。下列说法中错误的是( )
0℃ 10℃ 20℃ 30℃ 40℃ 50℃ 60℃
Na2CO3的溶解度(g/100g水) 7.1 12.5 21.5 39.7 49.0 48.5 46.0
NaHCO3的溶解度(g/100g水) 6.9 8.1 9.6 11.1 12.7 14.5 16.4
A.40℃的饱和Na2CO3溶液升温到60℃,会析出晶体
B.60℃的NaHCO3溶液蒸干并充分灼烧,可得到NaHCO3晶体
C.30℃的溶质质量分数为25%的Na2CO3溶液降温到20℃,有晶体析出
D.20℃的饱和Na2CO3溶液中通足量CO2,生成的NaHCO3会部分析出
12.(2021·四川达州·中考真题)某水溶液中可能含有以下几种离子中的一种或几种:Na+、Cl﹣、Ca2+、Ba2+、SO、CO,现取两份等质量的溶液进行如下实验:
(1)第一份加入AgNO3溶液产生白色沉淀;
(2)第二份加足量的Ba(NO3)2溶液产生白色沉淀,继续加入过量的稀硝酸,沉淀部分溶解。
根据上述实验现象,下列推测合理的是
A.一定存在Na+
B.一定存在CO,可能存在Ba2+
C.一定存在Cl﹣
D.一定存在SO,可能存在Ca2+
二、简答题
13.(2021·河南商丘·九年级期中)请用所学的知识回答下列问题:
(1)铵态氮肥为什么不能和碱性物质混合施用?
(2)电解水实验时,为什么要向水中加入少量硫酸钠或氢氧化钠?
14.(2019·广东·中考模拟)现有失去标签的4种固体物质,分别是BaCl2、BaCO3、Na2CO3和NaHSO4。
(1)在仅提供蒸馏水和所需仪器的条件下,鉴别出上述4种固体物质。
①最先鉴别出来的固体物质是 _____ 。
②利用①中鉴别出来的物质又可直接鉴别出的固体物质是 _____ ,依据的实验现象是 _____ 。
③利用②中鉴别出来的物质即可鉴别出其它物质。
(2)用鉴别出来的物质进行实验:向Na2CO3溶液中滴入BaCl2溶液至恰好完全反应。
①观察到的实验现象是 _____ 。
②下图表示该反应前后溶液中存在的主要离子,写出以下图形代表的离子(填离子符号):
_______________
15.(2016·河南·中考真题)以下是有关氨气(NH3)性质的趣味实验。
(1)如图圆底烧瓶中充满氨气,当挤压胶头滴管并打开止弹簧时,烧杯中的水迅速进入烧瓶,形成“红色喷泉”,推测氨气具有哪些性质?______________________________________
(2)氨气与酸反应可生成铵盐。将分别蘸有浓氨水和浓盐酸的玻璃棒接近(不接触),就有大量白烟产生,请解释白烟产生的原因。______________________________________
三、推断题
16.(2015·河北·九年级专题练习)已知A是固体碱式碳酸铜,其化学式是Cu2(OH)2CO3,它受热可分解为三种化合物,物质转化关系如图所示。其中C、F、H、I是无色气体,B通电时,在阴极产生I,在阳极产生H。根据推断回答下列问题:
(1)铜锈的主要成分是碱式碳酸铜。铜生锈与空气中氧气和水有关,还与空气中的 ____________ (填化学式)有关。
(2)E物质的化学式是 _______ 。
(3)在①~⑥反应中属于化合反应的是 _______ (填数字序号)。
(4)反应⑤的化学方程式 ___________________________________________________ 。
17.(2021·四川达州·中考真题)已知A~E分别是铁、氢氧化钙、盐酸、碳酸钠、氯化铜中的一种,A与B反应能生成气体,E的溶液呈蓝色。它们相互之间的关系如图所示,“—”表示两种物质之间可以相互反应。请回答下列问题:
(1)E物质的化学式为_______;
(2)B与D反应的实验现象是___________;
(3)B和C反应的实质是___________;
(4)写出A与C反应的化学方程式_______,其基本反应类型是________。
四、实验题
18.化学小组的同学探究二氧化碳与氢氧化钠的反应,实验方案如下:
实验装置 实验步骤及操作 实验现象
①将注射器1中的溶液推入充有CO2的瓶中 气球鼓起
②_____ 无明显现象
③将注射器2中的溶液推入瓶中 溶液中有气泡产生,气球变瘪
④向外拉注射器3 澄清石灰水变浑浊
(1)步骤①中气球鼓起的原因可能是_____.
(2)步骤②中的操作是_____,其目的是验证瓶内_____是否完全反应.
(3)本实验的结论是_____.
19.(2019·福建省泉州实验中学九年级阶段练习)小康同学在老师的指导下,设计如下装置验证碳酸钙的性质的同时,探究氧化钙与二氧化碳在加热的条件下是否也能发生反应生成碳酸钙。
(1)当B中出现 _________________ 的现象时,说明A中发生了反应,A中反应的化学方程式为 _______________________________________ 。
(2)实验后小弘同学对D中是否也发生了反应进行如下探究:
取一定量的D中固体于试管中,并加入一定量的水,振荡,有白色不溶物。小烨同学认为试管中的固体为碳酸钙,即D中确实发生了反应;小彭同学认为上述实验不足以证明D中发生了反应,其理由是 _________________________________________________ ;她又重新设计实验,她的实验步骤及现象为 ______________________________________________________________ 。
20.(2022·全国·九年级专题练习)工业烧碱具有较好的杀菌消毒作用且廉价易得,但工业烧碱中含有一种杂质碳酸钠。某科学学习小组同学围绕工业“烧碱”样品纯度测定问题,展开了讨论与探究。
【原理思路】利用Na2CO3与稀H2SO4反应产生CO2,通过CO2质量的测定,确定样品中碳酸钠的质量,从而计算工业“烧碱”样品纯度。
【实验方案】根据以上思路,小科设计的方案是:利用如图甲的装置(固定装置省略),通过测定反应前后整套装置和药品的总质量的减少量确定CO2质量。
(1)小科按该方案进行测定,加入足量稀硫酸充分反应后,发现最终测得碳酸钠的质量明显偏低。你认为导致测得的“碳酸钠”的质量明显偏低的原因是______;
【方案改进】为减少误差,小组同学经讨论,对小科方案进行改进,设计了如图乙的实验方案(固定装置省略)。通过测定反应前后D质量的变化。
(2)图乙B装置中样品在与足量稀硫酸反应前和停止反应后,都要鼓入足量的空气,在反应前通空气时,a、b、c三个弹簧夹的控制方法是______。
(3)若撤去图乙中的A和E装置,则测得工业“烧碱”的纯度将______(选填“偏高”“偏低”或“无影响”)。
(4)按改进后的图乙实验方案进行实验,发现测得的工业“烧碱”的纯度明显偏高,从实验操作上分析产生上述结果的原因是______(写出一种即可)。
五、计算题
21.(2020·湖北·罗田县万密斋初级中学九年级阶段练习)某中学化学课外实验兴趣小组欲测定一瓶混有氯化钠的苏打中碳酸钠的质量分数。从该瓶试剂中取出100克样品,放在锥形瓶中加水至全部溶解,再加入稀盐酸,实验相关数据如图。
(1)产生的二氧化碳气体是__________克;
(2)该瓶苏打中碳酸钠的质量分数是_________?(写出计算过程)
22.(2018·湖北咸宁·中考真题)为了测定一瓶硫酸铜溶液的溶质质量分数,取出50克该溶液,向其中逐滴加入溶质质量分数为16%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示:
请你仔细分析此关系图,并进行计算。
(1)当滴入氢氧化钠溶液_____克时,硫酸铜与氢氧化钠恰好完全反应。
(2)计算此硫酸铜溶液中溶质的质量分数为_________(写出计算过程)。
23.(2020·内蒙古·兴安盟教师发展中心中考真题)为测定某CuSO4溶液中溶质的质量分数,取150gCuSO4溶液,平均分为三份,每一份样品均按如图所示进行实验,实验数据见下表。请计算:
实验1 实验2 实验3
样品质量/g 50 50 50
NaOH溶液质量/g 20 40 60
m/g 44.9 49.8 49.8
(1)50gCuSO4溶液完全反应时,所得沉淀的质量为______________g。
(2)CuSO4溶液中溶质的质量分数。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.D
3.B
4.C
5.A
6.A
7.B
8.D
9.D
10.A
11.B
12.A
13.(1)铵态氮肥和碱性物质混合能生成氨气,从而降低肥效(2)增强水的导电性
14. BaCO3 NaHSO4 有气泡产生 产生白色沉淀 Cl- Na+ CO32-
15. 氨气易溶于水,溶液显碱性 浓盐酸易挥发出氯化氢气体,氯化氢气体能与氨气化合生成了氯化铵颗粒
16. CO2 CuSO4 ③
17. CuCl2 溶液变浅绿色,有气体生成 氢离子和氢氧根离子生成水 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH 复分解反应
18. 氢氧化钠与二氧化碳反应,消耗瓶内二氧化碳,气压减小 向外拉注射器 3 二氧化碳 二氧化碳能与氢氧化钠反应
19. 石灰水变浑浊 氧化钙和水反应生成的氢氧化钙是微溶物质,加入一定量的水后,有白色不溶物也可能是氢氧化钙; 取样品,加入足量的盐酸,有气体产生,证明有碳酸钙
20.(1)反应生成的二氧化碳部分留在装置中
(2)打开ab,关闭c
(3)偏低
(4)反应后没有鼓入足量的空气
21.(1)4.4(2)10.6%
22.(1)25(2)16%
23.(1)9.8g (2)32%
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
