化学人教版(2019)必修第一册2.2.氯及其化合物(共22张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册2.2.氯及其化合物(共22张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 659.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-16 00:00:00 | ||
图片预览





文档简介
(共22张PPT)
氯及其化合物
Contents
氯气
01
次氯酸
02
液氯、新制氯水、久置氯水比较
03
目录
氯气的发现
1810年,戴维经过大量实验研究,才确认这种气体是只有一种元素组成的单质。他将这种元素命名为Chlorine(希腊文),有绿色的意思。
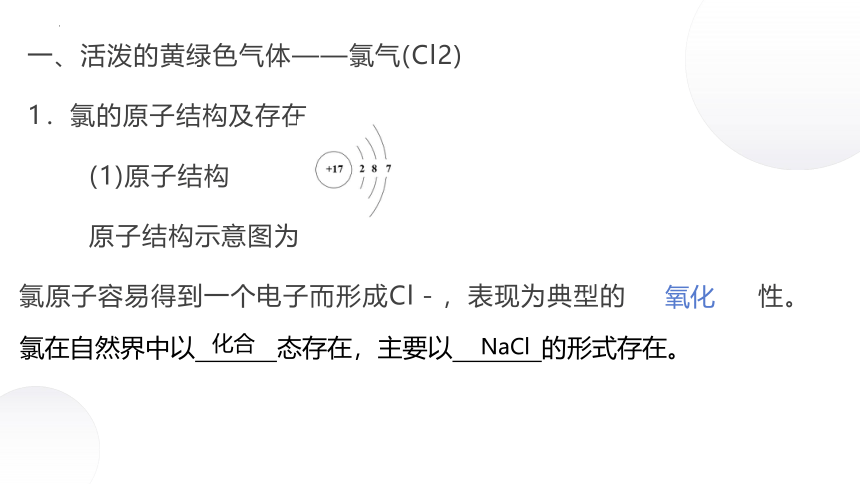
一、活泼的黄绿色气体——氯气(Cl2)
1.氯的原子结构及存在
(1)原子结构
原子结构示意图为
氯原子容易得到一个电子而形成Cl-,表现为典型的 性。
氧化
氯在自然界中以 态存在,主要以 的形式存在。
化合
NaCl
2.物理性质
颜色 状态 气味 溶解性
黄绿色 气体 刺激性 气味 1体积水溶解
2 体积氯气
氯气的密度比空气大,在低温和加压的条件下可以转化成液氯(液态),可存储于钢瓶中,便于运输和使用。
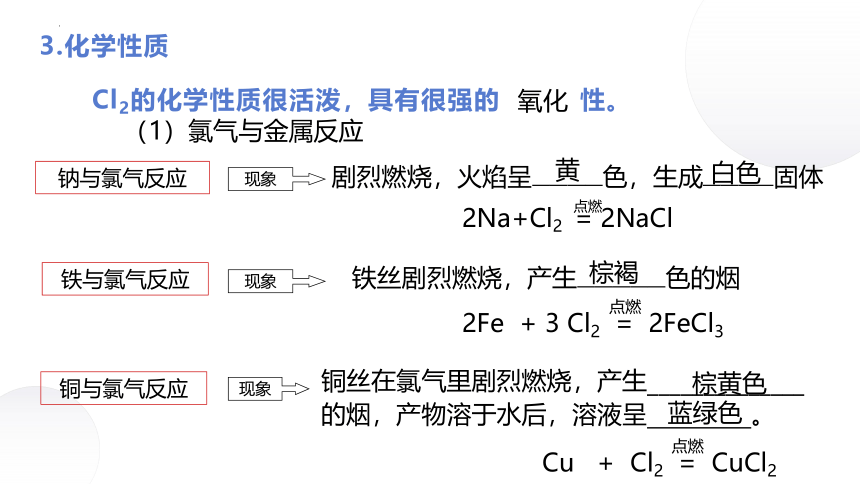
3.化学性质
Cl2的化学性质很活泼,具有很强的 性。
氧化
铜与氯气反应
铜丝在氯气里剧烈燃烧,产生______________ 的烟,产物溶于水后,溶液呈 。
现象
Cu + Cl2 = CuCl2
点燃
铁与氯气反应
铁丝剧烈燃烧,产生—————色的烟
棕褐
钠与氯气反应
剧烈燃烧,火焰呈————色,生成————固体
2Na+Cl2 = 2NaCl
点燃
2Fe + 3 Cl2 = 2FeCl3
点燃
白色
黄
(1)氯气与金属反应
现象
棕黄色
蓝绿色
现象
【讨论】
硫和氯气都能分别与铜、铁反应,试比较反应有何异同。
结论:氯气的氧化性比硫强
Fe + S = FeS
△
硫是氧化剂
2Cu + S = Cu2S
△
生成低价的金属硫化物
+1
+2
Cu + Cl2 = CuCl2
点燃
2Fe + 3Cl2 = 2FeCl3
△
氯气是氧化剂
生成高价的金属氯化物
+2
+3
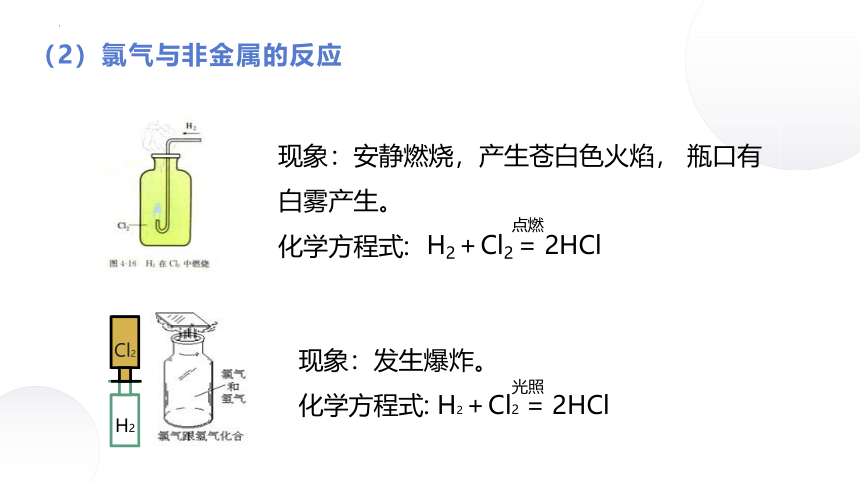
(2)氯气与非金属的反应
H2+Cl2===2HCl
点燃
H2
Cl2
现象:发生爆炸。
化学方程式: H2+Cl2 = 2HCl
光照
现象:安静燃烧,产生苍白色火焰, 瓶口有白雾产生。
化学方程式:
H2+Cl2 = 2HCl
点燃
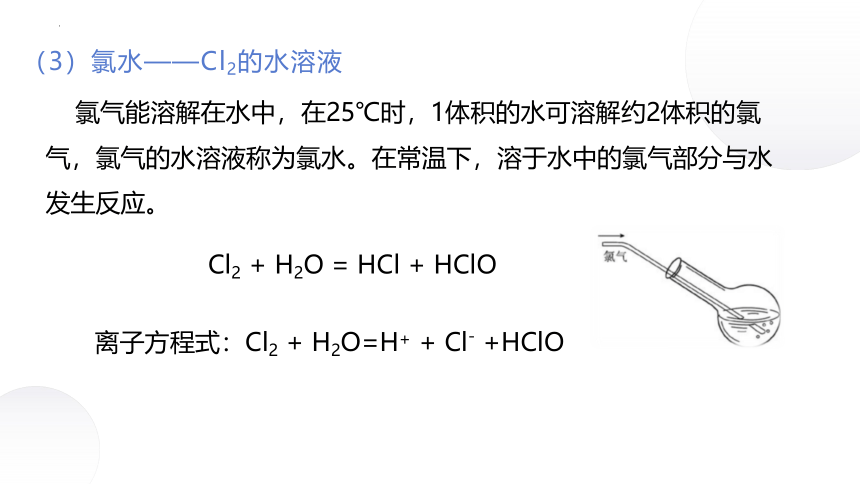
(3)氯水——Cl2的水溶液
氯气能溶解在水中,在25℃时,1体积的水可溶解约2体积的氯气,氯气的水溶液称为氯水。在常温下,溶于水中的氯气部分与水发生反应。
Cl2 + H2O = HCl + HClO
离子方程式:Cl2 + H2O=H+ + Cl- +HClO
(4)与碱反应
将氯气通入NaOH溶液中,即可得到漂白液,也就是我们平时所说的84消毒液。其主要成分是氯化钠和次氯酸钠,但有效成分为次氯酸钠。
Cl2+2NaOH=NaCl+NaClO+H2O
如果换用成本更低廉的氢氧化钙(事实上使用的是石灰浆),可得到漂白粉。漂白粉的主要成分是氯化钙和次氯酸钙,有效成分为次氯酸钙。
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
1.制备氯化物时,常用两种方法:①用金属与氯气直接化合制得②用金属与盐酸反应制得。用以上两种方法都可制得的氯化物是( )
A.AlCl3 B.FeCl3 C.FeCl2 D.CuCl2
A
【典型例题】
2.氯气是一种重要的化工原料,下列关于氯气的叙述中,不正确的是( )
①氯气是一种黄绿色、有刺激性气味的气体
②氯气能溶于水
③氯气、液氯和氯水是同一种物质
④铜丝在氯气中燃烧,生成蓝色的氯化铜
⑤氢气在氯气中燃烧,产生苍白色火焰
⑥新制的氯水显酸性,向其中滴加少量紫色石蕊试液后溶液呈红色
A.①② B.③④⑥ C.③⑤⑥ D.③⑥
【典型例题】
B
二、次氯酸
1.弱酸性
次氯酸是一元弱酸,HClO H++ClO-
2.强氧化性
生活中利用次氯酸的强氧化性不仅可以用作棉、麻和纸张等物质的漂白剂,而且还可以利用其强氧化性,杀死水中的细菌,起消毒作用。很多自来水厂用氯气来杀菌、消毒,其实就是氯水中次氯酸在起作用。
3.不稳定性
次氯酸不稳定,容易分解放出氧气。当氯水受到日光照射时,次氯酸分解加快。
2HClO = 2HCl+O2↑
次氯酸难以保存,使用起来很不方便,效果也不理想。在潮湿的环境下,漂白粉易与空气中的二氧化碳发生反应而变质。
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
光照
【思考】
漂白粉露置于空气中会变质,发生的主要反应有哪些?
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
2HClO = 2HCl+O2↑
氯水的漂白作用的探究
实验操作 实现现象 结论
有色布条 干燥的Cl2 漂白作用
有色布条 氯水有漂白作用
起漂白作用的是
不褪色
褪色
没有
HClO
1.下列有关次氯酸的叙述不正确的是( )
A.次氯酸不稳定,易分解
B.次氯酸是一种强氧化剂
C.次氯酸是弱酸,但酸性比碳酸强
D.次氯酸能使染料和有机色质褪色
【典型例题】
C
【典型例题】
2.下列叙述不正确的是( )
A.铜在氯气中燃烧,产生棕黄色烟,产物溶于水,溶液呈蓝绿色
B.新制的氯水是黄绿色透明的液体,有酸性和漂白性
C.光照氯水有气泡逸出,该气体是O2
D.新制的氯水中只含Cl2和H2O分子
D
三、液氯、新制氯水、久置氯水比较
液氯 新制氯水 久置氯水
颜色、状态
主要存在 的微粒
物质的类别
遇干燥的蓝色石蕊试纸
Cl2分子
Cl2、H2O、HClO
Cl-、H+、ClO-、OH-
H2O、OH-
Cl-、 H+
无明显变化
先变红后褪色
变红
黄绿色液体
淡黄绿色液体
无色液体
纯净物
混合物
混合物
【思考】检验新制氯水中的微粒
检验微粒 选择试剂 现象 离子方程式
Cl- AgNO3溶液
Cl2 淀粉KI溶液
H+ NaHCO3固体
Cl2 FeCl2溶液
H+ HClO 石蕊试液
Cl2 SO2
白色沉淀
溶液呈蓝色
气泡产生
溶液呈棕黄色
先红后褪色
氯水颜色变浅
Ag++ Cl- = AgCl↓
2I- +Cl2=I2+2Cl-
HCO3- + H+=H2O+CO2↑
2Fe2++ Cl2=2Fe3++2Cl-
SO2+Cl2+2H2O=4H++SO42-+2Cl-
1.探究新制饱和氯水成分的实验中,根据实验现象得出的结论正确的是( )
A.新制饱和氯水使红玫瑰变为白玫瑰,说明含有Cl2
B.加入石蕊溶液,溶液变红,说明该溶液不含HClO
C.光照新制氯水有气泡逸出,该气体是氧气
D.向氯水中加入KHCO3粉末,有气泡产生,说明氯水中含有HClO
【典型例题】
C
2.下列关于液氯和氯水的叙述中正确的是( )
A.液氯是纯净物,而氯水是混合物
B.液氯与氯水均有酸性
C.液氯较氯水的漂白作用更强
D.液氯无色,氯水呈黄绿色
【典型例题】
A
氯及其化合物
Contents
氯气
01
次氯酸
02
液氯、新制氯水、久置氯水比较
03
目录
氯气的发现
1810年,戴维经过大量实验研究,才确认这种气体是只有一种元素组成的单质。他将这种元素命名为Chlorine(希腊文),有绿色的意思。
一、活泼的黄绿色气体——氯气(Cl2)
1.氯的原子结构及存在
(1)原子结构
原子结构示意图为
氯原子容易得到一个电子而形成Cl-,表现为典型的 性。
氧化
氯在自然界中以 态存在,主要以 的形式存在。
化合
NaCl
2.物理性质
颜色 状态 气味 溶解性
黄绿色 气体 刺激性 气味 1体积水溶解
2 体积氯气
氯气的密度比空气大,在低温和加压的条件下可以转化成液氯(液态),可存储于钢瓶中,便于运输和使用。
3.化学性质
Cl2的化学性质很活泼,具有很强的 性。
氧化
铜与氯气反应
铜丝在氯气里剧烈燃烧,产生______________ 的烟,产物溶于水后,溶液呈 。
现象
Cu + Cl2 = CuCl2
点燃
铁与氯气反应
铁丝剧烈燃烧,产生—————色的烟
棕褐
钠与氯气反应
剧烈燃烧,火焰呈————色,生成————固体
2Na+Cl2 = 2NaCl
点燃
2Fe + 3 Cl2 = 2FeCl3
点燃
白色
黄
(1)氯气与金属反应
现象
棕黄色
蓝绿色
现象
【讨论】
硫和氯气都能分别与铜、铁反应,试比较反应有何异同。
结论:氯气的氧化性比硫强
Fe + S = FeS
△
硫是氧化剂
2Cu + S = Cu2S
△
生成低价的金属硫化物
+1
+2
Cu + Cl2 = CuCl2
点燃
2Fe + 3Cl2 = 2FeCl3
△
氯气是氧化剂
生成高价的金属氯化物
+2
+3
(2)氯气与非金属的反应
H2+Cl2===2HCl
点燃
H2
Cl2
现象:发生爆炸。
化学方程式: H2+Cl2 = 2HCl
光照
现象:安静燃烧,产生苍白色火焰, 瓶口有白雾产生。
化学方程式:
H2+Cl2 = 2HCl
点燃
(3)氯水——Cl2的水溶液
氯气能溶解在水中,在25℃时,1体积的水可溶解约2体积的氯气,氯气的水溶液称为氯水。在常温下,溶于水中的氯气部分与水发生反应。
Cl2 + H2O = HCl + HClO
离子方程式:Cl2 + H2O=H+ + Cl- +HClO
(4)与碱反应
将氯气通入NaOH溶液中,即可得到漂白液,也就是我们平时所说的84消毒液。其主要成分是氯化钠和次氯酸钠,但有效成分为次氯酸钠。
Cl2+2NaOH=NaCl+NaClO+H2O
如果换用成本更低廉的氢氧化钙(事实上使用的是石灰浆),可得到漂白粉。漂白粉的主要成分是氯化钙和次氯酸钙,有效成分为次氯酸钙。
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
1.制备氯化物时,常用两种方法:①用金属与氯气直接化合制得②用金属与盐酸反应制得。用以上两种方法都可制得的氯化物是( )
A.AlCl3 B.FeCl3 C.FeCl2 D.CuCl2
A
【典型例题】
2.氯气是一种重要的化工原料,下列关于氯气的叙述中,不正确的是( )
①氯气是一种黄绿色、有刺激性气味的气体
②氯气能溶于水
③氯气、液氯和氯水是同一种物质
④铜丝在氯气中燃烧,生成蓝色的氯化铜
⑤氢气在氯气中燃烧,产生苍白色火焰
⑥新制的氯水显酸性,向其中滴加少量紫色石蕊试液后溶液呈红色
A.①② B.③④⑥ C.③⑤⑥ D.③⑥
【典型例题】
B
二、次氯酸
1.弱酸性
次氯酸是一元弱酸,HClO H++ClO-
2.强氧化性
生活中利用次氯酸的强氧化性不仅可以用作棉、麻和纸张等物质的漂白剂,而且还可以利用其强氧化性,杀死水中的细菌,起消毒作用。很多自来水厂用氯气来杀菌、消毒,其实就是氯水中次氯酸在起作用。
3.不稳定性
次氯酸不稳定,容易分解放出氧气。当氯水受到日光照射时,次氯酸分解加快。
2HClO = 2HCl+O2↑
次氯酸难以保存,使用起来很不方便,效果也不理想。在潮湿的环境下,漂白粉易与空气中的二氧化碳发生反应而变质。
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
光照
【思考】
漂白粉露置于空气中会变质,发生的主要反应有哪些?
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO
2HClO = 2HCl+O2↑
氯水的漂白作用的探究
实验操作 实现现象 结论
有色布条 干燥的Cl2 漂白作用
有色布条 氯水有漂白作用
起漂白作用的是
不褪色
褪色
没有
HClO
1.下列有关次氯酸的叙述不正确的是( )
A.次氯酸不稳定,易分解
B.次氯酸是一种强氧化剂
C.次氯酸是弱酸,但酸性比碳酸强
D.次氯酸能使染料和有机色质褪色
【典型例题】
C
【典型例题】
2.下列叙述不正确的是( )
A.铜在氯气中燃烧,产生棕黄色烟,产物溶于水,溶液呈蓝绿色
B.新制的氯水是黄绿色透明的液体,有酸性和漂白性
C.光照氯水有气泡逸出,该气体是O2
D.新制的氯水中只含Cl2和H2O分子
D
三、液氯、新制氯水、久置氯水比较
液氯 新制氯水 久置氯水
颜色、状态
主要存在 的微粒
物质的类别
遇干燥的蓝色石蕊试纸
Cl2分子
Cl2、H2O、HClO
Cl-、H+、ClO-、OH-
H2O、OH-
Cl-、 H+
无明显变化
先变红后褪色
变红
黄绿色液体
淡黄绿色液体
无色液体
纯净物
混合物
混合物
【思考】检验新制氯水中的微粒
检验微粒 选择试剂 现象 离子方程式
Cl- AgNO3溶液
Cl2 淀粉KI溶液
H+ NaHCO3固体
Cl2 FeCl2溶液
H+ HClO 石蕊试液
Cl2 SO2
白色沉淀
溶液呈蓝色
气泡产生
溶液呈棕黄色
先红后褪色
氯水颜色变浅
Ag++ Cl- = AgCl↓
2I- +Cl2=I2+2Cl-
HCO3- + H+=H2O+CO2↑
2Fe2++ Cl2=2Fe3++2Cl-
SO2+Cl2+2H2O=4H++SO42-+2Cl-
1.探究新制饱和氯水成分的实验中,根据实验现象得出的结论正确的是( )
A.新制饱和氯水使红玫瑰变为白玫瑰,说明含有Cl2
B.加入石蕊溶液,溶液变红,说明该溶液不含HClO
C.光照新制氯水有气泡逸出,该气体是氧气
D.向氯水中加入KHCO3粉末,有气泡产生,说明氯水中含有HClO
【典型例题】
C
2.下列关于液氯和氯水的叙述中正确的是( )
A.液氯是纯净物,而氯水是混合物
B.液氯与氯水均有酸性
C.液氯较氯水的漂白作用更强
D.液氯无色,氯水呈黄绿色
【典型例题】
A
