鲁教版化学九年级上册4.3.1氧气课件(共16张PPT)
文档属性
| 名称 | 鲁教版化学九年级上册4.3.1氧气课件(共16张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 541.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-16 00:00:00 | ||
图片预览




文档简介
(共16张PPT)
4.3氧气第一课时
九年级
学习目标
1.了解氧气的主要物理性质。
2.掌握氧气的检验方法,知道碳、硫、铁在氧气中燃烧的实验现象,能够写出这些反应的文字表达式;知道氧气具有氧化性。
3.掌握化合反应的特点并能利用该特点对反应的类型进行准确地判断,掌握化合反应、氧化反应、缓慢氧化等概念之间的区别与联系。
4.知道氧化反应有剧烈和缓慢之分,并能举出相应的反应实例。
①色、味、态:
②密度:
③水溶性:
④熔沸点:
一般指颜色、状态、气味、熔点、沸点、硬度和密度、是否溶于水等。
不易溶于水
1、物理性质
气体物理性质的归纳一般包含三部分: ①色、味、态②密度③水溶性
一、氧气的性质
比空气密度略大
无色无味气体(标准状况)
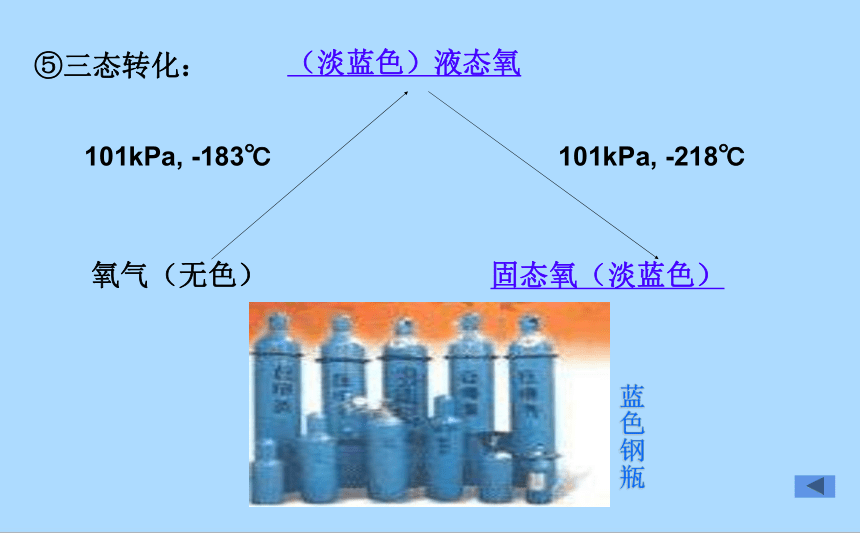
固态氧(淡蓝色)
氧气(无色)
(淡蓝色)液态氧
101kPa, -218℃
101kPa, -183℃
蓝色钢瓶
⑤三态转化:
把带有火星的木条伸到盛有氧气的集气瓶中,观察木条是否燃烧
二、氧气的检验
现象:带火星的木条复燃
说明:氧气能支持燃烧,有助燃性。 (这是特性)
【归纳】用什么简单的方法检验一瓶无色气体是氧气?
明确:将带火星的木条伸入集气瓶中,如果带火星的木条复燃,则证明瓶中气体是氧气
实验现象
实验操作
结论
【归纳】用什么简单的方法检验一瓶氧气已经收集满?
明确:将带火星的木条伸入集气瓶口,如果带火星的木条复燃,则证明瓶中氧气已收集满
实验现象
实验操作
结论
三、化学性质
(1)硫(淡黄色固体)与氧气反应(实验2—3)
观察实验的程序:
反应物质的色、态、味,反应条件和操作,
反应生成的物质的色、态、味及伴随出现的现象。
在空气中燃烧
在氧气中燃烧
【现象】1、产生微弱的淡蓝色火焰
2、放热
3、生成有刺激性气味气体
【现象】 1、发出明亮的蓝紫色火焰
2、放热
3、生成有刺激性气味气体
硫 + 氧气 → 二氧化硫
点燃
硫在氧气中燃烧
硫在空气中燃烧
文字表达式:
S + O2 → SO2
点燃
—溶解吸收二氧化硫(SO2) ,防止二氧化硫逸出污染空气
思考: 硫在氧气里燃烧,为什么集气瓶底要留少量水?
(2)木炭(灰黑色固体)与氧气反应
【现象】1、发出红光
2、放热
3、生成了一种能够使澄清石灰水变浑浊的无色气体
【现象】1、发出白光
2、放热
3、生成了一种能够使澄清石灰 水变浑浊的无色气体
木炭在氧气中燃烧
木炭在空气中燃烧
文字表达式:
碳 + 氧气
二氧化碳
点燃
C + O2
CO2
点燃
说明燃烧的剧烈程度跟氧气的含量有关,氧气含量越高,燃烧越剧烈。
思考:木炭和硫分别在空气里燃烧和在氧气里燃烧的现象不同,这说明什么?
(3)铁丝(银白色色固体)与氧气反应(实验2-4)
在氧气中:铁丝剧烈燃烧,
火星四射,
放出热量,
生成黑色固体。
在空气中:铁丝不能燃烧,
发生红热现象。
文字表达式:
铁 + 氧气
四氧化三铁
点燃
Fe + O2
Fe3O4
点燃
引燃铁丝。增大与氧气的接触面积聚热使铁丝容易燃烧。
为了防止燃烧时溅落的熔融物炸裂瓶底。
思考: (1)做这个实验时,为了实验成功,铁丝上为什么系一根火柴棒?还要将铁丝绕成螺旋状,为什么?
思考:(2)实验前为什么在瓶底放一些水或铺一层细沙?
小结:
①可燃物在氧气中燃烧比在空气中燃烧更剧烈。
②物质在空气中燃烧实质上是与空气中的氧气发生反应。
③氧气是一种化学性质比较活泼的气体,能与大多数物质发生反应。
④一些不能在空气中燃烧的物质(铁、铜等)能在氧气中燃烧,说明氧气具有很强的助燃性
小结
1、物理性质
氧气在通常状况下是无色无味的气体,不易溶于水,密度比空气略大。
2、化学性质
氧气是一种化学性质比较活泼的气体。具有氧化性,是一种常见的氧化剂。具有助燃性,能支持燃烧。
祝同学们学习愉快!
4.3氧气第一课时
九年级
学习目标
1.了解氧气的主要物理性质。
2.掌握氧气的检验方法,知道碳、硫、铁在氧气中燃烧的实验现象,能够写出这些反应的文字表达式;知道氧气具有氧化性。
3.掌握化合反应的特点并能利用该特点对反应的类型进行准确地判断,掌握化合反应、氧化反应、缓慢氧化等概念之间的区别与联系。
4.知道氧化反应有剧烈和缓慢之分,并能举出相应的反应实例。
①色、味、态:
②密度:
③水溶性:
④熔沸点:
一般指颜色、状态、气味、熔点、沸点、硬度和密度、是否溶于水等。
不易溶于水
1、物理性质
气体物理性质的归纳一般包含三部分: ①色、味、态②密度③水溶性
一、氧气的性质
比空气密度略大
无色无味气体(标准状况)
固态氧(淡蓝色)
氧气(无色)
(淡蓝色)液态氧
101kPa, -218℃
101kPa, -183℃
蓝色钢瓶
⑤三态转化:
把带有火星的木条伸到盛有氧气的集气瓶中,观察木条是否燃烧
二、氧气的检验
现象:带火星的木条复燃
说明:氧气能支持燃烧,有助燃性。 (这是特性)
【归纳】用什么简单的方法检验一瓶无色气体是氧气?
明确:将带火星的木条伸入集气瓶中,如果带火星的木条复燃,则证明瓶中气体是氧气
实验现象
实验操作
结论
【归纳】用什么简单的方法检验一瓶氧气已经收集满?
明确:将带火星的木条伸入集气瓶口,如果带火星的木条复燃,则证明瓶中氧气已收集满
实验现象
实验操作
结论
三、化学性质
(1)硫(淡黄色固体)与氧气反应(实验2—3)
观察实验的程序:
反应物质的色、态、味,反应条件和操作,
反应生成的物质的色、态、味及伴随出现的现象。
在空气中燃烧
在氧气中燃烧
【现象】1、产生微弱的淡蓝色火焰
2、放热
3、生成有刺激性气味气体
【现象】 1、发出明亮的蓝紫色火焰
2、放热
3、生成有刺激性气味气体
硫 + 氧气 → 二氧化硫
点燃
硫在氧气中燃烧
硫在空气中燃烧
文字表达式:
S + O2 → SO2
点燃
—溶解吸收二氧化硫(SO2) ,防止二氧化硫逸出污染空气
思考: 硫在氧气里燃烧,为什么集气瓶底要留少量水?
(2)木炭(灰黑色固体)与氧气反应
【现象】1、发出红光
2、放热
3、生成了一种能够使澄清石灰水变浑浊的无色气体
【现象】1、发出白光
2、放热
3、生成了一种能够使澄清石灰 水变浑浊的无色气体
木炭在氧气中燃烧
木炭在空气中燃烧
文字表达式:
碳 + 氧气
二氧化碳
点燃
C + O2
CO2
点燃
说明燃烧的剧烈程度跟氧气的含量有关,氧气含量越高,燃烧越剧烈。
思考:木炭和硫分别在空气里燃烧和在氧气里燃烧的现象不同,这说明什么?
(3)铁丝(银白色色固体)与氧气反应(实验2-4)
在氧气中:铁丝剧烈燃烧,
火星四射,
放出热量,
生成黑色固体。
在空气中:铁丝不能燃烧,
发生红热现象。
文字表达式:
铁 + 氧气
四氧化三铁
点燃
Fe + O2
Fe3O4
点燃
引燃铁丝。增大与氧气的接触面积聚热使铁丝容易燃烧。
为了防止燃烧时溅落的熔融物炸裂瓶底。
思考: (1)做这个实验时,为了实验成功,铁丝上为什么系一根火柴棒?还要将铁丝绕成螺旋状,为什么?
思考:(2)实验前为什么在瓶底放一些水或铺一层细沙?
小结:
①可燃物在氧气中燃烧比在空气中燃烧更剧烈。
②物质在空气中燃烧实质上是与空气中的氧气发生反应。
③氧气是一种化学性质比较活泼的气体,能与大多数物质发生反应。
④一些不能在空气中燃烧的物质(铁、铜等)能在氧气中燃烧,说明氧气具有很强的助燃性
小结
1、物理性质
氧气在通常状况下是无色无味的气体,不易溶于水,密度比空气略大。
2、化学性质
氧气是一种化学性质比较活泼的气体。具有氧化性,是一种常见的氧化剂。具有助燃性,能支持燃烧。
祝同学们学习愉快!
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
