鲁教版化学九年级下册8.2.1海水“晒盐”课件(共22张PPT)
文档属性
| 名称 | 鲁教版化学九年级下册8.2.1海水“晒盐”课件(共22张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-16 00:00:00 | ||
图片预览






文档简介
(共22张PPT)
8.2 海水“晒盐”
九年级
【学习目标】
1.知道蒸发结晶是海水晒盐的基本原理,是结晶的途径之一。
理解结晶的概念。
2.知道饱和溶液和不饱和溶液之间的转化的方法,理解饱和
溶液和不饱和溶液的概念。
【教学重点、难点】
1.理解饱和溶液的概念 。
2.理解饱和溶液和不饱和溶液之间的转化。
走近生活
1、一杯水中是否能无限的溶解蔗糖?
2、你怎样才能做成一杯比较甜的糖水?
3、你是如何判断你做成的糖水是最甜的?
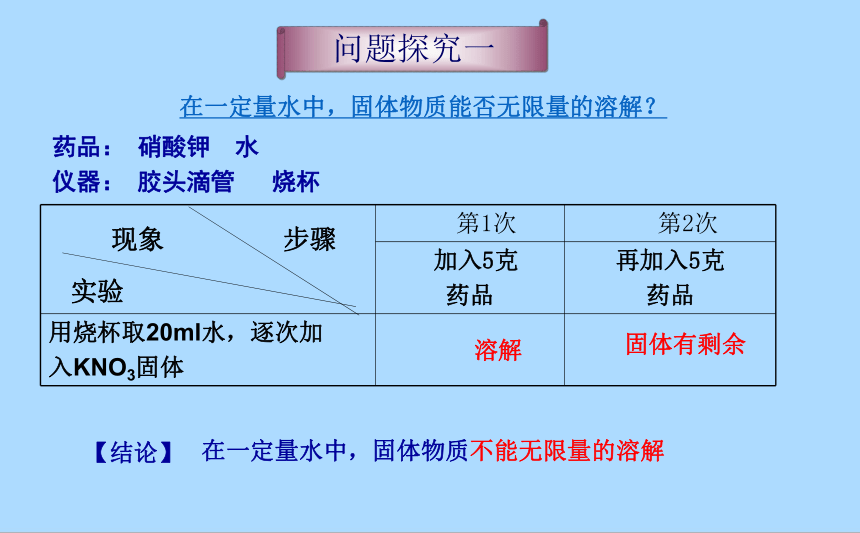
在一定量水中,固体物质能否无限量的溶解?
药品: 硝酸钾 水
仪器: 胶头滴管 烧杯
第1次 第2次
加入5克
药品 再加入5克
药品
用烧杯取20ml水,逐次加
入KNO3固体
问题探究一
现象
步骤
实验
溶解
固体有剩余
【结论】
在一定量水中,固体物质不能无限量的溶解
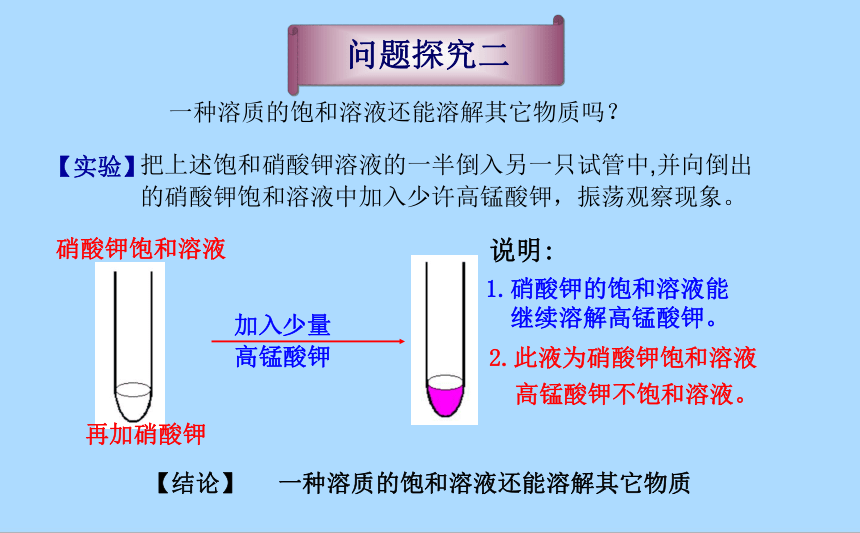
硝酸钾饱和溶液
加入少量
高锰酸钾
说明:
1.硝酸钾的饱和溶液能
继续溶解高锰酸钾。
2.此液为硝酸钾饱和溶液
高锰酸钾不饱和溶液。
再加硝酸钾
问题探究二
一种溶质的饱和溶液还能溶解其它物质吗?
把上述饱和硝酸钾溶液的一半倒入另一只试管中,并向倒出
的硝酸钾饱和溶液中加入少许高锰酸钾,振荡观察现象。
【实验】
【结论】
一种溶质的饱和溶液还能溶解其它物质
根据以上认识,你能说说什么是饱和溶液、不饱和溶液吗?
总结提升
饱和溶液 在一定温度下,在一定量的溶剂里,不能再继续溶解某种溶质的溶液就是该溶质的饱和溶液。
不饱和溶液 一定温度下,一定量的溶剂里,还能继续溶解某种溶质的溶液,叫做这种溶质的不饱和溶液。
溶液的饱和状态受哪些因素的影响?
实验 操 作 现象
KNO3饱和溶液
KNO3饱和溶液
加热
想办法,使未溶解的KNO3固体继续溶解
问题探究三
未溶解的KNO3继续溶解
加水
未溶解的KNO3继续溶解
影响溶液的饱和状态的因素有:
【结论】
温度、溶剂的量
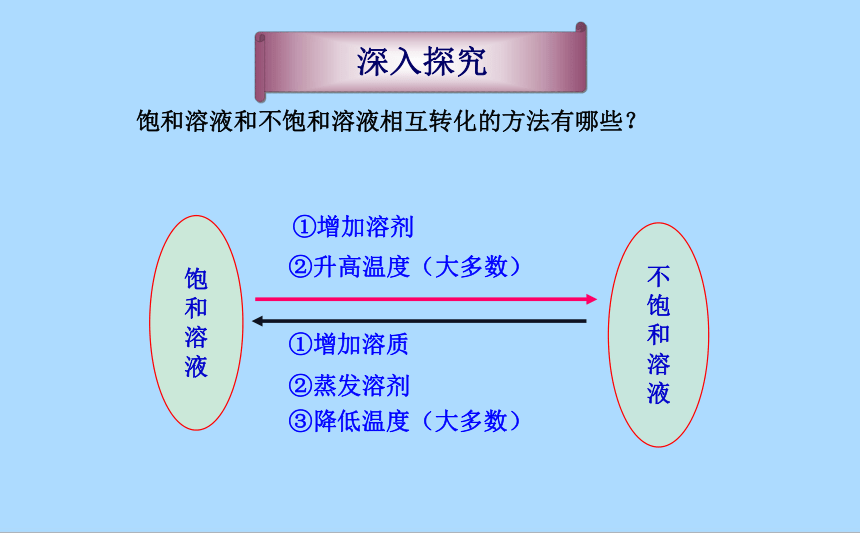
①增加溶质
③降低温度(大多数)
②蒸发溶剂
①增加溶剂
②升高温度(大多数)
深入探究
饱和溶液和不饱和溶液相互转化的方法有哪些?
饱
和
溶
液
不
饱
和
溶
液
怎样判断溶液是否达到饱和状态?
如果溶液中有未溶解的固体存在,
如果溶液中没有固体剩余,
则此时的溶液已经达到饱和状态。
再向溶液中加入 同种溶质看是否继续溶解,若不再继续溶解,则
此时的溶液已经达到饱和状态。
【交流讨论】
如何将一杯接近饱和的食盐溶液,转化成饱和的食盐溶液 你有哪些方法呢
不饱和食
盐溶液
饱和食
盐溶液
蒸发水分、降低温度、加入食盐
阅读教材的内容,回答下列问题:
1、目前,从海水中提取食盐的方法是什么?
2、“盐田法”通常由几部分组成?
3、海水“晒盐”的过程是什么?
【自学指导】
海 水
蒸发池
结晶池
母 液
粗 盐
海水晒盐的过程是怎样的?
阅读与思考
“盐田法”(“太阳能蒸发法”)
风吹
日晒
风吹
日晒
从获得饱和食盐溶液的方法来看,与海水“晒盐”有什么不同?
⑴海水“晒盐”
是利用的_________方法获得食盐饱和溶液。
⑵获得饱和食盐溶液
是用的_______________________________方法获得食盐饱和溶液。
蒸发水分
蒸发水分、降低温度、加入食盐
【交流讨论】
1、取一滴管食盐饱和溶液,滴在结晶皿中。
2、把结晶皿放在垫有石棉网的三脚架上,加热。
如何从食盐溶液中得到食盐固体呢?
结晶皿
问题探究四
食盐晶体
硫酸亚铁晶体
晶体:具有规则几何外形的固体。
蓝矾晶体
结晶:固体物质从它的饱和溶液中以晶体的形式析出的过程叫做结晶
【蒸发结晶】
海水
食盐饱和溶液
析出晶体
蒸发水分
继续蒸发
【人类“制盐”的历程】
古代 “煮盐”
现代 “制盐”
近代 “晒盐”
海水“晒盐”
海水“晒盐”的过程及原理
蒸发
结晶
人类”制
盐”的历程
海水“晒盐”的过程及原理
蒸发
结晶
人类”制
盐”的历程
饱和溶液的定义、配制、判断、与不饱和溶液的转化
【总结升华】
1、下列关于海水晒盐原理的分析 ,你认为正确的是 ( )
A.利用阳光照射使海水升温得到食盐
B.利用海风降温析出食盐
C.利用阳光和风力使水分蒸发得到食盐
D.利用阳光分解海水得到食盐
C
2、使一杯接近饱和的硝酸钾溶液变饱和,下列措施中错误的是( )
A.加入适量的硝酸钾固体
B.蒸发掉一部分水
C.降温至有固体析出
D.升高温度
D
如果将咸菜放置在空气中,过一段时间发现咸菜的表面有一层白色晶体析出。请简要解释其原因。
走进生活
在空气中水分的蒸发,使溶剂减少,咸菜里的盐以晶体的形式析出,主要成分为NaCl晶体,还有少量其它盐晶体。所以会有白色晶体。
走进生活
走进生活
祝同学们学习愉快!
8.2 海水“晒盐”
九年级
【学习目标】
1.知道蒸发结晶是海水晒盐的基本原理,是结晶的途径之一。
理解结晶的概念。
2.知道饱和溶液和不饱和溶液之间的转化的方法,理解饱和
溶液和不饱和溶液的概念。
【教学重点、难点】
1.理解饱和溶液的概念 。
2.理解饱和溶液和不饱和溶液之间的转化。
走近生活
1、一杯水中是否能无限的溶解蔗糖?
2、你怎样才能做成一杯比较甜的糖水?
3、你是如何判断你做成的糖水是最甜的?
在一定量水中,固体物质能否无限量的溶解?
药品: 硝酸钾 水
仪器: 胶头滴管 烧杯
第1次 第2次
加入5克
药品 再加入5克
药品
用烧杯取20ml水,逐次加
入KNO3固体
问题探究一
现象
步骤
实验
溶解
固体有剩余
【结论】
在一定量水中,固体物质不能无限量的溶解
硝酸钾饱和溶液
加入少量
高锰酸钾
说明:
1.硝酸钾的饱和溶液能
继续溶解高锰酸钾。
2.此液为硝酸钾饱和溶液
高锰酸钾不饱和溶液。
再加硝酸钾
问题探究二
一种溶质的饱和溶液还能溶解其它物质吗?
把上述饱和硝酸钾溶液的一半倒入另一只试管中,并向倒出
的硝酸钾饱和溶液中加入少许高锰酸钾,振荡观察现象。
【实验】
【结论】
一种溶质的饱和溶液还能溶解其它物质
根据以上认识,你能说说什么是饱和溶液、不饱和溶液吗?
总结提升
饱和溶液 在一定温度下,在一定量的溶剂里,不能再继续溶解某种溶质的溶液就是该溶质的饱和溶液。
不饱和溶液 一定温度下,一定量的溶剂里,还能继续溶解某种溶质的溶液,叫做这种溶质的不饱和溶液。
溶液的饱和状态受哪些因素的影响?
实验 操 作 现象
KNO3饱和溶液
KNO3饱和溶液
加热
想办法,使未溶解的KNO3固体继续溶解
问题探究三
未溶解的KNO3继续溶解
加水
未溶解的KNO3继续溶解
影响溶液的饱和状态的因素有:
【结论】
温度、溶剂的量
①增加溶质
③降低温度(大多数)
②蒸发溶剂
①增加溶剂
②升高温度(大多数)
深入探究
饱和溶液和不饱和溶液相互转化的方法有哪些?
饱
和
溶
液
不
饱
和
溶
液
怎样判断溶液是否达到饱和状态?
如果溶液中有未溶解的固体存在,
如果溶液中没有固体剩余,
则此时的溶液已经达到饱和状态。
再向溶液中加入 同种溶质看是否继续溶解,若不再继续溶解,则
此时的溶液已经达到饱和状态。
【交流讨论】
如何将一杯接近饱和的食盐溶液,转化成饱和的食盐溶液 你有哪些方法呢
不饱和食
盐溶液
饱和食
盐溶液
蒸发水分、降低温度、加入食盐
阅读教材的内容,回答下列问题:
1、目前,从海水中提取食盐的方法是什么?
2、“盐田法”通常由几部分组成?
3、海水“晒盐”的过程是什么?
【自学指导】
海 水
蒸发池
结晶池
母 液
粗 盐
海水晒盐的过程是怎样的?
阅读与思考
“盐田法”(“太阳能蒸发法”)
风吹
日晒
风吹
日晒
从获得饱和食盐溶液的方法来看,与海水“晒盐”有什么不同?
⑴海水“晒盐”
是利用的_________方法获得食盐饱和溶液。
⑵获得饱和食盐溶液
是用的_______________________________方法获得食盐饱和溶液。
蒸发水分
蒸发水分、降低温度、加入食盐
【交流讨论】
1、取一滴管食盐饱和溶液,滴在结晶皿中。
2、把结晶皿放在垫有石棉网的三脚架上,加热。
如何从食盐溶液中得到食盐固体呢?
结晶皿
问题探究四
食盐晶体
硫酸亚铁晶体
晶体:具有规则几何外形的固体。
蓝矾晶体
结晶:固体物质从它的饱和溶液中以晶体的形式析出的过程叫做结晶
【蒸发结晶】
海水
食盐饱和溶液
析出晶体
蒸发水分
继续蒸发
【人类“制盐”的历程】
古代 “煮盐”
现代 “制盐”
近代 “晒盐”
海水“晒盐”
海水“晒盐”的过程及原理
蒸发
结晶
人类”制
盐”的历程
海水“晒盐”的过程及原理
蒸发
结晶
人类”制
盐”的历程
饱和溶液的定义、配制、判断、与不饱和溶液的转化
【总结升华】
1、下列关于海水晒盐原理的分析 ,你认为正确的是 ( )
A.利用阳光照射使海水升温得到食盐
B.利用海风降温析出食盐
C.利用阳光和风力使水分蒸发得到食盐
D.利用阳光分解海水得到食盐
C
2、使一杯接近饱和的硝酸钾溶液变饱和,下列措施中错误的是( )
A.加入适量的硝酸钾固体
B.蒸发掉一部分水
C.降温至有固体析出
D.升高温度
D
如果将咸菜放置在空气中,过一段时间发现咸菜的表面有一层白色晶体析出。请简要解释其原因。
走进生活
在空气中水分的蒸发,使溶剂减少,咸菜里的盐以晶体的形式析出,主要成分为NaCl晶体,还有少量其它盐晶体。所以会有白色晶体。
走进生活
走进生活
祝同学们学习愉快!
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
