鲁教版化学九年级下册9.1.2常见的金属材料(共18张PPT)
文档属性
| 名称 | 鲁教版化学九年级下册9.1.2常见的金属材料(共18张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-16 00:00:00 | ||
图片预览






文档简介
(共18张PPT)
9.1.2常见的金属材料
九年级
教学目标
1、了解常见铁矿石的主要成分。
2、掌握炼铁的原理、装置、现象。
教学目标
1、了解常见铁矿石的主要成分。
2、掌握炼铁的原理、装置、现象。
2、掌握炼铁的原理、装置、现象。
1、炼铁方程式。还原反应。
2、炼铁的原理、装置、现象。
重点
难点
赤铁矿
黄铁矿
菱铁矿
辉铜矿
【活动一:认识金属矿物】
【铁的冶炼】
早在春秋战国时期,我国就开始生产和使用铁器,
从公元1世纪起,铁便成了一种最主要的金属材料。
磁铁矿(主要成分Fe3O4)
赤铁矿(主要成分Fe2O3)
菱铁矿(主要成分FeCO3)
常见的
铁矿石
黄铁矿(主要成分FeS2)
【活动二:炼铁的原理】
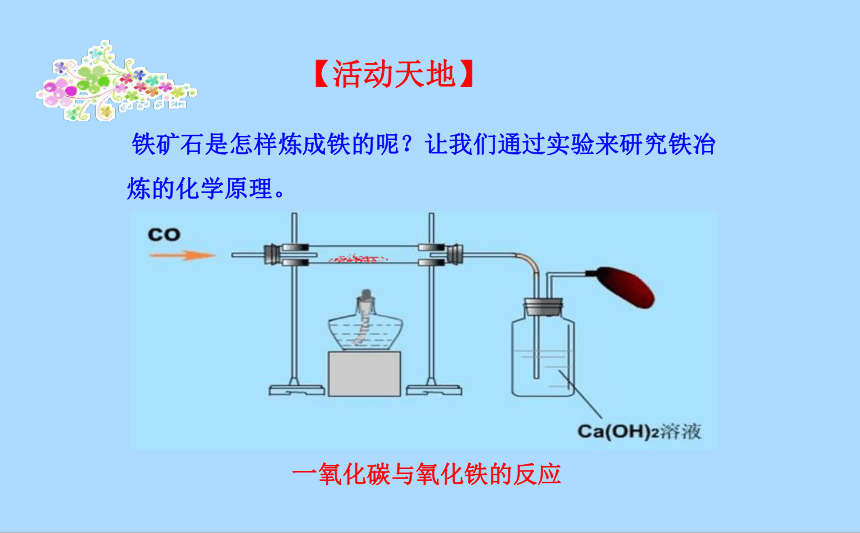
铁矿石是怎样炼成铁的呢?让我们通过实验来研究铁冶
炼的化学原理。
一氧化碳与氧化铁的反应
【活动天地】
【一氧化碳还原氧化铁实验】
(1)检查气密性
(2)装药品
(3)先通入一氧化碳;再点燃酒精喷灯;
目的:排出玻璃管中的空气,防止发生爆炸
(4)先停止加热,再通一会儿一氧化碳,直 至玻璃管冷却;目的:防止生成的铁被氧化;
Fe2O3 + 3CO === 2Fe + 3CO2
高温
1、实验原理:
2、实验操作:
巧记:一氧化碳早来晚走,酒精喷灯迟到早退
红色(氧化铁)粉末逐渐变成黑色,澄清的石灰水变浑浊。
【反应中的化学方程式】
CO2 + Ca(OH)2= CaCO3↓+ H2O
Fe2O3 + 3CO === 2Fe + 3CO2
高温
将产生的气体通入到澄清石灰水中,澄清石灰水变浑浊,则生成二氧化碳:CO2+Ca(OH)2=CaCO3↓+H2O ;红色粉末变黑色,用磁铁检验,证明黑色粉末为铁。(若用一氧化碳还原四氧化三铁,应将生成的黑色粉末加入盐酸中,若有气体生成,则证明有铁生成。由于四氧化三铁也有磁性,不能用磁铁吸引的方法检验。)
1、如何判断反应中生成了什么物质?
【交流讨论】
收集尾气,防止污染空气
2、装置中右边的气球起什么作用?
3、石灰水的作用有哪些?
澄清石灰水用来检验生成物二氧化碳,并吸收二氧化碳便于处理尾气
【交流讨论】
Fe2O3 + 3CO ==== 2Fe + 3CO2
高温
化学上把氧化物中氧被夺去的反应叫做还原反应。一氧化碳叫做还原剂,具有还原性。
【活动三:认识还原反应】
【活动四:认识高炉炼铁】
上述反应原理也用于工业炼铁。
1、原料: .
3、主要反应 .
铁矿石、焦炭、石灰石、空气
2、工业炼铁的主要设备: .
高炉
Fe2O3 + 3CO === 2Fe + 3CO2
高温
上海宝山钢铁公司炼铁高炉
【钢铁的用途】
B
(1)磁铁矿的主要成分是: ;(填化学式)
(2)写出CO与Fe2O3在高温条件下反应的化学方程式:
(3)高炉炼铁得到的主要产品是 ;(填序号)
A.纯铁 B.生铁 C.钢
Fe3O4
Fe2O3 + 3CO === 2Fe + 3CO2
高温
1、工业炼铁的主要化学反应原理;
3、反应的现象:红色(氧化铁)粉末逐渐变成黑色,澄清的石灰水变浑浊。
2、一氧化碳还原氧化铁的装置、操作注意事项;
祝同学们学习愉快!
9.1.2常见的金属材料
九年级
教学目标
1、了解常见铁矿石的主要成分。
2、掌握炼铁的原理、装置、现象。
教学目标
1、了解常见铁矿石的主要成分。
2、掌握炼铁的原理、装置、现象。
2、掌握炼铁的原理、装置、现象。
1、炼铁方程式。还原反应。
2、炼铁的原理、装置、现象。
重点
难点
赤铁矿
黄铁矿
菱铁矿
辉铜矿
【活动一:认识金属矿物】
【铁的冶炼】
早在春秋战国时期,我国就开始生产和使用铁器,
从公元1世纪起,铁便成了一种最主要的金属材料。
磁铁矿(主要成分Fe3O4)
赤铁矿(主要成分Fe2O3)
菱铁矿(主要成分FeCO3)
常见的
铁矿石
黄铁矿(主要成分FeS2)
【活动二:炼铁的原理】
铁矿石是怎样炼成铁的呢?让我们通过实验来研究铁冶
炼的化学原理。
一氧化碳与氧化铁的反应
【活动天地】
【一氧化碳还原氧化铁实验】
(1)检查气密性
(2)装药品
(3)先通入一氧化碳;再点燃酒精喷灯;
目的:排出玻璃管中的空气,防止发生爆炸
(4)先停止加热,再通一会儿一氧化碳,直 至玻璃管冷却;目的:防止生成的铁被氧化;
Fe2O3 + 3CO === 2Fe + 3CO2
高温
1、实验原理:
2、实验操作:
巧记:一氧化碳早来晚走,酒精喷灯迟到早退
红色(氧化铁)粉末逐渐变成黑色,澄清的石灰水变浑浊。
【反应中的化学方程式】
CO2 + Ca(OH)2= CaCO3↓+ H2O
Fe2O3 + 3CO === 2Fe + 3CO2
高温
将产生的气体通入到澄清石灰水中,澄清石灰水变浑浊,则生成二氧化碳:CO2+Ca(OH)2=CaCO3↓+H2O ;红色粉末变黑色,用磁铁检验,证明黑色粉末为铁。(若用一氧化碳还原四氧化三铁,应将生成的黑色粉末加入盐酸中,若有气体生成,则证明有铁生成。由于四氧化三铁也有磁性,不能用磁铁吸引的方法检验。)
1、如何判断反应中生成了什么物质?
【交流讨论】
收集尾气,防止污染空气
2、装置中右边的气球起什么作用?
3、石灰水的作用有哪些?
澄清石灰水用来检验生成物二氧化碳,并吸收二氧化碳便于处理尾气
【交流讨论】
Fe2O3 + 3CO ==== 2Fe + 3CO2
高温
化学上把氧化物中氧被夺去的反应叫做还原反应。一氧化碳叫做还原剂,具有还原性。
【活动三:认识还原反应】
【活动四:认识高炉炼铁】
上述反应原理也用于工业炼铁。
1、原料: .
3、主要反应 .
铁矿石、焦炭、石灰石、空气
2、工业炼铁的主要设备: .
高炉
Fe2O3 + 3CO === 2Fe + 3CO2
高温
上海宝山钢铁公司炼铁高炉
【钢铁的用途】
B
(1)磁铁矿的主要成分是: ;(填化学式)
(2)写出CO与Fe2O3在高温条件下反应的化学方程式:
(3)高炉炼铁得到的主要产品是 ;(填序号)
A.纯铁 B.生铁 C.钢
Fe3O4
Fe2O3 + 3CO === 2Fe + 3CO2
高温
1、工业炼铁的主要化学反应原理;
3、反应的现象:红色(氧化铁)粉末逐渐变成黑色,澄清的石灰水变浑浊。
2、一氧化碳还原氧化铁的装置、操作注意事项;
祝同学们学习愉快!
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
