单元复习与测试-2022-2023学年九年级化学上册同步精品课堂(课件21页)(鲁教版)
文档属性
| 名称 | 单元复习与测试-2022-2023学年九年级化学上册同步精品课堂(课件21页)(鲁教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-18 00:00:00 | ||
图片预览







文档简介
(共21张PPT)
单元复习与测试
第六单元 燃烧与燃料
PART
01
PART
02
从化学反应角度认识燃烧和灭火的原理;知道控制燃烧的条件就能达到促进燃烧和防火、灭火的目的。
知道化石燃料及其重要作用, 了解化石燃料综合利用的重要性,认识燃料燃烧对环境的影响及防治措施。
学习目标
PART
03
初步学习在实验室制取CO2的方法,培养分析、加工图片信息的能力,知道CO2的主要性质和用途。
【答案速填】①可燃物
②氧气
③着火点
④可燃物
⑤氧气
⑥着火点以下
一、燃烧和灭火
构建知识体系
【答案速填】
①碳
②碳、氢
③CH4+2O2点燃CO2+2H2O
④气化
⑤焦化
⑥液化
二、化学燃料的利用
【答案速填】
①化石燃料燃烧 ②光合作用
③温室效应
④大
⑤能溶
CO2+H2O===H2CO3 CO2+Ca(OH)2===
CaCO3↓+H2O
三、大自然中的二氧化碳
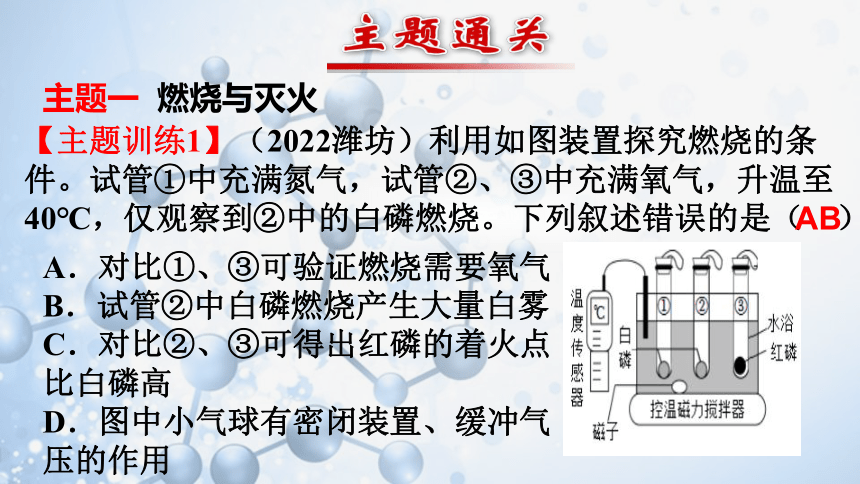
主题一 燃烧与灭火
【主题训练1】(2022潍坊)利用如图装置探究燃烧的条
件。试管①中充满氮气,试管②、③中充满氧气,升温至
40℃,仅观察到②中的白磷燃烧。下列叙述错误的是( )
A.对比①、③可验证燃烧需要氧气
B.试管②中白磷燃烧产生大量白雾
C.对比②、③可得出红磷的着火点比白磷高
D.图中小气球有密闭装置、缓冲气压的作用
AB
【关键点拨】
燃烧与灭火的关系
燃烧的条件 灭火的原理与方法
1.物质具有可燃性 → 1.隔离可燃物
2.与氧气充分接触 → 2.隔绝氧气
3.温度达到着火点 → 3.降温到该物质的着火点以下
(缺一不可) (缺一即可)
【真题体验】
1.(2022青岛)小明在做化学实验时用灯帽盖灭酒精灯,这样操作依据的灭火原理是( )
A. 移走可燃物 B. 隔绝氧气
C. 降低温度至可燃物的着火点以下 D. 以上原理都有
2.(2022海南)北京冬奥会吉祥物“冰墩墩”和火炬“飞扬”引起世人高度关注。
(1)制作“冰墩墩”的内充物聚酯塑料属于_____材
料(填“合成”或“天然”)。
(2)火炬“飞扬”的燃料是液氢,其优点有______(写出一点即可)。
(3)火炬传递结束后,关闭阀门熄灭火炬,其中蕴含的灭火原理是_____ 。
B
合成
产物无污染
清除可燃物
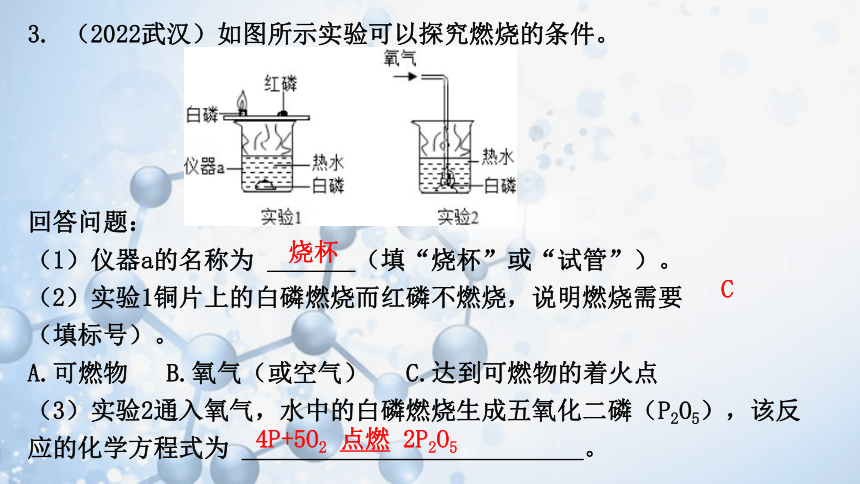
3. (2022武汉)如图所示实验可以探究燃烧的条件。
回答问题:
(1)仪器a的名称为 (填“烧杯”或“试管”)。
(2)实验1铜片上的白磷燃烧而红磷不燃烧,说明燃烧需要 (填标号)。
A.可燃物 B.氧气(或空气) C.达到可燃物的着火点
(3)实验2通入氧气,水中的白磷燃烧生成五氧化二磷(P2O5),该反应的化学方程式为 。
烧杯
C
4P+5O2 点燃 2P2O5
4.(2022永州)创新是社会进步的不竭动力。某化学兴趣小组设计了制取氧气和燃烧条件探究的创新实验。如图:
查阅资料:①白磷的着火点为40℃;
②P2O5+6NaOH═2Na3PO4+3H2O
请回答下列问题:
(1)仪器a的名称是 。
(2)按图连接好装置,将注射器内简向外拉出一段距离,装置C(装有水)中导管内立即形成一段水柱,片刻后观察到导管中的水柱不下降,这一操作的目的是检查装置的 性。
(3)向装置A中分别装入适量H2O2溶液和少量MnO2粉末,装置B中小试管装入一小颗白磷,装置C中装入适量NaOH溶液,连接好装置,缓慢推送注射器,向锥形瓶内注入H2O2溶液,立即观察到锥形瓶内产生气泡,装置B中白磷不燃烧。装置A中发生反应的化学方程式是 。
(4)向装置B的仪器a中注入90℃热水,片刻,可观察到白磷会
(填写实验现象)。
(5)装置C的作用是 。
烧杯
剧烈燃烧,产生大量的白烟
2H2O2 MnO2 2H2O+O2↑
气密
吸收P2O5,防止污染环境
主题二 化石燃料的利用
【主题训练2】(2022株洲)化石燃料是由古代生物的遗骸经过一系列复杂变化而形成的,是不可再生能源。
(1)化石燃料包括煤、石油、 等,是重要的能源。
(2)目前,多数汽车使用的燃料是 ,它们燃烧时会产生对空气造成污染的物质,为了减少汽车尾气对空气的污染,所以我国大力发展新能源汽车。
(3) 埋藏于海底的沉积物和陆地冻土层的岩石中,其中主要含有甲烷水合物,将成为未来新能源。
天然气
汽油
可燃冰
【关键点拨】
1.燃料燃烧对空气的影响:
(1)煤燃烧生成的SO2及氮氧化物会形成酸雨,生成的CO2会引起温室效应。
(2)汽车尾气中主要含有燃料燃烧生成的有毒气体CO和燃料中含氮物质燃烧生成的氮氧化合物。
2.化石燃料的综合利用。
使用优质煤、脱硫煤,在煤燃烧过程中,采取回收二氧化硫等措施;少使用化石燃料,多开发利用新型能源。对化石燃料进行综合利用,如煤的焦化、液化,石油的分馏等。
【真题体验】
1.(2022成都)成都以“碳达峰、碳中和”为目标,引领城市绿色低碳发展。下列做法利于实现此目标的是( )
石油炼制 B. 太阳能发电 C. 燃煤脱硫 D. 酒精作燃料
2.(2022眉山)我国政府工作报告中提出做好碳中和工作。碳中和是指通过植树造林、节能减排等措施,抵消因人类活动产生的二氧化碳等温室气体排放量,达到相对“零排放”。下列行为不利于实现碳中和的是( )
教科书循环使用
B. 用自行车代替汽车上下班出行
C. 燃烧农作物秸秆以增加土地肥效
D. 研发新工艺将二氧化碳转化为化工产品
B
C
3. (2022重庆A卷)2025年长安汽车厂将停止销售传统燃油车,新能源汽车发展成为主要趋势。
(1)下列不属于新能源的是______(填序号)。
A. 氢能 B. 汽油 C. 生物质能
(2)乙醇是一种生物燃料,它是______(填 “可再生”或“不可再生”)能源。乙醇在空气中完全燃烧生成水和______(写化学式),并放出大量热。
(3)肼-空气燃料电池有织应用于汽车工业,其原理是肼(N2H4)与氧气反应生成--种单质和水,反应化学方程式为
______ 。
B
可再生
CO2
N2H4 + O2 = N2 + 2H2O
4.(2022天津)能源利用和环境保护是人类共同关注的问题。
(1)化石燃料主要包括煤、______和天然气。
(2)化石燃料燃烧产生二氧化碳等气体,会影响环境,二氧化碳可用足量氢氧化钠溶液吸收,写出该反应的化学方程式
______ 。
(3)绿色植物经光合作用生成淀粉,淀粉在人体内变成葡萄糖(C6H12O6),葡萄糖在酶的催化作用下发生缓慢氧化生成二氧化碳和水,同时放出能量,写出葡萄糖与氧气发生缓慢氧化反应的化学方程式______ 。
(4)乙醇是常用的燃料,现有 9.2 g 乙醇与一定量氧气混合于密闭容器内,一定条件下反应物全部转化为一氧化碳、二氧化碳和水。恢复到室温,测得所得气体中氧元素质量分数为 60%,则反应过程中生成水的质量为______g,参加反应的氧气质量为______g。
烧杯
10.8
C6H12O6 + 6O2 酶 6CO2 + 6H2O
2NaOH + CO2 = Na2CO + H2O
13.6
主题三 大自然中的二氧化碳
【主题训练3】(2022宁夏)学习制取几种常见的
气体并探究其性质是初中阶段化学学习的重要门。
(1)上图是实验室制取气体的一些装置图。写一个用A装置制取某气体的化学方程式_________ 。如果将B装置与_________(写序号)装置连接,可以制取二氧化碳。
(2)依照下图所示实验,可得出以下结论:
①根据蜡烛熄灭的现象,说明二氧化碳不支持燃烧;
②根据_________的现象,说明二氧化碳不具有可燃性;
③根据_________ 的现象,说明二氧化碳的密度比空气的密度大。
2KClO32KCl + 3O2↑
C
蜡烛熄灭
底层蜡烛先熄灭,上层蜡烛后熄灭
【关键点拨】
实验室里制取气体的装置的确定
(1)气体发生装置。
依据反应物的状态和反应条件进行选择
①固+固 气,所选装置与“用KMnO4制取氧气”的装置类似。
②固+液 气,所选装置与制取H2、CO2的装置类似。
(2)气体收集装置。
①排空气法:密度与空气相差较大,且不与空气成分反应的气体。
②排水法:适用于不易溶于水,且不与水发生反应的气体。
△
【真题体验】
1. (2022湖南岳阳)如图是实验室制取气体的部分装置示意图,下列说法正确的是( )
A. 用过氧化氢溶液制取 O2,可选用装置②④组合
B. 用装置①制取 CO2,分液漏斗中应装稀硫酸
C. 用装置③收集 CO2,气体应从管口 c 通入
D. 要做铁丝燃烧实验,用④收集 O2时建议留部分水
D
2.在初中阶段,我们已经学习了利用某些仪器和药品制取气体,下图所示A~E装置可供实验室制取有关气体时选用。
(1)写出图中有标号仪器的名称:a 。
(2)实验室用大理石和稀盐酸制取CO2可选用的发生装置和收集装置是 ;
该反应的化学方程式是______ 。
(3)通过查阅资料得知:氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水,可用加热氯化铵和氢氧化钙的固体混合物制取。如果要制取氨气你应选择的发生装置和收集装是 。
酒精灯
BE
CaCO3+2HCl====CaCl2+H2O+CO2↑
AD
3.(2022台州)二氧化碳是一种与人类生产、生活有密切关系的气体,对地球生命具有重要意义。
(1)二氧化碳的发现
17世纪初,海尔蒙特发现木炭燃烧后不但有灰烬,还产生了一种不可见的气体,于是他将该气体命名为“森林之精”。蜡烛的火焰会在该气体中熄灭,说明了这种气体的化学性质有___________。
(2)二氧化碳的制取
实验室常用石灰石和稀盐酸反应制取二氧化碳。现要制取4.4克二氧化碳,至少需要含碳酸钙质量分数为80%的石灰石多少克?___________
(3)二氧化碳的减排和消耗
人类降低空气中的二氧化碳含量的研究有两个方向:一是减少二氧化碳的排放,二是增加二氧化碳的消耗。请写出一条你能做到的消耗二氧化碳的方式或途径:___________。
【答案】 ①不能燃烧也不支持燃烧
②解:设需要碳酸钙的质量为x
2HCl + CaCO = CaCl + H O + CO ↑
100 44
x 4.4g
100/44 = x/4.4g
x = 10g
石灰石的质量为10g/80% = 12.5g
答:至少需要含碳酸钙质量分数为80%的石灰石12.5g
③植树造林(合理即可)
单元复习与测试
第六单元 燃烧与燃料
PART
01
PART
02
从化学反应角度认识燃烧和灭火的原理;知道控制燃烧的条件就能达到促进燃烧和防火、灭火的目的。
知道化石燃料及其重要作用, 了解化石燃料综合利用的重要性,认识燃料燃烧对环境的影响及防治措施。
学习目标
PART
03
初步学习在实验室制取CO2的方法,培养分析、加工图片信息的能力,知道CO2的主要性质和用途。
【答案速填】①可燃物
②氧气
③着火点
④可燃物
⑤氧气
⑥着火点以下
一、燃烧和灭火
构建知识体系
【答案速填】
①碳
②碳、氢
③CH4+2O2点燃CO2+2H2O
④气化
⑤焦化
⑥液化
二、化学燃料的利用
【答案速填】
①化石燃料燃烧 ②光合作用
③温室效应
④大
⑤能溶
CO2+H2O===H2CO3 CO2+Ca(OH)2===
CaCO3↓+H2O
三、大自然中的二氧化碳
主题一 燃烧与灭火
【主题训练1】(2022潍坊)利用如图装置探究燃烧的条
件。试管①中充满氮气,试管②、③中充满氧气,升温至
40℃,仅观察到②中的白磷燃烧。下列叙述错误的是( )
A.对比①、③可验证燃烧需要氧气
B.试管②中白磷燃烧产生大量白雾
C.对比②、③可得出红磷的着火点比白磷高
D.图中小气球有密闭装置、缓冲气压的作用
AB
【关键点拨】
燃烧与灭火的关系
燃烧的条件 灭火的原理与方法
1.物质具有可燃性 → 1.隔离可燃物
2.与氧气充分接触 → 2.隔绝氧气
3.温度达到着火点 → 3.降温到该物质的着火点以下
(缺一不可) (缺一即可)
【真题体验】
1.(2022青岛)小明在做化学实验时用灯帽盖灭酒精灯,这样操作依据的灭火原理是( )
A. 移走可燃物 B. 隔绝氧气
C. 降低温度至可燃物的着火点以下 D. 以上原理都有
2.(2022海南)北京冬奥会吉祥物“冰墩墩”和火炬“飞扬”引起世人高度关注。
(1)制作“冰墩墩”的内充物聚酯塑料属于_____材
料(填“合成”或“天然”)。
(2)火炬“飞扬”的燃料是液氢,其优点有______(写出一点即可)。
(3)火炬传递结束后,关闭阀门熄灭火炬,其中蕴含的灭火原理是_____ 。
B
合成
产物无污染
清除可燃物
3. (2022武汉)如图所示实验可以探究燃烧的条件。
回答问题:
(1)仪器a的名称为 (填“烧杯”或“试管”)。
(2)实验1铜片上的白磷燃烧而红磷不燃烧,说明燃烧需要 (填标号)。
A.可燃物 B.氧气(或空气) C.达到可燃物的着火点
(3)实验2通入氧气,水中的白磷燃烧生成五氧化二磷(P2O5),该反应的化学方程式为 。
烧杯
C
4P+5O2 点燃 2P2O5
4.(2022永州)创新是社会进步的不竭动力。某化学兴趣小组设计了制取氧气和燃烧条件探究的创新实验。如图:
查阅资料:①白磷的着火点为40℃;
②P2O5+6NaOH═2Na3PO4+3H2O
请回答下列问题:
(1)仪器a的名称是 。
(2)按图连接好装置,将注射器内简向外拉出一段距离,装置C(装有水)中导管内立即形成一段水柱,片刻后观察到导管中的水柱不下降,这一操作的目的是检查装置的 性。
(3)向装置A中分别装入适量H2O2溶液和少量MnO2粉末,装置B中小试管装入一小颗白磷,装置C中装入适量NaOH溶液,连接好装置,缓慢推送注射器,向锥形瓶内注入H2O2溶液,立即观察到锥形瓶内产生气泡,装置B中白磷不燃烧。装置A中发生反应的化学方程式是 。
(4)向装置B的仪器a中注入90℃热水,片刻,可观察到白磷会
(填写实验现象)。
(5)装置C的作用是 。
烧杯
剧烈燃烧,产生大量的白烟
2H2O2 MnO2 2H2O+O2↑
气密
吸收P2O5,防止污染环境
主题二 化石燃料的利用
【主题训练2】(2022株洲)化石燃料是由古代生物的遗骸经过一系列复杂变化而形成的,是不可再生能源。
(1)化石燃料包括煤、石油、 等,是重要的能源。
(2)目前,多数汽车使用的燃料是 ,它们燃烧时会产生对空气造成污染的物质,为了减少汽车尾气对空气的污染,所以我国大力发展新能源汽车。
(3) 埋藏于海底的沉积物和陆地冻土层的岩石中,其中主要含有甲烷水合物,将成为未来新能源。
天然气
汽油
可燃冰
【关键点拨】
1.燃料燃烧对空气的影响:
(1)煤燃烧生成的SO2及氮氧化物会形成酸雨,生成的CO2会引起温室效应。
(2)汽车尾气中主要含有燃料燃烧生成的有毒气体CO和燃料中含氮物质燃烧生成的氮氧化合物。
2.化石燃料的综合利用。
使用优质煤、脱硫煤,在煤燃烧过程中,采取回收二氧化硫等措施;少使用化石燃料,多开发利用新型能源。对化石燃料进行综合利用,如煤的焦化、液化,石油的分馏等。
【真题体验】
1.(2022成都)成都以“碳达峰、碳中和”为目标,引领城市绿色低碳发展。下列做法利于实现此目标的是( )
石油炼制 B. 太阳能发电 C. 燃煤脱硫 D. 酒精作燃料
2.(2022眉山)我国政府工作报告中提出做好碳中和工作。碳中和是指通过植树造林、节能减排等措施,抵消因人类活动产生的二氧化碳等温室气体排放量,达到相对“零排放”。下列行为不利于实现碳中和的是( )
教科书循环使用
B. 用自行车代替汽车上下班出行
C. 燃烧农作物秸秆以增加土地肥效
D. 研发新工艺将二氧化碳转化为化工产品
B
C
3. (2022重庆A卷)2025年长安汽车厂将停止销售传统燃油车,新能源汽车发展成为主要趋势。
(1)下列不属于新能源的是______(填序号)。
A. 氢能 B. 汽油 C. 生物质能
(2)乙醇是一种生物燃料,它是______(填 “可再生”或“不可再生”)能源。乙醇在空气中完全燃烧生成水和______(写化学式),并放出大量热。
(3)肼-空气燃料电池有织应用于汽车工业,其原理是肼(N2H4)与氧气反应生成--种单质和水,反应化学方程式为
______ 。
B
可再生
CO2
N2H4 + O2 = N2 + 2H2O
4.(2022天津)能源利用和环境保护是人类共同关注的问题。
(1)化石燃料主要包括煤、______和天然气。
(2)化石燃料燃烧产生二氧化碳等气体,会影响环境,二氧化碳可用足量氢氧化钠溶液吸收,写出该反应的化学方程式
______ 。
(3)绿色植物经光合作用生成淀粉,淀粉在人体内变成葡萄糖(C6H12O6),葡萄糖在酶的催化作用下发生缓慢氧化生成二氧化碳和水,同时放出能量,写出葡萄糖与氧气发生缓慢氧化反应的化学方程式______ 。
(4)乙醇是常用的燃料,现有 9.2 g 乙醇与一定量氧气混合于密闭容器内,一定条件下反应物全部转化为一氧化碳、二氧化碳和水。恢复到室温,测得所得气体中氧元素质量分数为 60%,则反应过程中生成水的质量为______g,参加反应的氧气质量为______g。
烧杯
10.8
C6H12O6 + 6O2 酶 6CO2 + 6H2O
2NaOH + CO2 = Na2CO + H2O
13.6
主题三 大自然中的二氧化碳
【主题训练3】(2022宁夏)学习制取几种常见的
气体并探究其性质是初中阶段化学学习的重要门。
(1)上图是实验室制取气体的一些装置图。写一个用A装置制取某气体的化学方程式_________ 。如果将B装置与_________(写序号)装置连接,可以制取二氧化碳。
(2)依照下图所示实验,可得出以下结论:
①根据蜡烛熄灭的现象,说明二氧化碳不支持燃烧;
②根据_________的现象,说明二氧化碳不具有可燃性;
③根据_________ 的现象,说明二氧化碳的密度比空气的密度大。
2KClO32KCl + 3O2↑
C
蜡烛熄灭
底层蜡烛先熄灭,上层蜡烛后熄灭
【关键点拨】
实验室里制取气体的装置的确定
(1)气体发生装置。
依据反应物的状态和反应条件进行选择
①固+固 气,所选装置与“用KMnO4制取氧气”的装置类似。
②固+液 气,所选装置与制取H2、CO2的装置类似。
(2)气体收集装置。
①排空气法:密度与空气相差较大,且不与空气成分反应的气体。
②排水法:适用于不易溶于水,且不与水发生反应的气体。
△
【真题体验】
1. (2022湖南岳阳)如图是实验室制取气体的部分装置示意图,下列说法正确的是( )
A. 用过氧化氢溶液制取 O2,可选用装置②④组合
B. 用装置①制取 CO2,分液漏斗中应装稀硫酸
C. 用装置③收集 CO2,气体应从管口 c 通入
D. 要做铁丝燃烧实验,用④收集 O2时建议留部分水
D
2.在初中阶段,我们已经学习了利用某些仪器和药品制取气体,下图所示A~E装置可供实验室制取有关气体时选用。
(1)写出图中有标号仪器的名称:a 。
(2)实验室用大理石和稀盐酸制取CO2可选用的发生装置和收集装置是 ;
该反应的化学方程式是______ 。
(3)通过查阅资料得知:氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水,可用加热氯化铵和氢氧化钙的固体混合物制取。如果要制取氨气你应选择的发生装置和收集装是 。
酒精灯
BE
CaCO3+2HCl====CaCl2+H2O+CO2↑
AD
3.(2022台州)二氧化碳是一种与人类生产、生活有密切关系的气体,对地球生命具有重要意义。
(1)二氧化碳的发现
17世纪初,海尔蒙特发现木炭燃烧后不但有灰烬,还产生了一种不可见的气体,于是他将该气体命名为“森林之精”。蜡烛的火焰会在该气体中熄灭,说明了这种气体的化学性质有___________。
(2)二氧化碳的制取
实验室常用石灰石和稀盐酸反应制取二氧化碳。现要制取4.4克二氧化碳,至少需要含碳酸钙质量分数为80%的石灰石多少克?___________
(3)二氧化碳的减排和消耗
人类降低空气中的二氧化碳含量的研究有两个方向:一是减少二氧化碳的排放,二是增加二氧化碳的消耗。请写出一条你能做到的消耗二氧化碳的方式或途径:___________。
【答案】 ①不能燃烧也不支持燃烧
②解:设需要碳酸钙的质量为x
2HCl + CaCO = CaCl + H O + CO ↑
100 44
x 4.4g
100/44 = x/4.4g
x = 10g
石灰石的质量为10g/80% = 12.5g
答:至少需要含碳酸钙质量分数为80%的石灰石12.5g
③植树造林(合理即可)
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
