化学式
图片预览





文档简介
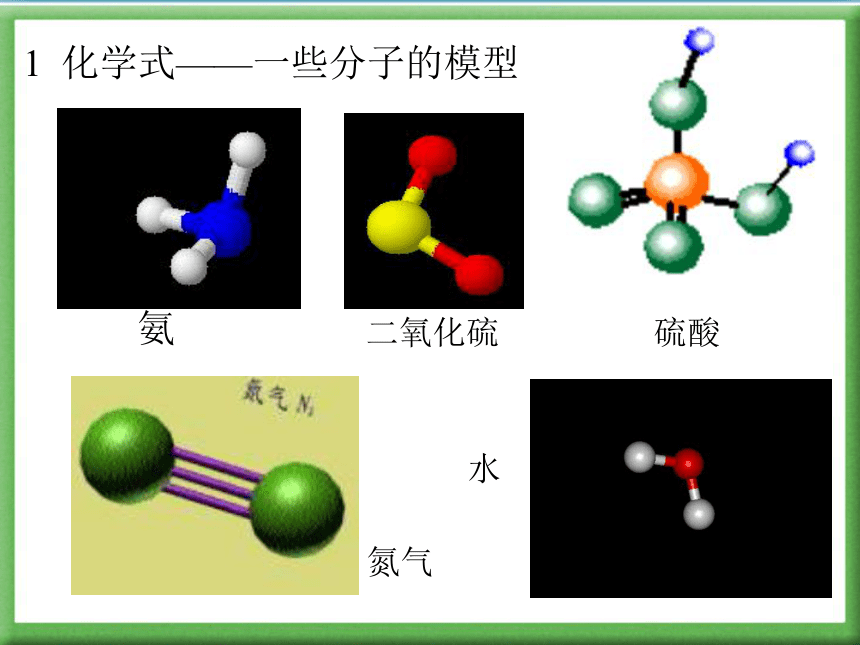
课件30张PPT。1 化学式2 化合价3 化学式的书写1 化学式4 相对原子质量和式量1 化学式——一些分子的模型氨二氧化硫水氮气硫酸1 化学式——概念用元素符号来表示物质组成的式子叫做化学式如:硫 S 铁 Fe 氧气 O2
水 H2O、 二氧化碳 CO2
四氧化三铁 Fe3O4
氯酸钾 KClO3、 高锰酸钾 KMnO4
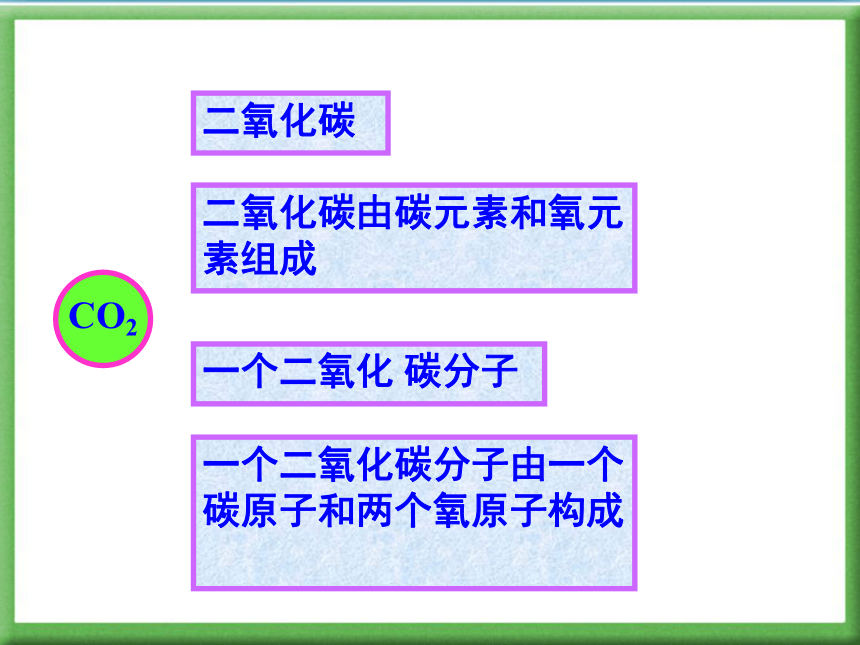
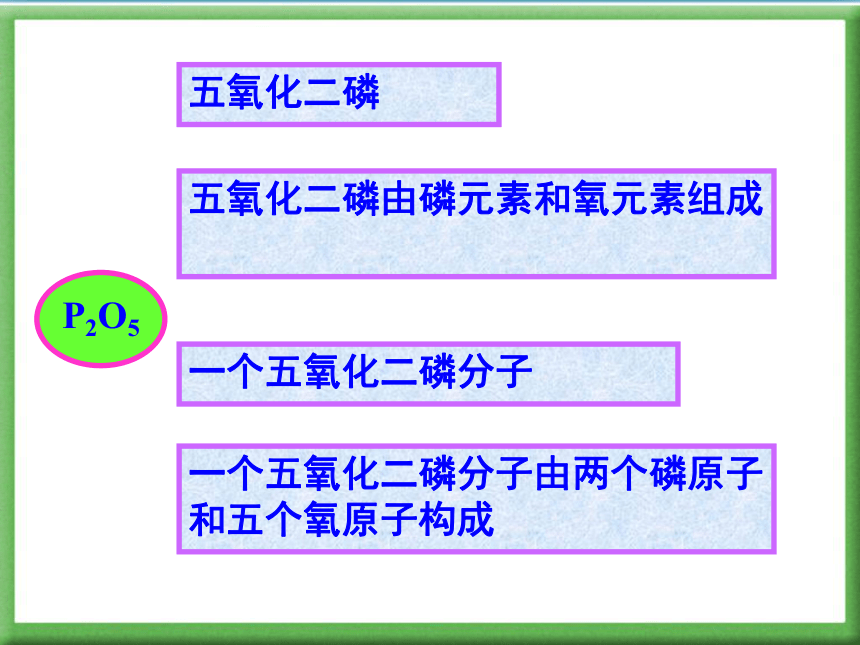
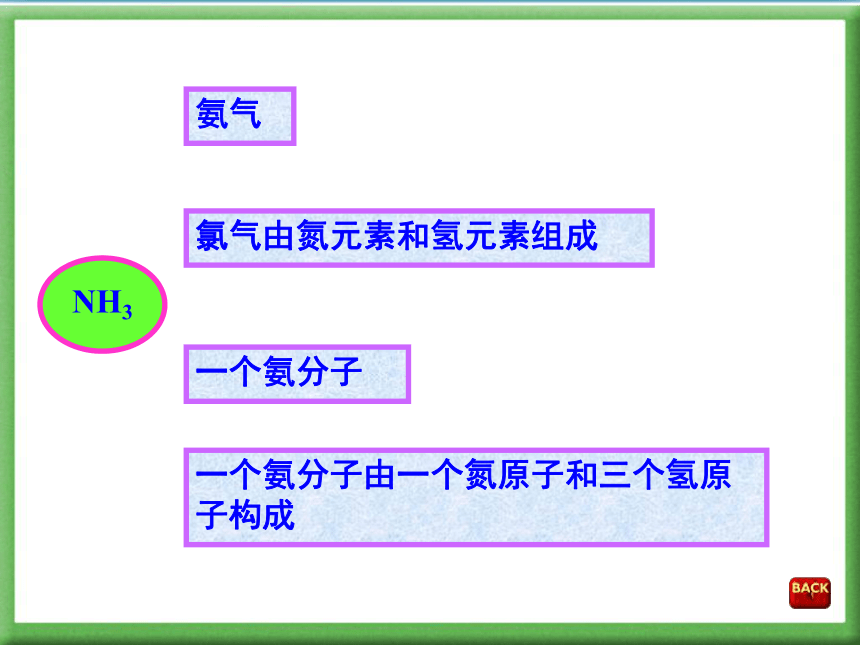
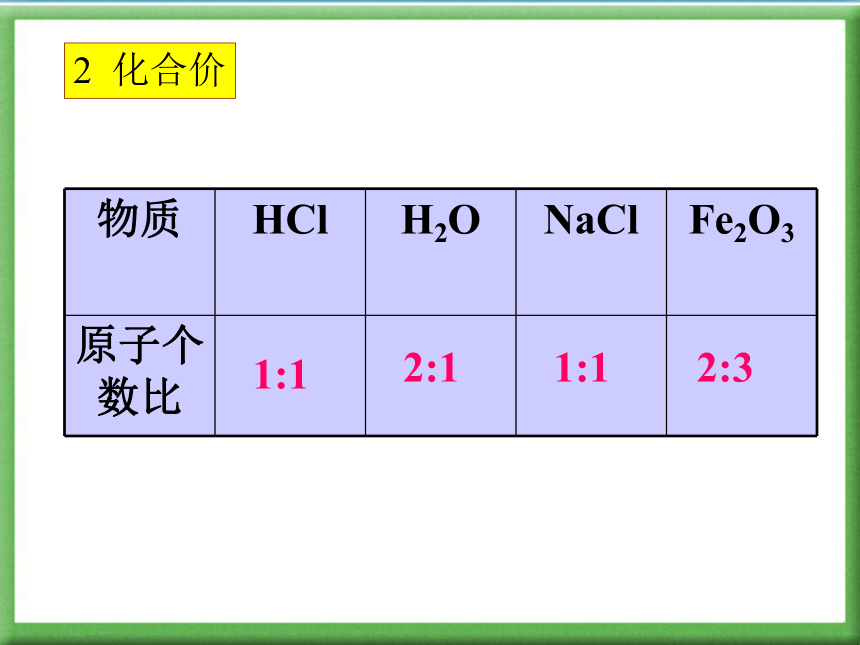
碱式碳酸铜 Cu2(OH)2CO3化学式表示的意义:一种物质该物质的组成元素该物质的一个分子该物质的分子构成宏观微观1 化学式——意义CO2二氧化碳二氧化碳由碳元素和氧元素组成一个二氧化 碳分子一个二氧化碳分子由一个碳原子和两个氧原子构成P2O5五氧化二磷五氧化二磷由磷元素和氧元素组成一个五氧化二磷分子一个五氧化二磷分子由两个磷原子和五个氧原子构成NH3氨气氯气由氮元素和氢元素组成一个氨分子一个氨分子由一个氮原子和三个氢原子构成1:12:11:12:32 化合价用来表示原子之间相互化合的数目2 化合价MgMg2+S2-+2化合价为+2价的镁元素带2个单位正电荷的镁离子带2个单位负电荷的硫离子HCl-1氯化氢中的氯元素为-1价A 化合价有正价和负价
B 金属通常显正价,非金属通常显负价
C 在化合物中氧元素通常显-2价,氢元
素 显+1价
D 在化合物里正负化合价的代数和为零。
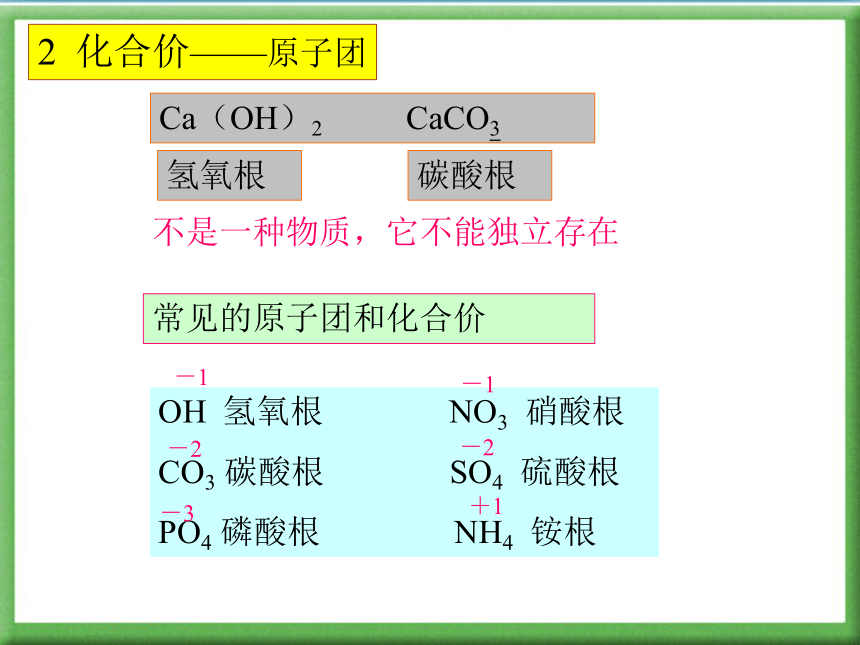
E 在单质分子里,元素的化合价为02 化合价——化合价的规律Ca(OH)2 CaCO3氢氧根碳酸根不是一种物质,它不能独立存在常见的原子团和化合价OH 氢氧根 NO3 硝酸根
CO3 碳酸根 SO4 硫酸根
PO4 磷酸根 NH4 铵根-1-1-2-3 -2+12 化合价——原子团一价钾钠氢与银,二价钙镁钡与锌
三价金属元素铝,一二铜、二三铁
负一氟氯溴与碘,负二氧硫最常见
负三氮磷多出现。2 化合价——熟记常见元素或原子团的化合价? 单质的化合价为零? 化合物中,通常氧显–2价,
氢显+1价? 在化合物中,正负化合价
的代数和零2 化合价——化合价的一般规律一价钾钠银“卤”氢
二价氧钡钙镁锌
三铝四硅记在心二三铁,二四碳
二四六七锰多样
铜汞二价最常见一一五七氯
三二四五氮
二四六硫,三三五磷说明:
?卤-氟 氯 溴 碘
?名称或数字为
蓝色的为负价2 化合价——顺口溜3 化学式的书写氧气 氢气用元素符号表示(直接由原子构成)气体单质:O2H2绝大多数是原子分子(除溴Br2 碘 I2) (1)单质
金属单质:铁 铝
固态非金属单质:硫 磷
稀有气体:氖气 氦气氧化物MgO CuO CO2 SO2 Fe3O4P2O5 MnO2氧在后写法:读法氧化某或几氧化几某
H2O
HCl
H2S
氢化物写法氢在前读法某化氢不过也有例外的喔!!!NH3(氨气)
CH4(甲烷)金属元素与非金属
元素组成的物质KCl NaCl写法金前非后读法某化某 硫酸 H2SO4
酸
碳酸 H2CO3 碳酸钙CaCO3
盐 硫酸钠Na2SO4
氯酸钾KClO3多种元素组成的化合物: 氢氧化钠NaOH
碱 氢氧化钙Ca(OH)2
氢氧化铜Cu (OH)2单质:
X—金属、稀有气体、固态非金属
X2 — N2、O2、H2等气态非金属金前非后,由后往前读做某化某氧化物:氧在后,
一般读做氧化某,适用于由两种元素组成的物质4、相对原子质量和式量什么是相对分子质量?它的国际单位制是什么? 化学式中各原子的相对原子质量的总和。 相对分子质量的国际单位制(SI)单位为1(一般不写出)。根据化学式的计算
1、计算物质的相对分子质量1、计算KMnO4的相对分子质量。
2、计算(NH4)2CO3的相对分子质量。例1.计算二氧化碳(CO2)的相对分子质量。二氧化碳(CO2)的相对分子质量=12+16× 2=44例2.计算Cu2(OH)2CO3的相对分子质量。Cu2(OH)2CO3的相对分子质量=
64 × 2+(16+1) × 2+12+16 × 3=222 计算组成物质的各元素的质量比。 练习1、计算水中氢元素和氧元素的质量比。练习2、求硫酸(H2SO4)中各元素的质量比。 例题:二氧化碳中碳元素和氧元素的质量比 C∶O=12∶16×2=3∶8H2O中氢元素和氧元素的质量比 H∶O=1×2∶16=1H2SO4中氢、硫、氧三种元素的质量比 H∶S∶O=1×2∶32∶16×4=1∶16∶32练习1、求水中氢元素的质量分数。练习2、求二氧化硫中硫元素的质量分数。解: H%= = =11.1%解:S%= = =50%
2HH2O218SSO23264 计算物质中某一元素的质量分数 练习:22克二氧化碳中氧元素的质量。mN=mCO2 ×二氧化碳中氧的质量分数
=22克× —— =16克2OCO2 计算纯净物中某一元素的质量 1、相对分子质量(定义和单位)。
2、掌握根据化学式计算:
(1)、计算物质的相对分子质量;
(2)、计算组成物质的各元素的质量比;
(3)、计算物质中某一元素的质量分数。
(4)、计算物质中某一元素的质量。
门捷列夫
水 H2O、 二氧化碳 CO2
四氧化三铁 Fe3O4
氯酸钾 KClO3、 高锰酸钾 KMnO4
碱式碳酸铜 Cu2(OH)2CO3化学式表示的意义:一种物质该物质的组成元素该物质的一个分子该物质的分子构成宏观微观1 化学式——意义CO2二氧化碳二氧化碳由碳元素和氧元素组成一个二氧化 碳分子一个二氧化碳分子由一个碳原子和两个氧原子构成P2O5五氧化二磷五氧化二磷由磷元素和氧元素组成一个五氧化二磷分子一个五氧化二磷分子由两个磷原子和五个氧原子构成NH3氨气氯气由氮元素和氢元素组成一个氨分子一个氨分子由一个氮原子和三个氢原子构成1:12:11:12:32 化合价用来表示原子之间相互化合的数目2 化合价MgMg2+S2-+2化合价为+2价的镁元素带2个单位正电荷的镁离子带2个单位负电荷的硫离子HCl-1氯化氢中的氯元素为-1价A 化合价有正价和负价
B 金属通常显正价,非金属通常显负价
C 在化合物中氧元素通常显-2价,氢元
素 显+1价
D 在化合物里正负化合价的代数和为零。
E 在单质分子里,元素的化合价为02 化合价——化合价的规律Ca(OH)2 CaCO3氢氧根碳酸根不是一种物质,它不能独立存在常见的原子团和化合价OH 氢氧根 NO3 硝酸根
CO3 碳酸根 SO4 硫酸根
PO4 磷酸根 NH4 铵根-1-1-2-3 -2+12 化合价——原子团一价钾钠氢与银,二价钙镁钡与锌
三价金属元素铝,一二铜、二三铁
负一氟氯溴与碘,负二氧硫最常见
负三氮磷多出现。2 化合价——熟记常见元素或原子团的化合价? 单质的化合价为零? 化合物中,通常氧显–2价,
氢显+1价? 在化合物中,正负化合价
的代数和零2 化合价——化合价的一般规律一价钾钠银“卤”氢
二价氧钡钙镁锌
三铝四硅记在心二三铁,二四碳
二四六七锰多样
铜汞二价最常见一一五七氯
三二四五氮
二四六硫,三三五磷说明:
?卤-氟 氯 溴 碘
?名称或数字为
蓝色的为负价2 化合价——顺口溜3 化学式的书写氧气 氢气用元素符号表示(直接由原子构成)气体单质:O2H2绝大多数是原子分子(除溴Br2 碘 I2) (1)单质
金属单质:铁 铝
固态非金属单质:硫 磷
稀有气体:氖气 氦气氧化物MgO CuO CO2 SO2 Fe3O4P2O5 MnO2氧在后写法:读法氧化某或几氧化几某
H2O
HCl
H2S
氢化物写法氢在前读法某化氢不过也有例外的喔!!!NH3(氨气)
CH4(甲烷)金属元素与非金属
元素组成的物质KCl NaCl写法金前非后读法某化某 硫酸 H2SO4
酸
碳酸 H2CO3 碳酸钙CaCO3
盐 硫酸钠Na2SO4
氯酸钾KClO3多种元素组成的化合物: 氢氧化钠NaOH
碱 氢氧化钙Ca(OH)2
氢氧化铜Cu (OH)2单质:
X—金属、稀有气体、固态非金属
X2 — N2、O2、H2等气态非金属金前非后,由后往前读做某化某氧化物:氧在后,
一般读做氧化某,适用于由两种元素组成的物质4、相对原子质量和式量什么是相对分子质量?它的国际单位制是什么? 化学式中各原子的相对原子质量的总和。 相对分子质量的国际单位制(SI)单位为1(一般不写出)。根据化学式的计算
1、计算物质的相对分子质量1、计算KMnO4的相对分子质量。
2、计算(NH4)2CO3的相对分子质量。例1.计算二氧化碳(CO2)的相对分子质量。二氧化碳(CO2)的相对分子质量=12+16× 2=44例2.计算Cu2(OH)2CO3的相对分子质量。Cu2(OH)2CO3的相对分子质量=
64 × 2+(16+1) × 2+12+16 × 3=222 计算组成物质的各元素的质量比。 练习1、计算水中氢元素和氧元素的质量比。练习2、求硫酸(H2SO4)中各元素的质量比。 例题:二氧化碳中碳元素和氧元素的质量比 C∶O=12∶16×2=3∶8H2O中氢元素和氧元素的质量比 H∶O=1×2∶16=1H2SO4中氢、硫、氧三种元素的质量比 H∶S∶O=1×2∶32∶16×4=1∶16∶32练习1、求水中氢元素的质量分数。练习2、求二氧化硫中硫元素的质量分数。解: H%= = =11.1%解:S%= = =50%
2HH2O218SSO23264 计算物质中某一元素的质量分数 练习:22克二氧化碳中氧元素的质量。mN=mCO2 ×二氧化碳中氧的质量分数
=22克× —— =16克2OCO2 计算纯净物中某一元素的质量 1、相对分子质量(定义和单位)。
2、掌握根据化学式计算:
(1)、计算物质的相对分子质量;
(2)、计算组成物质的各元素的质量比;
(3)、计算物质中某一元素的质量分数。
(4)、计算物质中某一元素的质量。
门捷列夫
同课章节目录
- 第1章 运动和力
- 1 机械运动
- 2 力
- 3 几种常见的力
- 4 运动和力
- 5 二力平衡的条件
- 第2章 压力 压强
- 1 压强
- 2 液体内部的压强
- 3 大气压强
- 4 流体的压强与流速的关系
- 第3章 浮力
- 1 密度
- 2 浮力
- 3 阿基米德原理
- 4 物体浮沉条件及其应用
- 第4章 植物的物质和能量的转化
- 1 绿色开花植物的营养器官
- 2 水在植物体中的代谢
- 3 无机盐在植物体内的代谢
- 4 植物的光合作用和呼吸作用
- 第5章 人体的物质和能量的转化
- 1 食物的消化和吸收
- 2 人体的呼吸
- 3 人体内的物质运输
- 4 人体的排泄
- 5 人体生命活动过程中物质和能量的转化
- 第6章 物质的构成
- 1 构成物质的微粒
- 2 元素
- 3 物质的分类
- 4 化学式
- 5 固态物质
