人教版九年级化学上册5.3 利用化学方程式的简单计算培优训练(无答案)
文档属性
| 名称 | 人教版九年级化学上册5.3 利用化学方程式的简单计算培优训练(无答案) |
|
|
| 格式 | zip | ||
| 文件大小 | 122.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-17 00:00:00 | ||
图片预览


文档简介
5.3 利用化学方程式的简单计算培优训练
将含3克氯酸钾和1克二氧化锰的混合物加热片刻,冷却,称得残余固体的质量为3.04克,根据质量守恒定律可知,生成氧气的质量为多少克?固体残余物中含有什么物质?
工业上煅烧石灰石(CaCO3)可制得生石灰(CaO)和二氧化碳,如果要制取2.8t氧化钙,计算需要碳酸钙的质量.(CaCO3 CaO+CO2↑)
3.某实验小组的同学为了测定实验室中氯酸钾样品的纯度,取一定质量的该样品与1克二氧化锰混合,其总质量为6克。依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体的质量,记录的有关数据入下表(样品中的杂质不参与反应):
试计算:(1)完全反应后产生的氧气的总质量为_______________________。
样品中氯酸钾的纯度为多少?
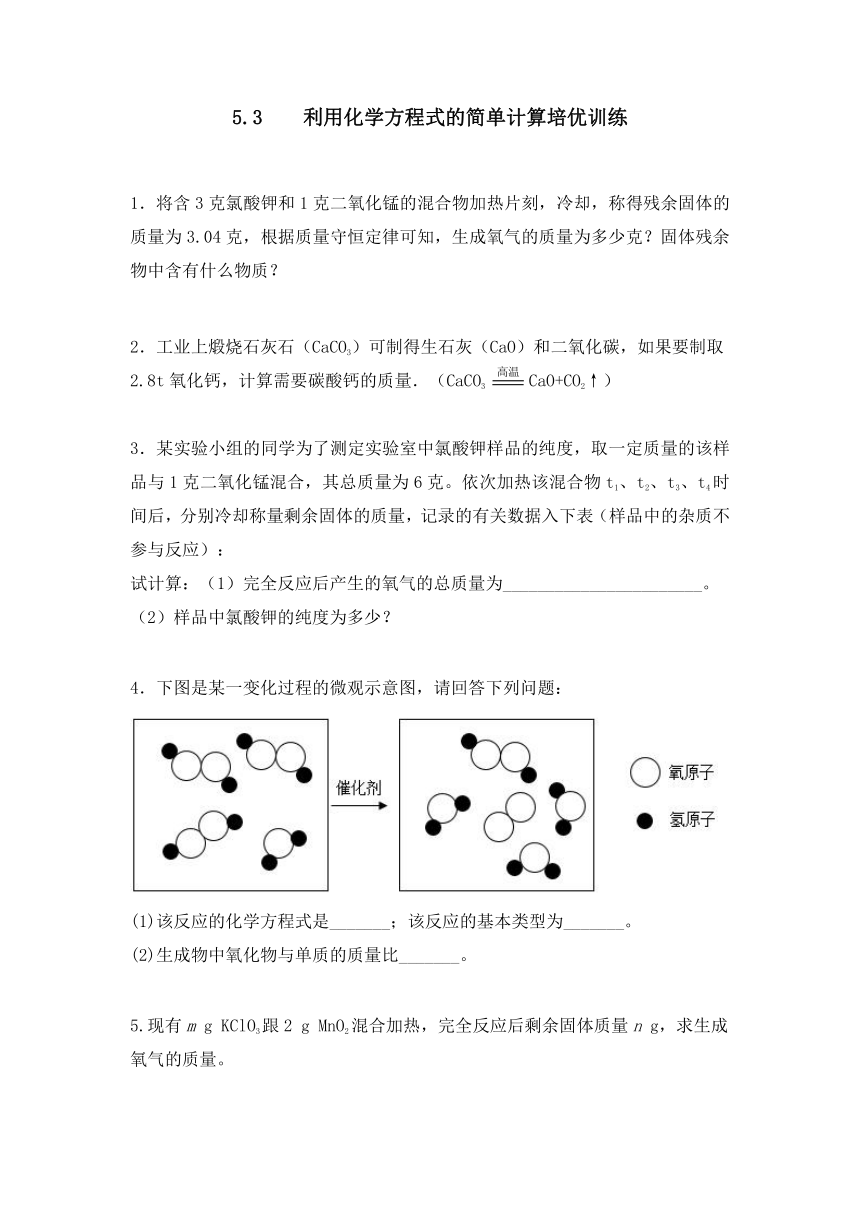
4.下图是某一变化过程的微观示意图,请回答下列问题:
(1)该反应的化学方程式是_______;该反应的基本类型为_______。
(2)生成物中氧化物与单质的质量比_______。
5.现有m g KClO3跟2 g MnO2混合加热,完全反应后剩余固体质量n g,求生成氧气的质量。
6.过氧化氢溶液长期存放会因分解而使溶液质量减轻。实验室有一瓶过氧化氢溶液,一段时间后,溶液质量共减少8 g,则该过程共有多少过氧化氢分解?
某工厂需要160kg氧气作原料。若用电解水的方法制取这些氧气,消耗水的质量是多少?(利用化学反应方程式计算,写出计算过程)
小义同学在实验室把木炭和氧化铜的混合物17.2 g,在老师的指导下,用酒精喷灯加热使之充分反应,冷却后称量固体剩余物为12.8 g,试问该同学所称量的CuO为多少克?
9.有一过氧化氢溶液(含过氧化氢和水)85克,在二氧化锰的催化作用之下完全分解可得到氧气3.2克,求:(1)该溶液中,含过氧化氢的质量为多少克?
(2)该样品中过氧化氢的质量分数是多少?
10.某工厂需要280g生石灰(CaO)作干燥剂,需要碳酸钙的质量是多少?至少需要含碳酸钙80%的石灰石(杂质不参加反应)的质量是多少?
11.“7150灭火剂”(C3H9B3O6,相对分子质量为174)以雾状喷射到燃着的金属时,立即发生燃烧反应:
2C3H9B3O6+9O23B2O3+9H2O+6CO2。反应能很快耗尽金属物品附近的氧气,生成的玻璃状B2O3覆盖在金属物品表面而隔绝空气,从而有效灭火。若充分燃烧348 g “7150灭火剂”,会消耗常温下的氧气多少升?(常温下氧气密度约为1.4 g·L-1,结果保留一位小数)
鸡蛋壳的主要成分是碳酸钙。某学生想测定鸡蛋壳中碳酸钙的质量分数,取15g干燥的碎鸡蛋壳放入烧杯中,向其中加入了40g稀盐酸恰好完全反应(假设鸡蛋壳中除碳酸钙外的其他成分都不溶于水,且不与稀盐酸反应),反应后烧杯中物质的总质量50.6g。计算鸡蛋壳中碳酸钙的质量分数(结果保留1位小数)。
13.过氧化氢不稳定会自然分解,久置的过氧化氢溶液,其溶质的质量分数会变小。某兴趣小组为测定实验室中一瓶久置的过氧化氢溶液中溶质的质量分数,进行实验。测得相关数据如下图所示:
(1)根据质量守恒定律,反应生成氧气的质量为 。
(2)计算该过氧化氢溶液中过氧化氢的质量。(写出计算过程)
14.实验室用68g过氧化氢溶液和2g二氧化锰制取氧气,实验的相关数据如图。
请回答:
(1)二氧化锰作为催化剂在化学反应前后本身的 都没有发生变化;
(2)反应生成氧气的质量为________g。
(3)参加反应过氧化氢溶液的质量分数是多少?
在化学反应中,已知与恰好完全反应,生成C和D的质量比为,又知B的相对分子质量为32,求D的相对分子质量。
16.实验室加热氯酸钾和二氧化锰的混合物28g制取氧气,完全反应后剩余固体质量为18.4g,请计算:
(1)生成氧气的质量;
(2)原混合物中氯酸钾的质量。
17.取20.0 g KMnO4固体制氧气,加热一段时间后,固体质量减少1.6 g。求已分解KMnO4的质量占取用KMnO4总质量的百分率。
18.小苏打常用作治疗胃酸过多的药剂。某小苏打中混有少量碳酸钠,为测定样品中碳酸氢钠的质量分数,取3.0g样品加热到质量不再减少时,共收集到二氧化碳0.66g。求该样品中碳酸氢钠的质量分数。
(碳酸氢钠受热分解的化学方程式:2 NaHCO3 Na2CO3 + H2O + CO2↑)
+
二氧化锰
0 .5 g
过氧化氢溶液34 .0 g
剩余的混合物
33.7 g
至质量不再减轻
将含3克氯酸钾和1克二氧化锰的混合物加热片刻,冷却,称得残余固体的质量为3.04克,根据质量守恒定律可知,生成氧气的质量为多少克?固体残余物中含有什么物质?
工业上煅烧石灰石(CaCO3)可制得生石灰(CaO)和二氧化碳,如果要制取2.8t氧化钙,计算需要碳酸钙的质量.(CaCO3 CaO+CO2↑)
3.某实验小组的同学为了测定实验室中氯酸钾样品的纯度,取一定质量的该样品与1克二氧化锰混合,其总质量为6克。依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体的质量,记录的有关数据入下表(样品中的杂质不参与反应):
试计算:(1)完全反应后产生的氧气的总质量为_______________________。
样品中氯酸钾的纯度为多少?
4.下图是某一变化过程的微观示意图,请回答下列问题:
(1)该反应的化学方程式是_______;该反应的基本类型为_______。
(2)生成物中氧化物与单质的质量比_______。
5.现有m g KClO3跟2 g MnO2混合加热,完全反应后剩余固体质量n g,求生成氧气的质量。
6.过氧化氢溶液长期存放会因分解而使溶液质量减轻。实验室有一瓶过氧化氢溶液,一段时间后,溶液质量共减少8 g,则该过程共有多少过氧化氢分解?
某工厂需要160kg氧气作原料。若用电解水的方法制取这些氧气,消耗水的质量是多少?(利用化学反应方程式计算,写出计算过程)
小义同学在实验室把木炭和氧化铜的混合物17.2 g,在老师的指导下,用酒精喷灯加热使之充分反应,冷却后称量固体剩余物为12.8 g,试问该同学所称量的CuO为多少克?
9.有一过氧化氢溶液(含过氧化氢和水)85克,在二氧化锰的催化作用之下完全分解可得到氧气3.2克,求:(1)该溶液中,含过氧化氢的质量为多少克?
(2)该样品中过氧化氢的质量分数是多少?
10.某工厂需要280g生石灰(CaO)作干燥剂,需要碳酸钙的质量是多少?至少需要含碳酸钙80%的石灰石(杂质不参加反应)的质量是多少?
11.“7150灭火剂”(C3H9B3O6,相对分子质量为174)以雾状喷射到燃着的金属时,立即发生燃烧反应:
2C3H9B3O6+9O23B2O3+9H2O+6CO2。反应能很快耗尽金属物品附近的氧气,生成的玻璃状B2O3覆盖在金属物品表面而隔绝空气,从而有效灭火。若充分燃烧348 g “7150灭火剂”,会消耗常温下的氧气多少升?(常温下氧气密度约为1.4 g·L-1,结果保留一位小数)
鸡蛋壳的主要成分是碳酸钙。某学生想测定鸡蛋壳中碳酸钙的质量分数,取15g干燥的碎鸡蛋壳放入烧杯中,向其中加入了40g稀盐酸恰好完全反应(假设鸡蛋壳中除碳酸钙外的其他成分都不溶于水,且不与稀盐酸反应),反应后烧杯中物质的总质量50.6g。计算鸡蛋壳中碳酸钙的质量分数(结果保留1位小数)。
13.过氧化氢不稳定会自然分解,久置的过氧化氢溶液,其溶质的质量分数会变小。某兴趣小组为测定实验室中一瓶久置的过氧化氢溶液中溶质的质量分数,进行实验。测得相关数据如下图所示:
(1)根据质量守恒定律,反应生成氧气的质量为 。
(2)计算该过氧化氢溶液中过氧化氢的质量。(写出计算过程)
14.实验室用68g过氧化氢溶液和2g二氧化锰制取氧气,实验的相关数据如图。
请回答:
(1)二氧化锰作为催化剂在化学反应前后本身的 都没有发生变化;
(2)反应生成氧气的质量为________g。
(3)参加反应过氧化氢溶液的质量分数是多少?
在化学反应中,已知与恰好完全反应,生成C和D的质量比为,又知B的相对分子质量为32,求D的相对分子质量。
16.实验室加热氯酸钾和二氧化锰的混合物28g制取氧气,完全反应后剩余固体质量为18.4g,请计算:
(1)生成氧气的质量;
(2)原混合物中氯酸钾的质量。
17.取20.0 g KMnO4固体制氧气,加热一段时间后,固体质量减少1.6 g。求已分解KMnO4的质量占取用KMnO4总质量的百分率。
18.小苏打常用作治疗胃酸过多的药剂。某小苏打中混有少量碳酸钠,为测定样品中碳酸氢钠的质量分数,取3.0g样品加热到质量不再减少时,共收集到二氧化碳0.66g。求该样品中碳酸氢钠的质量分数。
(碳酸氢钠受热分解的化学方程式:2 NaHCO3 Na2CO3 + H2O + CO2↑)
+
二氧化锰
0 .5 g
过氧化氢溶液34 .0 g
剩余的混合物
33.7 g
至质量不再减轻
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
