人教版化学九年级上册4.2水的净化课件(共28张PPT)
文档属性
| 名称 | 人教版化学九年级上册4.2水的净化课件(共28张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 678.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-17 20:10:52 | ||
图片预览








文档简介
(共28张PPT)
九年级
4.2 水的净化
1、了解纯水与自然水、硬水与软水的区别。
2、了解吸附、沉淀、过滤和蒸馏等净水的方法。
学习目标
自主学习
预习新课:P74-P78,完成以下几个问题:
1、如何净化自然界的水资源?
2、净化水需要哪些操作?
3、如何区分软水和硬水?
自主学习反馈
1.在野外和灾区可用下列几个步骤将河水转化成饮用水:①化学沉降(用明矾);②消毒杀菌(漂白粉);③自然沉降;④加热煮沸。以上处理过程最合理的顺序是( )
A.③②①④ B.③①②④ C.③①④② D.①③②④
B
2.下列方法不属于净化水的措施是( )
A.吸附 B.过滤 C.电解 D.蒸馏
C
3.硬水和软水的本质区别是( )
A.硬水浑浊,软水澄清
B.硬水含杂质多,软水含杂质少
C.硬水不是纯净物,软水是纯净物
D.硬水中含有较多的可溶性钙、镁化合物,软水不含或含少量的可溶性钙、镁化合物
D
自主学习反馈
情景导入
这杯透明的水中含有杂质吗?
纯水是无色、无臭、清澈透明的,而自然界中的河水、湖水等由于含有许多可溶性或不溶性的杂质,因此常呈现浑浊。
河水
自来水
纯净水
纯水:无色、无味、液体
标准状况下,4○C密度最大,为1g/cm3
标准大气压下,凝固点为0 ○C ,沸点为100 ○C
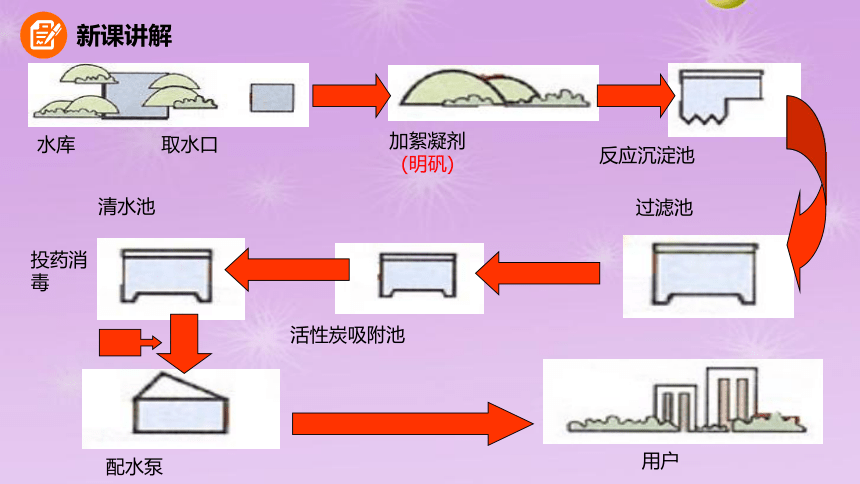
新课讲解
配水泵
活性炭吸附池
用户
过滤池
反应沉淀池
加絮凝剂
(明矾)
水库
取水口
清水池
投药消毒
新课讲解
明矾
学名:十二水合硫酸铝钾
化学式:KAl(SO4)2·12H2O
又称:明矾、白矾、钾矾、钾铝矾、钾明矾
Al3+很容易水解,生成胶状的氢氧化铝Al(OH)3:
Al3+ + 3H2O = Al(OH)3(胶体)+ 3H+
氢氧化铝胶体的吸附能力很强,可以吸附水里悬浮的杂质,并形成沉淀,使水澄清。所以,明矾是一种较好的净水剂。
新课讲解
沉淀:1.静置沉淀
2.吸附沉淀:加入絮凝剂(明矾),溶于水形成胶状物对悬浮杂质吸附,使杂质沉降。
【归纳】自来水厂用到的主要的净水方法:
沉淀→过滤→吸附→消毒
过滤: 除去水中不溶性的杂质。
吸附: 除去水中可溶性的杂质,如颜色、气味、有毒杂质等。
消毒: 向水中通入氯气(Cl2),氯气与水发生化学反应,产生次氯酸,杀灭细菌。
新课讲解
水中的杂质可以分为可溶性杂质和不溶性杂质两大类。我们一起学习除去这两类杂质的方法。
除去杂质的方法
(分离混合物的方法)
过 滤
吸 附
蒸 馏
新课讲解
【例】如何除去河水中的泥沙?
一、除去不溶性杂质的方法:
过滤
新课讲解
【操作要点】“一贴、二低、三靠”
铁架台
漏斗
玻璃棒
烧杯
滤纸
过 滤
新课讲解
一贴:滤纸紧贴漏斗内壁。
二低:①滤纸边缘要低于漏斗边缘;
②漏斗中的液面应低于滤纸的边缘
三靠:
①倾倒液体的烧杯口要紧靠玻璃棒;
②过滤时玻璃棒要靠在三层滤纸的一边;
③漏斗的下端要与烧杯内壁相靠
过 滤
新课讲解
水过滤后仍然浑浊的原因:
1. 滤纸可能破损。
2. 滤液边缘高于滤纸边缘。
3. 盛装滤液的烧杯不干净。
4. 过滤次数太少。
玻璃棒的作用:引流,防止液体冲 破滤纸或溅出
新课讲解
二、除去可溶性杂质的方法
【常用的吸附剂】活性炭、木炭 等。
【说明】吸附属于物理变化
1.吸附
颜色
异味
吸附
新课讲解
【硬水】含有较多可溶性钙、镁化合物的水叫硬水。
【软水】含有较少或不含可溶性钙、镁化合物的水叫硬水。
认识硬水的危害
硬水和软水
新课讲解
【区分方法】把肥皂水倒入水中搅拌,若出现大量泡沫,就是软水;若不出现泡沫或出现浮渣,就是硬水。
软水
硬水
区分软水和硬水的方法
新课讲解
蒸馏(实验室)
硬水
硬水软化:除去硬水中的钙、镁化合物
煮沸(生活中)
软水
产生水垢(主要成分氢氧化镁、碳酸钙)
Mg(OH)2
CaCO3
新课讲解
简易装置
1.冷凝水:下口进、上口出
烧瓶
冷凝作用
2.加沸石(或碎瓷片):防止暴沸
2.蒸馏
新课讲解
一、除去不溶性杂质的方法:
1.静置
2.过滤
二、除去可溶性杂质的方法:
1.吸附
2.蒸馏
课堂小结
水的净化
课堂练习
101试卷库
4.2水的净化—随堂检测1
请同学们认真作答哟!
课堂练习
1.人类生活和工农业生产都离不开水,图是自来水净化水的过程示意图。
(1)自来水厂生产水时,使用的净水方法有_______;
A.沉淀 B.过滤 C.煮沸 D.蒸馏 E.吸附
(2)取水后加入絮凝剂(明矾)的作用是_______;
(3)自来水厂常用ClO2来消毒,漂白粉[有效成分为Ca(ClO)2]也可用于饮用水消毒。工业上制备漂白粉的化学方程式为:2Cl2+2Ca(OH)2=X+Ca(ClO)2+2H2O,X的化学方程式为_______,反应前后Cl元素的化合价( )(填字母)。
A.升高 B.降低 C.既升高又降低 D.不变
ABE
使悬浮物沉淀(或使悬浮物沉降)
CaCl2
C
2 .为防止震后疾病传染要对饮用水源进行处理,采取的措施有:①煮沸;②消毒;③过滤;④自然沉降。合理处理的顺序是( )。
A.③①②④ B.②④③① C.④③①② D.④③②①
D
3.如图3-3-6所示为实验室制取蒸馏水的简易装置,据图回答问题。
(1)写出下列仪器的名称:a_________、b_________、c_________。
(2)水在_________ 中由液态变为气态。在_________中得到蒸馏水,在制取蒸馏水的过程中发生的是_________变化。
(3)在烧杯中装有冷水,它起_________ _________ 的作用。
蒸馏瓶 石棉网 酒精灯
蒸馏瓶
试管
物理
降温使水蒸气冷凝
任务一:请完成101试卷库《4.2水的净化课后作业1》
任务二:预习新课:P79-P82页完成以下几个问题:
1、水的组成是什么?
2、水的电解实质是什么?
3、如何对物质进行分类?
课后作业
九年级
4.2 水的净化
1、了解纯水与自然水、硬水与软水的区别。
2、了解吸附、沉淀、过滤和蒸馏等净水的方法。
学习目标
自主学习
预习新课:P74-P78,完成以下几个问题:
1、如何净化自然界的水资源?
2、净化水需要哪些操作?
3、如何区分软水和硬水?
自主学习反馈
1.在野外和灾区可用下列几个步骤将河水转化成饮用水:①化学沉降(用明矾);②消毒杀菌(漂白粉);③自然沉降;④加热煮沸。以上处理过程最合理的顺序是( )
A.③②①④ B.③①②④ C.③①④② D.①③②④
B
2.下列方法不属于净化水的措施是( )
A.吸附 B.过滤 C.电解 D.蒸馏
C
3.硬水和软水的本质区别是( )
A.硬水浑浊,软水澄清
B.硬水含杂质多,软水含杂质少
C.硬水不是纯净物,软水是纯净物
D.硬水中含有较多的可溶性钙、镁化合物,软水不含或含少量的可溶性钙、镁化合物
D
自主学习反馈
情景导入
这杯透明的水中含有杂质吗?
纯水是无色、无臭、清澈透明的,而自然界中的河水、湖水等由于含有许多可溶性或不溶性的杂质,因此常呈现浑浊。
河水
自来水
纯净水
纯水:无色、无味、液体
标准状况下,4○C密度最大,为1g/cm3
标准大气压下,凝固点为0 ○C ,沸点为100 ○C
新课讲解
配水泵
活性炭吸附池
用户
过滤池
反应沉淀池
加絮凝剂
(明矾)
水库
取水口
清水池
投药消毒
新课讲解
明矾
学名:十二水合硫酸铝钾
化学式:KAl(SO4)2·12H2O
又称:明矾、白矾、钾矾、钾铝矾、钾明矾
Al3+很容易水解,生成胶状的氢氧化铝Al(OH)3:
Al3+ + 3H2O = Al(OH)3(胶体)+ 3H+
氢氧化铝胶体的吸附能力很强,可以吸附水里悬浮的杂质,并形成沉淀,使水澄清。所以,明矾是一种较好的净水剂。
新课讲解
沉淀:1.静置沉淀
2.吸附沉淀:加入絮凝剂(明矾),溶于水形成胶状物对悬浮杂质吸附,使杂质沉降。
【归纳】自来水厂用到的主要的净水方法:
沉淀→过滤→吸附→消毒
过滤: 除去水中不溶性的杂质。
吸附: 除去水中可溶性的杂质,如颜色、气味、有毒杂质等。
消毒: 向水中通入氯气(Cl2),氯气与水发生化学反应,产生次氯酸,杀灭细菌。
新课讲解
水中的杂质可以分为可溶性杂质和不溶性杂质两大类。我们一起学习除去这两类杂质的方法。
除去杂质的方法
(分离混合物的方法)
过 滤
吸 附
蒸 馏
新课讲解
【例】如何除去河水中的泥沙?
一、除去不溶性杂质的方法:
过滤
新课讲解
【操作要点】“一贴、二低、三靠”
铁架台
漏斗
玻璃棒
烧杯
滤纸
过 滤
新课讲解
一贴:滤纸紧贴漏斗内壁。
二低:①滤纸边缘要低于漏斗边缘;
②漏斗中的液面应低于滤纸的边缘
三靠:
①倾倒液体的烧杯口要紧靠玻璃棒;
②过滤时玻璃棒要靠在三层滤纸的一边;
③漏斗的下端要与烧杯内壁相靠
过 滤
新课讲解
水过滤后仍然浑浊的原因:
1. 滤纸可能破损。
2. 滤液边缘高于滤纸边缘。
3. 盛装滤液的烧杯不干净。
4. 过滤次数太少。
玻璃棒的作用:引流,防止液体冲 破滤纸或溅出
新课讲解
二、除去可溶性杂质的方法
【常用的吸附剂】活性炭、木炭 等。
【说明】吸附属于物理变化
1.吸附
颜色
异味
吸附
新课讲解
【硬水】含有较多可溶性钙、镁化合物的水叫硬水。
【软水】含有较少或不含可溶性钙、镁化合物的水叫硬水。
认识硬水的危害
硬水和软水
新课讲解
【区分方法】把肥皂水倒入水中搅拌,若出现大量泡沫,就是软水;若不出现泡沫或出现浮渣,就是硬水。
软水
硬水
区分软水和硬水的方法
新课讲解
蒸馏(实验室)
硬水
硬水软化:除去硬水中的钙、镁化合物
煮沸(生活中)
软水
产生水垢(主要成分氢氧化镁、碳酸钙)
Mg(OH)2
CaCO3
新课讲解
简易装置
1.冷凝水:下口进、上口出
烧瓶
冷凝作用
2.加沸石(或碎瓷片):防止暴沸
2.蒸馏
新课讲解
一、除去不溶性杂质的方法:
1.静置
2.过滤
二、除去可溶性杂质的方法:
1.吸附
2.蒸馏
课堂小结
水的净化
课堂练习
101试卷库
4.2水的净化—随堂检测1
请同学们认真作答哟!
课堂练习
1.人类生活和工农业生产都离不开水,图是自来水净化水的过程示意图。
(1)自来水厂生产水时,使用的净水方法有_______;
A.沉淀 B.过滤 C.煮沸 D.蒸馏 E.吸附
(2)取水后加入絮凝剂(明矾)的作用是_______;
(3)自来水厂常用ClO2来消毒,漂白粉[有效成分为Ca(ClO)2]也可用于饮用水消毒。工业上制备漂白粉的化学方程式为:2Cl2+2Ca(OH)2=X+Ca(ClO)2+2H2O,X的化学方程式为_______,反应前后Cl元素的化合价( )(填字母)。
A.升高 B.降低 C.既升高又降低 D.不变
ABE
使悬浮物沉淀(或使悬浮物沉降)
CaCl2
C
2 .为防止震后疾病传染要对饮用水源进行处理,采取的措施有:①煮沸;②消毒;③过滤;④自然沉降。合理处理的顺序是( )。
A.③①②④ B.②④③① C.④③①② D.④③②①
D
3.如图3-3-6所示为实验室制取蒸馏水的简易装置,据图回答问题。
(1)写出下列仪器的名称:a_________、b_________、c_________。
(2)水在_________ 中由液态变为气态。在_________中得到蒸馏水,在制取蒸馏水的过程中发生的是_________变化。
(3)在烧杯中装有冷水,它起_________ _________ 的作用。
蒸馏瓶 石棉网 酒精灯
蒸馏瓶
试管
物理
降温使水蒸气冷凝
任务一:请完成101试卷库《4.2水的净化课后作业1》
任务二:预习新课:P79-P82页完成以下几个问题:
1、水的组成是什么?
2、水的电解实质是什么?
3、如何对物质进行分类?
课后作业
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
