九年级化学人教版上册第5单元 课题3 《利用化学方程式的简单计算》(课件21页)
文档属性
| 名称 | 九年级化学人教版上册第5单元 课题3 《利用化学方程式的简单计算》(课件21页) |

|
|
| 格式 | pptx | ||
| 文件大小 | 911.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-18 00:00:00 | ||
图片预览








文档简介
(共21张PPT)
化学方程式
课题3 利用化学方程式的简单计算
学习目标:
1、掌握根据化学方程式的计算方法。重点!
2、掌握解题的方法、步骤和格式。
(中考必考题型,约8分)
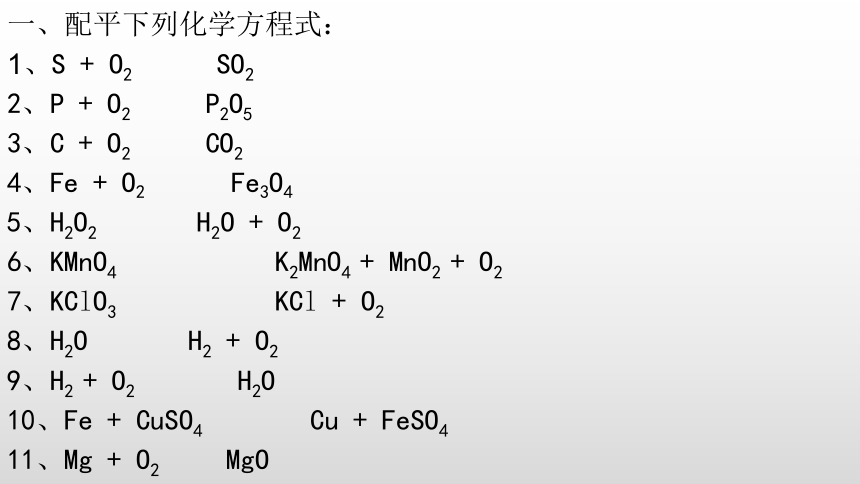
一、配平下列化学方程式:
1、S + O2 SO2
2、P + O2 P2O5
3、C + O2 CO2
4、Fe + O2 Fe3O4
5、H2O2 H2O + O2
6、KMnO4 K2MnO4 + MnO2 + O2
7、KClO3 KCl + O2
8、H2O H2 + O2
9、H2 + O2 H2O
10、Fe + CuSO4 Cu + FeSO4
11、Mg + O2 MgO
12、Na2CO3 + HCl NaCl + CO2+ H2O
13 、Hg+O2 HgO
14 、HgO Hg+O2
二、写出下列反应的化学方程式:
1、氢气与氧化铜共热,生成铜和水
2、有毒的一氧化碳燃烧生成无毒的二氧化碳
3、铁与硫酸铜溶液反应,生成铜和硫酸亚铁
4、碳酸钠与稀盐酸反应,生成氯化钠、二氧化碳和水
5、碳酸钙和稀盐酸HCl反应,生成氯化钙、二氧化碳和水
6、氢氧化钙溶液与二氧化碳反应,生成碳酸钙和水
ZnSO4 + KOH Zn(OH)2 ↓ + K2SO4
方法:1、原子团当成一个整体来考虑配平,不要把原子团拆开。2、一般先配“原子团” 。
问题:若化学方程式出现原子团时,怎样配平?
1) Fe + H2SO4—— H2 ↑ + FeSO4
2) CuSO4 + NaOH——Cu(OH)2 ↓ + Na2SO4
2
2
Al2O3 + H2SO4—— H2O + Al2 (SO4)3
3
3
1、计算下列各题:
1)CaCO3的相对分子质量
2)2KMnO4的相对分子质量的总和
2、计算下列反应中各物质间的质量比。
2H2O === 2H2↑ + O2 ↑
通电
36 : 4 : 32
每 份质量的水通电,可生成 份质量的氢气和 份质量的氧气。现有36克水通电可生成 克氢气,同时生成 克氧气。
在研究化学反应时,不仅研究反应是否发生、反应的快慢、生成物是什么、实验中有什么现象,更重要的是解决反应物和生成物的质量的关系。
在实际生产中要解决的问题:
如:原料(反应物) 产品(生成物)
经过
化学变化
(1)以一定量的反应物得到最多的产物。
(2)要得到一定量产物最少需要多少反应物。
请计算:2H2 + O2 === 2H2O
质量比为:
若: 4克 ( )克 ( )克
( )克 64克 ( )克
( )克 ( )克 18克
思考:从上面的计算,你得到各物质相对质量的总和与实际质量成 比例(填“正”或“反”)
点燃
32
36
8
72
2
16
正
4 : 32 : 36
2H2O === 2H2↑ + O2 ↑
通电
36 : 4 : 32
36g 4g 32g
18g 2g 16g
结论:在化学反应中,各物质之间的相对质量总和与实际质量的关系是成 比例。
正
因此,根据化学方程式和利用各物质间的质量成正比例关系,可进行有关的计算。只要已知的一种物质的质量,可求其它物质的质量。
用相对分子质量总和表示各物质的质量关系
各物质的实际质量关系
72g 8g 64g
2H2O === 2H2↑ + O2 ↑
通电
36 4 32
18g 2g 16g
化学计算包括:化学和数学两个因素,其中化学知识是化学计算的基础,数学是化学计算的工具。
用相对分子质量总和表示各物质的质量关系
各物质的实际质量关系
说明:在化学方程式中利用两种物质,四个量中知道三个量就可以求第四个量。
化学方程式的计算
例1:燃烧64Kg硫,产生二氧化硫的质量是多少?
2)正确的化学方程式
点燃
3)写出已知物和未知物的质量比和实际质量
32
32+16×2= 64
64Kg
X
4)列比例式
求结果
1)设未知数
解:设产生二氧化硫的质量为X
32 64Kg
64 X
=
X= 128Kg
5)写简答
答:产生二氧化硫128Kg
例2:加热分解6.3g高锰酸钾,可以得到多少克氧气?
△
2×(39+55+16×4) =2×158=316
16×2=32
6.3g
X
解:设可以得到氧气质量为X
316 6.3g
32 X
=
X= 0.6g
答:加热分解6.3g高锰酸钾,可以得到0.6g克氧气
小结:化学方程式进行计算的步骤
(1)解:设未知数
(2)写出反应化学方程式
(3)写出有关物质(与计算有关的已知物和未知物)的相对分子质量(质量比)和已知量、未知量
(4) 列比例式,求解
(5) 简明地写出答案
已知一种物质的质量,可求其它物质的质量
注:不能缺少一个步骤!
练1、把31克白磷完全燃烧,可生成五氧化二磷多少克?
点燃
4×31=124
2×(31×2+16×5)=284
31g
X
解:设可生成五氧化二磷质量为X
4×31 31g
284 X
=
X =71g
答:可生成五氧化二磷71克。
练2、实验室中需要1.6g氧气进行实验。若用电解水的方法制取这些氧气,需要消耗水多少克?同时得到多少克氢气?
通电
36 4 32
解:设需要消耗水的质量为X
X Y 1.6g
36 X
32 1.6g
=
X=1.8g
4 Y
32 1.6g
=
Y=0.2g
答:需要消耗水1.8g,同时得到氢气0.2g
,且得到氢气质量为Y
练3、加热12.25g氯酸钾,充分反应后可制得氧气多少克?
解:设生成氧气的质量为X
△
2KClO3 === KCl + O2↑
MnO2
2×39+35.5+16×3
X
12.25g
X= 4.8g
答:加热12.25g克氯酸钾完全分解制取氧气4.8g
(1) .
(2) .
(3) .
√
×
×
( )
=245
3 ×( )
245 12.25g
96 X
=96
16×2
2
3
练4、加热分解12.25克氯酸钾,可得到多少克的氧气 同时生成氯化钾多少克?
解:设:可得到氧气的质量为X.
2KClO3
=====
MnO2
△
2KCl
+3O2
↑
2×122.5=245 2×(39+35.5)=149 96
12.25g Y X
245
-------
96
=
12.25g
-------
X
X=4.8g
答:分解12.25克氯酸钾可得到氧气 4.8克,氯化钾7.45克。
245 12.25g
------- = ----------
149 Y
Y= 7.45克
生成氯化钾的质量为Y
求KCl质量的另一方法:12.25g-4.8g=7.45g
练5、多少克镁在氧气中充分燃烧,可以生成5克氧化镁?
解:设可需要镁的质量为X
2Mg + O2 ==== 2MgO
点燃
2×24 2×40
X 5g
48 X
80 5g
--- = ---
X= 3 g
答:3克镁在氧气中充分燃烧可生成氧化镁 5 克。
练6、现有24g碳在氧气中燃烧,能生成多少g二氧化碳?
解:设产生二氧化碳的质量为X
点燃
12
12 24g
44 X
=
答: 24g碳在氧气中燃烧,能生成88g二氧化碳
24g X
C + O2====CO2
X= 88g
12+16×2= 44
练7、燃烧2.4g镁能生成多少克氧化镁
解:设生成氧化镁的质量为X
2Mg + O2=== 2MgO
点燃
2×24=48
2×(24+16)=80
2.4g X
48 2.4g
80 X
X=4g
答:燃烧2.4g镁能生成4克氧化镁.
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
化学方程式
课题3 利用化学方程式的简单计算
学习目标:
1、掌握根据化学方程式的计算方法。重点!
2、掌握解题的方法、步骤和格式。
(中考必考题型,约8分)
一、配平下列化学方程式:
1、S + O2 SO2
2、P + O2 P2O5
3、C + O2 CO2
4、Fe + O2 Fe3O4
5、H2O2 H2O + O2
6、KMnO4 K2MnO4 + MnO2 + O2
7、KClO3 KCl + O2
8、H2O H2 + O2
9、H2 + O2 H2O
10、Fe + CuSO4 Cu + FeSO4
11、Mg + O2 MgO
12、Na2CO3 + HCl NaCl + CO2+ H2O
13 、Hg+O2 HgO
14 、HgO Hg+O2
二、写出下列反应的化学方程式:
1、氢气与氧化铜共热,生成铜和水
2、有毒的一氧化碳燃烧生成无毒的二氧化碳
3、铁与硫酸铜溶液反应,生成铜和硫酸亚铁
4、碳酸钠与稀盐酸反应,生成氯化钠、二氧化碳和水
5、碳酸钙和稀盐酸HCl反应,生成氯化钙、二氧化碳和水
6、氢氧化钙溶液与二氧化碳反应,生成碳酸钙和水
ZnSO4 + KOH Zn(OH)2 ↓ + K2SO4
方法:1、原子团当成一个整体来考虑配平,不要把原子团拆开。2、一般先配“原子团” 。
问题:若化学方程式出现原子团时,怎样配平?
1) Fe + H2SO4—— H2 ↑ + FeSO4
2) CuSO4 + NaOH——Cu(OH)2 ↓ + Na2SO4
2
2
Al2O3 + H2SO4—— H2O + Al2 (SO4)3
3
3
1、计算下列各题:
1)CaCO3的相对分子质量
2)2KMnO4的相对分子质量的总和
2、计算下列反应中各物质间的质量比。
2H2O === 2H2↑ + O2 ↑
通电
36 : 4 : 32
每 份质量的水通电,可生成 份质量的氢气和 份质量的氧气。现有36克水通电可生成 克氢气,同时生成 克氧气。
在研究化学反应时,不仅研究反应是否发生、反应的快慢、生成物是什么、实验中有什么现象,更重要的是解决反应物和生成物的质量的关系。
在实际生产中要解决的问题:
如:原料(反应物) 产品(生成物)
经过
化学变化
(1)以一定量的反应物得到最多的产物。
(2)要得到一定量产物最少需要多少反应物。
请计算:2H2 + O2 === 2H2O
质量比为:
若: 4克 ( )克 ( )克
( )克 64克 ( )克
( )克 ( )克 18克
思考:从上面的计算,你得到各物质相对质量的总和与实际质量成 比例(填“正”或“反”)
点燃
32
36
8
72
2
16
正
4 : 32 : 36
2H2O === 2H2↑ + O2 ↑
通电
36 : 4 : 32
36g 4g 32g
18g 2g 16g
结论:在化学反应中,各物质之间的相对质量总和与实际质量的关系是成 比例。
正
因此,根据化学方程式和利用各物质间的质量成正比例关系,可进行有关的计算。只要已知的一种物质的质量,可求其它物质的质量。
用相对分子质量总和表示各物质的质量关系
各物质的实际质量关系
72g 8g 64g
2H2O === 2H2↑ + O2 ↑
通电
36 4 32
18g 2g 16g
化学计算包括:化学和数学两个因素,其中化学知识是化学计算的基础,数学是化学计算的工具。
用相对分子质量总和表示各物质的质量关系
各物质的实际质量关系
说明:在化学方程式中利用两种物质,四个量中知道三个量就可以求第四个量。
化学方程式的计算
例1:燃烧64Kg硫,产生二氧化硫的质量是多少?
2)正确的化学方程式
点燃
3)写出已知物和未知物的质量比和实际质量
32
32+16×2= 64
64Kg
X
4)列比例式
求结果
1)设未知数
解:设产生二氧化硫的质量为X
32 64Kg
64 X
=
X= 128Kg
5)写简答
答:产生二氧化硫128Kg
例2:加热分解6.3g高锰酸钾,可以得到多少克氧气?
△
2×(39+55+16×4) =2×158=316
16×2=32
6.3g
X
解:设可以得到氧气质量为X
316 6.3g
32 X
=
X= 0.6g
答:加热分解6.3g高锰酸钾,可以得到0.6g克氧气
小结:化学方程式进行计算的步骤
(1)解:设未知数
(2)写出反应化学方程式
(3)写出有关物质(与计算有关的已知物和未知物)的相对分子质量(质量比)和已知量、未知量
(4) 列比例式,求解
(5) 简明地写出答案
已知一种物质的质量,可求其它物质的质量
注:不能缺少一个步骤!
练1、把31克白磷完全燃烧,可生成五氧化二磷多少克?
点燃
4×31=124
2×(31×2+16×5)=284
31g
X
解:设可生成五氧化二磷质量为X
4×31 31g
284 X
=
X =71g
答:可生成五氧化二磷71克。
练2、实验室中需要1.6g氧气进行实验。若用电解水的方法制取这些氧气,需要消耗水多少克?同时得到多少克氢气?
通电
36 4 32
解:设需要消耗水的质量为X
X Y 1.6g
36 X
32 1.6g
=
X=1.8g
4 Y
32 1.6g
=
Y=0.2g
答:需要消耗水1.8g,同时得到氢气0.2g
,且得到氢气质量为Y
练3、加热12.25g氯酸钾,充分反应后可制得氧气多少克?
解:设生成氧气的质量为X
△
2KClO3 === KCl + O2↑
MnO2
2×39+35.5+16×3
X
12.25g
X= 4.8g
答:加热12.25g克氯酸钾完全分解制取氧气4.8g
(1) .
(2) .
(3) .
√
×
×
( )
=245
3 ×( )
245 12.25g
96 X
=96
16×2
2
3
练4、加热分解12.25克氯酸钾,可得到多少克的氧气 同时生成氯化钾多少克?
解:设:可得到氧气的质量为X.
2KClO3
=====
MnO2
△
2KCl
+3O2
↑
2×122.5=245 2×(39+35.5)=149 96
12.25g Y X
245
-------
96
=
12.25g
-------
X
X=4.8g
答:分解12.25克氯酸钾可得到氧气 4.8克,氯化钾7.45克。
245 12.25g
------- = ----------
149 Y
Y= 7.45克
生成氯化钾的质量为Y
求KCl质量的另一方法:12.25g-4.8g=7.45g
练5、多少克镁在氧气中充分燃烧,可以生成5克氧化镁?
解:设可需要镁的质量为X
2Mg + O2 ==== 2MgO
点燃
2×24 2×40
X 5g
48 X
80 5g
--- = ---
X= 3 g
答:3克镁在氧气中充分燃烧可生成氧化镁 5 克。
练6、现有24g碳在氧气中燃烧,能生成多少g二氧化碳?
解:设产生二氧化碳的质量为X
点燃
12
12 24g
44 X
=
答: 24g碳在氧气中燃烧,能生成88g二氧化碳
24g X
C + O2====CO2
X= 88g
12+16×2= 44
练7、燃烧2.4g镁能生成多少克氧化镁
解:设生成氧化镁的质量为X
2Mg + O2=== 2MgO
点燃
2×24=48
2×(24+16)=80
2.4g X
48 2.4g
80 X
X=4g
答:燃烧2.4g镁能生成4克氧化镁.
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
