第二章 分子结构与性质 体系构建 体验高考(共22张ppt)
文档属性
| 名称 | 第二章 分子结构与性质 体系构建 体验高考(共22张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 831.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-18 00:00:00 | ||
图片预览







文档简介
(共22张PPT)
体系构建 理清脉络 / 体验高考 素养提升
体系构建 体验高考
第二章
内容索引
体系构建 理清脉络
体验高考 素养提升
体系构建 理清脉络
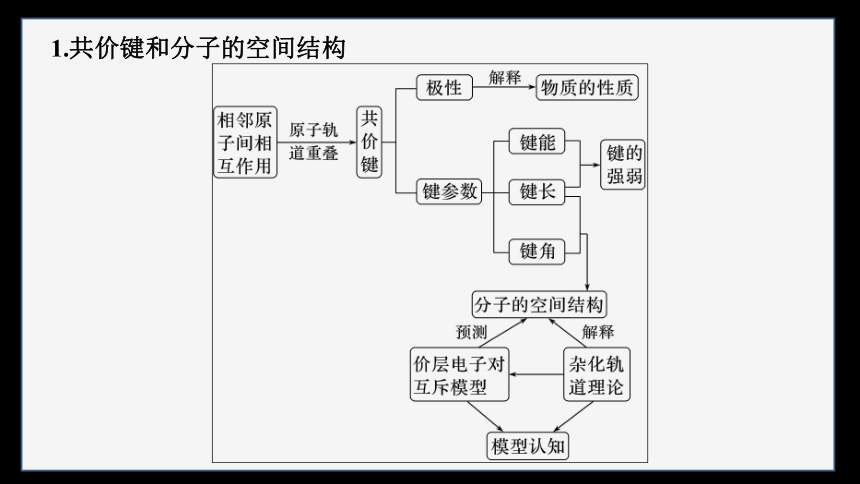
1.共价键和分子的空间结构
2.分子结构与物质的性质
返回
体验高考 素养提升
考向一 “两大理论”与微粒空间结构
例1
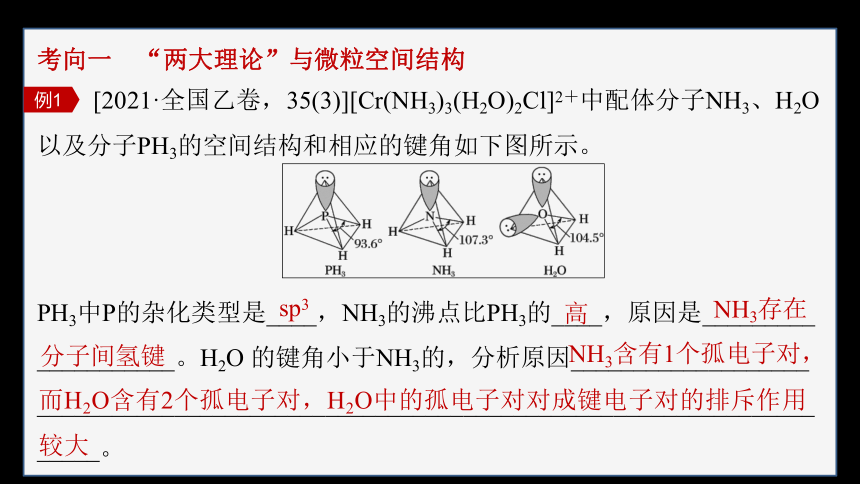
[2021·全国乙卷,35(3)][Cr(NH3)3(H2O)2Cl]2+中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如下图所示。
PH3中P的杂化类型是____,NH3的沸点比PH3的____,原因是_________
___________。H2O 的键角小于NH3的,分析原因___________________
______________________________________________________________
_____。
sp3
高
NH3存在
分子间氢键
NH3含有1个孤电子对,
而H2O含有2个孤电子对,H2O中的孤电子对对成键电子对的排斥作用较大
PH3中P的价层电子对数为3+1=4,故PH3中P的杂化类型是sp3; N原子的电负性较强,NH3存在分子间氢键,因此NH3的沸点比PH3的高;H2O的键角小于NH3的键角,原因是NH3含有1个孤电子对,而H2O含有2个孤电子对,H2O中的孤电子对对成键电子对的排斥作用较大。
(1)[2020·全国Ⅰ卷,35(3)]磷酸根离子的空间结构为___________,其中P的价层电子对数为____、杂化轨道类型为____。
例2
正四面体形
4
sp3
(2)[2021·河北,17(4)]已知KH2PO2是次磷酸的正盐,H3PO2的结构式为
______________,其中P采取______杂化方式。
sp3
含氧酸分子中只有羟基上的H可以电离;由KH2PO2是次磷酸的正盐可知,H3PO2为一元酸,其分子中只有一个羟基,另外2个H与P成键,还
有一个O与P形成双键,故其结构式为 ,其中P共形成4个σ
键、没有孤电子对,故其价层电子对数为4,采取sp3杂化。
sp2
(1)[2021·全国甲卷,35(3)]甲醇的沸点(64.7 ℃)介于水(100 ℃)和甲硫醇(CH3SH,7.6 ℃)之间,其原因是______________________________
_______________________________________。
例3
甲硫醇不能形成分子间氢键,而水
甲醇分子之间和水分子之间都存在氢键,因此沸点高于不含分子间氢键的甲硫醇,甲醇分子间氢键的总强度低于水分子间氢键的总强度,因此甲醇的沸点介于水和甲硫醇之间。
考向二 微粒作用与分子性质
和甲醇均能形成氢键,且水比甲醇的氢键多
(2)[2021·山东,16(2)节选]OF2的熔、沸点_____(填“高于”或“低于”)
Cl2O,原因是__________________________________________________
________。
低于
OF2和Cl2O结构相似,Cl2O的相对分子质量大,Cl2O的熔、
沸点高
例4
[2021·广东,20(2)(5)](2)H2S、CH4、H2O的沸点由高到低顺序为________________。
H2O>H2S>CH4
H2O分子间存在氢键,沸点较高,H2S、CH4的分子间范德华力随相对分子质量的增大而增加,因此沸点由高到低顺序为H2O>H2S>CH4。
(5)汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物Ⅰ 与化合物Ⅲ相比,水溶性较好的是___________。
化合物Ⅲ
中羟基能与水分子之间形成分子间氢键, 为易溶于水的钠盐,溶于水后电离出的 中O原子均能与水分子之间形成氢键,相同物质的量的两种物质溶于水后, 形成的氢键更多,因此化合物Ⅲ水溶性更好。
[2021·湖南,18(2)①节选]硅和卤素单质反应可以得到SiX4。
SiX4的熔、沸点
例5
SiF4 SiCl4 SiBr4 SiI4
熔点/K 183.0 203.2 278.6 393.7
沸点/K 187.2 330.8 427.2 560.7
0 ℃时,SiF4、SiCl4、SiBr4、SiI4呈液态的是________(填化学式),沸点依次升高的原因是___________________________________________
________________。
SiCl4
SiX4结构相似,相对分子质量依次增大,分子间
作用力依次增大
由题给熔、沸点数据可知,0 ℃时,四氟化硅为气态,四氯化硅为液态,四溴化硅、四碘化硅为固态;SiX4结构相似,相对分子质量依次增大,分子间作用力依次增大,则SiX4的沸点依次升高。
本课结束
第二章
体系构建 理清脉络 / 体验高考 素养提升
体系构建 体验高考
第二章
内容索引
体系构建 理清脉络
体验高考 素养提升
体系构建 理清脉络
1.共价键和分子的空间结构
2.分子结构与物质的性质
返回
体验高考 素养提升
考向一 “两大理论”与微粒空间结构
例1
[2021·全国乙卷,35(3)][Cr(NH3)3(H2O)2Cl]2+中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如下图所示。
PH3中P的杂化类型是____,NH3的沸点比PH3的____,原因是_________
___________。H2O 的键角小于NH3的,分析原因___________________
______________________________________________________________
_____。
sp3
高
NH3存在
分子间氢键
NH3含有1个孤电子对,
而H2O含有2个孤电子对,H2O中的孤电子对对成键电子对的排斥作用较大
PH3中P的价层电子对数为3+1=4,故PH3中P的杂化类型是sp3; N原子的电负性较强,NH3存在分子间氢键,因此NH3的沸点比PH3的高;H2O的键角小于NH3的键角,原因是NH3含有1个孤电子对,而H2O含有2个孤电子对,H2O中的孤电子对对成键电子对的排斥作用较大。
(1)[2020·全国Ⅰ卷,35(3)]磷酸根离子的空间结构为___________,其中P的价层电子对数为____、杂化轨道类型为____。
例2
正四面体形
4
sp3
(2)[2021·河北,17(4)]已知KH2PO2是次磷酸的正盐,H3PO2的结构式为
______________,其中P采取______杂化方式。
sp3
含氧酸分子中只有羟基上的H可以电离;由KH2PO2是次磷酸的正盐可知,H3PO2为一元酸,其分子中只有一个羟基,另外2个H与P成键,还
有一个O与P形成双键,故其结构式为 ,其中P共形成4个σ
键、没有孤电子对,故其价层电子对数为4,采取sp3杂化。
sp2
(1)[2021·全国甲卷,35(3)]甲醇的沸点(64.7 ℃)介于水(100 ℃)和甲硫醇(CH3SH,7.6 ℃)之间,其原因是______________________________
_______________________________________。
例3
甲硫醇不能形成分子间氢键,而水
甲醇分子之间和水分子之间都存在氢键,因此沸点高于不含分子间氢键的甲硫醇,甲醇分子间氢键的总强度低于水分子间氢键的总强度,因此甲醇的沸点介于水和甲硫醇之间。
考向二 微粒作用与分子性质
和甲醇均能形成氢键,且水比甲醇的氢键多
(2)[2021·山东,16(2)节选]OF2的熔、沸点_____(填“高于”或“低于”)
Cl2O,原因是__________________________________________________
________。
低于
OF2和Cl2O结构相似,Cl2O的相对分子质量大,Cl2O的熔、
沸点高
例4
[2021·广东,20(2)(5)](2)H2S、CH4、H2O的沸点由高到低顺序为________________。
H2O>H2S>CH4
H2O分子间存在氢键,沸点较高,H2S、CH4的分子间范德华力随相对分子质量的增大而增加,因此沸点由高到低顺序为H2O>H2S>CH4。
(5)汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物Ⅰ 与化合物Ⅲ相比,水溶性较好的是___________。
化合物Ⅲ
中羟基能与水分子之间形成分子间氢键, 为易溶于水的钠盐,溶于水后电离出的 中O原子均能与水分子之间形成氢键,相同物质的量的两种物质溶于水后, 形成的氢键更多,因此化合物Ⅲ水溶性更好。
[2021·湖南,18(2)①节选]硅和卤素单质反应可以得到SiX4。
SiX4的熔、沸点
例5
SiF4 SiCl4 SiBr4 SiI4
熔点/K 183.0 203.2 278.6 393.7
沸点/K 187.2 330.8 427.2 560.7
0 ℃时,SiF4、SiCl4、SiBr4、SiI4呈液态的是________(填化学式),沸点依次升高的原因是___________________________________________
________________。
SiCl4
SiX4结构相似,相对分子质量依次增大,分子间
作用力依次增大
由题给熔、沸点数据可知,0 ℃时,四氟化硅为气态,四氯化硅为液态,四溴化硅、四碘化硅为固态;SiX4结构相似,相对分子质量依次增大,分子间作用力依次增大,则SiX4的沸点依次升高。
本课结束
第二章
