化学人教版(2019)选择性必修3 3.4.2羧酸衍生物(共37张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 3.4.2羧酸衍生物(共37张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-18 00:00:00 | ||
图片预览








文档简介
(共37张PPT)
网
科
学
第三章 烃的衍生物
3.4.2 羧酸衍生物
学习目标
1.酯的组成和结构特点
2.酯的化学性质(水解反应)
3.酰胺和胺的结构特点及应用
4.酰胺和胺的化学性质
第四节 羧酸 羧酸衍生物
羧酸衍生物
羧酸分子中的羧基上的羟基被其他原子或原子团取代后的生成物
乙酸分子中的羧基上的羟基被乙氧基(__________)取代后生成__________,
乙酸分子中的羧基上的羟基被氨基(_____)取代后生成的____________.
例如
-OCH2CH3
乙酸乙酯
-NH2
乙酰胺
酯
戊酸戊酯
丁酸乙酯
乙酸异戊酯
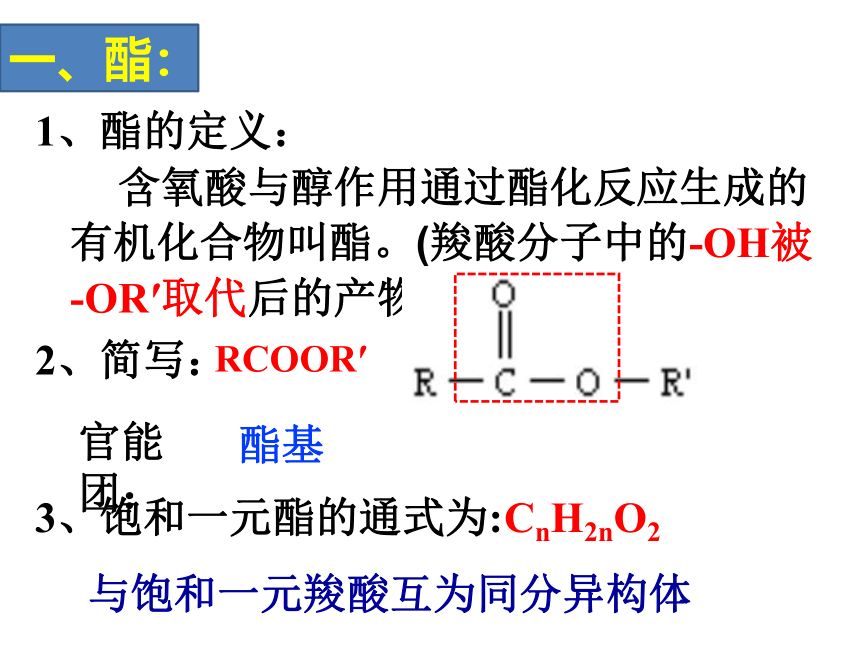
一、酯:
1、酯的定义:
含氧酸与醇作用通过酯化反应生成的有机化合物叫酯。(羧酸分子中的-OH被-OR′取代后的产物)
2、简写:
RCOOR′
官能团:
3、饱和一元酯的通式为:
酯基
CnH2nO2
与饱和一元羧酸互为同分异构体
4、酯的分类:
分类
①酸的不同
②酯基的数目
无机酸酯 如:CH3CH2-O-NO2
硝酸乙酯
有机酸酯 如:CH3COOCH3
一元酸酯 如:CH3COOCH3
二元酸酯 如:乙二酸二乙酯
多元酸酯 如:油脂
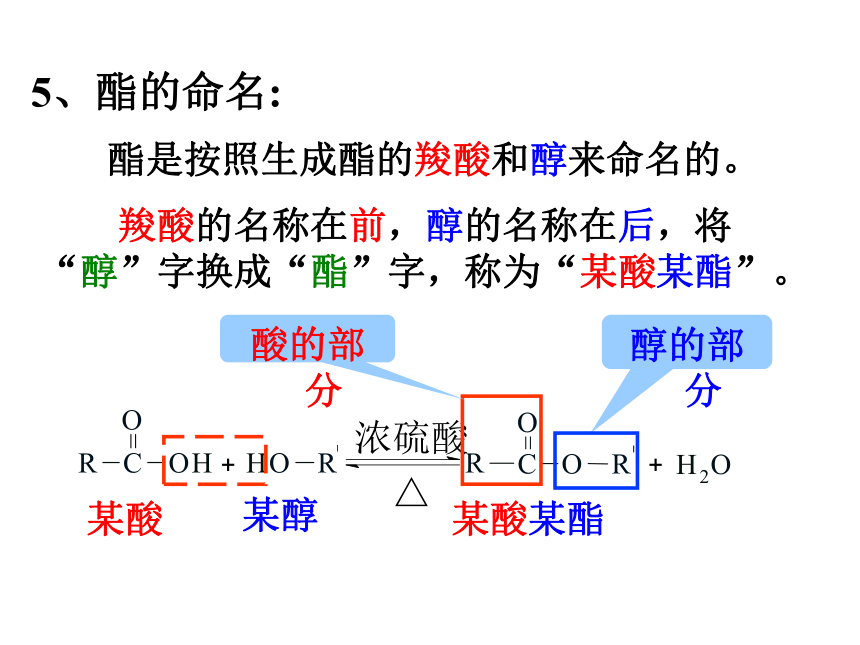
5、酯的命名:
羧酸的名称在前,醇的名称在后,将“醇”字换成“酯”字,称为“某酸某酯”。
酯是按照生成酯的羧酸和醇来命名的。
浓硫酸
△
某酸
某醇
某酸某酯
酸的部分
醇的部分
请说出下列酯的名称:
HCOOCH3
甲酸甲酯
CH3COOCH3
CH3CH2COOC2H5
丙酸乙酯
乙酸甲酯
乙二酸二乙酯
COOCH2CH3
COOCH2CH3
练习:
6、酯的同分异构现象:
①碳架异构、位置异构
②官能团异构
饱和一元酯和等碳的饱和一元羧酸互为同分异构体,通式都为:
CnH2nO2
例:写出C4H8O2的同分异构体
7、酯的物理性质、存在及用途:
(1)低级酯是具有芳香气味的液体
(2)密度一般小于水
(3)难溶于水,易溶于乙醇、乙醚等有机溶剂
物理性质:
存在:
酯类广泛存在于自然界。低级酯是有芳香气味的液体,存在于各种水果和花草中。
用途:
作溶剂,作制备饮料和糖果的香料。
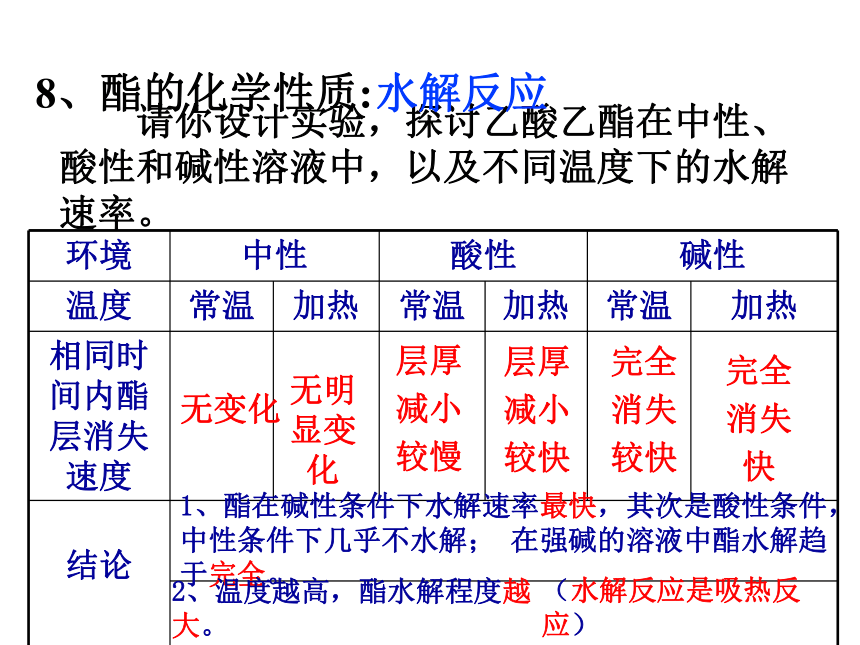
8、酯的化学性质:
请你设计实验,探讨乙酸乙酯在中性、酸性和碱性溶液中,以及不同温度下的水解速率。
水解反应
环境 中性 酸性 碱性
温度 常温 加热 常温 加热 常温 加热
相同时间内酯层消失速度
结论
无变化
无明显变化
层厚
减小
较慢
层厚
减小
较快
完全
消失
较快
完全
消失
快
1、酯在碱性条件下水解速率最快,其次是酸性条件,中性条件下几乎不水解; 在强碱的溶液中酯水解趋于完全。
2、温度越高,酯水解程度越大。
(水解反应是吸热反应)
结论:
酯类在酸或碱的条件下可以发生水解反应,且碱存在时水解更彻底。
水解速率:NaOH溶液>稀硫酸>水
加热>室温
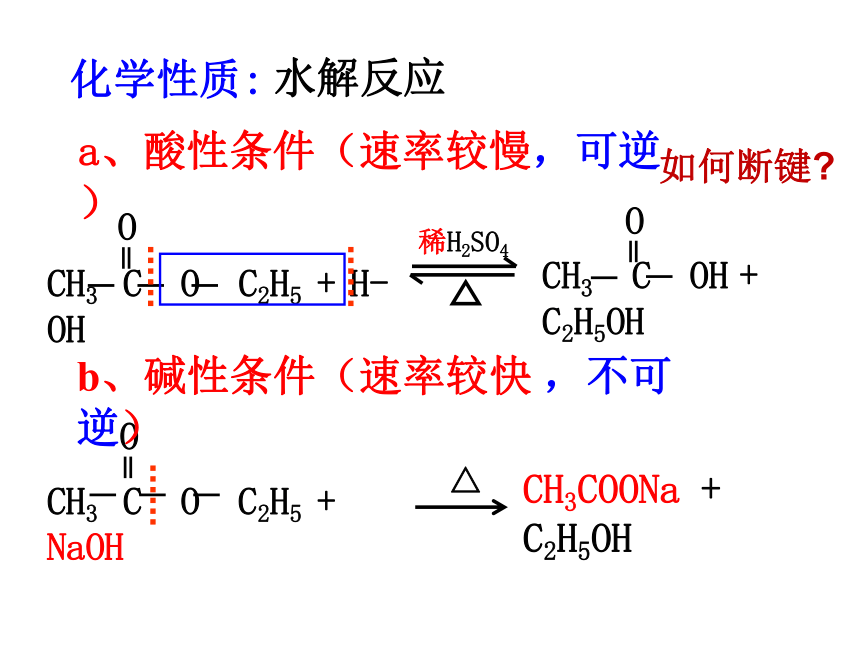
化学性质:
水解反应
CH3COONa + C2H5OH
CH3 C O C2H5 + NaOH
O
△
b、碱性条件(速率较快 ,不可逆)
a、酸性条件(速率较慢,可逆)
稀H2SO4
CH3 C OH + C2H5OH
O
CH3 C O C2H5 + H-OH
O
如何断键
思考:无机酸和碱在酯类水解的反应中分别起什么作用?
酸:
催化作用,不影响化学平衡。
(1)催化作用;
(2)中和生成的酸,使水解程度增大,
若碱过量则水解进行到底。
碱:
写出下列下列物质在酸性和碱性条件下的水解反应方程式。
练习:
(1)丙酸甲酯
(2)乙酸丙酯
HCOOCH3
(3)
HCOOCH3 +NaOH
△
CH3OH+HCOONa
CH3COOCH3
(4)
CH3COOCH3 +NaOH
CH3OH+CH3COONa
△
CH3OH+HCOOH
稀硫酸
△
+H2O
稀硫酸
△
CH3OH+CH3COOH
+H2O
COOC2H5
COOC2H5
(5)
COOC2H5
COOC2H5
+ NaOH
2
△
COONa
COONa
+ CH3CH2OH
2
CH2OOCCH3
CH2OOCCH3
(6)
CH2OOCCH3
CH2OOCCH3
+ NaOH
△
2
CH2OH
CH2OH
+ CH3COONa
2
COOH
COOH
+ CH3CH2OH
2
+ H2O
2
稀硫酸
△
稀硫酸
△
CH2OH
CH2OH
+ CH3COOH
2
+ H2O
2
酯化反应与酯水解反应的比较
酯 化 水 解
反应关系
催 化 剂
催化剂的 其他作用
加热方式
反应类型
NaOH中和酯水解生成的CH3COOH,提高酯的水解率
CH3COOH+C2H5OH CH3COOC2H5+H2O
浓 硫 酸
稀H2SO4或NaOH
吸水,提高CH3COOH与C2H5OH的转化率
酒精灯火焰加热
热水浴加热
酯化反应
取代反应
水解反应
取代反应
二、油脂:
油脂是重要的营养物质。日常生活中食用的油脂的主要成分是高级脂肪酸与甘油形成的酯,属于酯类化合物,结构可表示为:
R、R′、R″是高级脂肪酸的烃基,可以相同也可以不同
1、油脂:
2、油脂的分类:
CH2
O
C
O
R
CH
O
C
O
R’
CH2
O
C
O
R”
组成油脂的高级脂肪酸的种类很多,请写出硬脂酸、油酸分别与丙三醇反应的化学方程式
名称 饱和脂肪酸 不饱和脂肪酸
软脂酸 硬脂酸 油酸 亚油酸
表达式 C15H31COOH C17H31COOH
练习:
C17H35COOH
C17H33COOH
3、油脂的物理性质:
4、油脂的化学性质:
(1)水解反应
在酸、碱等催化剂的作用下油脂可以发生水解反应
CH2—O—C—C17H35
O
CH—O—C—C17H35
O
CH2—O—C—C17H35
O
硬脂酸甘油酯
硬脂酸
甘油
①在酸性条件下水解
油脂+3水
3高级脂肪酸+甘油
稀硫酸
△
稀硫酸
△
C17H35COOH +
3
CH2OH
CHOH
CH2OH
+3H2O
②在碱性条件下水解
硬脂酸甘油酯
硬脂酸钠
甘油
油脂+3氢氧化钠
3高级脂肪酸钠+甘油
△
油脂在碱性溶液中水解生成高级脂肪酸盐和甘油
生成肥皂
皂化反应
+3NaOH
△
C17H35COONa+
3
CH2OH
CHOH
CH2OH
CH2—O—C—C17H35
O
CH—O—C—C17H35
O
CH2—O—C—C17H35
O
制肥皂的简单流程:
脂肪、植物油
氢氧化钠
加热
高级脂肪酸钠、甘油、水
氯化钠
搅拌、静置
加入食盐的目的是发生盐析,可降低高级脂肪酸钠的溶解度,发生聚沉,使其分层析出。
上层:
下层:
高级脂肪酸钠
甘油、食盐溶液
加填充剂(松香、硅酸钠等)
压滤、干燥成型
成品肥皂
甘油
蒸馏
肥皂的主要成分为高级脂肪酸的盐
乙酸乙酯在碱性条件下也能发生水解反应,但不是皂化反应
油脂水解的应用:热的纯碱溶液可以提高去除油脂的效果。因为热的纯碱水解程度大,碱性强使油脂易水解
皂化
盐析
(2)油脂的氢化:
硬化油不易被空气氧化变质,便于储存和运输,可作为制造肥皂、人造奶油的原料。
不饱和程度较高、熔点较低的液态油
催化加氢
提高饱和度
半固态的脂肪
油脂的氢化,也称油脂的硬化
人造脂肪
硬化油
油酸甘油酯
硬脂酸甘油酯
(2)油脂的氢化:
CH2—O—C—C17H33
O
CH—O—C—C17H33
O
CH2—O—C—C17H33
O
+3 H2
△
催化剂
CH2—O—C—C17H35
O
CH—O—C—C17H35
O
CH2—O—C—C17H35
O
物质 油脂 矿物油
油 脂肪
组成 不饱和高级脂肪酸的甘油酯 饱和高级脂肪酸的甘油酯 多种烃(石油及其分馏产品)
状态 液态 固态 液态
化学 性质 能水解,兼有烯烃的性质 能水解 具有烃的性质,不能水解
存在 芝麻等油料作物中 动物脂肪 石油
油脂和矿物油的比较
1.如何利用化学方法鉴别植物油和矿物油
2.在油、脂肪、酯、汽油中一定能使酸性高锰酸钾溶液或溴水褪色的是哪种
油。从结构中是否含有碳碳双键进行考虑,油一定有碳碳双键,脂肪一般没有,酯可能有,直馏汽油一般没有而裂化汽油有。
取少量液体,加含酚酞的NaOH溶液,加热,若液体不分层,且红色变浅的为植物油,若液体分层,颜色无变化的为矿物油。
【思考】
三、酰胺:
1、胺:
烃基取代氨分子中的氢原子而形成的化合物
一般可写作:
官能团:
氨基(—NH2)
R-NH2
胺也可看作是烃分子中的氢原子被氨基所替代得到的化合物
苯胺
CH3—NH2
甲胺
①定义:
②胺的化学性质:
胺类化合物具有碱性,如苯胺能与盐酸反应,生成可溶于水的苯胺盐酸盐。
苯胺
苯胺盐酸盐
胺的用途很广,是重要的化工原料。例如,甲胺和苯胺都是合成医药、农药和染料等的重要原料。
2、酰胺:
①定义:
酰胺是羧酸分子中羟基被氨基所替代得到的化合物。
酰胺结构一般表示为:
酰基
酰胺基
R—C—NH2
O
②常见的酰胺:
乙酰胺
CH3
C
O
NH2
苯甲酰胺
C
O
NH2
N,N-二甲基甲酰胺
H
C
O
N(CH3)2
③酰胺的化学性质:
酰胺在酸或碱存在并加热的条件下可以发生水解反应。如果水解时加入碱,生成的酸就会变成盐,同时有氨气逸出。
④酰胺的应用:
酰胺常被用作溶剂和化工原料。例如:N,N-二甲基甲酰胺是良好的溶剂,可以溶解很多有机化合物和无机化合物,是生产多种化学纤维的溶剂,也用于合成农药、医药等
写出下列物质在酸或碱存在并加热的条件下可以发生水解反应的化学方程式。
R—C—NH2
O
O
CH3—C—OC2H5
CH3—C—NH2
O
练习:
氨 胺 酰胺 铵盐
组成元素
结构特点
化学性质
用途
NH3
三角锥形分子
N、H
C、N、H
C、O、N、H
N、H及其他元素
含有氨基
R-NH2
含有酰胺基
R
C
O
NH2
含有铵根离子
具有碱性,
与酸反应
生成铵盐
具有碱性,
与酸反应
生成盐
在酸或碱存在
并加热的条件
下可以发生
水解反应
受热易分解,
与碱共热
产生氨气
制冷剂,
生产硝酸和尿素
合成医药、
农药和染料
溶剂和
化工原料
生产化肥
和炸药
氨、胺、酰胺、铵盐性质比较
D
B
练习:
总结:重点:1.酯的组成和结构特点
2.酯的化学性质(水解反应)
3.酰胺和胺的结构特点及应用
4.酰胺和胺的化学性质
作业:
1、课后达标检测:P122—124
2、预习羧酸衍生物并完成优化方案:P52—55
网
科
学
第三章 烃的衍生物
3.4.2 羧酸衍生物
学习目标
1.酯的组成和结构特点
2.酯的化学性质(水解反应)
3.酰胺和胺的结构特点及应用
4.酰胺和胺的化学性质
第四节 羧酸 羧酸衍生物
羧酸衍生物
羧酸分子中的羧基上的羟基被其他原子或原子团取代后的生成物
乙酸分子中的羧基上的羟基被乙氧基(__________)取代后生成__________,
乙酸分子中的羧基上的羟基被氨基(_____)取代后生成的____________.
例如
-OCH2CH3
乙酸乙酯
-NH2
乙酰胺
酯
戊酸戊酯
丁酸乙酯
乙酸异戊酯
一、酯:
1、酯的定义:
含氧酸与醇作用通过酯化反应生成的有机化合物叫酯。(羧酸分子中的-OH被-OR′取代后的产物)
2、简写:
RCOOR′
官能团:
3、饱和一元酯的通式为:
酯基
CnH2nO2
与饱和一元羧酸互为同分异构体
4、酯的分类:
分类
①酸的不同
②酯基的数目
无机酸酯 如:CH3CH2-O-NO2
硝酸乙酯
有机酸酯 如:CH3COOCH3
一元酸酯 如:CH3COOCH3
二元酸酯 如:乙二酸二乙酯
多元酸酯 如:油脂
5、酯的命名:
羧酸的名称在前,醇的名称在后,将“醇”字换成“酯”字,称为“某酸某酯”。
酯是按照生成酯的羧酸和醇来命名的。
浓硫酸
△
某酸
某醇
某酸某酯
酸的部分
醇的部分
请说出下列酯的名称:
HCOOCH3
甲酸甲酯
CH3COOCH3
CH3CH2COOC2H5
丙酸乙酯
乙酸甲酯
乙二酸二乙酯
COOCH2CH3
COOCH2CH3
练习:
6、酯的同分异构现象:
①碳架异构、位置异构
②官能团异构
饱和一元酯和等碳的饱和一元羧酸互为同分异构体,通式都为:
CnH2nO2
例:写出C4H8O2的同分异构体
7、酯的物理性质、存在及用途:
(1)低级酯是具有芳香气味的液体
(2)密度一般小于水
(3)难溶于水,易溶于乙醇、乙醚等有机溶剂
物理性质:
存在:
酯类广泛存在于自然界。低级酯是有芳香气味的液体,存在于各种水果和花草中。
用途:
作溶剂,作制备饮料和糖果的香料。
8、酯的化学性质:
请你设计实验,探讨乙酸乙酯在中性、酸性和碱性溶液中,以及不同温度下的水解速率。
水解反应
环境 中性 酸性 碱性
温度 常温 加热 常温 加热 常温 加热
相同时间内酯层消失速度
结论
无变化
无明显变化
层厚
减小
较慢
层厚
减小
较快
完全
消失
较快
完全
消失
快
1、酯在碱性条件下水解速率最快,其次是酸性条件,中性条件下几乎不水解; 在强碱的溶液中酯水解趋于完全。
2、温度越高,酯水解程度越大。
(水解反应是吸热反应)
结论:
酯类在酸或碱的条件下可以发生水解反应,且碱存在时水解更彻底。
水解速率:NaOH溶液>稀硫酸>水
加热>室温
化学性质:
水解反应
CH3COONa + C2H5OH
CH3 C O C2H5 + NaOH
O
△
b、碱性条件(速率较快 ,不可逆)
a、酸性条件(速率较慢,可逆)
稀H2SO4
CH3 C OH + C2H5OH
O
CH3 C O C2H5 + H-OH
O
如何断键
思考:无机酸和碱在酯类水解的反应中分别起什么作用?
酸:
催化作用,不影响化学平衡。
(1)催化作用;
(2)中和生成的酸,使水解程度增大,
若碱过量则水解进行到底。
碱:
写出下列下列物质在酸性和碱性条件下的水解反应方程式。
练习:
(1)丙酸甲酯
(2)乙酸丙酯
HCOOCH3
(3)
HCOOCH3 +NaOH
△
CH3OH+HCOONa
CH3COOCH3
(4)
CH3COOCH3 +NaOH
CH3OH+CH3COONa
△
CH3OH+HCOOH
稀硫酸
△
+H2O
稀硫酸
△
CH3OH+CH3COOH
+H2O
COOC2H5
COOC2H5
(5)
COOC2H5
COOC2H5
+ NaOH
2
△
COONa
COONa
+ CH3CH2OH
2
CH2OOCCH3
CH2OOCCH3
(6)
CH2OOCCH3
CH2OOCCH3
+ NaOH
△
2
CH2OH
CH2OH
+ CH3COONa
2
COOH
COOH
+ CH3CH2OH
2
+ H2O
2
稀硫酸
△
稀硫酸
△
CH2OH
CH2OH
+ CH3COOH
2
+ H2O
2
酯化反应与酯水解反应的比较
酯 化 水 解
反应关系
催 化 剂
催化剂的 其他作用
加热方式
反应类型
NaOH中和酯水解生成的CH3COOH,提高酯的水解率
CH3COOH+C2H5OH CH3COOC2H5+H2O
浓 硫 酸
稀H2SO4或NaOH
吸水,提高CH3COOH与C2H5OH的转化率
酒精灯火焰加热
热水浴加热
酯化反应
取代反应
水解反应
取代反应
二、油脂:
油脂是重要的营养物质。日常生活中食用的油脂的主要成分是高级脂肪酸与甘油形成的酯,属于酯类化合物,结构可表示为:
R、R′、R″是高级脂肪酸的烃基,可以相同也可以不同
1、油脂:
2、油脂的分类:
CH2
O
C
O
R
CH
O
C
O
R’
CH2
O
C
O
R”
组成油脂的高级脂肪酸的种类很多,请写出硬脂酸、油酸分别与丙三醇反应的化学方程式
名称 饱和脂肪酸 不饱和脂肪酸
软脂酸 硬脂酸 油酸 亚油酸
表达式 C15H31COOH C17H31COOH
练习:
C17H35COOH
C17H33COOH
3、油脂的物理性质:
4、油脂的化学性质:
(1)水解反应
在酸、碱等催化剂的作用下油脂可以发生水解反应
CH2—O—C—C17H35
O
CH—O—C—C17H35
O
CH2—O—C—C17H35
O
硬脂酸甘油酯
硬脂酸
甘油
①在酸性条件下水解
油脂+3水
3高级脂肪酸+甘油
稀硫酸
△
稀硫酸
△
C17H35COOH +
3
CH2OH
CHOH
CH2OH
+3H2O
②在碱性条件下水解
硬脂酸甘油酯
硬脂酸钠
甘油
油脂+3氢氧化钠
3高级脂肪酸钠+甘油
△
油脂在碱性溶液中水解生成高级脂肪酸盐和甘油
生成肥皂
皂化反应
+3NaOH
△
C17H35COONa+
3
CH2OH
CHOH
CH2OH
CH2—O—C—C17H35
O
CH—O—C—C17H35
O
CH2—O—C—C17H35
O
制肥皂的简单流程:
脂肪、植物油
氢氧化钠
加热
高级脂肪酸钠、甘油、水
氯化钠
搅拌、静置
加入食盐的目的是发生盐析,可降低高级脂肪酸钠的溶解度,发生聚沉,使其分层析出。
上层:
下层:
高级脂肪酸钠
甘油、食盐溶液
加填充剂(松香、硅酸钠等)
压滤、干燥成型
成品肥皂
甘油
蒸馏
肥皂的主要成分为高级脂肪酸的盐
乙酸乙酯在碱性条件下也能发生水解反应,但不是皂化反应
油脂水解的应用:热的纯碱溶液可以提高去除油脂的效果。因为热的纯碱水解程度大,碱性强使油脂易水解
皂化
盐析
(2)油脂的氢化:
硬化油不易被空气氧化变质,便于储存和运输,可作为制造肥皂、人造奶油的原料。
不饱和程度较高、熔点较低的液态油
催化加氢
提高饱和度
半固态的脂肪
油脂的氢化,也称油脂的硬化
人造脂肪
硬化油
油酸甘油酯
硬脂酸甘油酯
(2)油脂的氢化:
CH2—O—C—C17H33
O
CH—O—C—C17H33
O
CH2—O—C—C17H33
O
+3 H2
△
催化剂
CH2—O—C—C17H35
O
CH—O—C—C17H35
O
CH2—O—C—C17H35
O
物质 油脂 矿物油
油 脂肪
组成 不饱和高级脂肪酸的甘油酯 饱和高级脂肪酸的甘油酯 多种烃(石油及其分馏产品)
状态 液态 固态 液态
化学 性质 能水解,兼有烯烃的性质 能水解 具有烃的性质,不能水解
存在 芝麻等油料作物中 动物脂肪 石油
油脂和矿物油的比较
1.如何利用化学方法鉴别植物油和矿物油
2.在油、脂肪、酯、汽油中一定能使酸性高锰酸钾溶液或溴水褪色的是哪种
油。从结构中是否含有碳碳双键进行考虑,油一定有碳碳双键,脂肪一般没有,酯可能有,直馏汽油一般没有而裂化汽油有。
取少量液体,加含酚酞的NaOH溶液,加热,若液体不分层,且红色变浅的为植物油,若液体分层,颜色无变化的为矿物油。
【思考】
三、酰胺:
1、胺:
烃基取代氨分子中的氢原子而形成的化合物
一般可写作:
官能团:
氨基(—NH2)
R-NH2
胺也可看作是烃分子中的氢原子被氨基所替代得到的化合物
苯胺
CH3—NH2
甲胺
①定义:
②胺的化学性质:
胺类化合物具有碱性,如苯胺能与盐酸反应,生成可溶于水的苯胺盐酸盐。
苯胺
苯胺盐酸盐
胺的用途很广,是重要的化工原料。例如,甲胺和苯胺都是合成医药、农药和染料等的重要原料。
2、酰胺:
①定义:
酰胺是羧酸分子中羟基被氨基所替代得到的化合物。
酰胺结构一般表示为:
酰基
酰胺基
R—C—NH2
O
②常见的酰胺:
乙酰胺
CH3
C
O
NH2
苯甲酰胺
C
O
NH2
N,N-二甲基甲酰胺
H
C
O
N(CH3)2
③酰胺的化学性质:
酰胺在酸或碱存在并加热的条件下可以发生水解反应。如果水解时加入碱,生成的酸就会变成盐,同时有氨气逸出。
④酰胺的应用:
酰胺常被用作溶剂和化工原料。例如:N,N-二甲基甲酰胺是良好的溶剂,可以溶解很多有机化合物和无机化合物,是生产多种化学纤维的溶剂,也用于合成农药、医药等
写出下列物质在酸或碱存在并加热的条件下可以发生水解反应的化学方程式。
R—C—NH2
O
O
CH3—C—OC2H5
CH3—C—NH2
O
练习:
氨 胺 酰胺 铵盐
组成元素
结构特点
化学性质
用途
NH3
三角锥形分子
N、H
C、N、H
C、O、N、H
N、H及其他元素
含有氨基
R-NH2
含有酰胺基
R
C
O
NH2
含有铵根离子
具有碱性,
与酸反应
生成铵盐
具有碱性,
与酸反应
生成盐
在酸或碱存在
并加热的条件
下可以发生
水解反应
受热易分解,
与碱共热
产生氨气
制冷剂,
生产硝酸和尿素
合成医药、
农药和染料
溶剂和
化工原料
生产化肥
和炸药
氨、胺、酰胺、铵盐性质比较
D
B
练习:
总结:重点:1.酯的组成和结构特点
2.酯的化学性质(水解反应)
3.酰胺和胺的结构特点及应用
4.酰胺和胺的化学性质
作业:
1、课后达标检测:P122—124
2、预习羧酸衍生物并完成优化方案:P52—55
