第二章 海水中的重要元素——钠和氯 第一节 钠及其化合物第2课时 钠的几种化合物 课时练(含答案)
文档属性
| 名称 | 第二章 海水中的重要元素——钠和氯 第一节 钠及其化合物第2课时 钠的几种化合物 课时练(含答案) |
|
|
| 格式 | doc | ||
| 文件大小 | 170.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-19 00:00:00 | ||
图片预览



文档简介
第2课时 钠的几种化合物
1. (2021·民乐第一中学高一期中)下列叙述正确的是( )
①Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
②Na2O与CO2发生化合反应生成Na2CO3,Na2O2与CO2发生置换反应生成O2
③Na2O是淡黄色物质,Na2O2是白色物质
④Na2O2可作供氧剂,而Na2O不行
⑤Na2O2和Na2O焰色试验的颜色均为黄色
A. 都正确 B. ①③④ C. ②③⑤ D. ④⑤
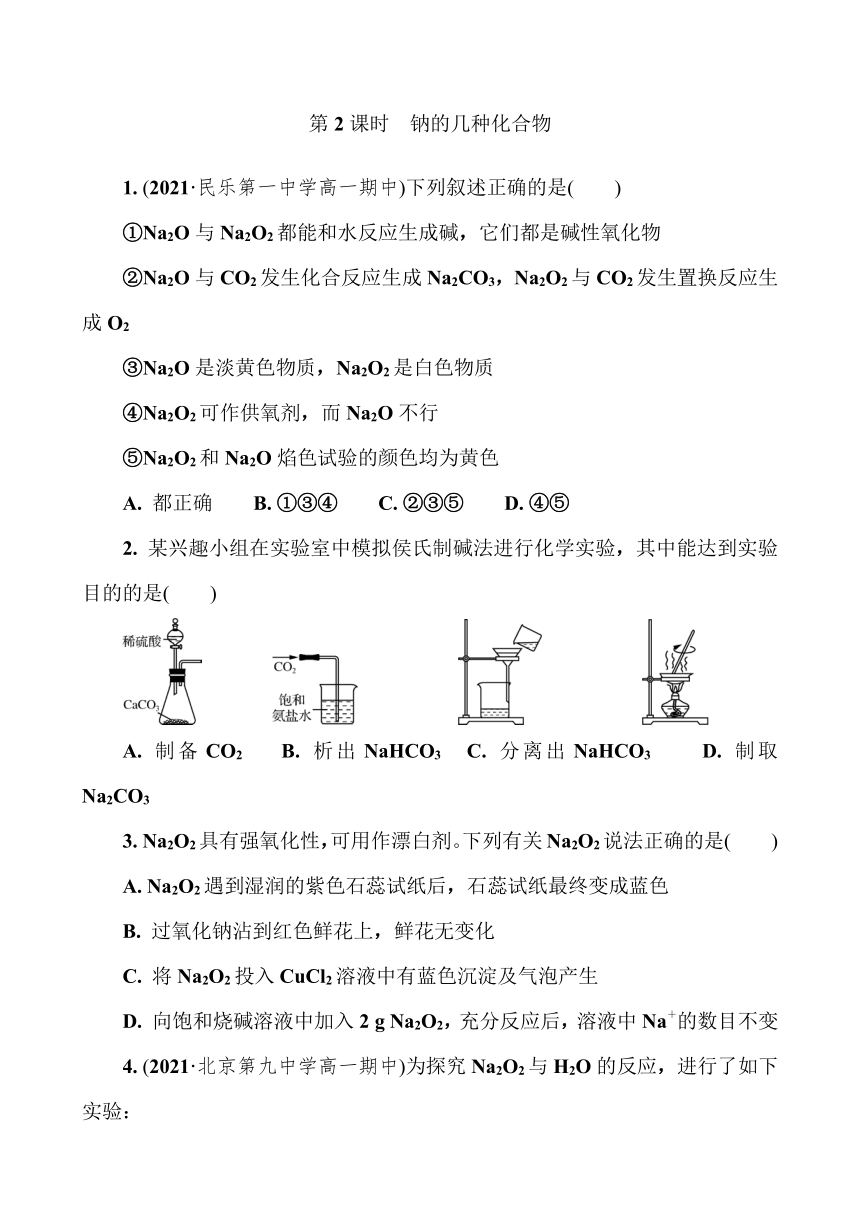
2. 某兴趣小组在实验室中模拟侯氏制碱法进行化学实验,其中能达到实验目的的是( )
A. 制备CO2 B. 析出NaHCO3 C. 分离出NaHCO3 D. 制取Na2CO3
3. Na2O2具有强氧化性,可用作漂白剂。下列有关Na2O2说法正确的是( )
A. Na2O2遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色
B. 过氧化钠沾到红色鲜花上,鲜花无变化
C. 将Na2O2投入CuCl2溶液中有蓝色沉淀及气泡产生
D. 向饱和烧碱溶液中加入2 g Na2O2,充分反应后,溶液中Na+的数目不变
4. (2021·北京第九中学高一期中)为探究Na2O2与H2O的反应,进行了如下实验:
下列说法不正确的是( )
A. 实验ⅰ中发生反应的化学方程式为2Na2O2+2H2O===4NaOH+O2↑
B. 实验ⅲ中MnO2作H2O2分解反应的催化剂
C. 综合实验ⅰ和ⅲ可以说明Na2O2与H2O反应有H2O2生成
D. 综合实验ⅱ和ⅲ可以说明使酚酞褪色的是O2
5. (2021·宝应期中)下列有关钠及其化合物的性质与用途具有对应关系的是( )
A. 钠单质熔点较低,可用于冶炼金属钛
B. 次氯酸钠具有强氧化性,可用作环境消毒剂
C. 氢氧化钠具有强碱性,可用作干燥剂
D. 碳酸氢钠受热易分解,可用于泡沫灭火器
6. 下列有关Na2CO3与NaHCO3的性质比较不正确的是( )
A. 相同浓度两溶液的碱性:Na2CO3>NaHCO3
B. 相同条件下在水中的溶解度:Na2CO3>NaHCO3
C. 与相同浓度的稀硫酸反应放出气泡的速率:NaHCO3D. 热稳定性:NaHCO37. (2020·贺柄炎中学高一阶段练习)过量的NaHCO3与Na2O2混合,在密闭容器中充分加热后,最后排出气体,残留的物质应是( )
A. Na2O和Na2O2 B. Na2O2和Na2CO3
C. Na2CO3 D. Na2O
8. 下列有关焰色反应实验操作注意事项的说法正确的是( )
①钾的火焰颜色要透过蓝色钴玻璃观察
②先将铂丝灼烧到与原来火焰的颜色相同,再蘸取被检验的物质
③每次实验后,要将铂丝用盐酸洗净
④实验时最好选择本身颜色较浅的火焰
⑤没有铂丝时,也可以用光洁无锈的铁丝代替
A. 仅有③不正确 B. 仅有④不正确
C. 仅有⑤不正确 D. 全对
9. 下图为几种物质的转化关系,其中A为金属,B为淡黄色固体粉末,每一物质均含有A元素。
(1) 写出下列物质的化学式:
B____________,C____________,E____________,F____________。
(2) 写出下列各步反应的化学方程式:
C→E___________________________________________________________;
C→F___________________________________________________________;
F→C____________________________________________________________。
10. (2020·存瑞中学高一期中)为了制取纯净干燥的气体A,可用如图所示装置,生成A的速度可通过滴入液体B的速度控制,已知A是一种无色、无味、不能使酸碱指示剂变色、不会在空气中燃烧的气体,但能使带火星的木条复燃。
(1) A是________。
(2) 若C是一种淡黄色固体,则烧瓶中发生反应的化学方程式
是________________________________。
(3) 若C是一种黑色粉末,则B物质是________,C物质的作用是________________。
(4) 洗气瓶(广口瓶)中装的试剂D是________,其作用是________________________。所制得的气体用______________法收集。
11. (2021·芜湖第一中学高一月考)某小组同学探究碳酸钠和碳酸氢钠的性质,请你与他们一起完成,并回答问题。
(1) 预测:从物质的类别来看,碳酸钠属于________类,可以与________等类别(至少写出两类)的物质发生反应。
(2) 设计实验并得出结论:
实验步骤 实验现象 结论或解释(用离子方程式表示)
①分别向盛有Na2CO3溶液和NaHCO3的试管中滴加少量澄清石灰水 均产生浑浊 碳酸钠溶液:Ca2++CO===CaCO3↓碳酸氢钠溶液:__________________________________________________________________
②向盛有Na2CO3溶液的试管中滴加稀盐酸 开始无气泡,一段时间后产生气泡 ①CO+H+===HCO②________________________________________________________________
(3) 下列试剂在一定条件下可以鉴别出Na2CO3溶液和NaHCO3溶液的是________。
A. 澄清石灰水 B. 稀盐酸 C. 酚酞
(4) 下列实验方案中,不能测定出Na2CO3和NaHCO3的混合物中Na2CO3质量分数的是________。
A. 取a g混合物充分加热,质量减少b g
B. 取a g混合物与足量的稀盐酸充分反应,加热、蒸干、灼烧,得到b g固体
C. 取a g混合物与足量的NaOH溶液充分反应,得到b g溶液
D. 取a g混合物与足量的稀硫酸充分反应,逸出气体用碱石灰吸收,质量增加b g
(5) 除去Na2CO3粉末中混有的少量NaHCO3固体的方法是________,所涉及的化学反应方程式为__________________________________________________。
第2课时 钠的几种化合物
1. D 2. B 3. C 4. D 5. B 6. C 7. C 8. D
9. (1) Na2O2 Na2CO3 NaOH(或NaCl) NaHCO3
(2) Na2CO3+Ba(OH)2===BaCO3↓+2NaOH
(或Na2CO3+2HCl===2NaCl+CO2↑+H2O)(答案合理即可)
Na2CO3+CO2+H2O===2NaHCO3
2NaHCO3Na2CO3+CO2↑+H2O
10. (1) O2
(2) 2Na2O2+2H2O===4NaOH+O2↑
(3) H2O2 催化剂
(4) 浓硫酸 除去O2中的水蒸气 向上排空气
11. (1) 盐 酸、碱、盐
(2) Ca2++2OH-+2HCO===CaCO3↓+ CO+2H2O
HCO +H+===CO2↑+H2O
(3) BC (4) CD
(5) 加热法 2NaHCO3Na2CO3+CO2↑+H2O
1. (2021·民乐第一中学高一期中)下列叙述正确的是( )
①Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
②Na2O与CO2发生化合反应生成Na2CO3,Na2O2与CO2发生置换反应生成O2
③Na2O是淡黄色物质,Na2O2是白色物质
④Na2O2可作供氧剂,而Na2O不行
⑤Na2O2和Na2O焰色试验的颜色均为黄色
A. 都正确 B. ①③④ C. ②③⑤ D. ④⑤
2. 某兴趣小组在实验室中模拟侯氏制碱法进行化学实验,其中能达到实验目的的是( )
A. 制备CO2 B. 析出NaHCO3 C. 分离出NaHCO3 D. 制取Na2CO3
3. Na2O2具有强氧化性,可用作漂白剂。下列有关Na2O2说法正确的是( )
A. Na2O2遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色
B. 过氧化钠沾到红色鲜花上,鲜花无变化
C. 将Na2O2投入CuCl2溶液中有蓝色沉淀及气泡产生
D. 向饱和烧碱溶液中加入2 g Na2O2,充分反应后,溶液中Na+的数目不变
4. (2021·北京第九中学高一期中)为探究Na2O2与H2O的反应,进行了如下实验:
下列说法不正确的是( )
A. 实验ⅰ中发生反应的化学方程式为2Na2O2+2H2O===4NaOH+O2↑
B. 实验ⅲ中MnO2作H2O2分解反应的催化剂
C. 综合实验ⅰ和ⅲ可以说明Na2O2与H2O反应有H2O2生成
D. 综合实验ⅱ和ⅲ可以说明使酚酞褪色的是O2
5. (2021·宝应期中)下列有关钠及其化合物的性质与用途具有对应关系的是( )
A. 钠单质熔点较低,可用于冶炼金属钛
B. 次氯酸钠具有强氧化性,可用作环境消毒剂
C. 氢氧化钠具有强碱性,可用作干燥剂
D. 碳酸氢钠受热易分解,可用于泡沫灭火器
6. 下列有关Na2CO3与NaHCO3的性质比较不正确的是( )
A. 相同浓度两溶液的碱性:Na2CO3>NaHCO3
B. 相同条件下在水中的溶解度:Na2CO3>NaHCO3
C. 与相同浓度的稀硫酸反应放出气泡的速率:NaHCO3
A. Na2O和Na2O2 B. Na2O2和Na2CO3
C. Na2CO3 D. Na2O
8. 下列有关焰色反应实验操作注意事项的说法正确的是( )
①钾的火焰颜色要透过蓝色钴玻璃观察
②先将铂丝灼烧到与原来火焰的颜色相同,再蘸取被检验的物质
③每次实验后,要将铂丝用盐酸洗净
④实验时最好选择本身颜色较浅的火焰
⑤没有铂丝时,也可以用光洁无锈的铁丝代替
A. 仅有③不正确 B. 仅有④不正确
C. 仅有⑤不正确 D. 全对
9. 下图为几种物质的转化关系,其中A为金属,B为淡黄色固体粉末,每一物质均含有A元素。
(1) 写出下列物质的化学式:
B____________,C____________,E____________,F____________。
(2) 写出下列各步反应的化学方程式:
C→E___________________________________________________________;
C→F___________________________________________________________;
F→C____________________________________________________________。
10. (2020·存瑞中学高一期中)为了制取纯净干燥的气体A,可用如图所示装置,生成A的速度可通过滴入液体B的速度控制,已知A是一种无色、无味、不能使酸碱指示剂变色、不会在空气中燃烧的气体,但能使带火星的木条复燃。
(1) A是________。
(2) 若C是一种淡黄色固体,则烧瓶中发生反应的化学方程式
是________________________________。
(3) 若C是一种黑色粉末,则B物质是________,C物质的作用是________________。
(4) 洗气瓶(广口瓶)中装的试剂D是________,其作用是________________________。所制得的气体用______________法收集。
11. (2021·芜湖第一中学高一月考)某小组同学探究碳酸钠和碳酸氢钠的性质,请你与他们一起完成,并回答问题。
(1) 预测:从物质的类别来看,碳酸钠属于________类,可以与________等类别(至少写出两类)的物质发生反应。
(2) 设计实验并得出结论:
实验步骤 实验现象 结论或解释(用离子方程式表示)
①分别向盛有Na2CO3溶液和NaHCO3的试管中滴加少量澄清石灰水 均产生浑浊 碳酸钠溶液:Ca2++CO===CaCO3↓碳酸氢钠溶液:__________________________________________________________________
②向盛有Na2CO3溶液的试管中滴加稀盐酸 开始无气泡,一段时间后产生气泡 ①CO+H+===HCO②________________________________________________________________
(3) 下列试剂在一定条件下可以鉴别出Na2CO3溶液和NaHCO3溶液的是________。
A. 澄清石灰水 B. 稀盐酸 C. 酚酞
(4) 下列实验方案中,不能测定出Na2CO3和NaHCO3的混合物中Na2CO3质量分数的是________。
A. 取a g混合物充分加热,质量减少b g
B. 取a g混合物与足量的稀盐酸充分反应,加热、蒸干、灼烧,得到b g固体
C. 取a g混合物与足量的NaOH溶液充分反应,得到b g溶液
D. 取a g混合物与足量的稀硫酸充分反应,逸出气体用碱石灰吸收,质量增加b g
(5) 除去Na2CO3粉末中混有的少量NaHCO3固体的方法是________,所涉及的化学反应方程式为__________________________________________________。
第2课时 钠的几种化合物
1. D 2. B 3. C 4. D 5. B 6. C 7. C 8. D
9. (1) Na2O2 Na2CO3 NaOH(或NaCl) NaHCO3
(2) Na2CO3+Ba(OH)2===BaCO3↓+2NaOH
(或Na2CO3+2HCl===2NaCl+CO2↑+H2O)(答案合理即可)
Na2CO3+CO2+H2O===2NaHCO3
2NaHCO3Na2CO3+CO2↑+H2O
10. (1) O2
(2) 2Na2O2+2H2O===4NaOH+O2↑
(3) H2O2 催化剂
(4) 浓硫酸 除去O2中的水蒸气 向上排空气
11. (1) 盐 酸、碱、盐
(2) Ca2++2OH-+2HCO===CaCO3↓+ CO+2H2O
HCO +H+===CO2↑+H2O
(3) BC (4) CD
(5) 加热法 2NaHCO3Na2CO3+CO2↑+H2O
