专题1 第二单元 科学家怎样研究有机物 微专题1 有机物分子式及结构式的确定(共27张ppt)
文档属性
| 名称 | 专题1 第二单元 科学家怎样研究有机物 微专题1 有机物分子式及结构式的确定(共27张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 600.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-20 00:00:00 | ||
图片预览







文档简介
(共27张PPT)
微专题1
WEIZHUANTIYI
有机物分子式及结构式的确定
专题1
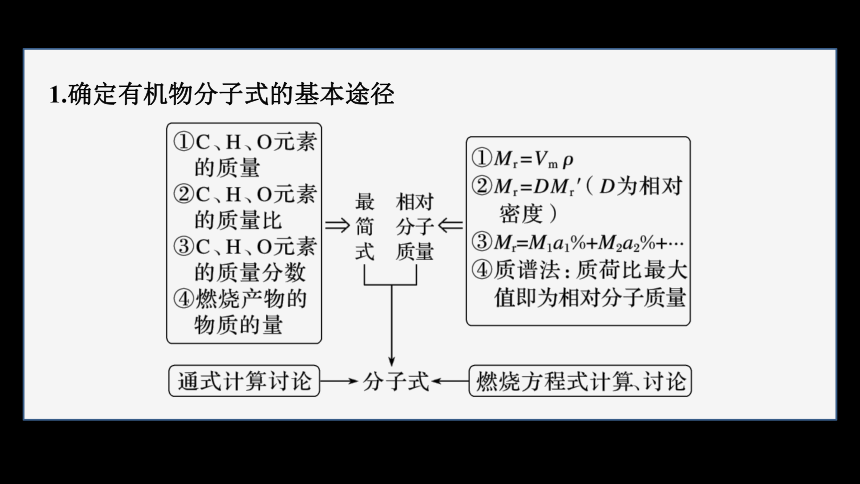
1.确定有机物分子式的基本途径
2.有机物分子式的确定方法
(1)直接法:有机物的密度(相对密度)→摩尔质量→1 mol有机物中各原子的物质的量→分子式。
(2)实验式法:各元素的质量分数→实验式 分子式。
(3)余数法:用烃的相对分子质量除以14,看商和余数。
(4)平均值法:根据有机混合物中各元素原子的平均原子数确定混合物的组成。常用十字交叉法使计算简化。平均值的特征:C小≤ ≤
C大,H小≤ ≤H大等。如测得两种烃的混合物的平均分子式是C1.7H4,则两种烃的组合有CH4和C2H4、CH4和C3H4等。
(5)化学方程式法:用有机反应中反应物、生成物之间“量”的关系,利用有机物燃烧的化学方程式求分子式的方法。
常用的化学方程式有:
(6)通式法:物质性质等→有机物类别及组成通式
→分子式。
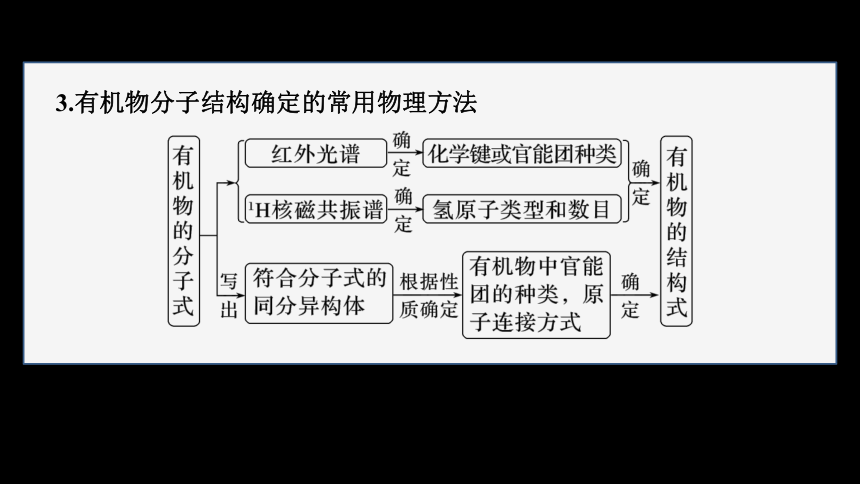
3.有机物分子结构确定的常用物理方法
(1)1H核磁共振谱
①原理:处于不同化学环境中的氢原子因产生共振时吸收电磁波的频率不同,在谱图上出现的位置不同,而且吸收峰的面积与__________成正比。
②作用:测定有机物分子中氢原子的 。
③分析:吸收峰数目= ,吸收峰面积比为________
。如CH3CH2OH的吸收峰面积比为 。
氢原子个数
类型和数目
氢原子的类型数目
氢原子个
数比
3∶2∶1
(2)红外光谱
①原理:不同基团或化学键吸收频率不同,在红外光谱图上将处于不同的位置。
②作用:初步判断有机物中含有的 或 。
如分子式为C2H6O的有机物A有如下两种可能的结构:Ⅰ(CH3CH2OH)或Ⅱ(CH3OCH3),利用红外光谱来测定,分子中有 或 可确定A的结构简式为Ⅰ(CH3CH2OH)。
基团
化学键
O—H
—OH
1
2
3
4
5
1.某物质在空气中完全燃烧时,生成水和二氧化碳的分子数之比为2∶1,则该物质可能是
①CH4 ②C2H4 ③C2H5OH ④CH3OH
A.②③ B.①④
C.①③ D.②④
√
1
2
3
4
5
该物质完全燃烧生成水和二氧化碳的分子数比为2∶1,即N(H2O)∶ N(CO2)=2∶1,则该物质中氢原子与碳原子个数之比为(2×2)∶1=4∶1,化学式满足N(C)∶N(H)=1∶4的有CH4、CH3OH,所以B正确。
2.(2021·济南高二阶段练习)用如图所示实验装置可以测定有机物中碳元素和氢元素的含量:取4.6 g某烃的含氧衍生物样品A置于氧气流中,用氧化铜作催化剂,在760 ℃左右样品A全部被氧化为二氧化碳和水,实验结束后测得装置a增重5.4 g,装置b增重8.8 g。下列有关说法错误的是
1
2
3
4
5
A.装置a、b中依次盛放的试剂可以为无水氯化钙和碱石灰
B.由实验数据只能确定A的最简式,无法确定A的分子式
C.开始加热前、停止加热后均需通入一段时间O2
D.采用1H核磁共振谱法可确定A的结构式
1
2
3
4
5
√
1
2
3
4
装置a、b中依次盛放的试剂可以为无水氯化钙和碱石灰,作用分别为吸收水和二氧化碳,故A正确;
5
1
2
3
4
5
1
2
3
4
开始加热前通入一段时间O2,赶走
装置中的水和二氧化碳,停止加热
后通入一段时间O2,使反应生成的
水和二氧化碳分别被无水氯化钙和
碱石灰完全吸收,使测量结果更准确,故C正确;
采用1H核磁共振谱法得出A中氢原子的种类,可确定A的结构式,故D正确。
5
3.如图所示是一种有机物的1H核磁共振谱图,请你观察图谱,分析其可能是下列物质中的
1
2
3
4
5
A.CH3CH2CH2CH3 B.(CH3)2CHCH3
C.CH3CH2CH2OH D.CH3CH2COOH
√
1
2
3
4
由图可知该有机物中有4种不同化学环境的氢原子。分析选项可知,A项有2种不同化学环境的氢原子,B项有2种不同化学环境的氢原子,C项有4种不同化学环境的氢原子,D项有3种不同化学环境的氢原子。
5
1
2
3
4
5
4.有机物C常用于食品行业。已知9.0 g C在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4 g和13.2 g,经检验剩余气体为O2。
(1)C分子的质谱图如图所示,
从图中可知其相对分子质量
是______,则C的分子式是
_________。
90
C3H6O3
1
2
3
4
5
由有机物质谱图可知,该有机物的相对分子质量为90;浓H2SO4吸水,所以生成的水是5.4 g,即0.3 mol,碱石灰吸收CO2,所以生成的CO2是13.2 g,即0.3 mol,所以9.0 g C中氧
原子的物质的量是 =0.3 mol,故此
有机物的实验式为CH2O,又因其相对分子质量为90,所以C的分子式
为C3H6O3。
1
2
3
4
5
(2)C能与NaHCO3溶液发生反应,C一定含有的官能团的名称是______。
羧基
C能与NaHCO3溶液发生反应,则C中含有羧基。
1
2
3
4
5
(3)C分子的 1H核磁共振谱图中有四组峰,峰面积之比是1∶1∶1∶3,
则C的结构简式是_____________。
根据氢原子的种类及个数之比可知,C的结构简式为 。
1
2
3
4
5
(4)0.1 mol C与足量Na反应,在标准状况下产生H2的体积是______L。
C中含有1个羟基和1个羧基,所以0.1 mol C与Na反应能生成0.1 mol H2,标准状况下的体积是2.24 L。
2.24
5.(2022·苏州高二质检)某有机化合物是汽车防冻液的成分之一,经元素分析测定,该有机化合物中各元素的质量分数是:碳38.7%,氢9.7%,氧51.6%。
(1)该有机化合物的实验式为_______。
1
2
3
4
5
CH3O
由题干信息可推知C、H、O原子个数比为
3∶1,则该有机物的实验式为CH3O。
1
2
3
4
5
(2)用相对密度法测得该有机化合物的密度是同温同压下氢气密度的31倍,则该物质的相对分子质量为____。
由题干信息知该物质的相对分子质量为2×31=62。
62
1
2
3
4
5
(3)根据该有机化合物的实验式和相对分子质量,推断其分子式为_________。
该有机物的实验式为CH3O,相对分子质量为62,则可推测该有机物的分子式为C2H6O2。
C2H6O2
1
2
3
4
5
(4)该有机化合物的红外光谱中有羟基(O—H)和烃基(C—H)的吸收峰,试写出其可能的结构简式:______________。
该有机化合物的红外光谱中有羟基(O—H)和烃基(C—H)的吸收峰,结合该有机物的分子式,该有机物的结构简式为HOCH2CH2OH。
HOCH2CH2OH
本课结束
专题1
微专题1
WEIZHUANTIYI
有机物分子式及结构式的确定
专题1
1.确定有机物分子式的基本途径
2.有机物分子式的确定方法
(1)直接法:有机物的密度(相对密度)→摩尔质量→1 mol有机物中各原子的物质的量→分子式。
(2)实验式法:各元素的质量分数→实验式 分子式。
(3)余数法:用烃的相对分子质量除以14,看商和余数。
(4)平均值法:根据有机混合物中各元素原子的平均原子数确定混合物的组成。常用十字交叉法使计算简化。平均值的特征:C小≤ ≤
C大,H小≤ ≤H大等。如测得两种烃的混合物的平均分子式是C1.7H4,则两种烃的组合有CH4和C2H4、CH4和C3H4等。
(5)化学方程式法:用有机反应中反应物、生成物之间“量”的关系,利用有机物燃烧的化学方程式求分子式的方法。
常用的化学方程式有:
(6)通式法:物质性质等→有机物类别及组成通式
→分子式。
3.有机物分子结构确定的常用物理方法
(1)1H核磁共振谱
①原理:处于不同化学环境中的氢原子因产生共振时吸收电磁波的频率不同,在谱图上出现的位置不同,而且吸收峰的面积与__________成正比。
②作用:测定有机物分子中氢原子的 。
③分析:吸收峰数目= ,吸收峰面积比为________
。如CH3CH2OH的吸收峰面积比为 。
氢原子个数
类型和数目
氢原子的类型数目
氢原子个
数比
3∶2∶1
(2)红外光谱
①原理:不同基团或化学键吸收频率不同,在红外光谱图上将处于不同的位置。
②作用:初步判断有机物中含有的 或 。
如分子式为C2H6O的有机物A有如下两种可能的结构:Ⅰ(CH3CH2OH)或Ⅱ(CH3OCH3),利用红外光谱来测定,分子中有 或 可确定A的结构简式为Ⅰ(CH3CH2OH)。
基团
化学键
O—H
—OH
1
2
3
4
5
1.某物质在空气中完全燃烧时,生成水和二氧化碳的分子数之比为2∶1,则该物质可能是
①CH4 ②C2H4 ③C2H5OH ④CH3OH
A.②③ B.①④
C.①③ D.②④
√
1
2
3
4
5
该物质完全燃烧生成水和二氧化碳的分子数比为2∶1,即N(H2O)∶ N(CO2)=2∶1,则该物质中氢原子与碳原子个数之比为(2×2)∶1=4∶1,化学式满足N(C)∶N(H)=1∶4的有CH4、CH3OH,所以B正确。
2.(2021·济南高二阶段练习)用如图所示实验装置可以测定有机物中碳元素和氢元素的含量:取4.6 g某烃的含氧衍生物样品A置于氧气流中,用氧化铜作催化剂,在760 ℃左右样品A全部被氧化为二氧化碳和水,实验结束后测得装置a增重5.4 g,装置b增重8.8 g。下列有关说法错误的是
1
2
3
4
5
A.装置a、b中依次盛放的试剂可以为无水氯化钙和碱石灰
B.由实验数据只能确定A的最简式,无法确定A的分子式
C.开始加热前、停止加热后均需通入一段时间O2
D.采用1H核磁共振谱法可确定A的结构式
1
2
3
4
5
√
1
2
3
4
装置a、b中依次盛放的试剂可以为无水氯化钙和碱石灰,作用分别为吸收水和二氧化碳,故A正确;
5
1
2
3
4
5
1
2
3
4
开始加热前通入一段时间O2,赶走
装置中的水和二氧化碳,停止加热
后通入一段时间O2,使反应生成的
水和二氧化碳分别被无水氯化钙和
碱石灰完全吸收,使测量结果更准确,故C正确;
采用1H核磁共振谱法得出A中氢原子的种类,可确定A的结构式,故D正确。
5
3.如图所示是一种有机物的1H核磁共振谱图,请你观察图谱,分析其可能是下列物质中的
1
2
3
4
5
A.CH3CH2CH2CH3 B.(CH3)2CHCH3
C.CH3CH2CH2OH D.CH3CH2COOH
√
1
2
3
4
由图可知该有机物中有4种不同化学环境的氢原子。分析选项可知,A项有2种不同化学环境的氢原子,B项有2种不同化学环境的氢原子,C项有4种不同化学环境的氢原子,D项有3种不同化学环境的氢原子。
5
1
2
3
4
5
4.有机物C常用于食品行业。已知9.0 g C在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4 g和13.2 g,经检验剩余气体为O2。
(1)C分子的质谱图如图所示,
从图中可知其相对分子质量
是______,则C的分子式是
_________。
90
C3H6O3
1
2
3
4
5
由有机物质谱图可知,该有机物的相对分子质量为90;浓H2SO4吸水,所以生成的水是5.4 g,即0.3 mol,碱石灰吸收CO2,所以生成的CO2是13.2 g,即0.3 mol,所以9.0 g C中氧
原子的物质的量是 =0.3 mol,故此
有机物的实验式为CH2O,又因其相对分子质量为90,所以C的分子式
为C3H6O3。
1
2
3
4
5
(2)C能与NaHCO3溶液发生反应,C一定含有的官能团的名称是______。
羧基
C能与NaHCO3溶液发生反应,则C中含有羧基。
1
2
3
4
5
(3)C分子的 1H核磁共振谱图中有四组峰,峰面积之比是1∶1∶1∶3,
则C的结构简式是_____________。
根据氢原子的种类及个数之比可知,C的结构简式为 。
1
2
3
4
5
(4)0.1 mol C与足量Na反应,在标准状况下产生H2的体积是______L。
C中含有1个羟基和1个羧基,所以0.1 mol C与Na反应能生成0.1 mol H2,标准状况下的体积是2.24 L。
2.24
5.(2022·苏州高二质检)某有机化合物是汽车防冻液的成分之一,经元素分析测定,该有机化合物中各元素的质量分数是:碳38.7%,氢9.7%,氧51.6%。
(1)该有机化合物的实验式为_______。
1
2
3
4
5
CH3O
由题干信息可推知C、H、O原子个数比为
3∶1,则该有机物的实验式为CH3O。
1
2
3
4
5
(2)用相对密度法测得该有机化合物的密度是同温同压下氢气密度的31倍,则该物质的相对分子质量为____。
由题干信息知该物质的相对分子质量为2×31=62。
62
1
2
3
4
5
(3)根据该有机化合物的实验式和相对分子质量,推断其分子式为_________。
该有机物的实验式为CH3O,相对分子质量为62,则可推测该有机物的分子式为C2H6O2。
C2H6O2
1
2
3
4
5
(4)该有机化合物的红外光谱中有羟基(O—H)和烃基(C—H)的吸收峰,试写出其可能的结构简式:______________。
该有机化合物的红外光谱中有羟基(O—H)和烃基(C—H)的吸收峰,结合该有机物的分子式,该有机物的结构简式为HOCH2CH2OH。
HOCH2CH2OH
本课结束
专题1
