专题4 第一单元 醇和酚 第1课时 醇(共86张ppt)
文档属性
| 名称 | 专题4 第一单元 醇和酚 第1课时 醇(共86张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-20 00:00:00 | ||
图片预览








文档简介
(共86张PPT)
第1课时
DIYIKESHI
醇的结构与性质 / 醇的重要应用 / 课时对点练
醇
专题4
核心素养
发展目标
1.通过认识羟基的结构,了解醇类的结构特点;进而从化学键、官能团的角度理解醇类消去反应、催化氧化反应的特征和规律。
2.通过乙醇性质的学习,能利用反应类型的规律判断、说明和预测醇类物质的性质。
内容索引
一、醇的结构与性质
二、醇的重要应用
课时对点练
醇的结构与性质
一
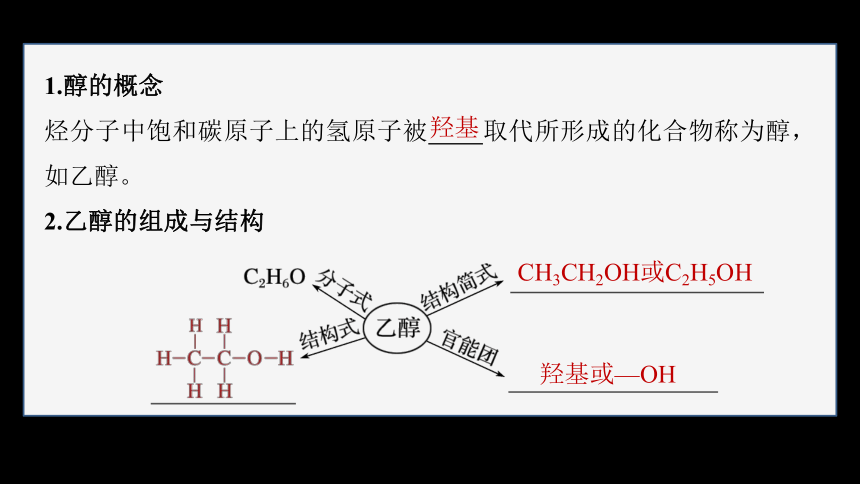
1.醇的概念
烃分子中饱和碳原子上的氢原子被 取代所形成的化合物称为醇,如乙醇。
2.乙醇的组成与结构
羟基
CH3CH2OH或C2H5OH
羟基或—OH
3.醇的化学性质
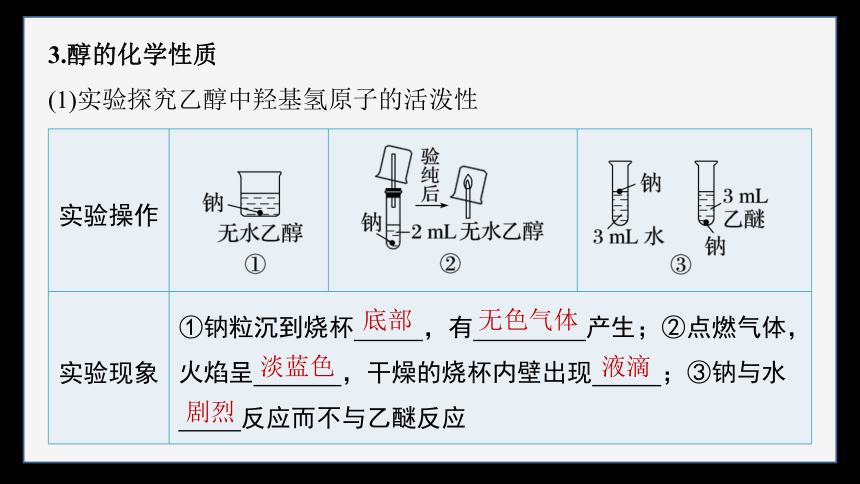
(1)实验探究乙醇中羟基氢原子的活泼性
实验操作
实验现象 ①钠粒沉到烧杯 ,有 产生;②点燃气体,火焰呈 ,干燥的烧杯内壁出现 ;③钠与水 反应而不与乙醚反应 底部
无色气体
淡蓝色
液滴
剧烈
实验结论 a.乙醇与钠反应生成乙醇钠,并放出 ,钠的密度比乙醇的 ;
b.乙醇中羟基氢原子比烃基氢原子_____
氢气
大
活泼
(2)氧化反应
①燃烧反应
CH3CH2OH+3O2 2CO2+3H2O
现象:产生淡蓝色火焰,同时放出大量的热。
②催化氧化:醇在 或 等催化剂存在下,可被氧气氧化为 或酮。
如: +O2 +2H2O、2CH3CH2OH
+O2 +2H2O。
③醇与酸性KMnO4溶液或K2Cr2O7溶液反应被氧化成羧酸。
2CH3CHO
铜
银
醛
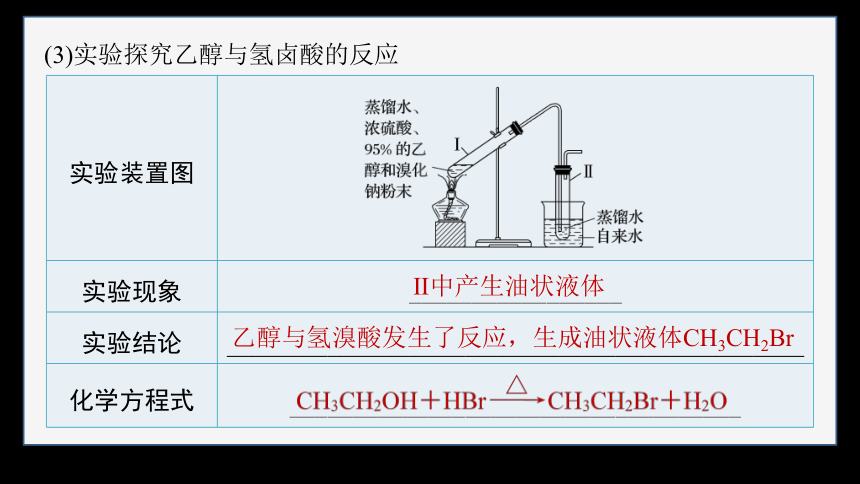
(3)实验探究乙醇与氢卤酸的反应
实验装置图
实验现象 _________________
实验结论 ______________________________________________
化学方程式 ____________________________________
Ⅱ中产生油状液体
乙醇与氢溴酸发生了反应,生成油状液体CH3CH2Br
醇不仅可以与氢溴酸反应,还可以与其他氢卤酸反应。在反应中,醇分子中的 被卤素原子取代生成卤代烃。
R—OH+HX―→ +H2O
在实验室和工业中,卤代烷烃常用 和 的反应来制备。
(4)脱水反应
乙醇可以在浓H2SO4、磷酸、Al2O3(400 ℃左右)或P2O5等催化剂的作用下发生脱水反应。
羟基
R—X
醇
氢卤酸
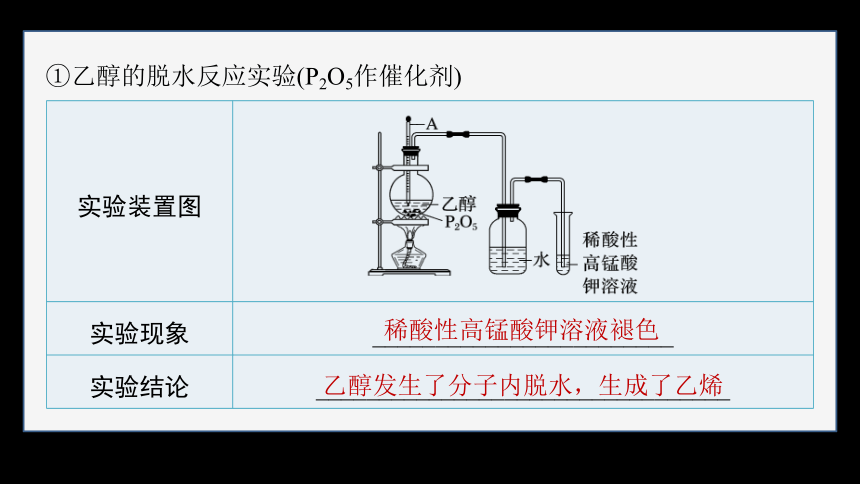
①乙醇的脱水反应实验(P2O5作催化剂)
实验装置图
实验现象 ________________________
实验结论 _________________________________
稀酸性高锰酸钾溶液褪色
乙醇发生了分子内脱水,生成了乙烯
实验室中经常采用乙醇和浓硫酸共热发生脱水反应来获得乙烯或乙醚。化学方程式分别为CH3CH2OH 、
2CH3CH2OH 。
②消去反应的概念
在一定条件下,一个有机化合物分子内脱去一个或几个 生成____
化合物(含双键或三键)的反应。
CH2==CH2↑+H2O
CH3CH2OCH2CH3+H2O
小分子
不饱
和
4.从微观结构分析醇的化学性质(以乙醇为例,如下图)
总结乙醇所能发生的化学反应:
乙醇发生反应的化学方程式 反应类型 断裂的共价键 反应条件
(1) 2CH3CH2OH+2Na―→ __________________ 反应 ___ Na
2CH3CH2ONa+H2↑
置换
e
(2) CH3CH2OH+HBr ________________ 反应 __ HBr,△
(3) 2CH3CH2OH+O2 _________________ 反应 ___ O2,Cu,△
(4) CH3CH2OH __________________ 反应 ___ 浓H2SO4,170 ℃
(5) 2CH3CH2OH _____________________ 反应 ___ 浓H2SO4,140 ℃
CH3CH2Br+H2O
2CH3CHO+2H2O
CH2==CH2↑+H2O
CH3CH2OCH2CH3+H2O
取代
d
氧化
ce
消去
ad
取代
de
实验室常用浓硫酸和乙醇混合加热制取乙烯,反应装置如
图所示,判断下列说法是否正确,正确的打“√”,错误
的打“×”。
(1)浓硫酸只作催化剂( )
(2)在反应容器中放入几片碎瓷片防止混合液暴沸( )
(3)反应温度缓慢上升至170 ℃( )
(4)用排水法或向下排空气法收集乙烯( )
×
正误判断
√
×
×
(5)圆底烧瓶中装的是4 mL乙醇和12 mL 3 mol·L-1 H2SO4
混合液( )
(6)温度计应插入反应溶液液面下,以便控制温度( )
(7)反应完毕后先熄灭酒精灯,再从水中取出导管( )
(8)该反应类型属于取代反应( )
(9)若a口出来的气体能使酸性 KMnO4溶液褪色,说明有乙烯生成( )
正误判断
×
√
×
×
×
资料表明C、H、O三种元素的电负性分别为2.5、2.1、3.5。
(1)请从化学键的活泼性的角度解释1 mol乙醇和足量的金属钠反应只能生成0.5 mol H2的原因。
深度思考
提示 O、H电负性的差值较大,O—H的极性比C—H的极性强,分子中只有一个O—H中的氢原子能与活泼金属反应。
(2)预测乙醇的同分异构体二甲醚( )能与金属钠反应吗?说明判断的理由。
提示 不能。二甲醚中没有O—H,而C—H的极性较弱,因而不能与金属钠反应。
深度思考
应用体验
1.(2022·苏州调研)下列有关乙醇的说法错误的是
A.钠的密度大于乙醇,实验室可用乙醇保存金属钠
B.可用无水CuSO4检验工业酒精中是否含水
C.乙醇不能萃取出溴水中的溴
D.分离乙醇和水常用蒸馏的方法
√
钠的密度大于乙醇,但乙醇可与钠反应生成乙醇钠和氢气,实验室不可用乙醇保存金属钠,故A错误;
可用无水CuSO4检验工业酒精中是否含水,如无水CuSO4变为蓝色,则说明工业酒精中含有水,故B正确;
乙醇与水互溶,不能萃取出溴水中的溴,故C正确;
乙醇和水沸点不同,分离乙醇和水常用蒸馏的方法,故D正确。
2.下列四种有机物的分子式均为C4H10O。
① ②CH3CH2CH2CH2OH
③ ④
(1)能被氧化成含相同碳原子数的醛的是 (填序号,下同)。
(2)能被氧化成酮的是 。
(3)写出①发生消去反应生成有机物的结构简式:___________________
_________________。
②③
①
CH3CH==CHCH3、
CH3CH2CH==CH2
能被氧化成醛的醇分子中必含有基团“—CH2OH”,②和③符合题意;
能被氧化成酮的醇分子中必含有基团“ ”,①符合题意;
若与羟基相连的碳原子的邻位碳原子上的氢原子类型不同,则发生消去反应时,可以得到不同产物。
3.某化学兴趣小组对教材中乙醇氧化及产物检验的实验进行了改进和创新,其改进实验装置如图所示,按图组装好仪器,装好试剂。下列有关改进实验的叙述不正确的是
A.点燃酒精灯,轻轻推动注射器
活塞即可实现乙醇氧化及部分
产物的检验
B.铜粉红黑颜色交替变化有关的
反应为2Cu+O2 2CuO、
C2H5OH+CuO CH3CHO+Cu+H2O
C.硫酸铜粉末变蓝色,说明乙醇氧化反应有水生成
D.实验中乙醇发生了消去反应
√
点燃酒精灯,轻轻推动注射器活塞即可反应,空气带着乙醇蒸气与热的铜粉发生反应,故A正确;
铜粉起到催化剂的作用,先消耗
后生成,铜粉红色变黑色,发生
反应:2Cu+O2 2CuO,之后又看到黑色变红色,发生反应:C2H5OH+CuO CH3CHO+Cu+H2O,故B正确;
硫酸铜粉末变蓝,是因为生成了五水硫酸铜,说明乙醇氧化反应有水生成,故C正确。
返回
醇的重要应用
二
1.醇的分类
分子中含有两个或两个以上 的醇又称为 。
醇类
根据烃基
类别
→脂肪醇,如CH3CH2OH
→芳香醇,如
根据分子中
含羟基数目
→一元醇,如CH3OH,名称:_____
→二元醇,如HOCH2CH2OH,名称:_______
→三元醇,如 ,名称:_______
甲醇
乙二醇
丙三醇
羟基
多元醇
2.三种重要的醇及应用
名称 俗名 结构简式 色、态 毒性 水溶性 主要用途
甲醇 _______ _____ _______ 色透明的_____ _____ 与水 互溶 化工原料、绿色燃料
乙二醇 _______ _______ 无色、黏稠、有甜味的液体 无毒 、化工原料
丙三醇 _____ 制日用化妆品和硝化甘油等
木精或
木醇
CH3OH
无
液体
剧毒
抗冻剂
HOCH2
CH2OH
甘油
(1)分子中含有—OH的有机物是醇( )
(2)质量分数为95%的乙醇常作消毒剂( )
(3)甘油属于三元醇,易溶于水( )
(4)硝化甘油是一种烈性炸药( )
(5)乙二醇的水溶液凝固点高,可用作汽车发动机的抗冻剂( )
×
正误判断
×
√
√
×
1.甲醇、乙二醇能发生催化氧化反应吗?若能,写出反应的化学方程式。
深度思考
提示 能;2CH3OH+O2 2HCHO+2H2O、
+O2 +2H2O。
2.请写出分子式为C3H8O的有机化合物的同分异构体的结构简式。
提示 CH3—CH2—CH2—OH、 、CH3—CH2—O—CH3
深度思考
应用体验
1.下列关于乙醇、乙二醇、丙三醇的说法不正确的是
A.均易溶于水,且丙三醇可作护肤剂,乙二醇可作汽车发动机的抗冻剂
B.均能被催化氧化成醛,也能脱水生成醚
C.均能发生酯化反应,丙三醇与硝酸反应的产物可以作炸药
D.若与足量的钠反应产生的氢气相等时,消耗三者的物质的量之比为
3∶2∶1
√
A项,乙醇、乙二醇、丙三醇含有—OH,属于低级醇,易溶于水,丙三醇具有吸湿性,可作护肤剂,乙二醇可作汽车发动机的抗冻剂,正确;
B项,都含有羟基,且与羟基相连的碳原子上含有氢原子,可以发生催化氧化反应生成醛,可以分子之间发生脱水反应生成醚,正确;
C项,都含有—OH,可以发生酯化反应,丙三醇与硝酸反应得到的硝化甘油为烈性炸药,正确;
D项,分子中—OH与Na反应,产生的氢气相等时,消耗乙醇、乙二醇、丙三醇的物质的量之比为 =6∶3∶2,错误。
2.观察下列几种物质的结构,回答下列问题。
①CH3CH2OH ②CH3CH2CH2OH ③
④ ⑤CH3—O—CH3 ⑥
(1)①和⑤的分子式都是 ,但是含有的 不同。
(2) (填序号,下同)和 的分子式都是C3H8O,但是在分子中______的位置不同。
(3)③属于 类,④不属于醇类,但它们的分子式 ,属于______
_______ 。
C2H6O
② ⑥ —OH
同分
醇
相同
异构体
官能团
返回
课时对点练
题组一 醇的概念、分类及用途
1.下列各组有机物中,互为同分异构体且都属于醇类的是
A.乙二醇和丙三醇
B. 和
C.2-丙醇和1-丙醇
D.2-丁醇和2-丙醇
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
A项,两种有机物的分子式不同,错误;
B项,两种有机物互为同分异构体,但前者是酚,后者是醇,错误;
C项,两种有机物都属于醇且属于位置异构,正确;
D项,两种有机物互为同系物,错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
2.结合下表数据分析,下列有关说法不正确的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
物质 分子式 沸点/℃ 溶解性
乙醇 C2H6O 78.5 与水以任意比互溶
乙二醇 C2H6O2 197.3 与水和乙醇以任意比互溶
A.乙醇与乙二醇含有的官能团相同,都能与NaOH发生反应
B.采用蒸馏的方法可以分离乙醇与乙二醇的混合物
C.乙二醇的水溶液凝固点很低,可作汽车发动机的抗冻剂
D.丙三醇的沸点应高于乙醇的沸点
√
乙醇与乙二醇含有的官能团相同,都含有—OH,都不能与NaOH发生反应,A不正确;
根据题意,二者的沸点不同,且相差较大,可以采用蒸馏的方法将两种互溶物质进行分离,B正确;
含有的羟基越多,形成氢键的几率越大,丙三醇含有的羟基多,所以丙三醇的沸点高,D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
3.从2020年1月开始,新型冠状病毒肺炎疫情全面爆发,关于新型冠状病毒肺炎至今还没有研发出特效药,75%乙醇溶液是一种常见的杀灭病毒的消毒剂,下列关于乙醇的说法不正确的是
A.它的结构简式为CH3CH2OH
B.100%乙醇消毒效果更好
C.它的官能团为羟基
D.它能与水以任意比互溶
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
乙醇是能与水以任意比互溶、有特殊香味的无色液体,分子式为C2H6O,结构简式为CH3CH2OH,官能团为羟基,75%乙醇溶液的消毒效果比100%乙醇的消毒效果好。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
题组二 醇的结构与性质
4.(2022·上海奉贤期中)2021年诺贝尔生理学或医学奖表彰了科
学家在“发现温度和触觉感受器”方面作出的贡献。薄荷醇
(见图)可用来识别TRPM8(一种能被凉爽激活的受体)。下列关于薄荷醇的说法正确的是
A.与乙醇互为同系物 B.可发生消去反应
C.可被氧化为醛 D.与 互为同分异构体
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
薄荷醇含有六元环,与乙醇的结构不相似,不互为同系物,
A错误;
与羟基相连的碳原子的邻位碳上有氢原子,可发生消去反应,B正确;
与羟基相连的碳上只有一个H原子,可被氧化为酮,C错误;
的分子式比薄荷醇的多一个CH2,分子式不同,不互
为同分异构体,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
5.(2022·济宁高二检测)下列有机物中,既能发生催化氧化又能发生消去反应,且消去产物中存在同分异构体的是
A.CH3—OH B.
C. D.
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
√
A项,甲醇能发生催化氧化反应,但不能发生消去反应,故错误;
B项,该物质能发生催化氧化反应,也能发生消去反应,但是消去产物只有丙烯一种,故错误;
C项,该物质不能发生催化氧化反应,故错误;
D项,该物质能发生催化氧化反应,也能发生消去反应,生成1-丁烯或2-丁烯,故正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
6.某化学反应过程如图所示,下列由图得出的判断正确的是
A.生成物是丙醛和丙酮
B.1-丙醇发生了还原反应
C.反应中有红黑颜色交替变化的现象
D.醇类都能发生图示的催化氧化反应
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
图示中发生的化学反应可以表述为2Cu+O2 2CuO,CuO+CH3CH2CH2OH CH3CH2CHO+Cu+H2O,总反应为醇的催化氧化反应。伯醇(—CH2OH)被氧化成醛,仲醇被氧化为酮,叔醇不能发生催化氧化反应,故只有C项正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
7.下列与乙醇相关实验的说法不正确的是
A.实验①中,在铜丝的中间部分加热,
片刻后开始有节奏地鼓入空气,可
观察到铜丝中间部分出现红黑交替
的现象
B.实验②中增加烧瓶上方的导管长度,
可减少原料的损失
C.实验②中若用CH3CH218OH和CH3COOH发生酯化反应,则乙酸乙酯中不含18O
D.实验③中,乙醇和金属钠的反应并不剧烈,钠粒逐渐变小,产生的气体具
有可燃性
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
乙醇在铜作催化剂时能够发生催化
氧化反应,2Cu+O2 2CuO、
CH3CH2OH+CuO CH3CHO+
Cu+H2O,因此有节奏地鼓入空气,
铜丝中间部分会出现黑红交替的现象,故A正确;
乙醇和乙酸均易挥发,增加②中烧瓶上方的导管长度,长直导管可以起冷凝回流作用,可减少原料的损失,故B正确;
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
根据酯化反应的原理,CH3COOH
+CH3CH218OH
CH3CO18OCH2CH3+H2O,乙酸乙
酯中含18O,故C错误;
乙醇与钠缓慢反应放出氢气,氢气点燃生成水,在火焰上罩一个干燥的烧杯,可以检验生成的水,可以验证产生的气体具有可燃性,故D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
题组三 醇的同分异构体
8.已知C4H10的同分异构体有两种: CH3CH2CH2CH3、 ,
则C4H9OH属于醇类的同分异构体共有
A.1种 B.2种
C.3种 D.4种
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
C4H9OH属于醇类的同分异构体,可以看作是C4H10分子中的1个氢原子被羟基代替的产物; C4H10的同分异构体各含有两种不同化学环境的氢原子,如下: ,所以羟基取代这些氢原子共得到4种属于醇类的同分异构体。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
9.今有组成为CH4O和C3H8O的混合物,在一定条件下进行脱水反应,可能生成的有机物的种数为
A.3种 B.4种 C.7种 D.8种
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
CH4O可写成CH3OH;C3H8O可写成CH3CH2CH2OH或 。分子内脱水产物为CH3CH==CH2。分子间脱水产物有CH3OCH3、
CH3CH2CH2OCH2CH2CH3、 、CH3OCH2CH2CH3、
、 ,共有7种。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
10.下列有机物由浓硝酸发生酯化反应而得到的是
A.TNT B.CH3CH2NO2
C.硝化甘油 D.C6H5NO2
√
醇和酸生成酯和水的反应是酯化反应,A、D是甲苯、苯和浓硝酸的硝化反应,B是乙烷和浓硝酸的取代反应,C是甘油和浓硝酸的酯化反应。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
11.(2022·成都高二月考)烷烃中一个氢原子被一个羟基取代后的衍生物为饱和一元醇,某饱和一元醇C5H12O的同分异构体中,能被催化氧化生成醛的有
A.2种 B.3种 C.4种 D.5种
√
含有5个碳原子的饱和一元醇C5H12O的同分异构体能被氧化生成醛,说明连接羟基的碳原子上连有2个氢原子,即结构中含有—CH2OH,可写作C4H9—CH2OH,—C4H9有4种结构,故符合条件的C5H12O的同分异构体有4种。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
12.(2022·北京高二期末)某一元醇具有如下性质:①能在加热时被 CuO氧化;②能发生消去反应得到烯烃;③生成的烯烃一定不存在顺反异构体。该一元醇可能是
A.1-丁醇 B.2-丁醇
C.2,2-二甲基丙醇 D.2-甲基-2-丙醇
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
1-丁醇( )是伯醇,与羟基相连的碳原子的邻位碳原子上含有氢原
子,能发生消去反应生成烯烃,生成的烯烃的双键上的一个碳上连接有相同的基团,所以一定不存在顺反异构体,A符合题意;
2-丁醇( )是仲醇,与羟基相连的碳原子的邻位碳原子上含有氢原子,能发生消去反应生成烯烃,生成的烯烃可能有两种,双键在1、2号碳上时不存在顺反异构体,双键在2、3号碳上时双键上的每个碳原子都连接不同的基团,所以生成的烯烃可能存在顺反异构体,B不符合题意;
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
2,2-二甲基丙醇( )是伯醇,与羟基相连的碳原子的邻位碳原子上不含氢原子,不能发生消去反应生成烯烃,C不符合题意;
2-甲基-2-丙醇( )是叔醇,不能被催化氧化,D不符合题意。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
13.已知维生素A的结构简式可写为 ,式中以线示键,
线的交点与端点处代表碳原子,并用氢原子补足四价,但碳、氢原子未标示出来,下列关于它的叙述正确的是
A.维生素A的分子式为C20H31O
B.维生素A是一种易溶于水的醇
C.维生素A的分子中有苯环结构,并能使酸性高锰酸钾溶液褪色
D.1 mol维生素A与足量钠反应可生成0.5 mol氢气
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
维生素A的分子式为C20H30O,烃基较大,难溶于水,结构中无苯环;1 mol维生素A中含有1 mol羟基,由关系式—OH~ H2知,生成
0.5 mol H2。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
14.(2022·吉林高二检测)用如图A、B组成实验装置测定产生氢气的体积,可确定反应物醇的物质的量、生成氢气的物质的量与醇分子中羟基数量的关系。若用乙醇、乙二醇、丙三醇分别与足量金属钠作用,产生的氢气在相同条件下体积之比为6∶2∶3。则下列判断不正确的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
A.装置A的分液漏斗与蒸馏烧瓶之间连接的导管
可减少测量实验误差
B.装置A的分液漏斗与蒸馏烧瓶之间连接的导管
可使分液漏斗中的醇顺利滴下
C.装置B用于测定氢气排出水的体积,读数时应使广口瓶与量筒中液面
最低处持平
D.乙醇、乙二醇、丙三醇的物质的量之比为3∶2∶6
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
√
装置A的分液漏斗与蒸馏烧瓶之间连接的导管有平衡压强的作用,使分液漏斗内的液体顺利滴下,同时可消除添加醇的体积影响,减少测量实验误差,故A、B正确;
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
量筒读数时应上下移动量筒,使量筒液面最低处与广口瓶液面在同一高度,故C正确;
由题意知,相同条件下,H2的体积比等于其物质的量之比,设乙醇、乙二醇、丙三醇的物质的量分别为x、y、z,则含有羟基的物质的量分别为x、2y、3z,由—OH~ H2知,三者产生的
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
氢气物质的量之比为 =6∶2∶3,故x∶y∶z=6∶1∶1。
15.已知:实验室制备乙烯的反应为CH3CH2OH CH2==CH2↑
+H2O,生成的乙烯中混有CO2、SO2等杂质。实验小组用如下装置制备并收集乙烯(尾气处理略去),下列说法不正确的是
A.配制①中混合液时,应将浓H2SO4加入
乙醇中
B.应先检验装置的气密性,再加入药品、
加热
C.试剂X可选择NaOH溶液
D.④和⑤均适宜作为收集装置
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
√
NaOH溶液可吸收CO2、SO2等杂质,C正确;
乙烯密度与空气非常接近,用排空气法收集会导致收集的气体不纯,④不适宜作为收集装置,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
16.有机物A(C4H10O)可用作增塑剂、溶剂等。A可以发生如下转化。
已知:R1—CH==CH—R2 R1—CHO+R2—CHO
(1)按官能团分类,A属于 。
醇
按官能团分类,A是 ,属于醇。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
17
15
16
(2)A→B的反应类型是 。
取代反应
A是 ,与氯气在光照条件下发生取代反应。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
17
15
16
(3)A→C的转化中Na的作用是 。
作还原剂
1
2
3
4
5
6
7
8
9
10
11
12
13
14
17
15
16
与Na发生置换反应生成 和H2,在该反应中Na元素的化合价由0价变为+1价,化合价升高,失去电子,表现还原性,所以A→C的转化中Na的作用是作还原剂。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
17
15
16
(4)写出A→D的化学方程式:_____________________________________
______。
+H2O
1
2
3
4
5
6
7
8
9
10
11
12
13
14
17
15
16
A是 ,与浓硫酸混合加热,发生消去反应生成CH3CH==CHCH3和H2O。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
17
15
16
(5)F的结构简式是 。
F是2-丁烯在一定条件下发生加聚反应生成的聚2-丁烯,其结构简式是 。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
17
15
16
17.(2022·石家庄高二检测)实验室用环己醇
( )与质量分数为85%的磷酸在
共热条件下制备环己烯( ),制备装
置如图所示。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
实验药品的物理性质:
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
名称 密度/(g·mL-1) 熔点/℃ 沸点/℃ 溶解性
环己醇 0.96 25.2 161 微溶于水
环己烯 0.81 -103 83 不溶于水
85%H3PO4 1.68 42.35 213(失水) 易溶于水
已知:环己醇能与水形成二元共沸物(含水80%),其沸点为97.8 ℃。
Ⅰ.实验原理
(1)该实验的反应原理与实验室制乙烯相似,
请用化学方程式表示:____________________
____________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
+H2O
实验室制乙烯是由乙醇和浓硫酸在170 ℃发生消去反应制得,该实验的反应原理与实验室制乙烯相似,则化学方程式为
+H2O。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
(2)该反应有副反应发生(产物为 ),
反应的化学方程式为______________________
____________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
2
+H2O
该反应有副反应发生,醇自身脱水缩合会生成醚,化学方程式为
+H2O。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
Ⅱ.制备粗产品
(3)在圆底烧瓶中加入20 mL(9.6 g)环己醇、10 mL 85% H3PO4、几粒碎瓷片,用电热包均匀缓慢加热。温度计的温度不应超过90 ℃,原因是________________________________________
________;85% H3PO4在反应中的作用是_____
___________;碎瓷片的作用是_________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
防止环己醇挥发出来(或提高反应物环己醇的转化率)
催化
剂、脱水剂
防止暴沸
温度计的温度不应超过90 ℃是因为环己醇的沸点比较低,如果温度太高,超过90 ℃,会使原料和产物一起蒸出,从而降低反应物环己醇的转化率;H3PO4是常见的脱水剂和催化剂;加几粒碎瓷片是为了防止暴沸。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
Ⅲ.粗产品提纯
(4)从分液漏斗中分离出来的环己烯还要转移到蒸馏烧瓶中,并加入少量的无水氯化钙进一步蒸馏,此时温度计下端的水银球应插在蒸馏烧瓶的_______位置,温度计显示的温度应为
______。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
支管口
83 ℃
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
从分液漏斗中分离出来的环己烯还要转移到蒸馏烧瓶中,环己烯的沸点是83 ℃,要分开环己烯和水,无水氯化钙是常用的干燥剂,要加入少量的无水氯化钙进一步蒸馏除去水,此时温度计下端的水银球应插在蒸馏烧瓶的支管口处。
返回
本课结束
专题4
第1课时
DIYIKESHI
醇的结构与性质 / 醇的重要应用 / 课时对点练
醇
专题4
核心素养
发展目标
1.通过认识羟基的结构,了解醇类的结构特点;进而从化学键、官能团的角度理解醇类消去反应、催化氧化反应的特征和规律。
2.通过乙醇性质的学习,能利用反应类型的规律判断、说明和预测醇类物质的性质。
内容索引
一、醇的结构与性质
二、醇的重要应用
课时对点练
醇的结构与性质
一
1.醇的概念
烃分子中饱和碳原子上的氢原子被 取代所形成的化合物称为醇,如乙醇。
2.乙醇的组成与结构
羟基
CH3CH2OH或C2H5OH
羟基或—OH
3.醇的化学性质
(1)实验探究乙醇中羟基氢原子的活泼性
实验操作
实验现象 ①钠粒沉到烧杯 ,有 产生;②点燃气体,火焰呈 ,干燥的烧杯内壁出现 ;③钠与水 反应而不与乙醚反应 底部
无色气体
淡蓝色
液滴
剧烈
实验结论 a.乙醇与钠反应生成乙醇钠,并放出 ,钠的密度比乙醇的 ;
b.乙醇中羟基氢原子比烃基氢原子_____
氢气
大
活泼
(2)氧化反应
①燃烧反应
CH3CH2OH+3O2 2CO2+3H2O
现象:产生淡蓝色火焰,同时放出大量的热。
②催化氧化:醇在 或 等催化剂存在下,可被氧气氧化为 或酮。
如: +O2 +2H2O、2CH3CH2OH
+O2 +2H2O。
③醇与酸性KMnO4溶液或K2Cr2O7溶液反应被氧化成羧酸。
2CH3CHO
铜
银
醛
(3)实验探究乙醇与氢卤酸的反应
实验装置图
实验现象 _________________
实验结论 ______________________________________________
化学方程式 ____________________________________
Ⅱ中产生油状液体
乙醇与氢溴酸发生了反应,生成油状液体CH3CH2Br
醇不仅可以与氢溴酸反应,还可以与其他氢卤酸反应。在反应中,醇分子中的 被卤素原子取代生成卤代烃。
R—OH+HX―→ +H2O
在实验室和工业中,卤代烷烃常用 和 的反应来制备。
(4)脱水反应
乙醇可以在浓H2SO4、磷酸、Al2O3(400 ℃左右)或P2O5等催化剂的作用下发生脱水反应。
羟基
R—X
醇
氢卤酸
①乙醇的脱水反应实验(P2O5作催化剂)
实验装置图
实验现象 ________________________
实验结论 _________________________________
稀酸性高锰酸钾溶液褪色
乙醇发生了分子内脱水,生成了乙烯
实验室中经常采用乙醇和浓硫酸共热发生脱水反应来获得乙烯或乙醚。化学方程式分别为CH3CH2OH 、
2CH3CH2OH 。
②消去反应的概念
在一定条件下,一个有机化合物分子内脱去一个或几个 生成____
化合物(含双键或三键)的反应。
CH2==CH2↑+H2O
CH3CH2OCH2CH3+H2O
小分子
不饱
和
4.从微观结构分析醇的化学性质(以乙醇为例,如下图)
总结乙醇所能发生的化学反应:
乙醇发生反应的化学方程式 反应类型 断裂的共价键 反应条件
(1) 2CH3CH2OH+2Na―→ __________________ 反应 ___ Na
2CH3CH2ONa+H2↑
置换
e
(2) CH3CH2OH+HBr ________________ 反应 __ HBr,△
(3) 2CH3CH2OH+O2 _________________ 反应 ___ O2,Cu,△
(4) CH3CH2OH __________________ 反应 ___ 浓H2SO4,170 ℃
(5) 2CH3CH2OH _____________________ 反应 ___ 浓H2SO4,140 ℃
CH3CH2Br+H2O
2CH3CHO+2H2O
CH2==CH2↑+H2O
CH3CH2OCH2CH3+H2O
取代
d
氧化
ce
消去
ad
取代
de
实验室常用浓硫酸和乙醇混合加热制取乙烯,反应装置如
图所示,判断下列说法是否正确,正确的打“√”,错误
的打“×”。
(1)浓硫酸只作催化剂( )
(2)在反应容器中放入几片碎瓷片防止混合液暴沸( )
(3)反应温度缓慢上升至170 ℃( )
(4)用排水法或向下排空气法收集乙烯( )
×
正误判断
√
×
×
(5)圆底烧瓶中装的是4 mL乙醇和12 mL 3 mol·L-1 H2SO4
混合液( )
(6)温度计应插入反应溶液液面下,以便控制温度( )
(7)反应完毕后先熄灭酒精灯,再从水中取出导管( )
(8)该反应类型属于取代反应( )
(9)若a口出来的气体能使酸性 KMnO4溶液褪色,说明有乙烯生成( )
正误判断
×
√
×
×
×
资料表明C、H、O三种元素的电负性分别为2.5、2.1、3.5。
(1)请从化学键的活泼性的角度解释1 mol乙醇和足量的金属钠反应只能生成0.5 mol H2的原因。
深度思考
提示 O、H电负性的差值较大,O—H的极性比C—H的极性强,分子中只有一个O—H中的氢原子能与活泼金属反应。
(2)预测乙醇的同分异构体二甲醚( )能与金属钠反应吗?说明判断的理由。
提示 不能。二甲醚中没有O—H,而C—H的极性较弱,因而不能与金属钠反应。
深度思考
应用体验
1.(2022·苏州调研)下列有关乙醇的说法错误的是
A.钠的密度大于乙醇,实验室可用乙醇保存金属钠
B.可用无水CuSO4检验工业酒精中是否含水
C.乙醇不能萃取出溴水中的溴
D.分离乙醇和水常用蒸馏的方法
√
钠的密度大于乙醇,但乙醇可与钠反应生成乙醇钠和氢气,实验室不可用乙醇保存金属钠,故A错误;
可用无水CuSO4检验工业酒精中是否含水,如无水CuSO4变为蓝色,则说明工业酒精中含有水,故B正确;
乙醇与水互溶,不能萃取出溴水中的溴,故C正确;
乙醇和水沸点不同,分离乙醇和水常用蒸馏的方法,故D正确。
2.下列四种有机物的分子式均为C4H10O。
① ②CH3CH2CH2CH2OH
③ ④
(1)能被氧化成含相同碳原子数的醛的是 (填序号,下同)。
(2)能被氧化成酮的是 。
(3)写出①发生消去反应生成有机物的结构简式:___________________
_________________。
②③
①
CH3CH==CHCH3、
CH3CH2CH==CH2
能被氧化成醛的醇分子中必含有基团“—CH2OH”,②和③符合题意;
能被氧化成酮的醇分子中必含有基团“ ”,①符合题意;
若与羟基相连的碳原子的邻位碳原子上的氢原子类型不同,则发生消去反应时,可以得到不同产物。
3.某化学兴趣小组对教材中乙醇氧化及产物检验的实验进行了改进和创新,其改进实验装置如图所示,按图组装好仪器,装好试剂。下列有关改进实验的叙述不正确的是
A.点燃酒精灯,轻轻推动注射器
活塞即可实现乙醇氧化及部分
产物的检验
B.铜粉红黑颜色交替变化有关的
反应为2Cu+O2 2CuO、
C2H5OH+CuO CH3CHO+Cu+H2O
C.硫酸铜粉末变蓝色,说明乙醇氧化反应有水生成
D.实验中乙醇发生了消去反应
√
点燃酒精灯,轻轻推动注射器活塞即可反应,空气带着乙醇蒸气与热的铜粉发生反应,故A正确;
铜粉起到催化剂的作用,先消耗
后生成,铜粉红色变黑色,发生
反应:2Cu+O2 2CuO,之后又看到黑色变红色,发生反应:C2H5OH+CuO CH3CHO+Cu+H2O,故B正确;
硫酸铜粉末变蓝,是因为生成了五水硫酸铜,说明乙醇氧化反应有水生成,故C正确。
返回
醇的重要应用
二
1.醇的分类
分子中含有两个或两个以上 的醇又称为 。
醇类
根据烃基
类别
→脂肪醇,如CH3CH2OH
→芳香醇,如
根据分子中
含羟基数目
→一元醇,如CH3OH,名称:_____
→二元醇,如HOCH2CH2OH,名称:_______
→三元醇,如 ,名称:_______
甲醇
乙二醇
丙三醇
羟基
多元醇
2.三种重要的醇及应用
名称 俗名 结构简式 色、态 毒性 水溶性 主要用途
甲醇 _______ _____ _______ 色透明的_____ _____ 与水 互溶 化工原料、绿色燃料
乙二醇 _______ _______ 无色、黏稠、有甜味的液体 无毒 、化工原料
丙三醇 _____ 制日用化妆品和硝化甘油等
木精或
木醇
CH3OH
无
液体
剧毒
抗冻剂
HOCH2
CH2OH
甘油
(1)分子中含有—OH的有机物是醇( )
(2)质量分数为95%的乙醇常作消毒剂( )
(3)甘油属于三元醇,易溶于水( )
(4)硝化甘油是一种烈性炸药( )
(5)乙二醇的水溶液凝固点高,可用作汽车发动机的抗冻剂( )
×
正误判断
×
√
√
×
1.甲醇、乙二醇能发生催化氧化反应吗?若能,写出反应的化学方程式。
深度思考
提示 能;2CH3OH+O2 2HCHO+2H2O、
+O2 +2H2O。
2.请写出分子式为C3H8O的有机化合物的同分异构体的结构简式。
提示 CH3—CH2—CH2—OH、 、CH3—CH2—O—CH3
深度思考
应用体验
1.下列关于乙醇、乙二醇、丙三醇的说法不正确的是
A.均易溶于水,且丙三醇可作护肤剂,乙二醇可作汽车发动机的抗冻剂
B.均能被催化氧化成醛,也能脱水生成醚
C.均能发生酯化反应,丙三醇与硝酸反应的产物可以作炸药
D.若与足量的钠反应产生的氢气相等时,消耗三者的物质的量之比为
3∶2∶1
√
A项,乙醇、乙二醇、丙三醇含有—OH,属于低级醇,易溶于水,丙三醇具有吸湿性,可作护肤剂,乙二醇可作汽车发动机的抗冻剂,正确;
B项,都含有羟基,且与羟基相连的碳原子上含有氢原子,可以发生催化氧化反应生成醛,可以分子之间发生脱水反应生成醚,正确;
C项,都含有—OH,可以发生酯化反应,丙三醇与硝酸反应得到的硝化甘油为烈性炸药,正确;
D项,分子中—OH与Na反应,产生的氢气相等时,消耗乙醇、乙二醇、丙三醇的物质的量之比为 =6∶3∶2,错误。
2.观察下列几种物质的结构,回答下列问题。
①CH3CH2OH ②CH3CH2CH2OH ③
④ ⑤CH3—O—CH3 ⑥
(1)①和⑤的分子式都是 ,但是含有的 不同。
(2) (填序号,下同)和 的分子式都是C3H8O,但是在分子中______的位置不同。
(3)③属于 类,④不属于醇类,但它们的分子式 ,属于______
_______ 。
C2H6O
② ⑥ —OH
同分
醇
相同
异构体
官能团
返回
课时对点练
题组一 醇的概念、分类及用途
1.下列各组有机物中,互为同分异构体且都属于醇类的是
A.乙二醇和丙三醇
B. 和
C.2-丙醇和1-丙醇
D.2-丁醇和2-丙醇
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
A项,两种有机物的分子式不同,错误;
B项,两种有机物互为同分异构体,但前者是酚,后者是醇,错误;
C项,两种有机物都属于醇且属于位置异构,正确;
D项,两种有机物互为同系物,错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
2.结合下表数据分析,下列有关说法不正确的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
物质 分子式 沸点/℃ 溶解性
乙醇 C2H6O 78.5 与水以任意比互溶
乙二醇 C2H6O2 197.3 与水和乙醇以任意比互溶
A.乙醇与乙二醇含有的官能团相同,都能与NaOH发生反应
B.采用蒸馏的方法可以分离乙醇与乙二醇的混合物
C.乙二醇的水溶液凝固点很低,可作汽车发动机的抗冻剂
D.丙三醇的沸点应高于乙醇的沸点
√
乙醇与乙二醇含有的官能团相同,都含有—OH,都不能与NaOH发生反应,A不正确;
根据题意,二者的沸点不同,且相差较大,可以采用蒸馏的方法将两种互溶物质进行分离,B正确;
含有的羟基越多,形成氢键的几率越大,丙三醇含有的羟基多,所以丙三醇的沸点高,D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
3.从2020年1月开始,新型冠状病毒肺炎疫情全面爆发,关于新型冠状病毒肺炎至今还没有研发出特效药,75%乙醇溶液是一种常见的杀灭病毒的消毒剂,下列关于乙醇的说法不正确的是
A.它的结构简式为CH3CH2OH
B.100%乙醇消毒效果更好
C.它的官能团为羟基
D.它能与水以任意比互溶
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
乙醇是能与水以任意比互溶、有特殊香味的无色液体,分子式为C2H6O,结构简式为CH3CH2OH,官能团为羟基,75%乙醇溶液的消毒效果比100%乙醇的消毒效果好。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
题组二 醇的结构与性质
4.(2022·上海奉贤期中)2021年诺贝尔生理学或医学奖表彰了科
学家在“发现温度和触觉感受器”方面作出的贡献。薄荷醇
(见图)可用来识别TRPM8(一种能被凉爽激活的受体)。下列关于薄荷醇的说法正确的是
A.与乙醇互为同系物 B.可发生消去反应
C.可被氧化为醛 D.与 互为同分异构体
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
薄荷醇含有六元环,与乙醇的结构不相似,不互为同系物,
A错误;
与羟基相连的碳原子的邻位碳上有氢原子,可发生消去反应,B正确;
与羟基相连的碳上只有一个H原子,可被氧化为酮,C错误;
的分子式比薄荷醇的多一个CH2,分子式不同,不互
为同分异构体,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
5.(2022·济宁高二检测)下列有机物中,既能发生催化氧化又能发生消去反应,且消去产物中存在同分异构体的是
A.CH3—OH B.
C. D.
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
√
A项,甲醇能发生催化氧化反应,但不能发生消去反应,故错误;
B项,该物质能发生催化氧化反应,也能发生消去反应,但是消去产物只有丙烯一种,故错误;
C项,该物质不能发生催化氧化反应,故错误;
D项,该物质能发生催化氧化反应,也能发生消去反应,生成1-丁烯或2-丁烯,故正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
6.某化学反应过程如图所示,下列由图得出的判断正确的是
A.生成物是丙醛和丙酮
B.1-丙醇发生了还原反应
C.反应中有红黑颜色交替变化的现象
D.醇类都能发生图示的催化氧化反应
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
图示中发生的化学反应可以表述为2Cu+O2 2CuO,CuO+CH3CH2CH2OH CH3CH2CHO+Cu+H2O,总反应为醇的催化氧化反应。伯醇(—CH2OH)被氧化成醛,仲醇被氧化为酮,叔醇不能发生催化氧化反应,故只有C项正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
7.下列与乙醇相关实验的说法不正确的是
A.实验①中,在铜丝的中间部分加热,
片刻后开始有节奏地鼓入空气,可
观察到铜丝中间部分出现红黑交替
的现象
B.实验②中增加烧瓶上方的导管长度,
可减少原料的损失
C.实验②中若用CH3CH218OH和CH3COOH发生酯化反应,则乙酸乙酯中不含18O
D.实验③中,乙醇和金属钠的反应并不剧烈,钠粒逐渐变小,产生的气体具
有可燃性
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
乙醇在铜作催化剂时能够发生催化
氧化反应,2Cu+O2 2CuO、
CH3CH2OH+CuO CH3CHO+
Cu+H2O,因此有节奏地鼓入空气,
铜丝中间部分会出现黑红交替的现象,故A正确;
乙醇和乙酸均易挥发,增加②中烧瓶上方的导管长度,长直导管可以起冷凝回流作用,可减少原料的损失,故B正确;
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
根据酯化反应的原理,CH3COOH
+CH3CH218OH
CH3CO18OCH2CH3+H2O,乙酸乙
酯中含18O,故C错误;
乙醇与钠缓慢反应放出氢气,氢气点燃生成水,在火焰上罩一个干燥的烧杯,可以检验生成的水,可以验证产生的气体具有可燃性,故D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
题组三 醇的同分异构体
8.已知C4H10的同分异构体有两种: CH3CH2CH2CH3、 ,
则C4H9OH属于醇类的同分异构体共有
A.1种 B.2种
C.3种 D.4种
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
C4H9OH属于醇类的同分异构体,可以看作是C4H10分子中的1个氢原子被羟基代替的产物; C4H10的同分异构体各含有两种不同化学环境的氢原子,如下: ,所以羟基取代这些氢原子共得到4种属于醇类的同分异构体。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
9.今有组成为CH4O和C3H8O的混合物,在一定条件下进行脱水反应,可能生成的有机物的种数为
A.3种 B.4种 C.7种 D.8种
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
CH4O可写成CH3OH;C3H8O可写成CH3CH2CH2OH或 。分子内脱水产物为CH3CH==CH2。分子间脱水产物有CH3OCH3、
CH3CH2CH2OCH2CH2CH3、 、CH3OCH2CH2CH3、
、 ,共有7种。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
10.下列有机物由浓硝酸发生酯化反应而得到的是
A.TNT B.CH3CH2NO2
C.硝化甘油 D.C6H5NO2
√
醇和酸生成酯和水的反应是酯化反应,A、D是甲苯、苯和浓硝酸的硝化反应,B是乙烷和浓硝酸的取代反应,C是甘油和浓硝酸的酯化反应。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
11.(2022·成都高二月考)烷烃中一个氢原子被一个羟基取代后的衍生物为饱和一元醇,某饱和一元醇C5H12O的同分异构体中,能被催化氧化生成醛的有
A.2种 B.3种 C.4种 D.5种
√
含有5个碳原子的饱和一元醇C5H12O的同分异构体能被氧化生成醛,说明连接羟基的碳原子上连有2个氢原子,即结构中含有—CH2OH,可写作C4H9—CH2OH,—C4H9有4种结构,故符合条件的C5H12O的同分异构体有4种。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
12.(2022·北京高二期末)某一元醇具有如下性质:①能在加热时被 CuO氧化;②能发生消去反应得到烯烃;③生成的烯烃一定不存在顺反异构体。该一元醇可能是
A.1-丁醇 B.2-丁醇
C.2,2-二甲基丙醇 D.2-甲基-2-丙醇
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
1-丁醇( )是伯醇,与羟基相连的碳原子的邻位碳原子上含有氢原
子,能发生消去反应生成烯烃,生成的烯烃的双键上的一个碳上连接有相同的基团,所以一定不存在顺反异构体,A符合题意;
2-丁醇( )是仲醇,与羟基相连的碳原子的邻位碳原子上含有氢原子,能发生消去反应生成烯烃,生成的烯烃可能有两种,双键在1、2号碳上时不存在顺反异构体,双键在2、3号碳上时双键上的每个碳原子都连接不同的基团,所以生成的烯烃可能存在顺反异构体,B不符合题意;
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
2,2-二甲基丙醇( )是伯醇,与羟基相连的碳原子的邻位碳原子上不含氢原子,不能发生消去反应生成烯烃,C不符合题意;
2-甲基-2-丙醇( )是叔醇,不能被催化氧化,D不符合题意。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
13.已知维生素A的结构简式可写为 ,式中以线示键,
线的交点与端点处代表碳原子,并用氢原子补足四价,但碳、氢原子未标示出来,下列关于它的叙述正确的是
A.维生素A的分子式为C20H31O
B.维生素A是一种易溶于水的醇
C.维生素A的分子中有苯环结构,并能使酸性高锰酸钾溶液褪色
D.1 mol维生素A与足量钠反应可生成0.5 mol氢气
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
维生素A的分子式为C20H30O,烃基较大,难溶于水,结构中无苯环;1 mol维生素A中含有1 mol羟基,由关系式—OH~ H2知,生成
0.5 mol H2。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
14.(2022·吉林高二检测)用如图A、B组成实验装置测定产生氢气的体积,可确定反应物醇的物质的量、生成氢气的物质的量与醇分子中羟基数量的关系。若用乙醇、乙二醇、丙三醇分别与足量金属钠作用,产生的氢气在相同条件下体积之比为6∶2∶3。则下列判断不正确的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
A.装置A的分液漏斗与蒸馏烧瓶之间连接的导管
可减少测量实验误差
B.装置A的分液漏斗与蒸馏烧瓶之间连接的导管
可使分液漏斗中的醇顺利滴下
C.装置B用于测定氢气排出水的体积,读数时应使广口瓶与量筒中液面
最低处持平
D.乙醇、乙二醇、丙三醇的物质的量之比为3∶2∶6
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
√
装置A的分液漏斗与蒸馏烧瓶之间连接的导管有平衡压强的作用,使分液漏斗内的液体顺利滴下,同时可消除添加醇的体积影响,减少测量实验误差,故A、B正确;
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
量筒读数时应上下移动量筒,使量筒液面最低处与广口瓶液面在同一高度,故C正确;
由题意知,相同条件下,H2的体积比等于其物质的量之比,设乙醇、乙二醇、丙三醇的物质的量分别为x、y、z,则含有羟基的物质的量分别为x、2y、3z,由—OH~ H2知,三者产生的
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
氢气物质的量之比为 =6∶2∶3,故x∶y∶z=6∶1∶1。
15.已知:实验室制备乙烯的反应为CH3CH2OH CH2==CH2↑
+H2O,生成的乙烯中混有CO2、SO2等杂质。实验小组用如下装置制备并收集乙烯(尾气处理略去),下列说法不正确的是
A.配制①中混合液时,应将浓H2SO4加入
乙醇中
B.应先检验装置的气密性,再加入药品、
加热
C.试剂X可选择NaOH溶液
D.④和⑤均适宜作为收集装置
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
√
NaOH溶液可吸收CO2、SO2等杂质,C正确;
乙烯密度与空气非常接近,用排空气法收集会导致收集的气体不纯,④不适宜作为收集装置,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
16.有机物A(C4H10O)可用作增塑剂、溶剂等。A可以发生如下转化。
已知:R1—CH==CH—R2 R1—CHO+R2—CHO
(1)按官能团分类,A属于 。
醇
按官能团分类,A是 ,属于醇。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
17
15
16
(2)A→B的反应类型是 。
取代反应
A是 ,与氯气在光照条件下发生取代反应。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
17
15
16
(3)A→C的转化中Na的作用是 。
作还原剂
1
2
3
4
5
6
7
8
9
10
11
12
13
14
17
15
16
与Na发生置换反应生成 和H2,在该反应中Na元素的化合价由0价变为+1价,化合价升高,失去电子,表现还原性,所以A→C的转化中Na的作用是作还原剂。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
17
15
16
(4)写出A→D的化学方程式:_____________________________________
______。
+H2O
1
2
3
4
5
6
7
8
9
10
11
12
13
14
17
15
16
A是 ,与浓硫酸混合加热,发生消去反应生成CH3CH==CHCH3和H2O。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
17
15
16
(5)F的结构简式是 。
F是2-丁烯在一定条件下发生加聚反应生成的聚2-丁烯,其结构简式是 。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
17
15
16
17.(2022·石家庄高二检测)实验室用环己醇
( )与质量分数为85%的磷酸在
共热条件下制备环己烯( ),制备装
置如图所示。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
实验药品的物理性质:
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
名称 密度/(g·mL-1) 熔点/℃ 沸点/℃ 溶解性
环己醇 0.96 25.2 161 微溶于水
环己烯 0.81 -103 83 不溶于水
85%H3PO4 1.68 42.35 213(失水) 易溶于水
已知:环己醇能与水形成二元共沸物(含水80%),其沸点为97.8 ℃。
Ⅰ.实验原理
(1)该实验的反应原理与实验室制乙烯相似,
请用化学方程式表示:____________________
____________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
+H2O
实验室制乙烯是由乙醇和浓硫酸在170 ℃发生消去反应制得,该实验的反应原理与实验室制乙烯相似,则化学方程式为
+H2O。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
(2)该反应有副反应发生(产物为 ),
反应的化学方程式为______________________
____________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
2
+H2O
该反应有副反应发生,醇自身脱水缩合会生成醚,化学方程式为
+H2O。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
Ⅱ.制备粗产品
(3)在圆底烧瓶中加入20 mL(9.6 g)环己醇、10 mL 85% H3PO4、几粒碎瓷片,用电热包均匀缓慢加热。温度计的温度不应超过90 ℃,原因是________________________________________
________;85% H3PO4在反应中的作用是_____
___________;碎瓷片的作用是_________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
防止环己醇挥发出来(或提高反应物环己醇的转化率)
催化
剂、脱水剂
防止暴沸
温度计的温度不应超过90 ℃是因为环己醇的沸点比较低,如果温度太高,超过90 ℃,会使原料和产物一起蒸出,从而降低反应物环己醇的转化率;H3PO4是常见的脱水剂和催化剂;加几粒碎瓷片是为了防止暴沸。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
Ⅲ.粗产品提纯
(4)从分液漏斗中分离出来的环己烯还要转移到蒸馏烧瓶中,并加入少量的无水氯化钙进一步蒸馏,此时温度计下端的水银球应插在蒸馏烧瓶的_______位置,温度计显示的温度应为
______。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
支管口
83 ℃
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
从分液漏斗中分离出来的环己烯还要转移到蒸馏烧瓶中,环己烯的沸点是83 ℃,要分开环己烯和水,无水氯化钙是常用的干燥剂,要加入少量的无水氯化钙进一步蒸馏除去水,此时温度计下端的水银球应插在蒸馏烧瓶的支管口处。
返回
本课结束
专题4
