实验活动2 二氧化碳的实验室制取和性质 (课件17页)
文档属性
| 名称 | 实验活动2 二氧化碳的实验室制取和性质 (课件17页) |

|
|
| 格式 | zip | ||
| 文件大小 | 473.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-21 00:00:00 | ||
图片预览






文档简介
(共18张PPT)
学习目标:
1.练习实验室里制取二氧化碳和用向上排空气法收集气体。
2.加深对二氧化碳性质的认识。
实验探究一、实验室制取二氧化碳
【实验药品】
大理石(或石灰石)、稀盐酸(1∶2)、澄清石灰水、紫色石蕊试液、蜡烛、木条、蒸馏水、火柴。
【实验仪器】
烧杯、集气瓶、量筒、玻璃导管、胶皮管、单孔橡胶塞、铁架台(带铁夹)、试管、试管夹、玻璃片、酒精灯。
实验探究一、实验室制取二氧化碳
我们已经学习了二氧化碳的制取与性质,请同学们回忆一下,实验室制取二氧化碳的实验用品是什么,实验原理是什么?
实验探究一、实验室制取二氧化碳
1.药品
大理石(或石灰石) 稀盐酸
2.实验原理
CaCO3+2HCl==CaCl2+H2O+CO2↑
实验探究一、实验室制取二氧化碳
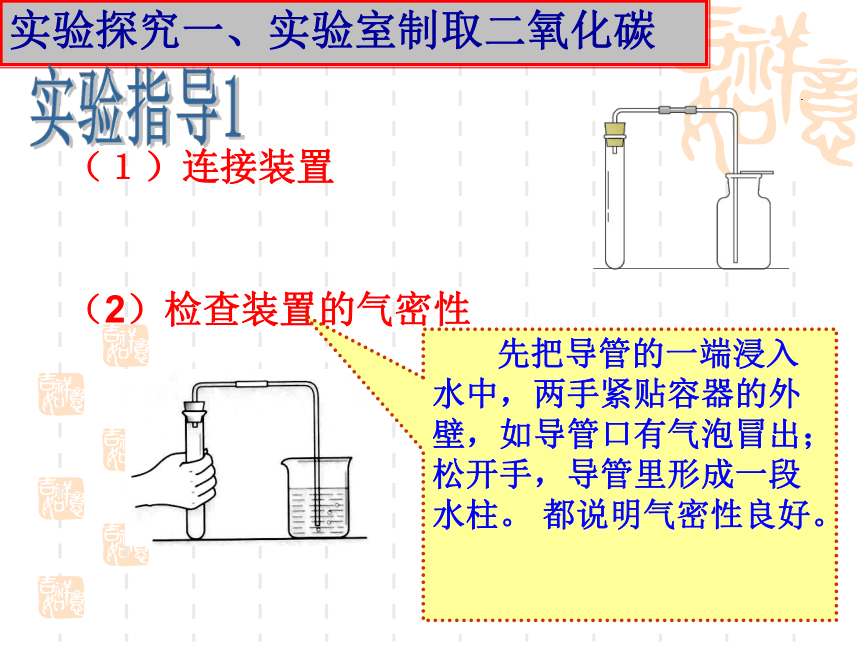
(1)连接装置
(2)检查装置的气密性
先把导管的一端浸入水中,两手紧贴容器的外壁,如导管口有气泡冒出;松开手,导管里形成一段水柱。 都说明气密性良好。
实验探究一、实验室制取二氧化碳
在试管里放入几小块大理石(或石灰石),然后小心地注入15mL稀盐酸。立即用带有导管的橡胶塞塞住管口,观察试管里发生的现象,以及反应中产生气体的颜色。过一会儿,检查集气瓶中是否已收集满二氧化碳。用玻璃片盖住已收集满二氧碳的集气瓶,备用。
实验探究一、实验室制取二氧化碳
先加入大理石或石灰石,再加入稀盐酸 ,立即用带有导管的橡胶塞塞住试管口,看到的现象有:
试管中有气泡生成
实验探究一、实验室制取二氧化碳
只能用
向上排气法
理由是:
二氧化碳的密度比空气大,且二氧化碳能溶于水。
检查集气瓶是否收集满:
用燃着木条平放在集气瓶口,木条熄灭,则已收集满
如果在实验中用了如下图所示的装置,又应该注意哪些问题呢?
① 应事先直接加入锥形瓶中;
②长颈漏斗的作用是加入 ;
③长颈漏斗的下端管口应伸入 ;
④锥形瓶中的导气管不应伸入反应液面以下,
应 为宜;
⑤伸入集气瓶中的导气管口应位于集气瓶 ,
而不应位于集气瓶 。
大理石(或石灰石)
稀盐酸
液面以下
稍露出橡胶塞
底部
中部及以上
实验探究二、二氧化碳的性质检验
1.将二氧化碳倒入烧杯中
(1)把一支短蜡烛固定在烧杯内,点燃。拿起收集满二气化碳的集气瓶,向烧杯内缓慢倾倒二氧化碳,观察现象。
现象:
燃着蜡烛熄灭
想一想:这个实验证明二氧化碳具有哪些性质?
说明二氧化碳具有不燃烧、不支持燃烧的性质
实验探究二、二氧化碳的性质检验
2.二氧化碳与水反应
(1)向两支试管中分别加入2 mL蒸馏水,然后各滴入1-2mL滴石蕊溶液;
2ml蒸馏水的试管1 2ml蒸馏水的试管2
现象
颜色无变化
颜色无变化
实验探究二、二氧化碳的性质检验
(2)向(1)其中的一支试管中通入二氧化碳,观察现象
无颜色变化
试管1静置 试管2通入二氧化碳
现象
结论
想一想:通过这个实验可以得出什么样的结论?
二氧化碳通入水中后的生成物能使石蕊溶液变红色。二氧化碳通入水中后生成了H2CO3
无色溶液变成红色溶液
实验探究二、二氧化碳的性质检验
(3)将(2)通入二氧化碳的试管放在酒精灯上加热;观察现象:
红色溶液又变成无色。
现象:
想一想:这又说明了什么问题呢?
结论:碳酸不稳定,加热分解,没有碳酸,不能使石蕊变红色。
实验探究二、二氧化碳的性质检验
3.二氧化碳与澄清的石灰水反应
取一支试管,向其中注入少量澄清石灰水,然后通入二氧化碳 :
实验现象:
澄清石灰水变浑浊
化学方程式:
CO2+Ca(OH)2=CaCO3 +H2O
怎样用实验证明碳酸型饮料(如汽水)中含有二氧化碳?请试一试。
打开汽水瓶盖,塞上带有导气管的橡胶塞,将瓶内的气体通入盛有澄清石灰水的试管中,若澄清石灰水变浑浊,证明汽水中有二氧化碳。
学习目标:
1.练习实验室里制取二氧化碳和用向上排空气法收集气体。
2.加深对二氧化碳性质的认识。
实验探究一、实验室制取二氧化碳
【实验药品】
大理石(或石灰石)、稀盐酸(1∶2)、澄清石灰水、紫色石蕊试液、蜡烛、木条、蒸馏水、火柴。
【实验仪器】
烧杯、集气瓶、量筒、玻璃导管、胶皮管、单孔橡胶塞、铁架台(带铁夹)、试管、试管夹、玻璃片、酒精灯。
实验探究一、实验室制取二氧化碳
我们已经学习了二氧化碳的制取与性质,请同学们回忆一下,实验室制取二氧化碳的实验用品是什么,实验原理是什么?
实验探究一、实验室制取二氧化碳
1.药品
大理石(或石灰石) 稀盐酸
2.实验原理
CaCO3+2HCl==CaCl2+H2O+CO2↑
实验探究一、实验室制取二氧化碳
(1)连接装置
(2)检查装置的气密性
先把导管的一端浸入水中,两手紧贴容器的外壁,如导管口有气泡冒出;松开手,导管里形成一段水柱。 都说明气密性良好。
实验探究一、实验室制取二氧化碳
在试管里放入几小块大理石(或石灰石),然后小心地注入15mL稀盐酸。立即用带有导管的橡胶塞塞住管口,观察试管里发生的现象,以及反应中产生气体的颜色。过一会儿,检查集气瓶中是否已收集满二氧化碳。用玻璃片盖住已收集满二氧碳的集气瓶,备用。
实验探究一、实验室制取二氧化碳
先加入大理石或石灰石,再加入稀盐酸 ,立即用带有导管的橡胶塞塞住试管口,看到的现象有:
试管中有气泡生成
实验探究一、实验室制取二氧化碳
只能用
向上排气法
理由是:
二氧化碳的密度比空气大,且二氧化碳能溶于水。
检查集气瓶是否收集满:
用燃着木条平放在集气瓶口,木条熄灭,则已收集满
如果在实验中用了如下图所示的装置,又应该注意哪些问题呢?
① 应事先直接加入锥形瓶中;
②长颈漏斗的作用是加入 ;
③长颈漏斗的下端管口应伸入 ;
④锥形瓶中的导气管不应伸入反应液面以下,
应 为宜;
⑤伸入集气瓶中的导气管口应位于集气瓶 ,
而不应位于集气瓶 。
大理石(或石灰石)
稀盐酸
液面以下
稍露出橡胶塞
底部
中部及以上
实验探究二、二氧化碳的性质检验
1.将二氧化碳倒入烧杯中
(1)把一支短蜡烛固定在烧杯内,点燃。拿起收集满二气化碳的集气瓶,向烧杯内缓慢倾倒二氧化碳,观察现象。
现象:
燃着蜡烛熄灭
想一想:这个实验证明二氧化碳具有哪些性质?
说明二氧化碳具有不燃烧、不支持燃烧的性质
实验探究二、二氧化碳的性质检验
2.二氧化碳与水反应
(1)向两支试管中分别加入2 mL蒸馏水,然后各滴入1-2mL滴石蕊溶液;
2ml蒸馏水的试管1 2ml蒸馏水的试管2
现象
颜色无变化
颜色无变化
实验探究二、二氧化碳的性质检验
(2)向(1)其中的一支试管中通入二氧化碳,观察现象
无颜色变化
试管1静置 试管2通入二氧化碳
现象
结论
想一想:通过这个实验可以得出什么样的结论?
二氧化碳通入水中后的生成物能使石蕊溶液变红色。二氧化碳通入水中后生成了H2CO3
无色溶液变成红色溶液
实验探究二、二氧化碳的性质检验
(3)将(2)通入二氧化碳的试管放在酒精灯上加热;观察现象:
红色溶液又变成无色。
现象:
想一想:这又说明了什么问题呢?
结论:碳酸不稳定,加热分解,没有碳酸,不能使石蕊变红色。
实验探究二、二氧化碳的性质检验
3.二氧化碳与澄清的石灰水反应
取一支试管,向其中注入少量澄清石灰水,然后通入二氧化碳 :
实验现象:
澄清石灰水变浑浊
化学方程式:
CO2+Ca(OH)2=CaCO3 +H2O
怎样用实验证明碳酸型饮料(如汽水)中含有二氧化碳?请试一试。
打开汽水瓶盖,塞上带有导气管的橡胶塞,将瓶内的气体通入盛有澄清石灰水的试管中,若澄清石灰水变浑浊,证明汽水中有二氧化碳。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
