【精讲】人教版化学九年级下册 8.2 金属的化学性质 同步学案
文档属性
| 名称 | 【精讲】人教版化学九年级下册 8.2 金属的化学性质 同步学案 |
|
|
| 格式 | doc | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-22 00:00:00 | ||
图片预览





文档简介
中小学教育资源及组卷应用平台
第八单元课题2 金属的化学性质
思维导图
二、考点精讲
考点一: 金属的化学性质
SHAPE \* MERGEFORMAT
SHAPE \* MERGEFORMAT
【精讲1】金和黄铜(铜锌合金)是生活中常见的物质,下列试剂或方法不能将其区分的是( )
A.稀硫酸 B.硝酸银溶液 C.观察颜色 D.灼烧
【答案】C
【解析】A、黄铜含有锌,可与硫酸反应生成氢气,有气泡产生,而黄金不反应,无明显现象,可以区分两种物质,故错误;B、黄铜含有锌、铜,可与硝酸银反应生成银,表面有银白色物质出现,而黄金不反应,无明显现象,可以区分两种物质,故错误;C、金和黄铜都为黄色,无法通过观察颜色进行区分,故正确;D、黄铜灼烧有氧化铜生成,变为黑色,而黄金不变色,可以区分两种物质,故错误;故选:C。
【精讲2】下列有关镁与稀盐酸反应的实验现象,描述正确的是( )
A.生成氢气 B.固体无变化
C.试管温度升高 D.溶液变成浅绿色
【答案】C
【解析】A、镁与稀盐酸反应生成氯化镁溶液和氢气,会观察到产生大量气泡,生成氢气是实验结论而不是实验现象,故选项说法错误。B、镁与稀盐酸反应生成氯化镁溶液和氢气,随着反应的进行,固体的质量逐渐减少,故选项说法错误。C、镁与稀盐酸反应属于放热反应,试管温度升高,故选项说法正确。D、镁与稀盐酸反应生成氯化镁溶液和氢气,溶液不变色,仍为无色,故选项说法错误。故选:C。
【跟踪练1】下列金属,不能与稀硫酸反应产生氢气的是( )
A.Mg B.Zn C.Al D.Cu
【答案】D所有
【解析】A、镁和稀硫酸反应生成硫酸镁和氢气,该选项不正确。B、锌和稀硫酸反应生成硫酸锌和氢气,该选项不正确。C、铝和稀硫酸反应生成硫酸铝和氢气,该选项不正确。D、铜不能和稀硫酸反应,该选项正确。故选:D。
【跟踪练2】相同质量的镁、铁、锌三种金属,分别与足量的、相同质量分数的稀硫酸充分反应,生成氢气质量与反应时间关系见如图,分析图像判断,下面说法正确的是( )
A.金属锌反应速率最大
B.金属锌的活动性最强
C.金属镁生成氢气质量最多
D.金属铁消耗稀硫酸质量最多
【答案】D所有
【解析】A、由图象可知,至完全反应,镁用的时间最短,则金属镁反应速率最大,故选项说法错误。B、由图象可知,至完全反应,镁用的时间最短,则金属镁的活动性最强,故选项说法错误。C、纵坐标表示生成氢气的质量,则金属镁生成氢气质量最多,故选项说法正确。D、由质量守恒定律,生成的氢气中氢元素的质量来自于硫酸中氢元素的质量,金属镁与稀硫酸反应生成氢气质量最多,则金属镁消耗稀硫酸质量最多,故选项说法错误。故选:C。
【跟踪练3】金属材料的广泛使用大大提高了我们的幸福指数。下列有关金属和金属材料的说法不正确的是( )
A.铝在空气中具有很好的抗腐蚀性能
B.生铁和钢都是铁的合金,属于混合物
C.黄铜片和铜片相互刻画,黄铜片上有较深划痕
D.铁能与硫酸铜溶液反应生成铜
【答案】C所有
【解析】A、铝和空气中的氧气反应生成致密的氧化铝薄膜,阻碍铝的进一步反应,所以铝在空气中具有很好的抗腐蚀性能,故A正确;B、生铁含碳量是2%﹣4.3%,钢的含碳量是0.03%﹣2%,所以生铁和钢都是铁的合金,属于混合物,故B正确;C、合金的硬度比组成其纯金属的硬度大,所以黄铜片和铜片相互刻画,铜片上有较深划痕,故C错误;D、铁能与硫酸铜溶液反应生成铜和硫酸亚铁,故D正确。故选:C。
考点二: 置换反应
【精讲1】下列反应中,属于置换反应的是( )
A.Cu2(OH)2CO32CuO+CO2↑+H2O B.SO3+H2O═H2SO4
C.H2+CuOCu+H2O D.FeCl3+3NaOH═Fe(OH)3↓+3NaCl
【答案】C所有
【解析】置换反应是由一种单质和一种化合物反应,生成另外一种单质和一种化合物的反应,据此进行分析判断。A、Cu2(OH)2CO32CuO+CO2↑+H2O,该反应符合“一变多”的形式,符合分解反应的特征,属于分解反应,故选项错误。B、SO3+H2O═H2SO4,该反应符合“多变一”的形式,符合化合反应的特征,属于化合反应,故选项错误。C、H2+CuOCu+H2O,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项正确。D、FeCl3+3NaOH═Fe(OH)3↓+3NaCl,该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应,故选项错误。故选:C。
【精讲2】下列推理正确的是( )
A.单质中只含有一种元素,因此只含有一种元素的物质一定是单质
B.置换反应中一定有单质生成,因此有单质生成的反应一定是置换反应
C.元素是具有相同核电荷数的一类原子的总称,因此同种元素核电荷数一定相同
D.原子核是由质子和中子构成的,则所有的原子核中一定都含有质子和中子
【答案】C所有
【解析】A、只含有一种元素的纯净物属于单质,只含有一种元素的物质不一定是单质,例如氧气和臭氧混合在一起属于混合物,故错误;B、置换反应一定有单质生成,但有单质生成的反应不一定是置换反应,例如水电解,故错误;C、元素是具有相同核电荷数(即质子数)的一类原子的总称,因此同种元素核电荷数(即质子数)一定相同,故正确;D、原子核中不一定都含有质子和中子,如氢原子没有中子,故错误;故选:C。
【跟踪练1】下列反应属于置换反应的是( )
A.2CO+O22CO2 B.C+2CuO2Cu+CO2↑
C.2H2O2H2↑+O2↑ D.CaCO3+2HCl═CaCl2+H2O+CO2↑
【答案】B
【解析】置换反应是由一种单质和一种化合物反应,生成另外一种单质和一种化合物的反应。A、2CO+O22CO2,该反应符合“多变一”的形式,符合化合反应的特征,属于化合反应,故选项错误。B、C+2CuO2Cu+CO2↑,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项正确。C、2H2O2H2↑+O2↑,该反应符合“一变多”的形式,符合分解反应的特征,属于分解反应,故选项错误。D、CaCO3+2HCl═CaCl2+H2O+CO2↑,该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应,故选项错误。故选:B。
【跟踪练2】下列反应中不属于置换反应的是( )
A.氢气与氧化铜反应得到铜和水 B.铁与稀硫酸反应得到氢气
C.一氧化碳和氧化铁反应得到铁 D.铜与硝酸银溶液反应得到银
【答案】C
【解析】置换反应是由一种单质和一种化合物反应,生成另外一种单质和一种化合物的反应。A、氢气与氧化铜反应得到铜和水,该反应属于置换反应B、铁与稀硫酸反应得到氢气,同时生成硫酸亚铁,该反应属于置换反应;C、一氧化碳和氧化铁反应得到铁和二氧化碳,该反应的反应物均为化合物,不属于置换反应;D、铜与硝酸银溶液反应生成银和硝酸铜溶液,该反应属于置换反应;故选:C。
考点三: 金属活动性顺序及其应用
【精讲1】下列金属活动性最强的是( )
A.铝 B.镁 C.铁 D.铜
【答案】B
【解析】常见金属活动性顺序为K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au;在金属活动性顺序中,金属的位置越靠前,金属的活动性就越强,选项提供的四种金属中镁的位置最靠前,故四种金属中金属活动性最强的是镁。故选:B。
【精讲2】把X、Y、Z三种金属分别放入稀盐酸中,X逐渐消失并有气泡产生,Y、Z不反应;取Y放入Z(NO3)2溶液中仍不反应。则X、Y、Z三种金属的活动性由强到弱的顺序是( )
A.X>Y>Z B.Y>Z>X C.Y>X>Z D.X>Z>Y
【答案】D
【解析】在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此来分析问题。把X、Y、Z三种金属分别放入稀盐酸中,X逐渐消失并有气泡产生,Y、Z不反应,说明X的金属活动性强于Y、Z,而把Y放入到Z(NO3)2溶液中仍不反应,说明Z的金属活动性强于Y,则X、Y、Z三种金属的活动性由强到弱的顺序为X>Z>Y。故选:D。
【精讲3】要证明Fe的活动性比Cu强,选用下列各组试剂进行实验时,不能验证此结论的是( )
A.Cu、FeCl2溶液 B.Fe、Cu、稀盐酸
C.Fe、Cu、ZnSO4溶液 D.Fe、CuCl2溶液
【答案】C
【解析】A、铜不会与氯化亚铁反应,说明铁比铜活泼,故正确;B、铁会与盐酸反应,铜不会,说明铁比铜活泼,故正确;C、铁、铜都不会与硫酸锌反应,不能验证,故C错误;D、铁会与氯化铜反应,铁比铜活泼,可以验证,故正确。故选:C。
【精讲4】为验证铁、铜、银的金属活动性顺序,某同学设计了以下四组实验。下列说法错误的是( )
A.通过实验①、②,能验证金属活动性:Fe>Cu
B.通过实验①、②、③,能验证金属活动性:Fe>Cu>Ag
C.实验④中X为Cu,Y为FeSO4,能验证金属活动性:Fe>Cu
D.实验④中X为Cu,Y为AgNO3,能验证金属活动性:Cu>Ag
【答案】B
【解析】A、①中产生气泡,是因为铁和稀硫酸反应生成了氢气,说明铁排在氢前面,②中铜与硫酸不反应,说明铜排在氢后面,能验证金属活动性:Fe>Cu,故正确;B、①中产生气泡,是因为铁和稀硫酸反应生成了氢气,说明铁排在氢前面,②中铜与硫酸不反应,说明铜排在氢后面,能验证金属活动性:Fe>Cu,③中铁表面析出银白色固体,是因为铁和硝酸银反应生成了银,说明铁比银活泼,不能比较铜和银的活泼性,故错误;C、若X是铜,则Y是硫酸亚铁,是因为铜不能和硫酸亚铁反应,说明铁比铜活泼,故正确;D、若X是铜,则Y是硝酸银,铜表面析出银白色固体,是因为铜和硝酸银反应生成了银,说明铜比银活泼,故正确。故选:B。
【精讲5】向硝酸铜和硝酸银的混合溶液中加入一定量的锌粉,充分反应后过滤,得到滤渣和滤液,滤液呈蓝色。下列说法正确的是( )
A.滤渣中一定有Ag和Cu
B.向滤渣中滴加稀盐酸,一定有气泡产生
C.滤液中一定有Cu2+、Zn2+
D.向滤液中滴加稀盐酸,一定有沉淀生成
【答案】C
【解析】向硝酸铜和硝酸银的混合溶液中加入一定量的锌粉,锌先和硝酸银反应生成硝酸锌和银,后和硝酸铜反应生成硝酸锌和铜,充分反应后过滤,得到滤渣和滤液,滤液呈蓝色,说明硝酸铜没有或部分反应。A、滤渣中一定含有银,不一定含有铜,该选项不正确。B、滤渣中不含有锌,加入稀盐酸,不产生气泡,该选项不正确。C、滤液中一定有Cu2+、Zn2+,该选项正确。D、向滤液中滴加稀盐酸,不一定有沉淀生成,是因为不知道硝酸银是否完全反应,该选项不正确。故选:C。
【跟踪练1】下列事实不能用金属活动性解释的是( )
A.铝制品比铁制品耐腐蚀
B.用硫酸铜溶液和铁制取铜
C.用硫酸铜溶液、铁、银验证铁、铜、银金属活动性
D.金属铜不能与稀硫酸反应
【答案】A
【解析】A、铝制品比铁制品耐腐蚀,是因为铝在空气中能与氧气反应,其表面生成一层致密的氧化铝薄膜,阻止内部的铝进一步被氧化,因此铝制品抗腐蚀性强,不能用金属活动性解释,故选项正确。B、用硫酸铜溶液和铁制取铜,是因为铁能与硫酸铜溶液发生置换反应,能用金属活动性解释,故选项错误。C、用硫酸铜溶液、铁、银验证铁、铜、银金属活动性,是因为铁能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,银不能与硫酸铜溶液反应,能用金属活动性解释,故选项错误。D、金属铜不能与稀硫酸反应,是因为在金属活动性顺序中,铜的位置排在氢的后面,能用金属活动性解释,故选项错误。故选:A。
【跟踪练2】可通过金属与稀盐酸反应直接得到的物质是( )
A.氯化锌 B.氯化银 C.氯化铜 D.氯化铁
【答案】A
【解析】A、在金属活动性顺序中,锌排在氢前面,锌和盐酸反应生成氯化锌和氢气,故选项正确。B、在金属活动性顺序中,银排在氢后面,银和盐酸不能发生反应,不能生成氯化银,故选项错误。C、在金属活动性顺序中,铜排在氢后面,铜和盐酸不能发生反应,不能生成氯化铜,故选项错误。D、在金属活动性顺序中,铁排在氢前面,能和盐酸反应生成氯化亚铁和氢气,不能生成氯化铁,故选项错误。故选:A。
【跟踪练3】为探究Zn、Fe、Cu三种金属的活动性顺序,以下四组实验方案中可行的是( )
A.将Zn分别加入FeCl2、CuCl2溶液中
B.将Zn、Fe分别加入CuCl2溶液中
C.将Zn、Fe分别加入稀盐酸中
D.将Fe分别加入ZnCl2和CuCl2溶液中
【答案】D
【解析】A、将Zn分别加入FeCl2、CuCl2溶液中,锌能置换出铁和铜,说明锌的活动性强于铁和铜,但无法确定铁和铜的活动性强弱,故选项错误。B、将Zn、Fe分别加入CuCl2溶液中,锌和铁都能置换出铜,说明锌和铁的活动性都强于铜,但无法确定锌和铁的活动性强弱,故选项错误。C、将Zn、Fe分别加入稀盐酸中,根据产生氢气的速率快慢可以比较锌、铁的活动性强弱,但无法确定与铜的活动性强弱,故选项错误。D、将Fe分别加入ZnCl2和CuCl2溶液中,铁与ZnCl2溶液不反应,说明锌的活动性强于铁;铁与CuSO4溶液反应置换出铜,说明铁的活动性强于铜,由此可得出三种金属活动性锌>铁>铜,故选项正确。故答案为:D。
【跟踪练4】向一定量的硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉质量关系如图,下列说法正确的是( )
A.a点溶液中的物质2种
B.b点得到的固体是Cu
C.c点溶液中只有Zn(NO3)2
D.d点得到的固体有2种
【答案】C
【解析】A、锌的金属活动性比银、铜强,向一定量的硝酸银和硝酸铜的混合溶液中加入锌粉,锌先与AgNO3反应生成硝酸锌和银,AgNO3反应完,锌才能与Cu(NO3)2反应生成硝酸锌和铜,a点发生的是锌与硝酸银的反应,硝酸银有剩余,a点溶液中的溶质有硝酸银、硝酸铜、硝酸锌3种,故选项说法错误。B、b点,锌和硝酸银恰好完全反应,则b点得到的固体是银,故选项说法错误。C、c点,锌与硝酸铜恰好完全反应,c点溶液中只有Zn(NO3)2,故选项说法正确。D、d点,锌过量,得到的固体有银、铜、锌3种,故选项说法错误。故选:C。
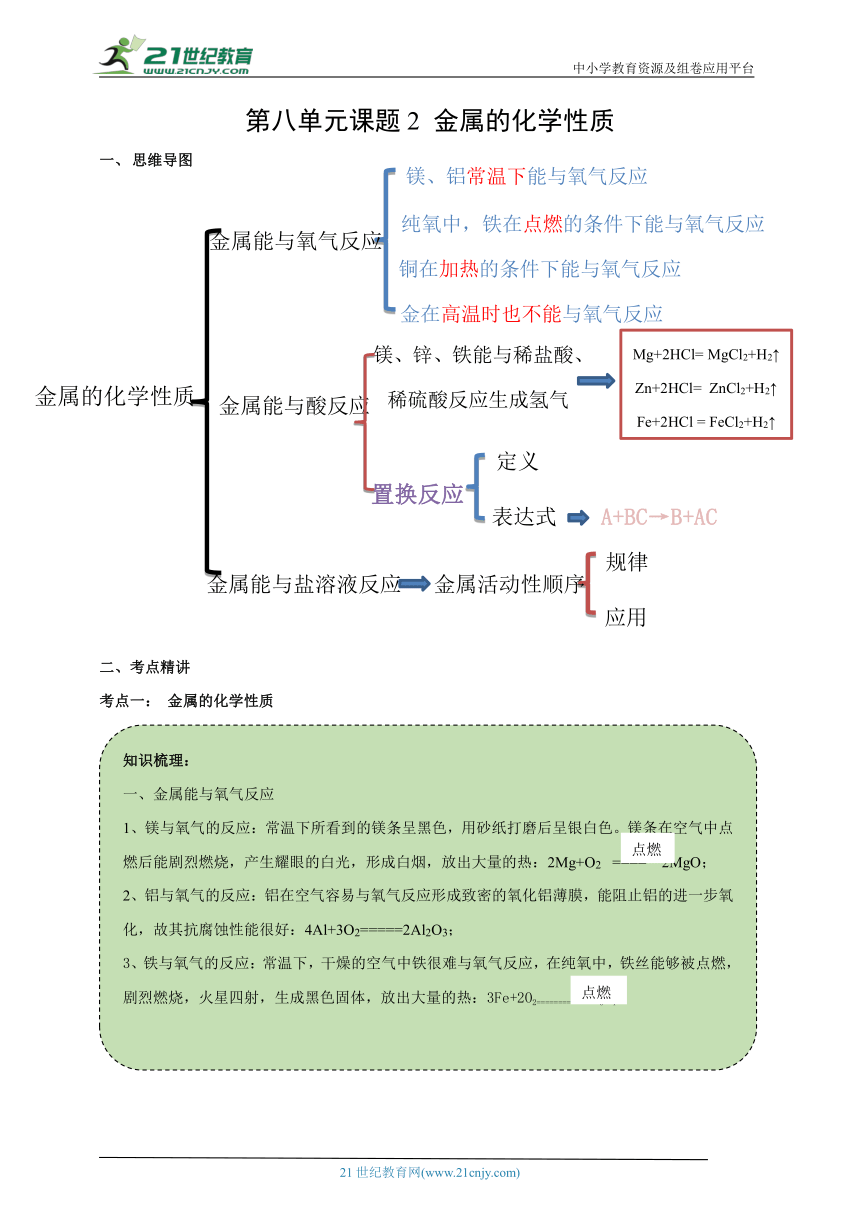
镁、铝常温下能与氧气反应
纯氧中,铁在点燃的条件下能与氧气反应
金属能与氧气反应
铜在加热的条件下能与氧气反应
金在高温时也不能与氧气反应
Mg+2HCl= MgCl2+H2↑
Zn+2HCl= ZnCl2+H2↑
Fe+2HCl = FeCl2+H2↑
镁、锌、铁能与稀盐酸、
稀硫酸反应生成氢气
金属能与酸反应
金属的化学性质
定义
置换反应
A+BC→B+AC
表达式
规律
金属能与盐溶液反应
金属活动性顺序
应用
点燃
点燃
知识梳理:
一、金属能与氧气反应
1、镁与氧气的反应:常温下所看到的镁条呈黑色,用砂纸打磨后呈银白色。镁条在空气中点燃后能剧烈燃烧,产生耀眼的白光,形成白烟,放出大量的热:2Mg+O2 ==== 2MgO;
2、铝与氧气的反应:铝在空气容易与氧气反应形成致密的氧化铝薄膜,能阻止铝的进一步氧化,故其抗腐蚀性能很好:4Al+3O2=====2Al2O3;
3、铁与氧气的反应:常温下,干燥的空气中铁很难与氧气反应,在纯氧中,铁丝能够被点燃,剧烈燃烧,火星四射,生成黑色固体,放出大量的热:3Fe+2O2===========Fe3O4;
△
4、铜与氧气的反应:在加热的情况下,铜能与氧气反应,生成黑色的物质(氧化铜);即2Cu+O2======2CuO。即使在纯氧中,铜也不能被点燃。
5、金即使在高温时也不与氧气反应。
二、金属能与稀盐酸、稀硫酸反应
酸金 属 现象 反应的化学方程式
盐酸/稀硫酸 盐酸 稀硫酸
镁 反应非常剧烈,产生大量气泡 Mg+2HCl= MgCl2+H2↑ Mg+H2SO4 = MgSO4+H2↑
锌 反应比较剧烈,产生大量气泡 Zn+2HCl= ZnCl2+H2↑ Zn+H2SO4 = ZnSO4+H2↑
铁 反应缓慢,有气泡产生,溶液由无色逐渐变为淡绿色 Fe+2HCl = FeCl2+H2↑ Fe+H2SO4= FeSO4+H2↑
铜 不反应
三、金属能与金属化合物溶液(即盐溶液)反应:
金属+盐==新金属+新盐 (条件:活动性:参加反应的金属>化合物中金属元素)
(1)铁丝浸入硫酸铜溶液中:Fe + CuSO4 == Cu + FeSO4
现象:铁的表面覆盖一层红色的物质,溶液有蓝色变成浅绿色
(2)铝丝浸入硫酸铜溶液中:2Al + 3CuSO4 == Al2(SO4)3 + 3Cu
现象:铝丝表面有红色物质出现,溶液由蓝色变为无色
(3)铜丝浸入硝酸银溶液中:Cu + 2AgNO3 == Cu(NO3)2 + 2Ag
现象:铜丝表面有银白色物质出现,溶液由无色变为蓝色
【知识点睛】
铝比铁更不容易被腐蚀是因为铝在空气容易与氧气反应形成致密的氧化铝薄膜,能阻止铝的进一步氧化;
2、越容易与氧气反应的金属其活动性越强;
3、在其他条件完全相同时,与酸反应越剧烈的金属活动性越强;
【命题方向】
该考点的命题方向主要是通过创设相关实验、问题情景或图表信息等,来考查学生对金属的化学性质的理解或掌握情况,以及对常见金属的特性及其应用、金属的物理性质及用途、合金与合金的性质、金属活动性顺序及其应用、实验现象及结论(包括反应化学方程式)等相关问题的分析、推断、表达的能力和对知识的迁移能力等;并且,经常将其与常见金属的特性及其应用、金属的物理性质及用途、金属活动性顺序及其应用、化学方程式的书写等关联起来,进行综合考查。
【解题方法点拨】
熟记金属的化学性质及各个反应的原理和现象。
知识梳理:
置换反应(四大基本反应类型之一)
1、定义:由一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应;
2、表达式:A+BC→B+AC
3、特点:反应物是单质与化合物,生成物也是单质与化合物。可以简记为:“单化变单化”。
【知识点睛】
1、有铁参与的置换反应生成的是+2价的亚铁;
2、置换反应中的置换关系是指组成化合物的某种元素被组成单质的元素所替代.因此,在判定置换反应时,一定要抓住它的特点,结合它的概念和通式,以及单质和化合物的判定方法来细心地判定。
【命题方向】
该考点的命题方向主要是通过创设相关问题情景或图表信息等,来考查学生对置换反应及其应用的理解和掌握情况。特别是,对“碳、氢气和金属等物质的化学性质,置换反应的判定及其与其它反应类型的判别,利用分解反应的原理来制取氢气和某些金属或鉴别和推断某些物质”等相关问题的考查,以及对有关知识的迁移能力的考查,是近几年中考命题的热点。
【解题方法点拨】
首先,要理解和熟记置换反应及其应用,以及与之相关的知识.然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可。
知识梳理:
常见金属的活动性顺序:
2、应用:
(1)在金属活动性顺序中,金属的位置越靠前;
注意点:金属的活动性就越强参加反应时,现象就越明显、越剧烈.
(2)排在氢前面的金属,能置换出酸中的氢,而排在氢后面的金属不能置换出酸中的氢;
注意点:①金属必须是排在金属活动性顺序中(H)前面的金属;
②酸应是盐酸、稀硫酸(即不具有强氧化性的酸),不包括浓硫酸和硝酸;
③单质铁与酸发生置换反应时生成亚铁盐;
④K、Ca、Na除与酸反应外,还能与水在常温下发生置换反应(如2Na+2H2O=2NaOH+H2↑),其余金属则不能;
(3)排在金属活动性顺序中前面的金属一般能把排在后面的金属从其盐溶液里置换出来。
注意点:①在金属活动性顺序中只要排在前面的金属就能把排在后面的金属从其盐溶液中置换出来,而与H的位置无关.但K、Ca、Na等金属例外;
②铁与盐溶液发生置换反应时,生成二价亚铁盐;
③用同种金属置换不同的盐溶液,盐中金属排在金属活动性顺序中较后的金属首先被置换出来.用不同的金属置换同种盐溶液,盐中金属先被排在金属活动性顺序中较前的金属置换出来。另外,若有一种金属和多种混合盐溶液反应,最先反应的是最不活泼的那个金属的盐溶液。
【知识点睛】
利用金属与酸或盐溶液之间的置换反应是否发生,通过具体的实验及其现象的分析,反过来可以反推金属的活动性顺序。
1.利用金属与酸能否发生置换反应,来反推金属的活动性顺序。例如,把铁和铜分别放在稀盐酸中时,铁的表面上有气泡冒出,这说明铁位居金属活动性顺序中氢的前面;而铜的表面无明显的现象,这说明铜位居金属活动性顺序中氢的后面;由此可推得铁活泼性比铜的要强。
2.利用金属与盐溶液能否发生置换反应,来反推金属的活动性顺序。例如,把铁钉放在硫酸铜溶液中,过一会儿,发现铁钉表面上出现了一层红色物质(即铜);由此可推得铁活泼性比铜的要强。
【命题方向】
该考点的命题方向主要是通过创设相关实验、问题情景或图表信息等,来考查学生对金属活动性顺序及其应用的理解或掌握情况;以及阅读、分析、推断、表达的能力和对知识的迁移能力等.并且,经常将其与“金属的性质及用途、常见金属的特性及其应用、合金与合金的性质、实验现象和结论(包括反应化学方程式)、其它的反应类型”等相关问题关联起来,进行综合考查.金属活动性顺序及其应用是历年来中考命题的热点;命题方式是根据金属活动性顺序及其应用来分析、推断、选择或解答有关金属的活动性强弱、某些置换反应是否发生、实验现象、实验结论(包括反应化学方程式)、金属的制备、金属的应用、生活中有关金属的实际问题,或者是反过来考查,或者是对所给的有关金属活动性顺序及其应用的表达进行判断,等等。
【解题方法点拨】
解答这类题目时,首先,要熟记和理解金属活动性顺序及其应用,以及与之相关的知识等;然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,细致地阅读、分析题意等,联系着生活实际,细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
第八单元课题2 金属的化学性质
思维导图
二、考点精讲
考点一: 金属的化学性质
SHAPE \* MERGEFORMAT
SHAPE \* MERGEFORMAT
【精讲1】金和黄铜(铜锌合金)是生活中常见的物质,下列试剂或方法不能将其区分的是( )
A.稀硫酸 B.硝酸银溶液 C.观察颜色 D.灼烧
【答案】C
【解析】A、黄铜含有锌,可与硫酸反应生成氢气,有气泡产生,而黄金不反应,无明显现象,可以区分两种物质,故错误;B、黄铜含有锌、铜,可与硝酸银反应生成银,表面有银白色物质出现,而黄金不反应,无明显现象,可以区分两种物质,故错误;C、金和黄铜都为黄色,无法通过观察颜色进行区分,故正确;D、黄铜灼烧有氧化铜生成,变为黑色,而黄金不变色,可以区分两种物质,故错误;故选:C。
【精讲2】下列有关镁与稀盐酸反应的实验现象,描述正确的是( )
A.生成氢气 B.固体无变化
C.试管温度升高 D.溶液变成浅绿色
【答案】C
【解析】A、镁与稀盐酸反应生成氯化镁溶液和氢气,会观察到产生大量气泡,生成氢气是实验结论而不是实验现象,故选项说法错误。B、镁与稀盐酸反应生成氯化镁溶液和氢气,随着反应的进行,固体的质量逐渐减少,故选项说法错误。C、镁与稀盐酸反应属于放热反应,试管温度升高,故选项说法正确。D、镁与稀盐酸反应生成氯化镁溶液和氢气,溶液不变色,仍为无色,故选项说法错误。故选:C。
【跟踪练1】下列金属,不能与稀硫酸反应产生氢气的是( )
A.Mg B.Zn C.Al D.Cu
【答案】D所有
【解析】A、镁和稀硫酸反应生成硫酸镁和氢气,该选项不正确。B、锌和稀硫酸反应生成硫酸锌和氢气,该选项不正确。C、铝和稀硫酸反应生成硫酸铝和氢气,该选项不正确。D、铜不能和稀硫酸反应,该选项正确。故选:D。
【跟踪练2】相同质量的镁、铁、锌三种金属,分别与足量的、相同质量分数的稀硫酸充分反应,生成氢气质量与反应时间关系见如图,分析图像判断,下面说法正确的是( )
A.金属锌反应速率最大
B.金属锌的活动性最强
C.金属镁生成氢气质量最多
D.金属铁消耗稀硫酸质量最多
【答案】D所有
【解析】A、由图象可知,至完全反应,镁用的时间最短,则金属镁反应速率最大,故选项说法错误。B、由图象可知,至完全反应,镁用的时间最短,则金属镁的活动性最强,故选项说法错误。C、纵坐标表示生成氢气的质量,则金属镁生成氢气质量最多,故选项说法正确。D、由质量守恒定律,生成的氢气中氢元素的质量来自于硫酸中氢元素的质量,金属镁与稀硫酸反应生成氢气质量最多,则金属镁消耗稀硫酸质量最多,故选项说法错误。故选:C。
【跟踪练3】金属材料的广泛使用大大提高了我们的幸福指数。下列有关金属和金属材料的说法不正确的是( )
A.铝在空气中具有很好的抗腐蚀性能
B.生铁和钢都是铁的合金,属于混合物
C.黄铜片和铜片相互刻画,黄铜片上有较深划痕
D.铁能与硫酸铜溶液反应生成铜
【答案】C所有
【解析】A、铝和空气中的氧气反应生成致密的氧化铝薄膜,阻碍铝的进一步反应,所以铝在空气中具有很好的抗腐蚀性能,故A正确;B、生铁含碳量是2%﹣4.3%,钢的含碳量是0.03%﹣2%,所以生铁和钢都是铁的合金,属于混合物,故B正确;C、合金的硬度比组成其纯金属的硬度大,所以黄铜片和铜片相互刻画,铜片上有较深划痕,故C错误;D、铁能与硫酸铜溶液反应生成铜和硫酸亚铁,故D正确。故选:C。
考点二: 置换反应
【精讲1】下列反应中,属于置换反应的是( )
A.Cu2(OH)2CO32CuO+CO2↑+H2O B.SO3+H2O═H2SO4
C.H2+CuOCu+H2O D.FeCl3+3NaOH═Fe(OH)3↓+3NaCl
【答案】C所有
【解析】置换反应是由一种单质和一种化合物反应,生成另外一种单质和一种化合物的反应,据此进行分析判断。A、Cu2(OH)2CO32CuO+CO2↑+H2O,该反应符合“一变多”的形式,符合分解反应的特征,属于分解反应,故选项错误。B、SO3+H2O═H2SO4,该反应符合“多变一”的形式,符合化合反应的特征,属于化合反应,故选项错误。C、H2+CuOCu+H2O,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项正确。D、FeCl3+3NaOH═Fe(OH)3↓+3NaCl,该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应,故选项错误。故选:C。
【精讲2】下列推理正确的是( )
A.单质中只含有一种元素,因此只含有一种元素的物质一定是单质
B.置换反应中一定有单质生成,因此有单质生成的反应一定是置换反应
C.元素是具有相同核电荷数的一类原子的总称,因此同种元素核电荷数一定相同
D.原子核是由质子和中子构成的,则所有的原子核中一定都含有质子和中子
【答案】C所有
【解析】A、只含有一种元素的纯净物属于单质,只含有一种元素的物质不一定是单质,例如氧气和臭氧混合在一起属于混合物,故错误;B、置换反应一定有单质生成,但有单质生成的反应不一定是置换反应,例如水电解,故错误;C、元素是具有相同核电荷数(即质子数)的一类原子的总称,因此同种元素核电荷数(即质子数)一定相同,故正确;D、原子核中不一定都含有质子和中子,如氢原子没有中子,故错误;故选:C。
【跟踪练1】下列反应属于置换反应的是( )
A.2CO+O22CO2 B.C+2CuO2Cu+CO2↑
C.2H2O2H2↑+O2↑ D.CaCO3+2HCl═CaCl2+H2O+CO2↑
【答案】B
【解析】置换反应是由一种单质和一种化合物反应,生成另外一种单质和一种化合物的反应。A、2CO+O22CO2,该反应符合“多变一”的形式,符合化合反应的特征,属于化合反应,故选项错误。B、C+2CuO2Cu+CO2↑,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,故选项正确。C、2H2O2H2↑+O2↑,该反应符合“一变多”的形式,符合分解反应的特征,属于分解反应,故选项错误。D、CaCO3+2HCl═CaCl2+H2O+CO2↑,该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应,故选项错误。故选:B。
【跟踪练2】下列反应中不属于置换反应的是( )
A.氢气与氧化铜反应得到铜和水 B.铁与稀硫酸反应得到氢气
C.一氧化碳和氧化铁反应得到铁 D.铜与硝酸银溶液反应得到银
【答案】C
【解析】置换反应是由一种单质和一种化合物反应,生成另外一种单质和一种化合物的反应。A、氢气与氧化铜反应得到铜和水,该反应属于置换反应B、铁与稀硫酸反应得到氢气,同时生成硫酸亚铁,该反应属于置换反应;C、一氧化碳和氧化铁反应得到铁和二氧化碳,该反应的反应物均为化合物,不属于置换反应;D、铜与硝酸银溶液反应生成银和硝酸铜溶液,该反应属于置换反应;故选:C。
考点三: 金属活动性顺序及其应用
【精讲1】下列金属活动性最强的是( )
A.铝 B.镁 C.铁 D.铜
【答案】B
【解析】常见金属活动性顺序为K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au;在金属活动性顺序中,金属的位置越靠前,金属的活动性就越强,选项提供的四种金属中镁的位置最靠前,故四种金属中金属活动性最强的是镁。故选:B。
【精讲2】把X、Y、Z三种金属分别放入稀盐酸中,X逐渐消失并有气泡产生,Y、Z不反应;取Y放入Z(NO3)2溶液中仍不反应。则X、Y、Z三种金属的活动性由强到弱的顺序是( )
A.X>Y>Z B.Y>Z>X C.Y>X>Z D.X>Z>Y
【答案】D
【解析】在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此来分析问题。把X、Y、Z三种金属分别放入稀盐酸中,X逐渐消失并有气泡产生,Y、Z不反应,说明X的金属活动性强于Y、Z,而把Y放入到Z(NO3)2溶液中仍不反应,说明Z的金属活动性强于Y,则X、Y、Z三种金属的活动性由强到弱的顺序为X>Z>Y。故选:D。
【精讲3】要证明Fe的活动性比Cu强,选用下列各组试剂进行实验时,不能验证此结论的是( )
A.Cu、FeCl2溶液 B.Fe、Cu、稀盐酸
C.Fe、Cu、ZnSO4溶液 D.Fe、CuCl2溶液
【答案】C
【解析】A、铜不会与氯化亚铁反应,说明铁比铜活泼,故正确;B、铁会与盐酸反应,铜不会,说明铁比铜活泼,故正确;C、铁、铜都不会与硫酸锌反应,不能验证,故C错误;D、铁会与氯化铜反应,铁比铜活泼,可以验证,故正确。故选:C。
【精讲4】为验证铁、铜、银的金属活动性顺序,某同学设计了以下四组实验。下列说法错误的是( )
A.通过实验①、②,能验证金属活动性:Fe>Cu
B.通过实验①、②、③,能验证金属活动性:Fe>Cu>Ag
C.实验④中X为Cu,Y为FeSO4,能验证金属活动性:Fe>Cu
D.实验④中X为Cu,Y为AgNO3,能验证金属活动性:Cu>Ag
【答案】B
【解析】A、①中产生气泡,是因为铁和稀硫酸反应生成了氢气,说明铁排在氢前面,②中铜与硫酸不反应,说明铜排在氢后面,能验证金属活动性:Fe>Cu,故正确;B、①中产生气泡,是因为铁和稀硫酸反应生成了氢气,说明铁排在氢前面,②中铜与硫酸不反应,说明铜排在氢后面,能验证金属活动性:Fe>Cu,③中铁表面析出银白色固体,是因为铁和硝酸银反应生成了银,说明铁比银活泼,不能比较铜和银的活泼性,故错误;C、若X是铜,则Y是硫酸亚铁,是因为铜不能和硫酸亚铁反应,说明铁比铜活泼,故正确;D、若X是铜,则Y是硝酸银,铜表面析出银白色固体,是因为铜和硝酸银反应生成了银,说明铜比银活泼,故正确。故选:B。
【精讲5】向硝酸铜和硝酸银的混合溶液中加入一定量的锌粉,充分反应后过滤,得到滤渣和滤液,滤液呈蓝色。下列说法正确的是( )
A.滤渣中一定有Ag和Cu
B.向滤渣中滴加稀盐酸,一定有气泡产生
C.滤液中一定有Cu2+、Zn2+
D.向滤液中滴加稀盐酸,一定有沉淀生成
【答案】C
【解析】向硝酸铜和硝酸银的混合溶液中加入一定量的锌粉,锌先和硝酸银反应生成硝酸锌和银,后和硝酸铜反应生成硝酸锌和铜,充分反应后过滤,得到滤渣和滤液,滤液呈蓝色,说明硝酸铜没有或部分反应。A、滤渣中一定含有银,不一定含有铜,该选项不正确。B、滤渣中不含有锌,加入稀盐酸,不产生气泡,该选项不正确。C、滤液中一定有Cu2+、Zn2+,该选项正确。D、向滤液中滴加稀盐酸,不一定有沉淀生成,是因为不知道硝酸银是否完全反应,该选项不正确。故选:C。
【跟踪练1】下列事实不能用金属活动性解释的是( )
A.铝制品比铁制品耐腐蚀
B.用硫酸铜溶液和铁制取铜
C.用硫酸铜溶液、铁、银验证铁、铜、银金属活动性
D.金属铜不能与稀硫酸反应
【答案】A
【解析】A、铝制品比铁制品耐腐蚀,是因为铝在空气中能与氧气反应,其表面生成一层致密的氧化铝薄膜,阻止内部的铝进一步被氧化,因此铝制品抗腐蚀性强,不能用金属活动性解释,故选项正确。B、用硫酸铜溶液和铁制取铜,是因为铁能与硫酸铜溶液发生置换反应,能用金属活动性解释,故选项错误。C、用硫酸铜溶液、铁、银验证铁、铜、银金属活动性,是因为铁能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,银不能与硫酸铜溶液反应,能用金属活动性解释,故选项错误。D、金属铜不能与稀硫酸反应,是因为在金属活动性顺序中,铜的位置排在氢的后面,能用金属活动性解释,故选项错误。故选:A。
【跟踪练2】可通过金属与稀盐酸反应直接得到的物质是( )
A.氯化锌 B.氯化银 C.氯化铜 D.氯化铁
【答案】A
【解析】A、在金属活动性顺序中,锌排在氢前面,锌和盐酸反应生成氯化锌和氢气,故选项正确。B、在金属活动性顺序中,银排在氢后面,银和盐酸不能发生反应,不能生成氯化银,故选项错误。C、在金属活动性顺序中,铜排在氢后面,铜和盐酸不能发生反应,不能生成氯化铜,故选项错误。D、在金属活动性顺序中,铁排在氢前面,能和盐酸反应生成氯化亚铁和氢气,不能生成氯化铁,故选项错误。故选:A。
【跟踪练3】为探究Zn、Fe、Cu三种金属的活动性顺序,以下四组实验方案中可行的是( )
A.将Zn分别加入FeCl2、CuCl2溶液中
B.将Zn、Fe分别加入CuCl2溶液中
C.将Zn、Fe分别加入稀盐酸中
D.将Fe分别加入ZnCl2和CuCl2溶液中
【答案】D
【解析】A、将Zn分别加入FeCl2、CuCl2溶液中,锌能置换出铁和铜,说明锌的活动性强于铁和铜,但无法确定铁和铜的活动性强弱,故选项错误。B、将Zn、Fe分别加入CuCl2溶液中,锌和铁都能置换出铜,说明锌和铁的活动性都强于铜,但无法确定锌和铁的活动性强弱,故选项错误。C、将Zn、Fe分别加入稀盐酸中,根据产生氢气的速率快慢可以比较锌、铁的活动性强弱,但无法确定与铜的活动性强弱,故选项错误。D、将Fe分别加入ZnCl2和CuCl2溶液中,铁与ZnCl2溶液不反应,说明锌的活动性强于铁;铁与CuSO4溶液反应置换出铜,说明铁的活动性强于铜,由此可得出三种金属活动性锌>铁>铜,故选项正确。故答案为:D。
【跟踪练4】向一定量的硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉质量关系如图,下列说法正确的是( )
A.a点溶液中的物质2种
B.b点得到的固体是Cu
C.c点溶液中只有Zn(NO3)2
D.d点得到的固体有2种
【答案】C
【解析】A、锌的金属活动性比银、铜强,向一定量的硝酸银和硝酸铜的混合溶液中加入锌粉,锌先与AgNO3反应生成硝酸锌和银,AgNO3反应完,锌才能与Cu(NO3)2反应生成硝酸锌和铜,a点发生的是锌与硝酸银的反应,硝酸银有剩余,a点溶液中的溶质有硝酸银、硝酸铜、硝酸锌3种,故选项说法错误。B、b点,锌和硝酸银恰好完全反应,则b点得到的固体是银,故选项说法错误。C、c点,锌与硝酸铜恰好完全反应,c点溶液中只有Zn(NO3)2,故选项说法正确。D、d点,锌过量,得到的固体有银、铜、锌3种,故选项说法错误。故选:C。
镁、铝常温下能与氧气反应
纯氧中,铁在点燃的条件下能与氧气反应
金属能与氧气反应
铜在加热的条件下能与氧气反应
金在高温时也不能与氧气反应
Mg+2HCl= MgCl2+H2↑
Zn+2HCl= ZnCl2+H2↑
Fe+2HCl = FeCl2+H2↑
镁、锌、铁能与稀盐酸、
稀硫酸反应生成氢气
金属能与酸反应
金属的化学性质
定义
置换反应
A+BC→B+AC
表达式
规律
金属能与盐溶液反应
金属活动性顺序
应用
点燃
点燃
知识梳理:
一、金属能与氧气反应
1、镁与氧气的反应:常温下所看到的镁条呈黑色,用砂纸打磨后呈银白色。镁条在空气中点燃后能剧烈燃烧,产生耀眼的白光,形成白烟,放出大量的热:2Mg+O2 ==== 2MgO;
2、铝与氧气的反应:铝在空气容易与氧气反应形成致密的氧化铝薄膜,能阻止铝的进一步氧化,故其抗腐蚀性能很好:4Al+3O2=====2Al2O3;
3、铁与氧气的反应:常温下,干燥的空气中铁很难与氧气反应,在纯氧中,铁丝能够被点燃,剧烈燃烧,火星四射,生成黑色固体,放出大量的热:3Fe+2O2===========Fe3O4;
△
4、铜与氧气的反应:在加热的情况下,铜能与氧气反应,生成黑色的物质(氧化铜);即2Cu+O2======2CuO。即使在纯氧中,铜也不能被点燃。
5、金即使在高温时也不与氧气反应。
二、金属能与稀盐酸、稀硫酸反应
酸金 属 现象 反应的化学方程式
盐酸/稀硫酸 盐酸 稀硫酸
镁 反应非常剧烈,产生大量气泡 Mg+2HCl= MgCl2+H2↑ Mg+H2SO4 = MgSO4+H2↑
锌 反应比较剧烈,产生大量气泡 Zn+2HCl= ZnCl2+H2↑ Zn+H2SO4 = ZnSO4+H2↑
铁 反应缓慢,有气泡产生,溶液由无色逐渐变为淡绿色 Fe+2HCl = FeCl2+H2↑ Fe+H2SO4= FeSO4+H2↑
铜 不反应
三、金属能与金属化合物溶液(即盐溶液)反应:
金属+盐==新金属+新盐 (条件:活动性:参加反应的金属>化合物中金属元素)
(1)铁丝浸入硫酸铜溶液中:Fe + CuSO4 == Cu + FeSO4
现象:铁的表面覆盖一层红色的物质,溶液有蓝色变成浅绿色
(2)铝丝浸入硫酸铜溶液中:2Al + 3CuSO4 == Al2(SO4)3 + 3Cu
现象:铝丝表面有红色物质出现,溶液由蓝色变为无色
(3)铜丝浸入硝酸银溶液中:Cu + 2AgNO3 == Cu(NO3)2 + 2Ag
现象:铜丝表面有银白色物质出现,溶液由无色变为蓝色
【知识点睛】
铝比铁更不容易被腐蚀是因为铝在空气容易与氧气反应形成致密的氧化铝薄膜,能阻止铝的进一步氧化;
2、越容易与氧气反应的金属其活动性越强;
3、在其他条件完全相同时,与酸反应越剧烈的金属活动性越强;
【命题方向】
该考点的命题方向主要是通过创设相关实验、问题情景或图表信息等,来考查学生对金属的化学性质的理解或掌握情况,以及对常见金属的特性及其应用、金属的物理性质及用途、合金与合金的性质、金属活动性顺序及其应用、实验现象及结论(包括反应化学方程式)等相关问题的分析、推断、表达的能力和对知识的迁移能力等;并且,经常将其与常见金属的特性及其应用、金属的物理性质及用途、金属活动性顺序及其应用、化学方程式的书写等关联起来,进行综合考查。
【解题方法点拨】
熟记金属的化学性质及各个反应的原理和现象。
知识梳理:
置换反应(四大基本反应类型之一)
1、定义:由一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应;
2、表达式:A+BC→B+AC
3、特点:反应物是单质与化合物,生成物也是单质与化合物。可以简记为:“单化变单化”。
【知识点睛】
1、有铁参与的置换反应生成的是+2价的亚铁;
2、置换反应中的置换关系是指组成化合物的某种元素被组成单质的元素所替代.因此,在判定置换反应时,一定要抓住它的特点,结合它的概念和通式,以及单质和化合物的判定方法来细心地判定。
【命题方向】
该考点的命题方向主要是通过创设相关问题情景或图表信息等,来考查学生对置换反应及其应用的理解和掌握情况。特别是,对“碳、氢气和金属等物质的化学性质,置换反应的判定及其与其它反应类型的判别,利用分解反应的原理来制取氢气和某些金属或鉴别和推断某些物质”等相关问题的考查,以及对有关知识的迁移能力的考查,是近几年中考命题的热点。
【解题方法点拨】
首先,要理解和熟记置换反应及其应用,以及与之相关的知识.然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可。
知识梳理:
常见金属的活动性顺序:
2、应用:
(1)在金属活动性顺序中,金属的位置越靠前;
注意点:金属的活动性就越强参加反应时,现象就越明显、越剧烈.
(2)排在氢前面的金属,能置换出酸中的氢,而排在氢后面的金属不能置换出酸中的氢;
注意点:①金属必须是排在金属活动性顺序中(H)前面的金属;
②酸应是盐酸、稀硫酸(即不具有强氧化性的酸),不包括浓硫酸和硝酸;
③单质铁与酸发生置换反应时生成亚铁盐;
④K、Ca、Na除与酸反应外,还能与水在常温下发生置换反应(如2Na+2H2O=2NaOH+H2↑),其余金属则不能;
(3)排在金属活动性顺序中前面的金属一般能把排在后面的金属从其盐溶液里置换出来。
注意点:①在金属活动性顺序中只要排在前面的金属就能把排在后面的金属从其盐溶液中置换出来,而与H的位置无关.但K、Ca、Na等金属例外;
②铁与盐溶液发生置换反应时,生成二价亚铁盐;
③用同种金属置换不同的盐溶液,盐中金属排在金属活动性顺序中较后的金属首先被置换出来.用不同的金属置换同种盐溶液,盐中金属先被排在金属活动性顺序中较前的金属置换出来。另外,若有一种金属和多种混合盐溶液反应,最先反应的是最不活泼的那个金属的盐溶液。
【知识点睛】
利用金属与酸或盐溶液之间的置换反应是否发生,通过具体的实验及其现象的分析,反过来可以反推金属的活动性顺序。
1.利用金属与酸能否发生置换反应,来反推金属的活动性顺序。例如,把铁和铜分别放在稀盐酸中时,铁的表面上有气泡冒出,这说明铁位居金属活动性顺序中氢的前面;而铜的表面无明显的现象,这说明铜位居金属活动性顺序中氢的后面;由此可推得铁活泼性比铜的要强。
2.利用金属与盐溶液能否发生置换反应,来反推金属的活动性顺序。例如,把铁钉放在硫酸铜溶液中,过一会儿,发现铁钉表面上出现了一层红色物质(即铜);由此可推得铁活泼性比铜的要强。
【命题方向】
该考点的命题方向主要是通过创设相关实验、问题情景或图表信息等,来考查学生对金属活动性顺序及其应用的理解或掌握情况;以及阅读、分析、推断、表达的能力和对知识的迁移能力等.并且,经常将其与“金属的性质及用途、常见金属的特性及其应用、合金与合金的性质、实验现象和结论(包括反应化学方程式)、其它的反应类型”等相关问题关联起来,进行综合考查.金属活动性顺序及其应用是历年来中考命题的热点;命题方式是根据金属活动性顺序及其应用来分析、推断、选择或解答有关金属的活动性强弱、某些置换反应是否发生、实验现象、实验结论(包括反应化学方程式)、金属的制备、金属的应用、生活中有关金属的实际问题,或者是反过来考查,或者是对所给的有关金属活动性顺序及其应用的表达进行判断,等等。
【解题方法点拨】
解答这类题目时,首先,要熟记和理解金属活动性顺序及其应用,以及与之相关的知识等;然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,细致地阅读、分析题意等,联系着生活实际,细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
