【精讲】人教版化学九年级下册 8.3 金属资源的利用与保护 同步学案
文档属性
| 名称 | 【精讲】人教版化学九年级下册 8.3 金属资源的利用与保护 同步学案 |
|
|
| 格式 | doc | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-22 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
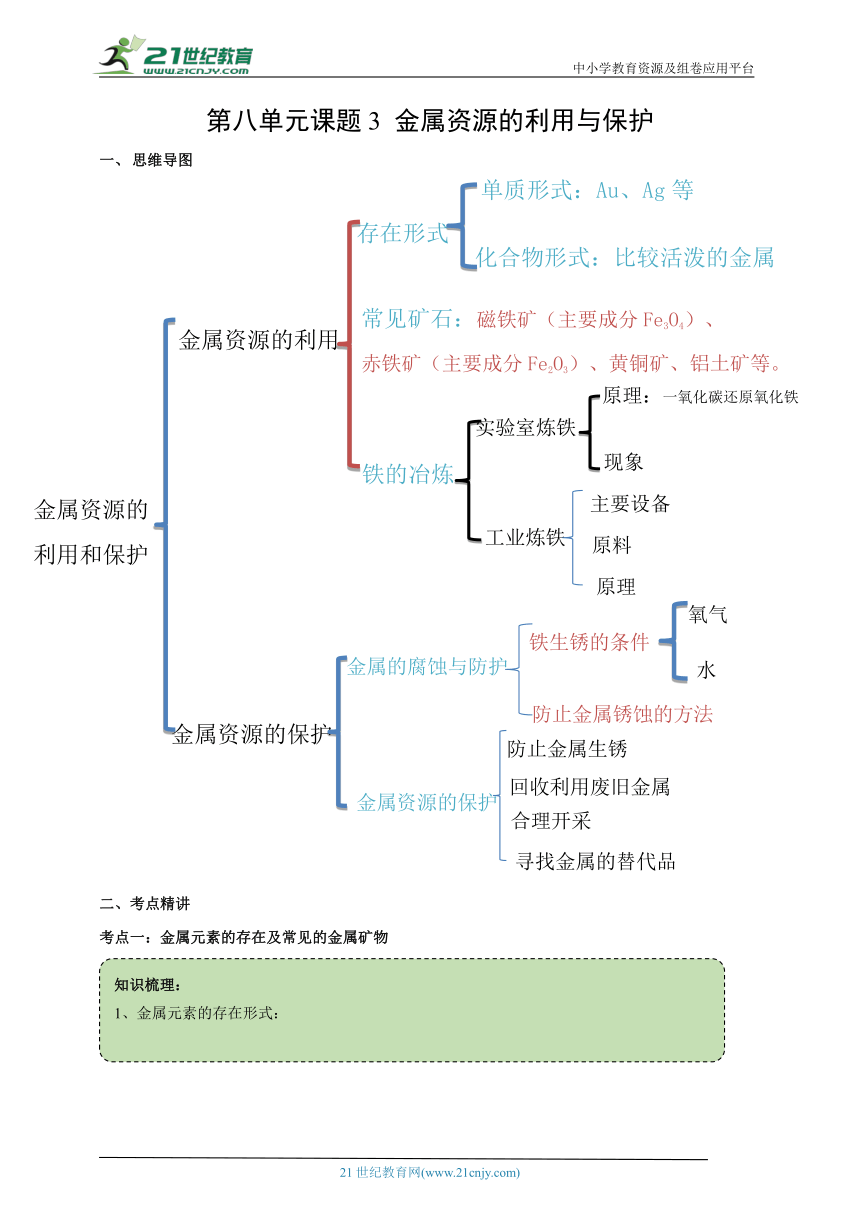
第八单元课题3 金属资源的利用与保护
思维导图
二、考点精讲
考点一:金属元素的存在及常见的金属矿物
【精讲1】常见的金属矿石赤铁矿的主要成分是( )
A.Fe2O3 B.Fe3O4 C.FeCO3 D.Al2O3
【答案】A
【解析】赤铁矿的主要成分是氧化铁,其化学式为:Fe2O3。故选:A。
【精讲2】下列金属中一定以化合物形态存在于矿物之中的是( )
A.金 B.银 C.铂 D.铁
【答案】D
【解析】A、金的化学性质稳定,可以以单质的形态存在,故A不选;B、银的化学性质很稳定,可以以单质的形态存在,故B不选;C、铂的化学性质很稳定,可以以单质的形态存在,故C不选;D、铁的化学性质比较活泼,容易与空气中的氧气反应,以化合物的形态存在,故D选;故选:D
【跟踪练1】大自然向人类提供了丰富的金属矿物资源,在以下四种矿石中,可用于炼铁的是( )
A.赤铁矿(主要成分是Fe2O3) B.炉甘石(主要成分是ZnCO3)
C.铝土矿(主要成分是A12O3) D.赤铜矿(主要成分是Cu2O)
【答案】A
【解析】炼铁是将铁矿石中的铁氧化物还原成金属铁,故矿石中必须含有铁元素;A、赤铁矿(主要成分是Fe2O3)中含有铁元素,可用于炼铁,符合题意;B、 炉甘石(主要成分是ZnCO3)中不含有铁元素,不可用于炼铁,不符合题意;C、 铝土矿(主要成分是A12O3) 中不含有铁元素,不可用于炼铁,不符合题意;D、 赤铜矿(主要成分是Cu2O)中不含有铁元素,不可用于炼铁,不符合题意;故选A。
【跟踪练2】多角度认识物质能帮助我们更全面地了解物质世界。以金属为例回答下列问题:
(1)认识金属元素的存在
①在自然界中,大多数金属以化合物存在,而金、铂等极少数金属因为化学性质 (填“活泼”或“不活泼”)却能以单质存在。
②常见铁矿石有:黄铁矿(主要成分 FeS2)、磁铁矿(主要成分 Fe3O4)等。这两种铁矿石的主要成分含铁元素质量分数较大的是 。
(2)认识金属的性质 用粗木棍在涂有蜡的锌板上写“南”、平”两个字,露出下面的锌板。向“南”字上滴加稀盐酸,向“平”字上滴加 CuSO4 溶液。
①“南”字上的现象是 。
②“平”字上有红色物质析出,用化学方程式解释: 。
(3)认识金属的制备
工业上,金属钨(W)可由氢气和三氧化钨(WO3)在高温下发生置换反应制得。 反应中化合价升高的元素是 。
(4)认识金属的用途烤制食物时常用到铝箔,主要利用了金属铝的 (填性质)。
【答案】(1)①不活泼;②Fe3O4;(2)①冒气泡;②Zn+CuSO4=Cu+ZnSO4;
(3)氢元素;(4)延展性
【解析】(1)①在自然界中,极少数化学性质不活泼的金属如金、铂等以单质存在;
②由于一个硫原子的质量相当于两个氧原子的质量,故FeS2中铁原子和硫原子的个数比相当于为:Fe:O═1:4,Fe3O4中铁原子和氧原子的个数比为:Fe:O═3:4,故铁元素的质量分数高的是Fe3O4;
(2)①锌与稀盐酸反应产生氢气;与硫酸铜反应生成红色铜和硫酸锌;
(3)三氧化钨与氢气在高温的条件下反应生成金属钨和水,故反应方程式为:WO3+3H2 3H2O+W,该反应前后氢元素的化合价由0变为+1,升高了;
(4)金属铝能压成铝箔,说明金属铝具有优良的延展性。
考点二: 铁的冶炼
SHAPE \* MERGEFORMAT
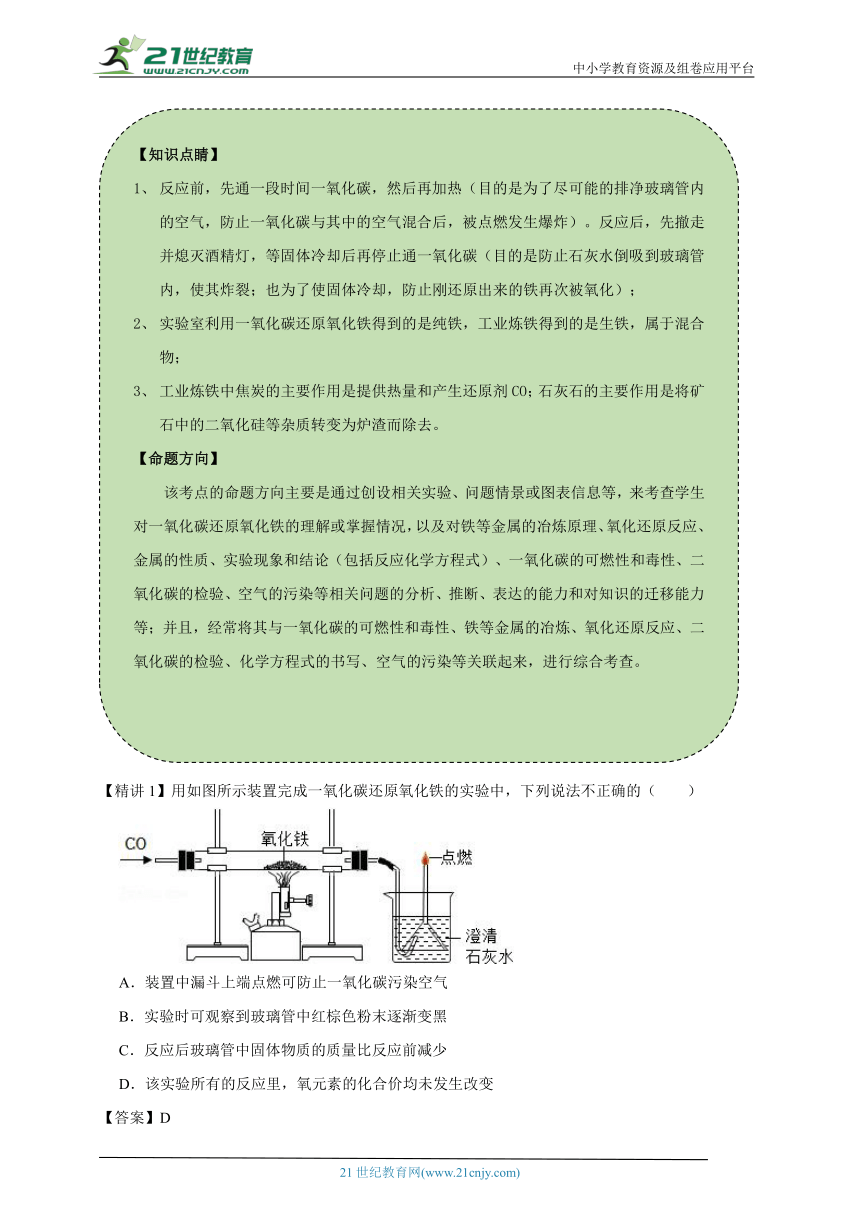
【精讲1】用如图所示装置完成一氧化碳还原氧化铁的实验中,下列说法不正确的( )
A.装置中漏斗上端点燃可防止一氧化碳污染空气
B.实验时可观察到玻璃管中红棕色粉末逐渐变黑
C.反应后玻璃管中固体物质的质量比反应前减少
D.该实验所有的反应里,氧元素的化合价均未发生改变
【答案】D
【解析】A、一氧化碳和氧气在点燃的条件下生成二氧化碳,装置中漏斗上端点燃可防止一氧化碳污染空气,故A正确;B、实验时可观察到玻璃管中红棕色粉末逐渐变黑,故B正确;C、反应后玻璃管中固体物质的质量比反应前减少,故C正确;D、该实验所有的反应里,一氧化碳和氧气在点燃的条件下生成二氧化碳,氧气中的氧元素的化合价为0,生成的二氧化碳中,氧元素为﹣2价,化合价降低,故D错误。故选:D。
【精讲2】早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用一氧化碳和氧化铁的反应。
某中学化学兴趣小组利用如图装置进行实验探究,请按要求填空:
(1)除CO外,还有哪些物质可以还原Fe2O3 (请写一种物质的化学式)。
(2)实验中可观察到的现象是 。
(3)右边导气管口放置点燃的酒精灯的作用是 。
(4)实验开始时要先通入CO的目的是 。
【答案】(1)C或H2;(2)红棕色粉末逐渐变黑;(3)点燃尾气,防止污染空气;
(4)排尽装置中的空气,防止加热时发生爆炸。
【解析】(1)除CO外,碳(C)、氢气(H2)也具有还原性,也可以还原Fe2O3。
(2)一氧化碳具有还原性,高温下能与氧化铁反应生成铁和二氧化碳,实验进行一段时间后,玻璃管中出现的现象是红棕色粉末逐渐变黑。
(3)一氧化碳有毒,直接排放到空气中会污染环境,在装置图末端的导管口放一盏燃着的酒精灯,是为了点燃尾气,防止污染空气。
(4)实验开始先通入一氧化碳,再点燃酒精喷灯加热玻璃管中的氧化铁,目的是排尽装置中的空气,防止加热时发生爆炸。
【跟踪练1】把赤铁矿、焦炭和石灰石一起加入高炉中进行冶炼,下列说法正确的是( )
A.高炉得到的产物是纯铁
B.赤铁矿的主要成分是Fe3O4
C.焦炭既可以提供热量又可以提供一氧化碳
D.石灰石用于除去尾气
【答案】C
【解析】A、把铁矿石、焦炭和石灰石一起加入高炉中进行冶炼,得到的产物是生铁,不是纯铁,故选项说法错误。B、赤铁矿的主要成分是Fe2O3,故选项说法错误。C、工业炼铁中利用了焦炭的可燃性,提供热量;又利用其还原性,与二氧化碳反应生成一氧化碳气体,故选项说法正确。D、高炉炼铁时用的原料中石灰石的作用是将矿石中的二氧化硅等杂质转变为炉渣而除去,故选项说法错误。故选:C。
【跟踪练2】实验室模拟炼铁的实验装置如图所示。
试回答下列问题:
(1)写出有标号仪器的名称:a ,b 。
(2)实验中看到的实验现象为:玻璃管中的粉末 ,试管里的澄清石灰水 。
(3)玻璃管中反应的化学方程式为 。
(4)加热氧化铁之前,先通一会儿一氧化碳的作用是 。
(5)该实验设计装置C的目的是 。
【答案】(1)铁架台;导管(2)由红色逐渐变黑;变浑浊
(3)Fe2O3+3CO2Fe+3CO2(4)排尽玻璃管中的空气,防止发生爆炸
(5)把一氧化碳转化成二氧化碳,防止污染环境
【解析】(1)题中标号仪器的名称为a为铁架台、b为导管。
(2)一氧化碳具有还原性,高温条件下能与氧化铁反应生成铁和二氧化碳,二氧化碳能使澄清石灰水变浑浊,实验中看到的实验现象为:玻璃管中的粉末由黑色变红色,试管里的澄淸石灰水变浑浊。
(3)玻璃管中反应的化学方程式为Fe2O3+3CO2Fe+3CO2。
(4)CO具有可燃性,与玻璃管中的空气混合受热会发生爆炸,因此应先通CO排尽玻璃管中的空气,然后再点燃酒精灯加热氧化铁。加热氧化铁之前,先通一会儿一氧化碳的作用是排进装置内的空气防止发生爆炸。
(5)一氧化碳有毒,直接排放到空气中会污染环境,该实验设计装置C的目的是处理尾气,防止污染空气。
考点三: 铁生锈的条件
【精讲1】下列说法正确的是( )
A.铁锈的主要成分是Fe3O4 B.生了锈的铁应随手丢弃
C.铁在干燥空气中容易生锈 D.赤铁矿可用于冶炼钢铁
【答案】D
【解析】A、铁锈的主要成分是Fe2O3,故选项说法错误;B、生锈的铁可以回收利用,既能节约资源,又能保护环境,故选项说法错误;C、铁在与氧气、水同时存在时会发生锈蚀,所以铁在干燥空气中不容易生锈,故选项说法错误;D、赤铁矿的主要成分是氧化铁,所以赤铁矿可用于冶炼钢铁,故选项说法正确。故选D。
【精讲2】为了减缓铁制品的锈蚀,下列做法错误的是( )
A.在车船的表面喷涂油漆 B.将使用后的菜刀用布擦干
C.洗净铁制品表面的油膜 D.在铁制品表面镀上一层锌
【答案】C
【解析】铁与水、氧气充分接触时容易生锈,使铁制品与氧气和水隔绝可以防止生锈。A、在车船的表面喷涂油漆,能使铁制品与氧气和水隔绝,可以防锈,故选项说法正确。B、将使用后的菜刀用布擦干,使菜刀不易与水接触,可以防锈,故选项说法正确C、油膜能使铁制品与氧气和水隔绝,可以防锈;用洗涤剂把铁制品表面的油膜洗净,铁制品与水和氧气接触,会加快生锈,故选项说法错误D、在铁制品表面镀上一层锌,能使铁制品与氧气和水隔绝,可以防锈,故选项说法正确.故选C。
【跟踪练1】下列关于金属的说法正确的是( )
A.钨的合金的熔点高,可用于制造保险丝
B.铝制品抗腐蚀能力比铁制品强
C.用 FeSO4 溶液、Cu 和 Ag 三种物质可以验证 Fe、Cu、Ag 三种金属的活动性强弱 D.铁制品生锈产生的铁锈是一种疏松多孔的物质,它的主要成分是 Fe3O4
【答案】B
【解析】A.钨的合金的熔点低,可用于制造保险丝,故错误;B.铝和空气中的氧气反应会生成致密的氧化铝薄膜,所以铝制品抗腐蚀能力比铁制品强,故正确;C.铁比铜活泼,铜比银活泼,把铜和银分别伸入硫酸亚铁溶液中时,都无明显现象,说明铁比铜和银活泼,但是无法确定银和铜的活泼性,故错误;D.铁制品生锈产生的铁锈是一种疏松多孔的物质,它的主要成分是Fe2O3,故错误;故选:B。
【跟踪练2】为预防金属制品锈蚀,下列措施或做法不当的是( )
A.用钢丝球清除铝锅内的氧化层 B.在铁制门窗表面喷涂油漆
C.在铁制水管表面镀一层锌 D.将使用后的菜刀洗净擦干
【答案】A
【解析】A、铝制品表面有一层氧化膜,对铝锅起保护作用,阻止铝被进一步氧化,所以擦去表面的氧化层是错误的做法,故A符合题意;B、在在铁制门窗表面喷涂油漆,使铁与氧气和水隔绝,有利于防锈,故B不符合题意;C、在铁制水管表面镀一层锌,使铁与氧气和水隔绝,有利于防锈,故D不符合题意;D、使用后的菜刀洗净擦干有利于防锈,故D不符合题意。故应选A。
考点四: 含杂质物质的计算
【精讲1】在某次家庭作业中,一位同学的计算题书写过程如下,请你作为小组长,组织组内同学仔细观察,帮他纠正错误。
工业上用含氧化铁80%的赤铁矿石炼铁,欲生产含铁112t的生铁,请计算所需赤铁矿石的质量。
解:设生产112t铁,所需氧化铁的质量为x。
FeO+COFe+CO2.........第1步
72 56
x 112........第2步
x=144..........第3步
144t×80%=115.2t.............第4步
答:生产112t铁,所需赤铁矿石的质量为115.2t
【发现问题】上述作业中有多个步骤书写错误。
【交流讨论】上述作业中有一个错误步骤 ,其错误原因是 。
【纠正错误】请你将该题正确的解答过程重新完整地写在答题卡上。
【答案】
【交流讨论】1(合理即可);氧化铁的化学式书写错误,方程式没有配平(合理即可);
【纠正错误】设生产112t铁,所需氧化铁的质量为x.
Fe2O3+3CO2Fe+3CO2
160 112
x 112t
解得:x=160t
所需赤铁矿石的质量是:=200t
答:需要赤铁矿石200t.
【解析】【交流讨论】上述作业中有一个错误步骤1等,其错误原因是:氧化铁的化学式书写错误,方程式没有配平等。
【纠正错误】
设生产112t铁,所需氧化铁的质量为x。
Fe2O3+3CO2Fe+3CO2
160 112
x 112t
解得:x=160t
所需赤铁矿石的质量是:=200t
答:需要赤铁矿石200t.
【跟踪练1】根据Fe3O4+4CO3Fe+4CO2反应原理,工业上可用来冶炼铁。现用100t含四氧化三铁为46.4%的某铁矿石冶炼金属铁。请完成下列问题,写出必要的计算过程。
(1)该铁矿石中含四氧化三铁质量是多少?
(2)理论上可炼出含铁96%的生铁的质量是多少?
【答案】(1)46.4t(2)35t
【解析】(1)铁矿石中含四氧化三铁质量是100t×46.4%=46.4t。
(2)设理论上可炼出含铁96%的生铁的质量是x。
Fe3O4+4CO3Fe+4CO2
232 168
46.4t 96%x
x=35t
答:(1)铁矿石中含四氧化三铁质量是46.4t
(2)理论上可炼出含铁96%的生铁的质量是35t。
考点五: 金属资源的保护
【精讲1】金属资源是不可再生的资源,保护金属资源是我们刻不容缓的职责。下列有关叙述不正确的是( )
A.大力开采矿物以保障金属材料的供用 B.用特种塑料代替金属制造机器的零部件
C.提高废旧金属的回收利用率 D.在金属制品上刷漆、涂油等防止金属腐蚀
【答案】A
【解析】A、金属资源属于不可再生资源,需要合理、适度开采,故A错误;B、金属资源有限,所以可逐步使用可替代的材料来代替部分金属材料,故B正确;C、金属资源需要合理高效利用,所以可通过回收利用的方式提高金属利用率,故C正确;D、金属与空气的部分成分接触时生锈,可通过隔绝空气的方式防止金属生锈,如刷漆、涂油等方式,故D正确;故选A。
【精讲2】随着新能源汽车的推广应用,电池生产和消费迅猛增长,为了“变废为宝,减少污染”,废旧电池必须回收,回收的主要目的是( )
A.进行重新加工和再生
B.回收其中的金属资源
C.防止电池中的重金属污染环境
D.充电电池回收翻新后又可以高价卖出
【答案】C
【解析】废旧电池中的铅、镉等元素,则被定为致癌物质;汞中毒,会患中枢神经疾病。电池腐烂后,其中的汞、铅、镉等重金属溶出会污染地下水和土壤,即造成地下水和土壤的污染,威胁人体健康。故废旧电池必须回收,回收的主要目的是防止电池中的重金属污染环境。故选:C。
【跟踪练1】“绿箱子环保计划﹣﹣废弃手机及配件同收联合行动”已在全国40个重点城市中开展了近两年。下列有关说法不正确的是( )
A.回收废电池可以节约金属资源
B.“绿箱子”上的“”是回收标志
C.回收废电池可以减少环境污染
D.回收废弃手机中的金属材料没有任何价值
【答案】D
【解析】A、可以节约金属资源的说法正确,因为回收的金属可以再次进行利用。故对;B、此标志是循环再使用的回收标志;故对;C、手机中的一些重金属废弃后会污染土壤,回收后会减少对环境的污染,故对;D、回收利用可节约资源减小由于冶炼这些金属而消耗的能源,同时也可减小对环境的污染。故错。故选:D。
【跟踪练2】中国筹划高铁“大棋局”,国人有望乘高铁2天到达美国,请回答下列问题:
(1)为了节约能源,高铁的车体材料最好选用的是 。
A.耐腐蚀的不锈钢 B.硬度大、密度小的铝合金 C.熔点高、可塑性好的金属钛
(2)若高铁列车使用了氢氧燃料电池,则高铁列车在整个行驶过程中的能量转化是 。
(3)在高铁轨道铺设过程中用到了大量的铁合金。工业上可以用黄铁矿(主要成分为FeS2,其中硫元素的化合价为﹣1价)来炼铁,其中发生的一个反应:黄铁矿和氧气在高温下反应生成氧化铁和一种空气污染物,请写出该反应的化学方程式 ,该反应中铁元素的化合价变化为 。
(4)为了保护金属资源,我们可以采取的措施有 (答一条)。
【答案】(1)AB;(2)化学能转化为电能再转化为机械能;
(3)4FeS2+11O22Fe2O3+8SO2;由+2价变为+3价;
(4)防止金属的腐蚀或废旧金属回收利用或有计划合理开采金属资源或寻找金属替代品(合理即可)。
【解析】(1)高铁的车体材料要求强度大、密度小、耐腐蚀,因此选用不锈钢、铝合金,而钛合金的价格比较昂贵,故选:AB;
(2)氢氧燃料电池提供的是化学能,因此高铁列车在行驶过程中的能量来源是化学能转化为电能再转化为机械能;
(3)黄铁矿和氧气在高温下反应生成氧化铁和一种空气污染物,根据质量守恒定律,该空气污染物是二氧化硫,该反应的化学方程式4FeS2+11O22Fe2O3+8SO2;化合物中各元素的化合价的代数和为0可知,该反应中铁元素的化合价变化为由+2价变为+3价;
(4)防止金属的腐蚀、废旧金属回收利用、有计划合理开采金属资源、寻找金属替代品都可以保护金属资源。
单质形式:Au、Ag等
存在形式
化合物形式:比较活泼的金属
金属资源的利用
常见矿石:磁铁矿(主要成分Fe3O4)、
赤铁矿(主要成分Fe2O3)、黄铜矿、铝土矿等。
原理:一氧化碳还原氧化铁
实验室炼铁
现象
铁的冶炼
金属资源的
利用和保护
主要设备
工业炼铁
原料
原理
氧气
铁生锈的条件
水
金属的腐蚀与防护
金属资源的保护
防止金属锈蚀的方法
防止金属生锈
金属资源的保护
回收利用废旧金属
合理开采
寻找金属的替代品
知识梳理:
1、金属元素的存在形式:
地球上的金属资源广泛地存在于地壳和浩瀚的海洋中,除少数很不活泼的金属(如金、银等)以单质形式存在外,其余的都以化合物的形式存在。
2、常见的矿石
(1)铁矿石有赤铁矿(主要成分是Fe2O3)、磁铁矿(主要成分是Fe3O4)、菱铁矿(主要成分是FeCO3)和黄铁矿(主要成分是FeS2)等;
(2)铜矿石有孔雀石[主要成分是Cu2(OH)2CO3]、赤铜矿(主要成分是Cu2O)、黄铜矿(主要成分是CuFeS2)和辉铜矿(主要成分是Cu2S)等;
(3)铝矿石有铝土矿(主要成分是Al2O3)、明矾(KAlSO4 12H2O)或水铝石(主要成分是Al2O3 H2O)等。
【知识点睛】
地壳中含量最多的金属元素是铝,其次是铁;
【命题方向】
该考点的命题方向主要是通过设置问题情景,让学生阅读、思考后,根据所学的金属元素的存在及常见的金属矿物,以及与其相关的金属活动性顺序及其应用、物质的分类和元素组成、常见金属的冶炼、空气的污染、化学式的书写和意义等知识,来分析、解答相关的实际问题。
【解题方法点拨】
熟记和理解金属元素的存在及常见的金属矿物。
高温
知识梳理:
工业炼铁 实验室炼铁(一氧化碳还原氧化铁)
原料 铁矿石、焦炭、石灰石 装置
设备 高炉
原理 在高温条件下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来
主要化学反应 Fe2O3+3CO=====2Fe+3CO2 现象 红色的粉末逐渐变为黑色;澄清石灰水变浑浊
实际应用 在实际生产中,所用的原料或产物一般都含有杂质,在计算用料和产量时,应考虑到杂质问题 注意事项 ①先通CO,后加热;实验完毕,先熄灯,继续通CO至冷却;②尾气处理:烧掉或用塑料袋收集起来,防止未反应的CO污染空气;
【知识点睛】
反应前,先通一段时间一氧化碳,然后再加热(目的是为了尽可能的排净玻璃管内的空气,防止一氧化碳与其中的空气混合后,被点燃发生爆炸)。反应后,先撤走并熄灭酒精灯,等固体冷却后再停止通一氧化碳(目的是防止石灰水倒吸到玻璃管内,使其炸裂;也为了使固体冷却,防止刚还原出来的铁再次被氧化);
实验室利用一氧化碳还原氧化铁得到的是纯铁,工业炼铁得到的是生铁,属于混合物;
工业炼铁中焦炭的主要作用是提供热量和产生还原剂CO;石灰石的主要作用是将矿石中的二氧化硅等杂质转变为炉渣而除去。
【命题方向】
该考点的命题方向主要是通过创设相关实验、问题情景或图表信息等,来考查学生对一氧化碳还原氧化铁的理解或掌握情况,以及对铁等金属的冶炼原理、氧化还原反应、金属的性质、实验现象和结论(包括反应化学方程式)、一氧化碳的可燃性和毒性、二氧化碳的检验、空气的污染等相关问题的分析、推断、表达的能力和对知识的迁移能力等;并且,经常将其与一氧化碳的可燃性和毒性、铁等金属的冶炼、氧化还原反应、二氧化碳的检验、化学方程式的书写、空气的污染等关联起来,进行综合考查。
【解题方法点拨】
熟记和理解一氧化碳还原氧化铁的所有内容,还有,铁等金属的冶炼原理、氧化还原反应的原理、一氧化碳的可燃性和毒性、金属的性质、化学方程式的书写、空气的污染等相关知识;然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,细致地阅读、分析题意等,联系着生活实际,细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可。
知识梳理:
1、铁生锈的条件:
铁与空气中的水蒸气、氧气同时接触,发生了复杂的化学反应,生成了铁锈。即铁生锈的条件是水和氧气。
2、防止铁制品生锈
(1)原理:破坏铁生锈的条件
(2)方法:①保持铁制品表面的洁净和干燥;②在铁表面涂油、刷漆、烧制搪瓷、镀耐磨和耐腐蚀的金属、烤蓝(即表面生成氧化膜);③改变其内部组成,制成耐腐蚀的合金,如不锈钢等。
【知识点睛】
铁锈是普通钢铁制品在潮湿的空气中,先从其表面慢慢生成的一种红褐色的物质,是就是铁和空气中所氧气、水蒸气等起作用,生成的铁的多种氧化物的水合物.铁锈的成分比较复杂,其主要成分是Fe2O3 xH2O,所以铁锈可以说是混合物.铁锈的结构很疏松,不但不能阻碍里层的铁继续与氧气、水等反应,而且因它具有吸附性,还会使铁生锈的速度加快。
【命题方向】
中考重点是考查学生对铁锈的主要成分,以及与其相关的铁的生锈条件及其防护措施、赤铁矿的主要成分、铝耐腐蚀的原因、混合物和纯净物的判别、物质的结构与性质的关系、金属资源的保护等知识的理解和掌握情况,以及运用它们来分析、解答相关的实际问题的能力等.特别是,铁锈的主要成分及其化学式等是历年来中考命题的热点,当然也是中考考查这块知识的重中之重。
【解题方法点拨】
熟记和理解铁的生锈条件及其防护措施。
知识梳理:
含杂质物质的化学反应的有关计算是指在实际生产中,所用的原料或产物一般都含有杂质,在利用化学方程式进行计算用料和产量时,由于化学方程式表示的是纯净物质之间的质量关系,而不表示不纯物质之间的质量关系;故计算时一定考虑到杂质的问题(即不纯物质和纯物质之间的相互转化问题)。
不纯物质的质量与纯物质的质量的相互转化方法及纯度的计算公式是:
例题:用1000t含氧化铁为80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少?
审题:首先要找到有关的反应的化学方程式、已知量(即1000t、80%、96%)、未知量(生铁的质量);然后,要弄清楚不纯物质与纯物质之间的联系(即赤铁矿~氧化铁~铁~生铁);最后,根据化学方程式计算的步骤、格式(或者根据质量守恒定律和化学式的计算技巧),结合着不纯物质和纯物质之间的相互转化方法,细心地进行计算即可。
【知识点睛】
代入化学方程式中计算的量一定是纯净物的质量,若是混合物则要根据公式进行换算。同理,利用化学方程式计算出来的量也是纯净物的质量。
【命题方向】
该考点的命题方向主要是通过创设有关含杂质物质的化学反应的有关计算的问题情景或图表信息等,来考查学生对含杂质物质的化学反应的有关计算的方法、步骤和格式的理解或掌握情况,以及对不纯物质的质量与纯物质的质量的相互转化方法、纯度的计算公式、铁的冶炼原理、一氧化碳还原氧化铁、化学方程式的书写和意义、根据化学方程式的有关计算等相关问题的分析、推断、表达的能力和对知识的迁移能力等;并且,经常将其与这些相关知识等关联起来,进行综合考查。
【解题方法点拨】
解答这类题目时,首先,要熟记和理解有关含杂质物质的化学反应的有关计算的方法、步骤和格式等相关知识;然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,特别是有关化学方程式的书写和意义、不纯物质的质量与纯物质的质量的相互转化方法,以及根据化学方程式计算的方法、步骤和格式等,细致地阅读、分析题意,联系着生产、生活实际,细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可。
知识梳理:
金属资源的保护主要有以下四种措施:
1、减缓或防止金属的腐蚀;
2、回收利用废旧金属,这样不仅可以节约金属资源,而且还可以减少对环境的污染.
3、有计划、合理地开采矿物,严禁不顾国家利益的乱采矿.
4、寻找金属的代用品,例如,现在经常用塑料来代替钢和其它合金制造管道、齿轮和汽车外壳等。
【命题方向】
该考点的命题方向主要是通过设置相关的问题情景,让学生阅读、思考后,根据所学的金属资源的保护措施,以及与其相关的铁的生锈条件及其防护措施、物质的结构与性质的关系、废弃金属对环境污染、金属的回收利用及其重要性等知识,来分析、解答相关的实际问题;并且,经常将其与这些相关知识联系起来,进行综合考查。
【解题方法点拨】
熟记和理解金属资源的保护措施,以及与其相关的铁的生锈条件及其防护措施、物质的结构与性质的关系、废弃金属对环境污染、金属的回收利用及其重要性等知识。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
第八单元课题3 金属资源的利用与保护
思维导图
二、考点精讲
考点一:金属元素的存在及常见的金属矿物
【精讲1】常见的金属矿石赤铁矿的主要成分是( )
A.Fe2O3 B.Fe3O4 C.FeCO3 D.Al2O3
【答案】A
【解析】赤铁矿的主要成分是氧化铁,其化学式为:Fe2O3。故选:A。
【精讲2】下列金属中一定以化合物形态存在于矿物之中的是( )
A.金 B.银 C.铂 D.铁
【答案】D
【解析】A、金的化学性质稳定,可以以单质的形态存在,故A不选;B、银的化学性质很稳定,可以以单质的形态存在,故B不选;C、铂的化学性质很稳定,可以以单质的形态存在,故C不选;D、铁的化学性质比较活泼,容易与空气中的氧气反应,以化合物的形态存在,故D选;故选:D
【跟踪练1】大自然向人类提供了丰富的金属矿物资源,在以下四种矿石中,可用于炼铁的是( )
A.赤铁矿(主要成分是Fe2O3) B.炉甘石(主要成分是ZnCO3)
C.铝土矿(主要成分是A12O3) D.赤铜矿(主要成分是Cu2O)
【答案】A
【解析】炼铁是将铁矿石中的铁氧化物还原成金属铁,故矿石中必须含有铁元素;A、赤铁矿(主要成分是Fe2O3)中含有铁元素,可用于炼铁,符合题意;B、 炉甘石(主要成分是ZnCO3)中不含有铁元素,不可用于炼铁,不符合题意;C、 铝土矿(主要成分是A12O3) 中不含有铁元素,不可用于炼铁,不符合题意;D、 赤铜矿(主要成分是Cu2O)中不含有铁元素,不可用于炼铁,不符合题意;故选A。
【跟踪练2】多角度认识物质能帮助我们更全面地了解物质世界。以金属为例回答下列问题:
(1)认识金属元素的存在
①在自然界中,大多数金属以化合物存在,而金、铂等极少数金属因为化学性质 (填“活泼”或“不活泼”)却能以单质存在。
②常见铁矿石有:黄铁矿(主要成分 FeS2)、磁铁矿(主要成分 Fe3O4)等。这两种铁矿石的主要成分含铁元素质量分数较大的是 。
(2)认识金属的性质 用粗木棍在涂有蜡的锌板上写“南”、平”两个字,露出下面的锌板。向“南”字上滴加稀盐酸,向“平”字上滴加 CuSO4 溶液。
①“南”字上的现象是 。
②“平”字上有红色物质析出,用化学方程式解释: 。
(3)认识金属的制备
工业上,金属钨(W)可由氢气和三氧化钨(WO3)在高温下发生置换反应制得。 反应中化合价升高的元素是 。
(4)认识金属的用途烤制食物时常用到铝箔,主要利用了金属铝的 (填性质)。
【答案】(1)①不活泼;②Fe3O4;(2)①冒气泡;②Zn+CuSO4=Cu+ZnSO4;
(3)氢元素;(4)延展性
【解析】(1)①在自然界中,极少数化学性质不活泼的金属如金、铂等以单质存在;
②由于一个硫原子的质量相当于两个氧原子的质量,故FeS2中铁原子和硫原子的个数比相当于为:Fe:O═1:4,Fe3O4中铁原子和氧原子的个数比为:Fe:O═3:4,故铁元素的质量分数高的是Fe3O4;
(2)①锌与稀盐酸反应产生氢气;与硫酸铜反应生成红色铜和硫酸锌;
(3)三氧化钨与氢气在高温的条件下反应生成金属钨和水,故反应方程式为:WO3+3H2 3H2O+W,该反应前后氢元素的化合价由0变为+1,升高了;
(4)金属铝能压成铝箔,说明金属铝具有优良的延展性。
考点二: 铁的冶炼
SHAPE \* MERGEFORMAT
【精讲1】用如图所示装置完成一氧化碳还原氧化铁的实验中,下列说法不正确的( )
A.装置中漏斗上端点燃可防止一氧化碳污染空气
B.实验时可观察到玻璃管中红棕色粉末逐渐变黑
C.反应后玻璃管中固体物质的质量比反应前减少
D.该实验所有的反应里,氧元素的化合价均未发生改变
【答案】D
【解析】A、一氧化碳和氧气在点燃的条件下生成二氧化碳,装置中漏斗上端点燃可防止一氧化碳污染空气,故A正确;B、实验时可观察到玻璃管中红棕色粉末逐渐变黑,故B正确;C、反应后玻璃管中固体物质的质量比反应前减少,故C正确;D、该实验所有的反应里,一氧化碳和氧气在点燃的条件下生成二氧化碳,氧气中的氧元素的化合价为0,生成的二氧化碳中,氧元素为﹣2价,化合价降低,故D错误。故选:D。
【精讲2】早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用一氧化碳和氧化铁的反应。
某中学化学兴趣小组利用如图装置进行实验探究,请按要求填空:
(1)除CO外,还有哪些物质可以还原Fe2O3 (请写一种物质的化学式)。
(2)实验中可观察到的现象是 。
(3)右边导气管口放置点燃的酒精灯的作用是 。
(4)实验开始时要先通入CO的目的是 。
【答案】(1)C或H2;(2)红棕色粉末逐渐变黑;(3)点燃尾气,防止污染空气;
(4)排尽装置中的空气,防止加热时发生爆炸。
【解析】(1)除CO外,碳(C)、氢气(H2)也具有还原性,也可以还原Fe2O3。
(2)一氧化碳具有还原性,高温下能与氧化铁反应生成铁和二氧化碳,实验进行一段时间后,玻璃管中出现的现象是红棕色粉末逐渐变黑。
(3)一氧化碳有毒,直接排放到空气中会污染环境,在装置图末端的导管口放一盏燃着的酒精灯,是为了点燃尾气,防止污染空气。
(4)实验开始先通入一氧化碳,再点燃酒精喷灯加热玻璃管中的氧化铁,目的是排尽装置中的空气,防止加热时发生爆炸。
【跟踪练1】把赤铁矿、焦炭和石灰石一起加入高炉中进行冶炼,下列说法正确的是( )
A.高炉得到的产物是纯铁
B.赤铁矿的主要成分是Fe3O4
C.焦炭既可以提供热量又可以提供一氧化碳
D.石灰石用于除去尾气
【答案】C
【解析】A、把铁矿石、焦炭和石灰石一起加入高炉中进行冶炼,得到的产物是生铁,不是纯铁,故选项说法错误。B、赤铁矿的主要成分是Fe2O3,故选项说法错误。C、工业炼铁中利用了焦炭的可燃性,提供热量;又利用其还原性,与二氧化碳反应生成一氧化碳气体,故选项说法正确。D、高炉炼铁时用的原料中石灰石的作用是将矿石中的二氧化硅等杂质转变为炉渣而除去,故选项说法错误。故选:C。
【跟踪练2】实验室模拟炼铁的实验装置如图所示。
试回答下列问题:
(1)写出有标号仪器的名称:a ,b 。
(2)实验中看到的实验现象为:玻璃管中的粉末 ,试管里的澄清石灰水 。
(3)玻璃管中反应的化学方程式为 。
(4)加热氧化铁之前,先通一会儿一氧化碳的作用是 。
(5)该实验设计装置C的目的是 。
【答案】(1)铁架台;导管(2)由红色逐渐变黑;变浑浊
(3)Fe2O3+3CO2Fe+3CO2(4)排尽玻璃管中的空气,防止发生爆炸
(5)把一氧化碳转化成二氧化碳,防止污染环境
【解析】(1)题中标号仪器的名称为a为铁架台、b为导管。
(2)一氧化碳具有还原性,高温条件下能与氧化铁反应生成铁和二氧化碳,二氧化碳能使澄清石灰水变浑浊,实验中看到的实验现象为:玻璃管中的粉末由黑色变红色,试管里的澄淸石灰水变浑浊。
(3)玻璃管中反应的化学方程式为Fe2O3+3CO2Fe+3CO2。
(4)CO具有可燃性,与玻璃管中的空气混合受热会发生爆炸,因此应先通CO排尽玻璃管中的空气,然后再点燃酒精灯加热氧化铁。加热氧化铁之前,先通一会儿一氧化碳的作用是排进装置内的空气防止发生爆炸。
(5)一氧化碳有毒,直接排放到空气中会污染环境,该实验设计装置C的目的是处理尾气,防止污染空气。
考点三: 铁生锈的条件
【精讲1】下列说法正确的是( )
A.铁锈的主要成分是Fe3O4 B.生了锈的铁应随手丢弃
C.铁在干燥空气中容易生锈 D.赤铁矿可用于冶炼钢铁
【答案】D
【解析】A、铁锈的主要成分是Fe2O3,故选项说法错误;B、生锈的铁可以回收利用,既能节约资源,又能保护环境,故选项说法错误;C、铁在与氧气、水同时存在时会发生锈蚀,所以铁在干燥空气中不容易生锈,故选项说法错误;D、赤铁矿的主要成分是氧化铁,所以赤铁矿可用于冶炼钢铁,故选项说法正确。故选D。
【精讲2】为了减缓铁制品的锈蚀,下列做法错误的是( )
A.在车船的表面喷涂油漆 B.将使用后的菜刀用布擦干
C.洗净铁制品表面的油膜 D.在铁制品表面镀上一层锌
【答案】C
【解析】铁与水、氧气充分接触时容易生锈,使铁制品与氧气和水隔绝可以防止生锈。A、在车船的表面喷涂油漆,能使铁制品与氧气和水隔绝,可以防锈,故选项说法正确。B、将使用后的菜刀用布擦干,使菜刀不易与水接触,可以防锈,故选项说法正确C、油膜能使铁制品与氧气和水隔绝,可以防锈;用洗涤剂把铁制品表面的油膜洗净,铁制品与水和氧气接触,会加快生锈,故选项说法错误D、在铁制品表面镀上一层锌,能使铁制品与氧气和水隔绝,可以防锈,故选项说法正确.故选C。
【跟踪练1】下列关于金属的说法正确的是( )
A.钨的合金的熔点高,可用于制造保险丝
B.铝制品抗腐蚀能力比铁制品强
C.用 FeSO4 溶液、Cu 和 Ag 三种物质可以验证 Fe、Cu、Ag 三种金属的活动性强弱 D.铁制品生锈产生的铁锈是一种疏松多孔的物质,它的主要成分是 Fe3O4
【答案】B
【解析】A.钨的合金的熔点低,可用于制造保险丝,故错误;B.铝和空气中的氧气反应会生成致密的氧化铝薄膜,所以铝制品抗腐蚀能力比铁制品强,故正确;C.铁比铜活泼,铜比银活泼,把铜和银分别伸入硫酸亚铁溶液中时,都无明显现象,说明铁比铜和银活泼,但是无法确定银和铜的活泼性,故错误;D.铁制品生锈产生的铁锈是一种疏松多孔的物质,它的主要成分是Fe2O3,故错误;故选:B。
【跟踪练2】为预防金属制品锈蚀,下列措施或做法不当的是( )
A.用钢丝球清除铝锅内的氧化层 B.在铁制门窗表面喷涂油漆
C.在铁制水管表面镀一层锌 D.将使用后的菜刀洗净擦干
【答案】A
【解析】A、铝制品表面有一层氧化膜,对铝锅起保护作用,阻止铝被进一步氧化,所以擦去表面的氧化层是错误的做法,故A符合题意;B、在在铁制门窗表面喷涂油漆,使铁与氧气和水隔绝,有利于防锈,故B不符合题意;C、在铁制水管表面镀一层锌,使铁与氧气和水隔绝,有利于防锈,故D不符合题意;D、使用后的菜刀洗净擦干有利于防锈,故D不符合题意。故应选A。
考点四: 含杂质物质的计算
【精讲1】在某次家庭作业中,一位同学的计算题书写过程如下,请你作为小组长,组织组内同学仔细观察,帮他纠正错误。
工业上用含氧化铁80%的赤铁矿石炼铁,欲生产含铁112t的生铁,请计算所需赤铁矿石的质量。
解:设生产112t铁,所需氧化铁的质量为x。
FeO+COFe+CO2.........第1步
72 56
x 112........第2步
x=144..........第3步
144t×80%=115.2t.............第4步
答:生产112t铁,所需赤铁矿石的质量为115.2t
【发现问题】上述作业中有多个步骤书写错误。
【交流讨论】上述作业中有一个错误步骤 ,其错误原因是 。
【纠正错误】请你将该题正确的解答过程重新完整地写在答题卡上。
【答案】
【交流讨论】1(合理即可);氧化铁的化学式书写错误,方程式没有配平(合理即可);
【纠正错误】设生产112t铁,所需氧化铁的质量为x.
Fe2O3+3CO2Fe+3CO2
160 112
x 112t
解得:x=160t
所需赤铁矿石的质量是:=200t
答:需要赤铁矿石200t.
【解析】【交流讨论】上述作业中有一个错误步骤1等,其错误原因是:氧化铁的化学式书写错误,方程式没有配平等。
【纠正错误】
设生产112t铁,所需氧化铁的质量为x。
Fe2O3+3CO2Fe+3CO2
160 112
x 112t
解得:x=160t
所需赤铁矿石的质量是:=200t
答:需要赤铁矿石200t.
【跟踪练1】根据Fe3O4+4CO3Fe+4CO2反应原理,工业上可用来冶炼铁。现用100t含四氧化三铁为46.4%的某铁矿石冶炼金属铁。请完成下列问题,写出必要的计算过程。
(1)该铁矿石中含四氧化三铁质量是多少?
(2)理论上可炼出含铁96%的生铁的质量是多少?
【答案】(1)46.4t(2)35t
【解析】(1)铁矿石中含四氧化三铁质量是100t×46.4%=46.4t。
(2)设理论上可炼出含铁96%的生铁的质量是x。
Fe3O4+4CO3Fe+4CO2
232 168
46.4t 96%x
x=35t
答:(1)铁矿石中含四氧化三铁质量是46.4t
(2)理论上可炼出含铁96%的生铁的质量是35t。
考点五: 金属资源的保护
【精讲1】金属资源是不可再生的资源,保护金属资源是我们刻不容缓的职责。下列有关叙述不正确的是( )
A.大力开采矿物以保障金属材料的供用 B.用特种塑料代替金属制造机器的零部件
C.提高废旧金属的回收利用率 D.在金属制品上刷漆、涂油等防止金属腐蚀
【答案】A
【解析】A、金属资源属于不可再生资源,需要合理、适度开采,故A错误;B、金属资源有限,所以可逐步使用可替代的材料来代替部分金属材料,故B正确;C、金属资源需要合理高效利用,所以可通过回收利用的方式提高金属利用率,故C正确;D、金属与空气的部分成分接触时生锈,可通过隔绝空气的方式防止金属生锈,如刷漆、涂油等方式,故D正确;故选A。
【精讲2】随着新能源汽车的推广应用,电池生产和消费迅猛增长,为了“变废为宝,减少污染”,废旧电池必须回收,回收的主要目的是( )
A.进行重新加工和再生
B.回收其中的金属资源
C.防止电池中的重金属污染环境
D.充电电池回收翻新后又可以高价卖出
【答案】C
【解析】废旧电池中的铅、镉等元素,则被定为致癌物质;汞中毒,会患中枢神经疾病。电池腐烂后,其中的汞、铅、镉等重金属溶出会污染地下水和土壤,即造成地下水和土壤的污染,威胁人体健康。故废旧电池必须回收,回收的主要目的是防止电池中的重金属污染环境。故选:C。
【跟踪练1】“绿箱子环保计划﹣﹣废弃手机及配件同收联合行动”已在全国40个重点城市中开展了近两年。下列有关说法不正确的是( )
A.回收废电池可以节约金属资源
B.“绿箱子”上的“”是回收标志
C.回收废电池可以减少环境污染
D.回收废弃手机中的金属材料没有任何价值
【答案】D
【解析】A、可以节约金属资源的说法正确,因为回收的金属可以再次进行利用。故对;B、此标志是循环再使用的回收标志;故对;C、手机中的一些重金属废弃后会污染土壤,回收后会减少对环境的污染,故对;D、回收利用可节约资源减小由于冶炼这些金属而消耗的能源,同时也可减小对环境的污染。故错。故选:D。
【跟踪练2】中国筹划高铁“大棋局”,国人有望乘高铁2天到达美国,请回答下列问题:
(1)为了节约能源,高铁的车体材料最好选用的是 。
A.耐腐蚀的不锈钢 B.硬度大、密度小的铝合金 C.熔点高、可塑性好的金属钛
(2)若高铁列车使用了氢氧燃料电池,则高铁列车在整个行驶过程中的能量转化是 。
(3)在高铁轨道铺设过程中用到了大量的铁合金。工业上可以用黄铁矿(主要成分为FeS2,其中硫元素的化合价为﹣1价)来炼铁,其中发生的一个反应:黄铁矿和氧气在高温下反应生成氧化铁和一种空气污染物,请写出该反应的化学方程式 ,该反应中铁元素的化合价变化为 。
(4)为了保护金属资源,我们可以采取的措施有 (答一条)。
【答案】(1)AB;(2)化学能转化为电能再转化为机械能;
(3)4FeS2+11O22Fe2O3+8SO2;由+2价变为+3价;
(4)防止金属的腐蚀或废旧金属回收利用或有计划合理开采金属资源或寻找金属替代品(合理即可)。
【解析】(1)高铁的车体材料要求强度大、密度小、耐腐蚀,因此选用不锈钢、铝合金,而钛合金的价格比较昂贵,故选:AB;
(2)氢氧燃料电池提供的是化学能,因此高铁列车在行驶过程中的能量来源是化学能转化为电能再转化为机械能;
(3)黄铁矿和氧气在高温下反应生成氧化铁和一种空气污染物,根据质量守恒定律,该空气污染物是二氧化硫,该反应的化学方程式4FeS2+11O22Fe2O3+8SO2;化合物中各元素的化合价的代数和为0可知,该反应中铁元素的化合价变化为由+2价变为+3价;
(4)防止金属的腐蚀、废旧金属回收利用、有计划合理开采金属资源、寻找金属替代品都可以保护金属资源。
单质形式:Au、Ag等
存在形式
化合物形式:比较活泼的金属
金属资源的利用
常见矿石:磁铁矿(主要成分Fe3O4)、
赤铁矿(主要成分Fe2O3)、黄铜矿、铝土矿等。
原理:一氧化碳还原氧化铁
实验室炼铁
现象
铁的冶炼
金属资源的
利用和保护
主要设备
工业炼铁
原料
原理
氧气
铁生锈的条件
水
金属的腐蚀与防护
金属资源的保护
防止金属锈蚀的方法
防止金属生锈
金属资源的保护
回收利用废旧金属
合理开采
寻找金属的替代品
知识梳理:
1、金属元素的存在形式:
地球上的金属资源广泛地存在于地壳和浩瀚的海洋中,除少数很不活泼的金属(如金、银等)以单质形式存在外,其余的都以化合物的形式存在。
2、常见的矿石
(1)铁矿石有赤铁矿(主要成分是Fe2O3)、磁铁矿(主要成分是Fe3O4)、菱铁矿(主要成分是FeCO3)和黄铁矿(主要成分是FeS2)等;
(2)铜矿石有孔雀石[主要成分是Cu2(OH)2CO3]、赤铜矿(主要成分是Cu2O)、黄铜矿(主要成分是CuFeS2)和辉铜矿(主要成分是Cu2S)等;
(3)铝矿石有铝土矿(主要成分是Al2O3)、明矾(KAlSO4 12H2O)或水铝石(主要成分是Al2O3 H2O)等。
【知识点睛】
地壳中含量最多的金属元素是铝,其次是铁;
【命题方向】
该考点的命题方向主要是通过设置问题情景,让学生阅读、思考后,根据所学的金属元素的存在及常见的金属矿物,以及与其相关的金属活动性顺序及其应用、物质的分类和元素组成、常见金属的冶炼、空气的污染、化学式的书写和意义等知识,来分析、解答相关的实际问题。
【解题方法点拨】
熟记和理解金属元素的存在及常见的金属矿物。
高温
知识梳理:
工业炼铁 实验室炼铁(一氧化碳还原氧化铁)
原料 铁矿石、焦炭、石灰石 装置
设备 高炉
原理 在高温条件下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来
主要化学反应 Fe2O3+3CO=====2Fe+3CO2 现象 红色的粉末逐渐变为黑色;澄清石灰水变浑浊
实际应用 在实际生产中,所用的原料或产物一般都含有杂质,在计算用料和产量时,应考虑到杂质问题 注意事项 ①先通CO,后加热;实验完毕,先熄灯,继续通CO至冷却;②尾气处理:烧掉或用塑料袋收集起来,防止未反应的CO污染空气;
【知识点睛】
反应前,先通一段时间一氧化碳,然后再加热(目的是为了尽可能的排净玻璃管内的空气,防止一氧化碳与其中的空气混合后,被点燃发生爆炸)。反应后,先撤走并熄灭酒精灯,等固体冷却后再停止通一氧化碳(目的是防止石灰水倒吸到玻璃管内,使其炸裂;也为了使固体冷却,防止刚还原出来的铁再次被氧化);
实验室利用一氧化碳还原氧化铁得到的是纯铁,工业炼铁得到的是生铁,属于混合物;
工业炼铁中焦炭的主要作用是提供热量和产生还原剂CO;石灰石的主要作用是将矿石中的二氧化硅等杂质转变为炉渣而除去。
【命题方向】
该考点的命题方向主要是通过创设相关实验、问题情景或图表信息等,来考查学生对一氧化碳还原氧化铁的理解或掌握情况,以及对铁等金属的冶炼原理、氧化还原反应、金属的性质、实验现象和结论(包括反应化学方程式)、一氧化碳的可燃性和毒性、二氧化碳的检验、空气的污染等相关问题的分析、推断、表达的能力和对知识的迁移能力等;并且,经常将其与一氧化碳的可燃性和毒性、铁等金属的冶炼、氧化还原反应、二氧化碳的检验、化学方程式的书写、空气的污染等关联起来,进行综合考查。
【解题方法点拨】
熟记和理解一氧化碳还原氧化铁的所有内容,还有,铁等金属的冶炼原理、氧化还原反应的原理、一氧化碳的可燃性和毒性、金属的性质、化学方程式的书写、空气的污染等相关知识;然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,细致地阅读、分析题意等,联系着生活实际,细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可。
知识梳理:
1、铁生锈的条件:
铁与空气中的水蒸气、氧气同时接触,发生了复杂的化学反应,生成了铁锈。即铁生锈的条件是水和氧气。
2、防止铁制品生锈
(1)原理:破坏铁生锈的条件
(2)方法:①保持铁制品表面的洁净和干燥;②在铁表面涂油、刷漆、烧制搪瓷、镀耐磨和耐腐蚀的金属、烤蓝(即表面生成氧化膜);③改变其内部组成,制成耐腐蚀的合金,如不锈钢等。
【知识点睛】
铁锈是普通钢铁制品在潮湿的空气中,先从其表面慢慢生成的一种红褐色的物质,是就是铁和空气中所氧气、水蒸气等起作用,生成的铁的多种氧化物的水合物.铁锈的成分比较复杂,其主要成分是Fe2O3 xH2O,所以铁锈可以说是混合物.铁锈的结构很疏松,不但不能阻碍里层的铁继续与氧气、水等反应,而且因它具有吸附性,还会使铁生锈的速度加快。
【命题方向】
中考重点是考查学生对铁锈的主要成分,以及与其相关的铁的生锈条件及其防护措施、赤铁矿的主要成分、铝耐腐蚀的原因、混合物和纯净物的判别、物质的结构与性质的关系、金属资源的保护等知识的理解和掌握情况,以及运用它们来分析、解答相关的实际问题的能力等.特别是,铁锈的主要成分及其化学式等是历年来中考命题的热点,当然也是中考考查这块知识的重中之重。
【解题方法点拨】
熟记和理解铁的生锈条件及其防护措施。
知识梳理:
含杂质物质的化学反应的有关计算是指在实际生产中,所用的原料或产物一般都含有杂质,在利用化学方程式进行计算用料和产量时,由于化学方程式表示的是纯净物质之间的质量关系,而不表示不纯物质之间的质量关系;故计算时一定考虑到杂质的问题(即不纯物质和纯物质之间的相互转化问题)。
不纯物质的质量与纯物质的质量的相互转化方法及纯度的计算公式是:
例题:用1000t含氧化铁为80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少?
审题:首先要找到有关的反应的化学方程式、已知量(即1000t、80%、96%)、未知量(生铁的质量);然后,要弄清楚不纯物质与纯物质之间的联系(即赤铁矿~氧化铁~铁~生铁);最后,根据化学方程式计算的步骤、格式(或者根据质量守恒定律和化学式的计算技巧),结合着不纯物质和纯物质之间的相互转化方法,细心地进行计算即可。
【知识点睛】
代入化学方程式中计算的量一定是纯净物的质量,若是混合物则要根据公式进行换算。同理,利用化学方程式计算出来的量也是纯净物的质量。
【命题方向】
该考点的命题方向主要是通过创设有关含杂质物质的化学反应的有关计算的问题情景或图表信息等,来考查学生对含杂质物质的化学反应的有关计算的方法、步骤和格式的理解或掌握情况,以及对不纯物质的质量与纯物质的质量的相互转化方法、纯度的计算公式、铁的冶炼原理、一氧化碳还原氧化铁、化学方程式的书写和意义、根据化学方程式的有关计算等相关问题的分析、推断、表达的能力和对知识的迁移能力等;并且,经常将其与这些相关知识等关联起来,进行综合考查。
【解题方法点拨】
解答这类题目时,首先,要熟记和理解有关含杂质物质的化学反应的有关计算的方法、步骤和格式等相关知识;然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,特别是有关化学方程式的书写和意义、不纯物质的质量与纯物质的质量的相互转化方法,以及根据化学方程式计算的方法、步骤和格式等,细致地阅读、分析题意,联系着生产、生活实际,细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可。
知识梳理:
金属资源的保护主要有以下四种措施:
1、减缓或防止金属的腐蚀;
2、回收利用废旧金属,这样不仅可以节约金属资源,而且还可以减少对环境的污染.
3、有计划、合理地开采矿物,严禁不顾国家利益的乱采矿.
4、寻找金属的代用品,例如,现在经常用塑料来代替钢和其它合金制造管道、齿轮和汽车外壳等。
【命题方向】
该考点的命题方向主要是通过设置相关的问题情景,让学生阅读、思考后,根据所学的金属资源的保护措施,以及与其相关的铁的生锈条件及其防护措施、物质的结构与性质的关系、废弃金属对环境污染、金属的回收利用及其重要性等知识,来分析、解答相关的实际问题;并且,经常将其与这些相关知识联系起来,进行综合考查。
【解题方法点拨】
熟记和理解金属资源的保护措施,以及与其相关的铁的生锈条件及其防护措施、物质的结构与性质的关系、废弃金属对环境污染、金属的回收利用及其重要性等知识。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
