专题1 第二单元 化学能与电能的转化 第3课时 燃料电池(共73张ppt)
文档属性
| 名称 | 专题1 第二单元 化学能与电能的转化 第3课时 燃料电池(共73张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-21 00:00:00 | ||
图片预览











文档简介
(共73张PPT)
DISANKESHI
氢氧燃料电池 / 形形色色的燃料电池 / 制作简单的燃料电池 / 课时对点练
燃料电池
专题1
第3课时
1.证据推理和模型认知:
能基于原电池装置的认知模型分析陌生的化学电池,设计简单的燃料电池,实现能量转化。
2.科学态度与社会责任:
能分析、评价实际生产和生活中的能量转化现象,并能从能源利用率、环境保护等角度综合考虑。
内容索引
一、氢氧燃料电池
二、形形色色的燃料电池
三、制作简单的燃料电池
课时对点练
氢氧燃料电池
一
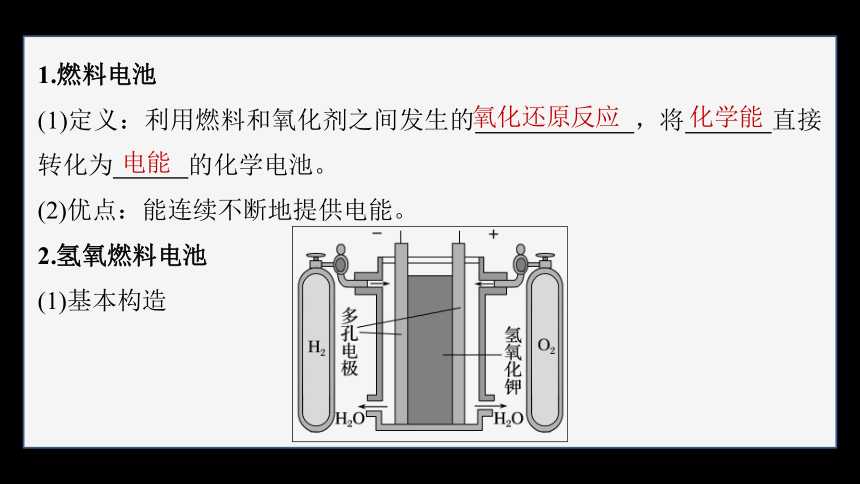
1.燃料电池
(1)定义:利用燃料和氧化剂之间发生的 ,将 直接转化为 的化学电池。
(2)优点:能连续不断地提供电能。
2.氢氧燃料电池
(1)基本构造
氧化还原反应
化学能
电能
(2)工作原理
氢氧燃料电池用多孔金属作电极,不断充入的氢气和氧气,分别在两极发生 反应和 反应。其反应表示如下:
氧化
还原
酸性电解质(H2SO4) 碱性电解质(KOH)
负极反应 2H2-4e-===4H+ __________________________
正极反应 O2+4e-+4H+===2H2O __________________________
总反应 ____________________ 2H2-4e-+4OH-===4H2O
O2+4e-+2H2O===4OH-
2H2+O2===2H2O
(1)燃料电池工作时负极材料一定发生氧化反应( )
(2)氢氧燃料电池是清洁的化学电源( )
(3)氢氧燃料电池放电时化学能全部转化为电能( )
(4)在书写燃料电池的电极反应式时,无需考虑电解质溶液的酸碱性( )
(5)氢氧燃料电池中,当转移2 mol电子时消耗2 mol氢气( )
正误判断
×
√
×
×
×
1.燃料电池和一次电池及二次电池相比较,有哪些优点?
提示 (1)燃料电池的氧化剂和还原剂不是储藏在电池内部,结构更简单;
(2)氧化剂和还原剂可连续地由外部供给,可长时间放电;
(3)能量转换效率高,废弃物排放少,运行噪音小。
2.以氢氧燃料电池为例,燃料电池的电极反应有何特点?电解质溶液为酸性或碱性,电池反应本质相同吗?
提示 两个电极均为惰性电极,本身不参加反应,在反应中H2失去电子发生氧化反应,作负极反应物,O2获得电子发生还原反应,作正极反应物,生成的水不断的被排出电池;无论电解质溶液为酸性或碱性,反应原理相同,都是2H2+O2===2H2O。
3.假如将地球上化石燃料燃烧产生的能量均能通过氢氧燃料电池获得,将大大提高能源利用效率,减少污染,而其中关键的问题就是将化石燃料经济合理地转化为H2,现以煤为原料,写出生产H2的相关反应。
应用体验
1.氢氧燃料电池已用于航天飞机,它以铂作电极,以KOH溶液作电解质溶液,下列叙述不正确的是
A.H2在负极发生氧化反应
B.燃料电池的化学能可以全部转化为电能
C.产物为无污染的水,属于环境友好电池
D.供电时的总反应:2H2+O2===2H2O
√
由电极反应式可知,通入氢气的一极为电池的负极,发生氧化反应,A项正确;
氢氧燃料电池是将化学能转化为电能的装置,还会伴有热能等能量的释放,能量转化率不会达100%,B项错误;
氢氧燃料电池产物是水,对环境无污染,且能量转化率高,C项正确;
电池总反应与氢气在氧气中燃烧的化学方程式一致,供电时的总反应为2H2+O2===2H2O,D项正确。
2.质子交换膜燃料电池的工作原理如图所示,下列叙述正确的是
A.通入氧气的电极发生氧化反应
B.通入氢气的电极为正极
C.导电离子为质子,且在电池内部由正极定向
移动至负极
D.正极的电极反应式为O2+4H++4e-===2H2O
√
通入氧气的电极是正极,正极上得电子发生还原反应,故A错误;
通入氢气的电极是负极,负极上失电子发生氧化反应,故B错误;
质子移向正极,故C错误;
正极的电极反应式为O2+4H++4e-===2H2O,故D正确。
返回
形形色色的燃料电池
二
1.能量转换
所有的燃烧均为放热反应,若能量以电的形式向外释放,则形成燃料电池,所以燃料电池的总化学方程式类似燃烧的总化学方程式,条件不同。
理论上来说,所有的燃烧反应均可设计成燃料电池,所以燃料电池的燃料除氢气外,还有烃、肼、甲醇、氨、煤气等气体或液体,且能量转化率超高。
2.燃料电池电极反应式的书写方法
负极为燃料失电子,发生氧化反应;
正极为O2得电子,发生还原反应。
如CH4碱性(KOH溶液)燃料电池负极反应式的书写方法:
第一步 确定生成物
第二步 确定电子转移和变价元素原子守恒
第三步 依据电解质性质,用OH-使电荷守恒
第四步 依据氢原子守恒配平H2O的化学计量数
(1)甲烷燃料电池中,通入氧气的一极为负极( )
(2)燃料电池中发生的化学反应可以不是氧化还原反应( )
(3)肼(N2H4)、氨不能作为燃料电池的燃料,因为其燃烧会产生污染性气体( )
(4)应用燃料电池的发电站,具有能量转换率高、废弃物排放少等优点
( )
(5)燃料电池的电池反应式和燃料燃烧的化学方程式一定相同( )
正误判断
×
×
×
√
×
如图为燃料电池装置图,结合原电池原理回答相关问题。
(1)如电解质为稀硫酸溶液,写出甲烷燃料电池的正、负极反应式和总的电池反应式。
提示 负极反应式:CH4-8e-+2H2O===CO2+8H+;正极反应式:2O2+8e-+8H+===4H2O;总反应式:CH4+2O2===CO2+2H2O。
(2)如电解质为KOH溶液,写出甲烷燃料电池的正、负极反应式和总的电池反应式。
提示 负极反应式:CH4-8e-+10OH-=== +7H2O;正极反应式:2O2+8e-+4H2O===8OH-;总反应式:CH4+2O2+2KOH===K2CO3+3H2O。
(3)如电解质为熔融的K2CO3,正极除O2外,还有辅助气体CO2参与电极反应,写出电池正、负极电极反应式。
提示 负极反应式:CH4-8e-+4 ===5CO2+2H2O;正极反应式:2O2+8e-+4CO2===4 。
(4)如电解质为可以传递O2-的固体氧化物,写出电池正、负极电极反应式。
提示 负极反应式:CH4-8e-+4O2-===CO2+2H2O;正极反应式:2O2+8e-===4O2-。
易错提示 ①电极反应式的书写本质为离子反应,只有溶于水的强电解质才能写成离子。
②书写电极反应式时,要紧抓电解质的性质,如酸性溶液中H+将电极反应式的电荷守恒,碱性溶液中应为OH-将电荷守恒。
③含碳的燃料在负极失电子,只有电解质溶液呈碱性,才会生成 ,其他情况一般都生成CO2。
应用体验
1.一种熔融碳酸盐燃料电池原理示意图如下。下列有关该电池的说法正确的是
A.反应CH4+H2O 3H2+CO,每消耗
1 mol CH4转移12 mol电子
B.电极A上H2参与的电极反应为H2+2OH--
2e-===2H2O
C.电池工作时, 向电极B移动
D.电极B上发生的电极反应为O2+2CO2+4e-===2
√
A项,由化合价变化可知,每消耗1 mol CH4转移6 mol电子,错误;
B项,电极A为负极,电极反应式为H2+CO+2 -4e-===H2O+3CO2,
错误;
C项,电池工作时, 向电极A移动,错误;
D项,电极B是正极,电极反应式为O2+2CO2+4e-===2 ,正确。
2.如图为肼燃料电池示意图,请写出正、负极的电极反应式及总反应式。
答案 负极:N2H4-4e-+4OH-===4H2O+N2
正极:O2+4e-+2H2O===4OH-
总反应式:N2H4+O2===N2+2H2O
归纳总结
常见的燃料电池
(1)H2、CH4、N2H4、CH3OH、NH3、煤气等均可作为燃料电池的燃料。
(2)电解质可以是酸(如H2SO4)、碱(如KOH)也可以是熔融盐(如Li2CO3-Na2CO3混合物)。
(3)燃料电池电极反应式的书写与电解质溶液有密切关系,酸性溶液中电极反应式不能出现OH-,碱性溶液中电极反应式不能出现H+。
返回
制作简单的燃料电池
三
1.设计思路
将用学生电源电解稀硫酸得到的氢气(H2)和氧气(O2)在两个石墨电极上反应,使化学能转化为电能。
2.装置图
(1)连接时钟时,如何判断燃料电池的正、负极?
提示 接通学生电源,两端产生氢气和氧气的体积比为2∶1,由于氢气的体积大,玻璃导管内的液柱先溢出,作燃料电池的负极。
(2)什么现象可以证明处于不同电极的氢气和氧气发生了反应?
提示 时钟的指针发生了偏转。
(3)在制备氢气和氧气时,用蒸馏水代替6 mol·L-1稀硫酸行吗?KOH溶液呢?
提示 不行。蒸馏水导电能力弱,可以加入KOH溶液以增强导电性,故KOH溶液可以代替6 mol·L-1稀硫酸。
应用体验
1.下列关于氢氧燃料电池说法正确的是
A.正极发生氧化反应,负极发生还原反应
B.若电解质溶液为H2SO4溶液,硫酸根离子移向正极
C.若电解质溶液为KOH溶液,随着反应的进行,溶液的pH不变
D.氢氧燃料电池是一种绿色电池,未来有很大的发展前景
√
2.将氢气、甲烷、乙醇等物质在氧气中燃烧时的化学能直接转化为电能的装置叫燃料电池。燃料电池的基本组成为电极、电解质、燃料和氧化剂。此种电池能量利用率可高达80%(一般柴油发电机只有40%左右),产物污染也少。下列有关燃料电池的说法错误的是
A.上述燃料电池的负极反应物是氢气、甲烷、乙醇等物质
B.氢氧燃料电池常用于航天飞行器,原因之一是该电池的产物为水,经过处理之后可
供宇航员使用
C.乙醇燃料电池的电解质常用KOH,该电池的负极反应为C2H5OH-12e-===2CO2↑+
3H2O
D.以KOH溶液作为电解质溶液,甲烷燃料电池的正极反应为O2+2H2O+4e-===4OH-
√
A项,燃料电池中,燃料作负极,负极反应物可以是氢气、甲烷、乙醇等物质,正确;
B项,航天飞行器中氢氧燃料电池的产物是水,经过处理之后可供宇航员使用,正确;
C项,乙醇燃料电池的电解质为KOH时,生成的二氧化碳会和其反应生成碳酸盐,负极反应式:C2H5OH-12e-+16OH-===2 +11H2O,错误;
D项,燃料电池中正极上氧气得电子,在碱性环境下,正极反应式为O2+2H2O+4e-===4OH-,正确。
返回
课时对点练
题组一 酸性燃料电池
1.以N2和H2为反应物、溶有A的稀盐酸为电解质溶液,可制成能固氮的新型燃料电池,原理如图所示。下列说法错误的是
A.b电极为负极,发生氧化反应
B.a电极发生的反应为N2+8H++6e-===2
C.A溶液中所含溶质为NH4Cl
D.当反应消耗1 mol N2时,则消耗的H2为67.2 L
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
B项,环境是酸性环境,因此有N2+8H++6e-===2 ,正确;
C项,根据选项A中总反应式知,分离出的A为NH4Cl,正确;
D项,题目没有说明是否是标准状况,错误。
A项,此电池总反应式是N2+3H2+2HCl===
2NH4Cl,氢气中的氢元素的化合价升高,根据原电池的工作原理,负极失去电子,化合价升高,因此b极为负极,发生氧化反应,正确;
2.一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O===CH3COOH+4H+。下列有关说法正确的是
A.检测时,电解质溶液中的H+向负极移动
B.若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气
C.电池反应的化学方程式:CH3CH2OH+O2===CH3COOH+H2O
D.正极上发生的反应:O2+4e-+2H2O===4OH-
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
电子从负极流出经导线转移到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动,A项错误;
1 mol氧气在反应中得到4 mol电子,所以若有0.4 mol电子转移,则在标准状况下消耗2.24 L氧气,B项错误;
溶液显酸性,因此正极反应式是O2+4e-+4H+===2H2O,D项错误;
正极和负极反应式相加可得总反应,C项正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
3.环境监察局常用“定电位”NOx传感器来监测化工厂的氮氧化物气体是否达到排放标准,其工作原理如图所示。下列说法正确的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
A.对电极是正极
B.工作电极上发生的电极反应为NO2+2H+-2e-===NO+H2O
C.传感器工作时,H+由工作电极移向对电极
D.对电极的材料可能为活泼金属锌
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
工作电极是NO2变为NO,化合价降低,是原电池的正极,对电极为负极,故A错误;
工作电极上发生的电极反应为NO2+2H++2e-===NO+H2O,故B错误;
传感器工作时,H+由对电极移向工作电极,故C错误;
对电极为负极,材料可能为活泼金属锌,故D正确。
题组二 碱性燃料电池
4.一种新型的燃料电池以多孔镍板为电极,并将两极插入KOH溶液中,然后分别向两极通入乙烷和氧气,其总反应为2C2H6+7O2+8KOH===
4K2CO3+10H2O,有关此电池的推断正确的是
A.放电一段时间后,负极周围溶液的pH增大
B.正极反应式为14H2O+7O2+28e-===28OH-
C.每消耗1 mol C2H6,则电路中转移12 mol电子
D.放电过程中KOH溶液的物质的量浓度不变
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
负极发生氧化反应,电极反应式为C2H6+18OH--14e-=== +
12H2O,负极消耗OH-,负极周围溶液的pH减小,A错误;
正极发生还原反应,电极反应式为14H2O+7O2+28e-===28OH-,B正确;
由负极反应式可知每消耗1 mol C2H6,电路中转移14 mol电子,C错误;
该电池总反应为2C2H6+7O2+8KOH===4K2CO3+10H2O,KOH参加反应,物质的量减少,且有水生成,所以KOH溶液的物质的量浓度减小,D错误。
5.液体燃料电池相比于气体燃料电池具有体积小等优点,一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。下列关于该电池的叙述正确的是
A.b电极发生氧化反应
B.a电极为该电池的正极
C.放电时,电流从a电极经过负载流向b电极
D.a电极的电极反应式:N2H4+4OH--4e-
===N2+4H2O
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
该燃料电池中,通入氧化剂空气的b电极为正极,正极上氧气得电子发生还原反应,故A项错误;
该燃料电池中,通入燃料的电极为负极,即a电极为负极,故B项错误;
放电时,电流从b电极经过负载流向a电极,故C项错误;
通入燃料的电极为负极,负极上燃料失电子发生氧化反应,在碱性条件下,电极反应式为N2H4+4OH--4e-===N2+4H2O,故D项正确。
题组三 离子交换膜燃料电池
6.如图是甲醇燃料电池的结构示意图,甲醇在催化剂作用下提供质子(H+)
和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为2CH3OH+3O2===2CO2+4H2O。下列说法不正确的是
A.左电极为电池的负极,a处通入的物质是甲醇
B.正极反应式为O2+2H2O+4e-===4OH-
C.负极反应式为CH3OH+H2O-6e-=== CO2+6H+
D.该电池提供1 mol e-,消耗氧气0.25 mol
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
负极反应式为2CH3OH-12e-+2H2O===2CO2+12H+,正极反应式为3O2+12e-+12H+===6H2O;根据电子流向,可以判断a处通甲醇,b处通O2;当电池提供 1 mol电子时,消耗O2为1× mol=0.25 mol。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
7.以引火性高的联氨(N2H4)为燃料的环保电池,工作时产生稳定无污染的物质,原理如图所示。下列说法正确的是
A.N极为电源负极,联氨从c口通入
B.负极上每消耗1 mol N2H4,转移6 mol电子
C.正极的电极反应式为O2+2H2O+4e-===4OH-
D.可将联氨改进为引火性低、稳定性好的N2H4·H2O
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
由图中氢离子移动方向可知,电极N为正极,氧气在正极上发生还原反应,电极反应式为O2+4H++4e-===2H2O,则氧气从c口通入,A、C项错误;
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
联氨在负极上发生氧化反应,电极反应式为N2H4-4e-===N2+4H+,每消耗1 mol N2H4可转移4 mol电子,B项错误;
将联氨改进为引火性低、稳定性好的N2H4·H2O,则电池的安全性会更高,D项正确。
8.如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测,下列说法不正确的是
A.电流由O2所在的铂电极经外电路流向另一电极
B.O2所在的铂电极处发生还原反应
C.该电池的负极反应式为CH3CH2OH+3H2O-12e-
===2CO2↑+12H+
D.微处理器通过检测电流大小而计算出被测气体中酒精的含量
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
乙醇燃料电池中,负极上乙醇失电子发生氧化反应,正极上氧气得电子发生还原反应,电流由正极流向负极,即从O2所在的铂电极经外电路流向另一电极,故A、B项正确;
由装置图可知酒精在负极被氧气氧化生成醋酸:CH3CH2OH-4e-+H2O===4H++CH3COOH,故C项错误;
微处理器通过检测电流大小可以得出电子转移的物质的量,根据电极反应式可以计算出被测气体中酒精的含量,故D项正确。
题组四 熔融盐(或固体氧化物)燃料电池
9.据报道,美国一个海军航空站安装了一台250 kW的MCFC型燃料电池。该电池可同时供应电和水蒸气,其燃料为H2,电解质为熔融的K2CO3,工作温度为600~700 ℃。已知该电池的总反应为2H2+O2===2H2O,负极反应为H2+ -2e-===H2O+CO2。下列推断正确的是
A.正极反应为4OH--4e-===O2+2H2O
B.放电时, 向负极移动
C.电池供应1 mol水蒸气,转移电子的物质的量为4 mol
D.通入O2的一极为正极,发生氧化反应
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
该电池的正极反应为O2+4e-+2CO2===2 ,A项错误;
原电池工作时,阴离子向负极移动,B项正确;
电池提供1 mol水蒸气时,转移电子的物质的量为2 mol,C项错误;
通入O2的一极为正极,发生还原反应,D项错误。
10.H2S燃料电池应用前景非常广阔,该电池示意图如下。下列说法正确的是
A.电极a是正极
B.O2-由电极a移向电极b
C.电极 a 的反应式为2H2S+2O2--4e-===
S2+2H2O
D.当通入11.2 L O2时,转移电子数为2NA
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
根据原电池原理及图示电池构造分析,电池总反应为2H2S+O2===S2+2H2O,则负极H2S失电子发生氧化反应,正极O2得电子发生还原反应,电极a为电池的负极,故A错误;
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
原电池中阴离子向负极移动,则O2-由电极b移向电极a,故B错误;
电极a为电池的负极,发生氧化反应,反应式为2H2S+2O2--4e-===S2+2H2O,故C正确;
未注明是否为标准状况,无法确定11.2 L O2的物质的量,故D错误。
11.设计出燃料电池使汽油(主要成分为C5H12)氧化直接产生电流是21世纪富有挑战性的课题。有人设计了一种固体燃料电池,以固体氧化铝-氧化钇为电解质,这种固体电解质在高温下允许O2-在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断不正确的是
A.有O2放电的电极a为电池的负极
B.电极b对应的电极反应式为C5H12+16O2--32e-
===5CO2+6H2O
C.该电池的总反应式为C5H12+8O2===5CO2+6H2O
D.汽油燃料电池的技术障碍是氧化反应不完全,产生碳单质堵塞电极的气体
通道,从而使输电效能减弱
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
根据题图可知,O2在电极a获得电子,发生还原反应,电极a为电池的正极,A错误;
电极b上C5H12失去电子,发生氧化反应,电极反应式为C5H12+16O2--32e-===5CO2+6H2O,B正确;
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
正极反应式为8O2+32e-===16O2-,将正、负极反应式相加,可得电池的总反应式为C5H12+8O2===5CO2+6H2O,C正确。
题组五 金属—空气电池
12.锌—空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,总反应为2Zn+O2+4OH-+2H2O 。下列说法正确的是
A.放电时,电解质溶液中K+向负极移动
B.充电时,电解质溶液中c(OH-)逐渐减小
C.放电时,负极反应为Zn+4OH--2e-===
D.放电时,电路中通过2 mol电子,消耗氧气22.4 L(标准状况)
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
A错,放电时溶液中的阳离子向正极移动;
B错,充电时的总反应为放电时反应的逆过程:2 ===2Zn+O2↑
+4OH-+2H2O,c(OH-)逐渐增大;
C对,放电时负极失电子发生氧化反应,由放电时的总反应可知,负极反应为Zn+4OH--2e-=== ;
D错,由放电时的总反应可知,电路中通过2 mol电子时,消耗0.5 mol O2,其体积为11.2 L(标准状况)。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
13.近年来AIST正在研制一种高容量、低成本的锂—铜空气燃料电池。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O===2Cu+2Li++2OH-,下列说法不正确的是
A.放电时,Li+透过固体电解质向Cu极移动
B.放电时,负极的电极反应式为Cu2O+H2O
+2e-===2Cu+2OH-
C.通空气时,铜被腐蚀,表面产生Cu2O
D.整个反应过程中,铜相当于催化剂
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
放电时,锂是负极,发生失电子的氧化反应;在电池内部Li+(阳离子)透过固体电解质向正极(铜电极)移动;由题意可知,通空气时铜被腐蚀,表面产生Cu2O,放电时Cu2O又转化成铜,整个反应过程中,铜相当于催化剂。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
14.如图是甲烷燃料电池原理示意图,回答下列问题:
(1)电池的负极是___(填“a”或“b”)电极,该极的电极反应式为___________________
_______________。
a
CH4-8e-+10OH-
碱性甲烷燃料电池中通入甲烷的一极a电极为原电池的负极,该极上是燃料发生失电子的氧化反应,电极反应式为CH4-8e-+10OH-===
+7H2O。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(2)电池工作一段时间后电解质溶液的pH______(填“增大”“减小”或“不变”)。
减小
在碱性溶液中,甲烷燃料电池的总反应式为CH4+2O2+2OH-=== +3H2O,电池工作一段时间后,由于氢氧根离子被消耗且反应生成H2O,所以电解质溶液的pH会减小。
15.氨气是一种富氢燃料,可以直接用于燃料电池,如图是供氨水式燃料电池工作原理:
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(1)氨气燃料电池的电解质溶液最好选择________(填“酸性”“碱性”或“中性”)溶液。
碱性
氨气是碱性气体,所以电解液最好选择碱性溶液。
(2)空气在进入电池装置前需要通过过滤器除去的气体是______。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
CO2
空气中的CO2能和氨水反应,所以滤去的气体是CO2。
(3)氨气燃料电池的反应是氨气与氧气生成一种常见的无毒气体和水,该电池的总反应式是____________________________,正极的电极反应是________________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
4NH3 + 3O2===2N2 + 6H2O
O2 +4e-+2H2O===4OH-
正极发生还原反应,碱性环境下,电极反应式为O2+4e-+2H2O===4OH-。
16.(1)二氧化硫—空气质子交换膜燃料电池可以利用大气所含SO2快速启动,其装置示意图如图:
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
①质子的流动方向为___________(填“从A到B”或“从B到A”)。
从A到B
根据图示,A为燃料电池的负极,B为燃料电池的正极,在原电池电解液中,正电荷由负极向正极移动,即从A到B;
②负极的电极反应式为_____________________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
负极二氧化硫被氧化为硫酸根离子,电极反应式为SO2-2e-+2H2O===
+4H+。
(2)NH3—O2燃料电池的结构如图所示:
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
①a极为电池的____(填“正”或“负”)极。
负
a极通入氨气,是负极,b极通入氧气,是正极;
②当生成1 mol N2时 ,电路中流过电子的物质的量为_______。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
6 mol
氨气中N的化合价由-3变成0,当生成1 mol N2时,转移电子的物质的量为6 mol。
返回
专题1
本课结束
DISANKESHI
氢氧燃料电池 / 形形色色的燃料电池 / 制作简单的燃料电池 / 课时对点练
燃料电池
专题1
第3课时
1.证据推理和模型认知:
能基于原电池装置的认知模型分析陌生的化学电池,设计简单的燃料电池,实现能量转化。
2.科学态度与社会责任:
能分析、评价实际生产和生活中的能量转化现象,并能从能源利用率、环境保护等角度综合考虑。
内容索引
一、氢氧燃料电池
二、形形色色的燃料电池
三、制作简单的燃料电池
课时对点练
氢氧燃料电池
一
1.燃料电池
(1)定义:利用燃料和氧化剂之间发生的 ,将 直接转化为 的化学电池。
(2)优点:能连续不断地提供电能。
2.氢氧燃料电池
(1)基本构造
氧化还原反应
化学能
电能
(2)工作原理
氢氧燃料电池用多孔金属作电极,不断充入的氢气和氧气,分别在两极发生 反应和 反应。其反应表示如下:
氧化
还原
酸性电解质(H2SO4) 碱性电解质(KOH)
负极反应 2H2-4e-===4H+ __________________________
正极反应 O2+4e-+4H+===2H2O __________________________
总反应 ____________________ 2H2-4e-+4OH-===4H2O
O2+4e-+2H2O===4OH-
2H2+O2===2H2O
(1)燃料电池工作时负极材料一定发生氧化反应( )
(2)氢氧燃料电池是清洁的化学电源( )
(3)氢氧燃料电池放电时化学能全部转化为电能( )
(4)在书写燃料电池的电极反应式时,无需考虑电解质溶液的酸碱性( )
(5)氢氧燃料电池中,当转移2 mol电子时消耗2 mol氢气( )
正误判断
×
√
×
×
×
1.燃料电池和一次电池及二次电池相比较,有哪些优点?
提示 (1)燃料电池的氧化剂和还原剂不是储藏在电池内部,结构更简单;
(2)氧化剂和还原剂可连续地由外部供给,可长时间放电;
(3)能量转换效率高,废弃物排放少,运行噪音小。
2.以氢氧燃料电池为例,燃料电池的电极反应有何特点?电解质溶液为酸性或碱性,电池反应本质相同吗?
提示 两个电极均为惰性电极,本身不参加反应,在反应中H2失去电子发生氧化反应,作负极反应物,O2获得电子发生还原反应,作正极反应物,生成的水不断的被排出电池;无论电解质溶液为酸性或碱性,反应原理相同,都是2H2+O2===2H2O。
3.假如将地球上化石燃料燃烧产生的能量均能通过氢氧燃料电池获得,将大大提高能源利用效率,减少污染,而其中关键的问题就是将化石燃料经济合理地转化为H2,现以煤为原料,写出生产H2的相关反应。
应用体验
1.氢氧燃料电池已用于航天飞机,它以铂作电极,以KOH溶液作电解质溶液,下列叙述不正确的是
A.H2在负极发生氧化反应
B.燃料电池的化学能可以全部转化为电能
C.产物为无污染的水,属于环境友好电池
D.供电时的总反应:2H2+O2===2H2O
√
由电极反应式可知,通入氢气的一极为电池的负极,发生氧化反应,A项正确;
氢氧燃料电池是将化学能转化为电能的装置,还会伴有热能等能量的释放,能量转化率不会达100%,B项错误;
氢氧燃料电池产物是水,对环境无污染,且能量转化率高,C项正确;
电池总反应与氢气在氧气中燃烧的化学方程式一致,供电时的总反应为2H2+O2===2H2O,D项正确。
2.质子交换膜燃料电池的工作原理如图所示,下列叙述正确的是
A.通入氧气的电极发生氧化反应
B.通入氢气的电极为正极
C.导电离子为质子,且在电池内部由正极定向
移动至负极
D.正极的电极反应式为O2+4H++4e-===2H2O
√
通入氧气的电极是正极,正极上得电子发生还原反应,故A错误;
通入氢气的电极是负极,负极上失电子发生氧化反应,故B错误;
质子移向正极,故C错误;
正极的电极反应式为O2+4H++4e-===2H2O,故D正确。
返回
形形色色的燃料电池
二
1.能量转换
所有的燃烧均为放热反应,若能量以电的形式向外释放,则形成燃料电池,所以燃料电池的总化学方程式类似燃烧的总化学方程式,条件不同。
理论上来说,所有的燃烧反应均可设计成燃料电池,所以燃料电池的燃料除氢气外,还有烃、肼、甲醇、氨、煤气等气体或液体,且能量转化率超高。
2.燃料电池电极反应式的书写方法
负极为燃料失电子,发生氧化反应;
正极为O2得电子,发生还原反应。
如CH4碱性(KOH溶液)燃料电池负极反应式的书写方法:
第一步 确定生成物
第二步 确定电子转移和变价元素原子守恒
第三步 依据电解质性质,用OH-使电荷守恒
第四步 依据氢原子守恒配平H2O的化学计量数
(1)甲烷燃料电池中,通入氧气的一极为负极( )
(2)燃料电池中发生的化学反应可以不是氧化还原反应( )
(3)肼(N2H4)、氨不能作为燃料电池的燃料,因为其燃烧会产生污染性气体( )
(4)应用燃料电池的发电站,具有能量转换率高、废弃物排放少等优点
( )
(5)燃料电池的电池反应式和燃料燃烧的化学方程式一定相同( )
正误判断
×
×
×
√
×
如图为燃料电池装置图,结合原电池原理回答相关问题。
(1)如电解质为稀硫酸溶液,写出甲烷燃料电池的正、负极反应式和总的电池反应式。
提示 负极反应式:CH4-8e-+2H2O===CO2+8H+;正极反应式:2O2+8e-+8H+===4H2O;总反应式:CH4+2O2===CO2+2H2O。
(2)如电解质为KOH溶液,写出甲烷燃料电池的正、负极反应式和总的电池反应式。
提示 负极反应式:CH4-8e-+10OH-=== +7H2O;正极反应式:2O2+8e-+4H2O===8OH-;总反应式:CH4+2O2+2KOH===K2CO3+3H2O。
(3)如电解质为熔融的K2CO3,正极除O2外,还有辅助气体CO2参与电极反应,写出电池正、负极电极反应式。
提示 负极反应式:CH4-8e-+4 ===5CO2+2H2O;正极反应式:2O2+8e-+4CO2===4 。
(4)如电解质为可以传递O2-的固体氧化物,写出电池正、负极电极反应式。
提示 负极反应式:CH4-8e-+4O2-===CO2+2H2O;正极反应式:2O2+8e-===4O2-。
易错提示 ①电极反应式的书写本质为离子反应,只有溶于水的强电解质才能写成离子。
②书写电极反应式时,要紧抓电解质的性质,如酸性溶液中H+将电极反应式的电荷守恒,碱性溶液中应为OH-将电荷守恒。
③含碳的燃料在负极失电子,只有电解质溶液呈碱性,才会生成 ,其他情况一般都生成CO2。
应用体验
1.一种熔融碳酸盐燃料电池原理示意图如下。下列有关该电池的说法正确的是
A.反应CH4+H2O 3H2+CO,每消耗
1 mol CH4转移12 mol电子
B.电极A上H2参与的电极反应为H2+2OH--
2e-===2H2O
C.电池工作时, 向电极B移动
D.电极B上发生的电极反应为O2+2CO2+4e-===2
√
A项,由化合价变化可知,每消耗1 mol CH4转移6 mol电子,错误;
B项,电极A为负极,电极反应式为H2+CO+2 -4e-===H2O+3CO2,
错误;
C项,电池工作时, 向电极A移动,错误;
D项,电极B是正极,电极反应式为O2+2CO2+4e-===2 ,正确。
2.如图为肼燃料电池示意图,请写出正、负极的电极反应式及总反应式。
答案 负极:N2H4-4e-+4OH-===4H2O+N2
正极:O2+4e-+2H2O===4OH-
总反应式:N2H4+O2===N2+2H2O
归纳总结
常见的燃料电池
(1)H2、CH4、N2H4、CH3OH、NH3、煤气等均可作为燃料电池的燃料。
(2)电解质可以是酸(如H2SO4)、碱(如KOH)也可以是熔融盐(如Li2CO3-Na2CO3混合物)。
(3)燃料电池电极反应式的书写与电解质溶液有密切关系,酸性溶液中电极反应式不能出现OH-,碱性溶液中电极反应式不能出现H+。
返回
制作简单的燃料电池
三
1.设计思路
将用学生电源电解稀硫酸得到的氢气(H2)和氧气(O2)在两个石墨电极上反应,使化学能转化为电能。
2.装置图
(1)连接时钟时,如何判断燃料电池的正、负极?
提示 接通学生电源,两端产生氢气和氧气的体积比为2∶1,由于氢气的体积大,玻璃导管内的液柱先溢出,作燃料电池的负极。
(2)什么现象可以证明处于不同电极的氢气和氧气发生了反应?
提示 时钟的指针发生了偏转。
(3)在制备氢气和氧气时,用蒸馏水代替6 mol·L-1稀硫酸行吗?KOH溶液呢?
提示 不行。蒸馏水导电能力弱,可以加入KOH溶液以增强导电性,故KOH溶液可以代替6 mol·L-1稀硫酸。
应用体验
1.下列关于氢氧燃料电池说法正确的是
A.正极发生氧化反应,负极发生还原反应
B.若电解质溶液为H2SO4溶液,硫酸根离子移向正极
C.若电解质溶液为KOH溶液,随着反应的进行,溶液的pH不变
D.氢氧燃料电池是一种绿色电池,未来有很大的发展前景
√
2.将氢气、甲烷、乙醇等物质在氧气中燃烧时的化学能直接转化为电能的装置叫燃料电池。燃料电池的基本组成为电极、电解质、燃料和氧化剂。此种电池能量利用率可高达80%(一般柴油发电机只有40%左右),产物污染也少。下列有关燃料电池的说法错误的是
A.上述燃料电池的负极反应物是氢气、甲烷、乙醇等物质
B.氢氧燃料电池常用于航天飞行器,原因之一是该电池的产物为水,经过处理之后可
供宇航员使用
C.乙醇燃料电池的电解质常用KOH,该电池的负极反应为C2H5OH-12e-===2CO2↑+
3H2O
D.以KOH溶液作为电解质溶液,甲烷燃料电池的正极反应为O2+2H2O+4e-===4OH-
√
A项,燃料电池中,燃料作负极,负极反应物可以是氢气、甲烷、乙醇等物质,正确;
B项,航天飞行器中氢氧燃料电池的产物是水,经过处理之后可供宇航员使用,正确;
C项,乙醇燃料电池的电解质为KOH时,生成的二氧化碳会和其反应生成碳酸盐,负极反应式:C2H5OH-12e-+16OH-===2 +11H2O,错误;
D项,燃料电池中正极上氧气得电子,在碱性环境下,正极反应式为O2+2H2O+4e-===4OH-,正确。
返回
课时对点练
题组一 酸性燃料电池
1.以N2和H2为反应物、溶有A的稀盐酸为电解质溶液,可制成能固氮的新型燃料电池,原理如图所示。下列说法错误的是
A.b电极为负极,发生氧化反应
B.a电极发生的反应为N2+8H++6e-===2
C.A溶液中所含溶质为NH4Cl
D.当反应消耗1 mol N2时,则消耗的H2为67.2 L
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
B项,环境是酸性环境,因此有N2+8H++6e-===2 ,正确;
C项,根据选项A中总反应式知,分离出的A为NH4Cl,正确;
D项,题目没有说明是否是标准状况,错误。
A项,此电池总反应式是N2+3H2+2HCl===
2NH4Cl,氢气中的氢元素的化合价升高,根据原电池的工作原理,负极失去电子,化合价升高,因此b极为负极,发生氧化反应,正确;
2.一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O===CH3COOH+4H+。下列有关说法正确的是
A.检测时,电解质溶液中的H+向负极移动
B.若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气
C.电池反应的化学方程式:CH3CH2OH+O2===CH3COOH+H2O
D.正极上发生的反应:O2+4e-+2H2O===4OH-
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
电子从负极流出经导线转移到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动,A项错误;
1 mol氧气在反应中得到4 mol电子,所以若有0.4 mol电子转移,则在标准状况下消耗2.24 L氧气,B项错误;
溶液显酸性,因此正极反应式是O2+4e-+4H+===2H2O,D项错误;
正极和负极反应式相加可得总反应,C项正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
3.环境监察局常用“定电位”NOx传感器来监测化工厂的氮氧化物气体是否达到排放标准,其工作原理如图所示。下列说法正确的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
A.对电极是正极
B.工作电极上发生的电极反应为NO2+2H+-2e-===NO+H2O
C.传感器工作时,H+由工作电极移向对电极
D.对电极的材料可能为活泼金属锌
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
工作电极是NO2变为NO,化合价降低,是原电池的正极,对电极为负极,故A错误;
工作电极上发生的电极反应为NO2+2H++2e-===NO+H2O,故B错误;
传感器工作时,H+由对电极移向工作电极,故C错误;
对电极为负极,材料可能为活泼金属锌,故D正确。
题组二 碱性燃料电池
4.一种新型的燃料电池以多孔镍板为电极,并将两极插入KOH溶液中,然后分别向两极通入乙烷和氧气,其总反应为2C2H6+7O2+8KOH===
4K2CO3+10H2O,有关此电池的推断正确的是
A.放电一段时间后,负极周围溶液的pH增大
B.正极反应式为14H2O+7O2+28e-===28OH-
C.每消耗1 mol C2H6,则电路中转移12 mol电子
D.放电过程中KOH溶液的物质的量浓度不变
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
负极发生氧化反应,电极反应式为C2H6+18OH--14e-=== +
12H2O,负极消耗OH-,负极周围溶液的pH减小,A错误;
正极发生还原反应,电极反应式为14H2O+7O2+28e-===28OH-,B正确;
由负极反应式可知每消耗1 mol C2H6,电路中转移14 mol电子,C错误;
该电池总反应为2C2H6+7O2+8KOH===4K2CO3+10H2O,KOH参加反应,物质的量减少,且有水生成,所以KOH溶液的物质的量浓度减小,D错误。
5.液体燃料电池相比于气体燃料电池具有体积小等优点,一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。下列关于该电池的叙述正确的是
A.b电极发生氧化反应
B.a电极为该电池的正极
C.放电时,电流从a电极经过负载流向b电极
D.a电极的电极反应式:N2H4+4OH--4e-
===N2+4H2O
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
该燃料电池中,通入氧化剂空气的b电极为正极,正极上氧气得电子发生还原反应,故A项错误;
该燃料电池中,通入燃料的电极为负极,即a电极为负极,故B项错误;
放电时,电流从b电极经过负载流向a电极,故C项错误;
通入燃料的电极为负极,负极上燃料失电子发生氧化反应,在碱性条件下,电极反应式为N2H4+4OH--4e-===N2+4H2O,故D项正确。
题组三 离子交换膜燃料电池
6.如图是甲醇燃料电池的结构示意图,甲醇在催化剂作用下提供质子(H+)
和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为2CH3OH+3O2===2CO2+4H2O。下列说法不正确的是
A.左电极为电池的负极,a处通入的物质是甲醇
B.正极反应式为O2+2H2O+4e-===4OH-
C.负极反应式为CH3OH+H2O-6e-=== CO2+6H+
D.该电池提供1 mol e-,消耗氧气0.25 mol
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
负极反应式为2CH3OH-12e-+2H2O===2CO2+12H+,正极反应式为3O2+12e-+12H+===6H2O;根据电子流向,可以判断a处通甲醇,b处通O2;当电池提供 1 mol电子时,消耗O2为1× mol=0.25 mol。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
7.以引火性高的联氨(N2H4)为燃料的环保电池,工作时产生稳定无污染的物质,原理如图所示。下列说法正确的是
A.N极为电源负极,联氨从c口通入
B.负极上每消耗1 mol N2H4,转移6 mol电子
C.正极的电极反应式为O2+2H2O+4e-===4OH-
D.可将联氨改进为引火性低、稳定性好的N2H4·H2O
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
由图中氢离子移动方向可知,电极N为正极,氧气在正极上发生还原反应,电极反应式为O2+4H++4e-===2H2O,则氧气从c口通入,A、C项错误;
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
联氨在负极上发生氧化反应,电极反应式为N2H4-4e-===N2+4H+,每消耗1 mol N2H4可转移4 mol电子,B项错误;
将联氨改进为引火性低、稳定性好的N2H4·H2O,则电池的安全性会更高,D项正确。
8.如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测,下列说法不正确的是
A.电流由O2所在的铂电极经外电路流向另一电极
B.O2所在的铂电极处发生还原反应
C.该电池的负极反应式为CH3CH2OH+3H2O-12e-
===2CO2↑+12H+
D.微处理器通过检测电流大小而计算出被测气体中酒精的含量
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
乙醇燃料电池中,负极上乙醇失电子发生氧化反应,正极上氧气得电子发生还原反应,电流由正极流向负极,即从O2所在的铂电极经外电路流向另一电极,故A、B项正确;
由装置图可知酒精在负极被氧气氧化生成醋酸:CH3CH2OH-4e-+H2O===4H++CH3COOH,故C项错误;
微处理器通过检测电流大小可以得出电子转移的物质的量,根据电极反应式可以计算出被测气体中酒精的含量,故D项正确。
题组四 熔融盐(或固体氧化物)燃料电池
9.据报道,美国一个海军航空站安装了一台250 kW的MCFC型燃料电池。该电池可同时供应电和水蒸气,其燃料为H2,电解质为熔融的K2CO3,工作温度为600~700 ℃。已知该电池的总反应为2H2+O2===2H2O,负极反应为H2+ -2e-===H2O+CO2。下列推断正确的是
A.正极反应为4OH--4e-===O2+2H2O
B.放电时, 向负极移动
C.电池供应1 mol水蒸气,转移电子的物质的量为4 mol
D.通入O2的一极为正极,发生氧化反应
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
该电池的正极反应为O2+4e-+2CO2===2 ,A项错误;
原电池工作时,阴离子向负极移动,B项正确;
电池提供1 mol水蒸气时,转移电子的物质的量为2 mol,C项错误;
通入O2的一极为正极,发生还原反应,D项错误。
10.H2S燃料电池应用前景非常广阔,该电池示意图如下。下列说法正确的是
A.电极a是正极
B.O2-由电极a移向电极b
C.电极 a 的反应式为2H2S+2O2--4e-===
S2+2H2O
D.当通入11.2 L O2时,转移电子数为2NA
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
根据原电池原理及图示电池构造分析,电池总反应为2H2S+O2===S2+2H2O,则负极H2S失电子发生氧化反应,正极O2得电子发生还原反应,电极a为电池的负极,故A错误;
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
原电池中阴离子向负极移动,则O2-由电极b移向电极a,故B错误;
电极a为电池的负极,发生氧化反应,反应式为2H2S+2O2--4e-===S2+2H2O,故C正确;
未注明是否为标准状况,无法确定11.2 L O2的物质的量,故D错误。
11.设计出燃料电池使汽油(主要成分为C5H12)氧化直接产生电流是21世纪富有挑战性的课题。有人设计了一种固体燃料电池,以固体氧化铝-氧化钇为电解质,这种固体电解质在高温下允许O2-在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断不正确的是
A.有O2放电的电极a为电池的负极
B.电极b对应的电极反应式为C5H12+16O2--32e-
===5CO2+6H2O
C.该电池的总反应式为C5H12+8O2===5CO2+6H2O
D.汽油燃料电池的技术障碍是氧化反应不完全,产生碳单质堵塞电极的气体
通道,从而使输电效能减弱
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
根据题图可知,O2在电极a获得电子,发生还原反应,电极a为电池的正极,A错误;
电极b上C5H12失去电子,发生氧化反应,电极反应式为C5H12+16O2--32e-===5CO2+6H2O,B正确;
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
正极反应式为8O2+32e-===16O2-,将正、负极反应式相加,可得电池的总反应式为C5H12+8O2===5CO2+6H2O,C正确。
题组五 金属—空气电池
12.锌—空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,总反应为2Zn+O2+4OH-+2H2O 。下列说法正确的是
A.放电时,电解质溶液中K+向负极移动
B.充电时,电解质溶液中c(OH-)逐渐减小
C.放电时,负极反应为Zn+4OH--2e-===
D.放电时,电路中通过2 mol电子,消耗氧气22.4 L(标准状况)
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
A错,放电时溶液中的阳离子向正极移动;
B错,充电时的总反应为放电时反应的逆过程:2 ===2Zn+O2↑
+4OH-+2H2O,c(OH-)逐渐增大;
C对,放电时负极失电子发生氧化反应,由放电时的总反应可知,负极反应为Zn+4OH--2e-=== ;
D错,由放电时的总反应可知,电路中通过2 mol电子时,消耗0.5 mol O2,其体积为11.2 L(标准状况)。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
13.近年来AIST正在研制一种高容量、低成本的锂—铜空气燃料电池。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O===2Cu+2Li++2OH-,下列说法不正确的是
A.放电时,Li+透过固体电解质向Cu极移动
B.放电时,负极的电极反应式为Cu2O+H2O
+2e-===2Cu+2OH-
C.通空气时,铜被腐蚀,表面产生Cu2O
D.整个反应过程中,铜相当于催化剂
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
放电时,锂是负极,发生失电子的氧化反应;在电池内部Li+(阳离子)透过固体电解质向正极(铜电极)移动;由题意可知,通空气时铜被腐蚀,表面产生Cu2O,放电时Cu2O又转化成铜,整个反应过程中,铜相当于催化剂。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
14.如图是甲烷燃料电池原理示意图,回答下列问题:
(1)电池的负极是___(填“a”或“b”)电极,该极的电极反应式为___________________
_______________。
a
CH4-8e-+10OH-
碱性甲烷燃料电池中通入甲烷的一极a电极为原电池的负极,该极上是燃料发生失电子的氧化反应,电极反应式为CH4-8e-+10OH-===
+7H2O。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(2)电池工作一段时间后电解质溶液的pH______(填“增大”“减小”或“不变”)。
减小
在碱性溶液中,甲烷燃料电池的总反应式为CH4+2O2+2OH-=== +3H2O,电池工作一段时间后,由于氢氧根离子被消耗且反应生成H2O,所以电解质溶液的pH会减小。
15.氨气是一种富氢燃料,可以直接用于燃料电池,如图是供氨水式燃料电池工作原理:
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
(1)氨气燃料电池的电解质溶液最好选择________(填“酸性”“碱性”或“中性”)溶液。
碱性
氨气是碱性气体,所以电解液最好选择碱性溶液。
(2)空气在进入电池装置前需要通过过滤器除去的气体是______。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
CO2
空气中的CO2能和氨水反应,所以滤去的气体是CO2。
(3)氨气燃料电池的反应是氨气与氧气生成一种常见的无毒气体和水,该电池的总反应式是____________________________,正极的电极反应是________________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
4NH3 + 3O2===2N2 + 6H2O
O2 +4e-+2H2O===4OH-
正极发生还原反应,碱性环境下,电极反应式为O2+4e-+2H2O===4OH-。
16.(1)二氧化硫—空气质子交换膜燃料电池可以利用大气所含SO2快速启动,其装置示意图如图:
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
①质子的流动方向为___________(填“从A到B”或“从B到A”)。
从A到B
根据图示,A为燃料电池的负极,B为燃料电池的正极,在原电池电解液中,正电荷由负极向正极移动,即从A到B;
②负极的电极反应式为_____________________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
负极二氧化硫被氧化为硫酸根离子,电极反应式为SO2-2e-+2H2O===
+4H+。
(2)NH3—O2燃料电池的结构如图所示:
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
①a极为电池的____(填“正”或“负”)极。
负
a极通入氨气,是负极,b极通入氧气,是正极;
②当生成1 mol N2时 ,电路中流过电子的物质的量为_______。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
6 mol
氨气中N的化合价由-3变成0,当生成1 mol N2时,转移电子的物质的量为6 mol。
返回
专题1
本课结束
