9.2 溶解度(教学课件)-2022-2023学年九年级化学下册同步教学课件 (33页)(人教版)
文档属性
| 名称 | 9.2 溶解度(教学课件)-2022-2023学年九年级化学下册同步教学课件 (33页)(人教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 65.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-23 00:00:00 | ||
图片预览









文档简介
(共33张PPT)
2022-2023学年九年级化学下册 (人教版)
第九单元 溶液 Solution
课题2 溶解度
本课件内嵌3个视频,即点即播,使用方便(此页可删除)。
说明:本课件使用WPS制作,使用WPS体验更佳效果。
视频1:氯化钠在水中的溶解
视频2:硝酸钾在水中的溶解
视频3:海水晒盐
- Learning objectives -
第
1
课
时
1.
了解饱和溶液、不饱和溶液的概念
2.
了解使饱和溶液结晶的方法
我们知道,蔗糖或食盐很容易溶解在水里形成溶液。但是,它们能不能无限制地溶解在一定量的水中呢?
视频:氯化钠在水中的溶解
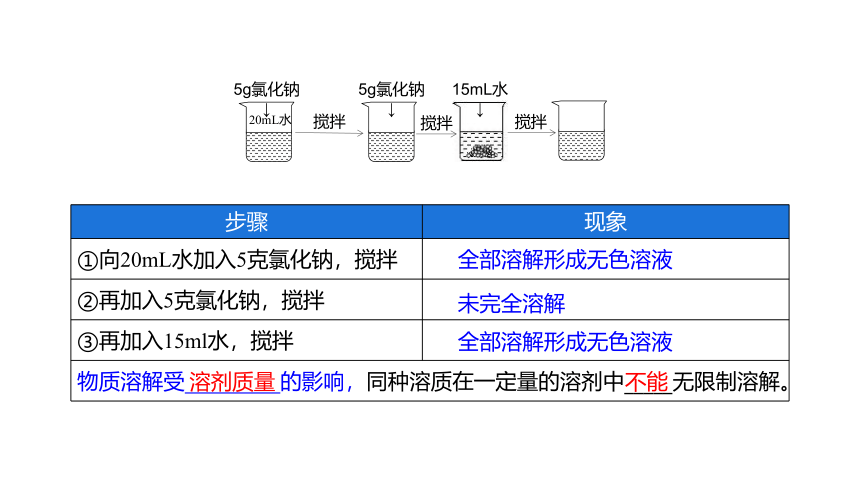
步骤 现象
①向20mL水加入5克氯化钠,搅拌
②再加入5克氯化钠,搅拌
③再加入15ml水,搅拌
物质溶解受 的影响,同种溶质在一定量的溶剂中_____无限制溶解。 全部溶解形成无色溶液
溶剂质量
不能
未完全溶解
全部溶解形成无色溶液
搅拌
20mL水
搅拌
5g氯化钠
↓
搅拌
5g氯化钠
↓
15mL水
↓
视频:硝酸钾在水中的溶解
搅拌
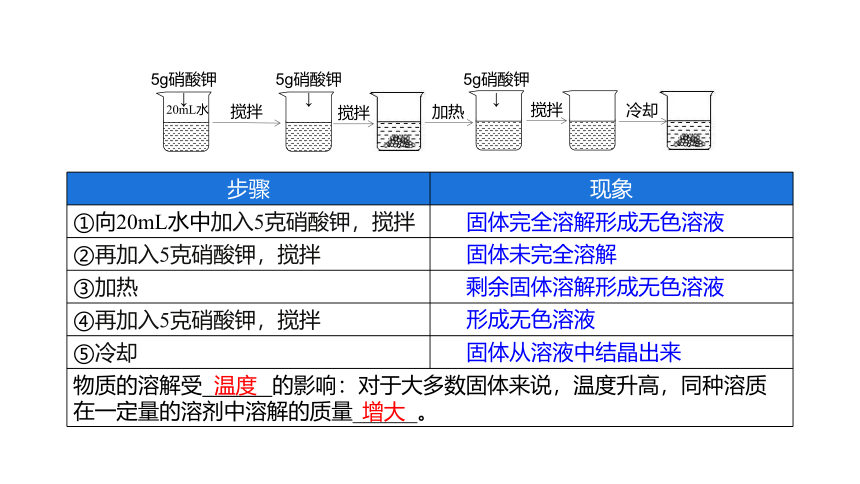
步骤 现象
①向20mL水中加入5克硝酸钾,搅拌
②再加入5克硝酸钾,搅拌
③加热
④再加入5克硝酸钾,搅拌
⑤冷却
物质的溶解受 的影响:对于大多数固体来说,温度升高,同种溶质在一定量的溶剂中溶解的质量______。 固体完全溶解形成无色溶液
固体未完全溶解
剩余固体溶解形成无色溶液
形成无色溶液
固体从溶液中结晶出来
温度
增大
20mL水
加热
冷却
5g硝酸钾
↓
搅拌
搅拌
5g硝酸钾
↓
5g硝酸钾
↓
一、饱和溶液与不饱和溶液
1.定义:在 ,向 里加入某种溶质,当溶质_______________所得到的溶液叫做这种溶质的饱和溶液;还能继续溶解的溶液,叫做这种溶质的 溶液。
一定温度下
一定量溶剂
不饱和
(1)必须指明“一定温度”、“一定量的溶剂”;
(2)应明确“某溶质”的饱和溶液或不饱和溶液;
如:在一定条件下的NaCl的饱和溶液,不能再溶解NaCl,但是还能溶解蔗糖。对NaCl来说饱和,对蔗糖来说不饱和。
不能继续溶解时
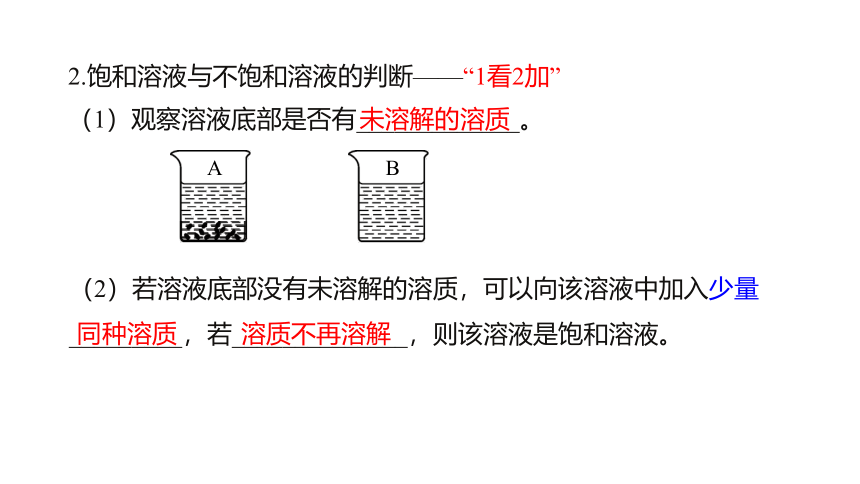
2.饱和溶液与不饱和溶液的判断——“1看2加”
(1)观察溶液底部是否有_____________。
(2)若溶液底部没有未溶解的溶质,可以向该溶液中加入少量_________,若______________,则该溶液是饱和溶液。
未溶解的溶质
同种溶质
溶质不再溶解
一、饱和溶液与不饱和溶液
A
B
不饱和溶液
增加溶质、蒸发溶剂或降低温度
增加溶剂或升高温度
(1)大多数固体溶质:
一、饱和溶液与不饱和溶液
3.饱和溶液与不饱和溶液的相互转化
饱和溶液
(2)少数如:熟石灰Ca(OH)2的溶解度随温度升高而减小。
不饱和溶液
增加溶质、蒸发溶剂或升高温度
增加溶剂或降低温度
饱和溶液
析出晶体后的溶液叫做母液,母液是 (饱和/不饱和)溶液。
4.结晶:溶液中的溶质以_____的形式析出的过程叫做结晶。
饱和溶液 结晶
降温结晶
蒸发结晶
饱和
又称为冷却热饱和溶液
晶体
一、饱和溶液与不饱和溶液
饱和溶液、不饱和溶液与浓溶液、稀溶液
相同溶质、相同温度
相同溶质、不同温度
不同溶质、相同温度 饱和溶液一定比不饱和溶液浓
稀溶液不一定是不饱和溶液。
浓溶液不一定是饱和溶液;
20℃
20℃
A
B
饱和
不饱和
5gA
↓
20gB
↓
100mL水
20℃
20℃
A
A
饱和
不饱和
5gA
↓
4gA
↓
100mL水
20℃
40℃
A
A
饱和
不饱和
5gA
↓
10gA
↓
100mL水
视频:海水晒盐
海水
贮水池
蒸发池
结晶池
食盐
母液
氯化钠
多种化
工产品
海水晒盐属于______结晶
蒸发
1.饱和溶液与不饱和溶液
①“一定温度”;②“一定量溶剂”;③“某溶质”。
2.饱和溶液的判断:“1看2加”
3.转化:
不饱和溶液
增加溶质、蒸发溶剂或改变温度
增加溶剂或改变温度
饱和溶液
4.结晶:
饱和溶液 结晶
降温结晶
蒸发结晶
1.下列有关饱和溶液和不饱和溶液的说法中,不正确的是( )
A.在一定条件下,不能继续溶解该溶质的溶液即为该溶质的饱和溶液B.浓溶液一定是饱和溶液
C.析出晶体后的溶液还是当时条件下的饱和溶液
D.冷却或蒸发溶剂都有可能使不饱和氯化钾溶液达到饱和
B
2.在一定温度下,将一瓶接近饱和的硝酸钾溶液转变为饱和溶液可采取的方法有( )
①升高温度; ②降低温度; ③增加硝酸钾;
④减少硝酸钾; ⑤增加溶剂; ⑥减少溶剂。
A.①②③ B.②③④ C.③④⑤ D.②③⑥
D
- Learning objectives -
第
2课
时
1.
理解固体溶解度的含义和溶解度曲线
2.
了解气体溶解度概念及影响因素
1.固态物质的溶解度:在一定______下,某固态物质在_____溶剂里达到_____状态时所溶解的_____。用“S”表示。
条件 ——
标准 ——
状态 ——
单位 ——
温度
饱和
100g
质量
溶解度
四要素
易错
一定温度
100克溶剂(水)
饱和
g
二、溶解度
例:NaCl在20℃时的溶解度为36g。
1. 20℃时,在100g水中达到_____状态时所溶解的NaCl的质量为36g。
2. 20℃时,在100g水中最___(多/少)溶解36gNaCl。
3. 20℃时,完全溶解36gNaCl,最___(多/少)需要100g水。
对固体溶解度的理解
饱和
多
少
温度 溶质的质量 溶剂的质量 饱和溶液的质量
20℃
36g
100g
136g
4.
一、判断下列说法是否正确,并指明错误原因。
1. 把20克某物质溶解在100克水里恰好制成饱和溶液,这种物质的溶解度就是20克。( )
2. 20℃时10克氯化钠溶解在水里制成饱和溶液,故20℃时氯化钠的溶解度是10克。( )
3. 20℃时10克氯化钠可溶解在100克水里,故20℃时氯化钠的溶解度是10克。( )
4. 20℃时36克食盐溶解在100克水中恰好饱和,故20℃时食盐的溶解度是36。( )
一定温度
标准:100g溶剂
状态:饱和
单位:g
溶解度与溶质、溶剂的质量无关
(1)20℃,100g水中最多溶解20gA达到饱和,A的溶解度=________。
(2)20℃,200g水中最多溶解40gA达到饱和,A的溶解度=________。
(3)20℃,50g水中最多溶解10gA达到饱和,A的溶解度=_________。
1.内部因素:______和_____的性质;
2.外部因素:_____
温度
溶剂
溶质
固体物质溶解度的影响因素
【练习】要使KNO3溶解度增大,采用的方法是( )
A.加水 B.增加KNO3 C.搅拌 D.升温
D
20g
20g
20g
搅拌/振荡只能加快溶解速率,不能增大溶解度
固体物质溶解度与溶解性的关系
溶解性 易溶 可溶 微溶 难溶
溶解度 (200c/g) >10 1~10 0.01~1 <0.01
.
.
.
0.01g
1g
10g
易溶
可溶
微溶
难(不)溶
上升 陡 物质溶解度受温度变化影响较 ,如 ,适于 结晶
平 物质溶解度受温度影响较 ,如 ,适于 结晶
下降 物质溶解度随温度升高而 ,如 。
2.固体溶解度曲线纵坐标表示_______,用横坐标表示_____。
意义:来表示固体物质的溶解度受_____变化影响。
溶解度
温度
温度
大
KNO3
小
NaCl
减小
Ca(OH)2
Ca(OH)2的溶解度曲线
降温
蒸发
二、溶解度
位置 溶液状态 意 义
在曲线上 表示该温度下该物质的__________
交点
曲线下方
该温度下两种物质的溶解度相同
溶解度
曲线上各点的意义
饱和
不饱和
P
N
(1)点P表示_________________________。
(2)t2℃时,A、B、C的溶解度由大到小为_______。
(3)要使接近饱和的C的溶液变为饱和,需要_____温度。
(4)t2℃时,向50g水中加入20gA,能否达到A的饱和溶液?加入30g?
(5)t2℃时,A物质的饱和溶液150g降温到t1℃析出A____g。
(6)t2℃时,将等质量A、B、C三种物质的饱和溶液降温到t1℃时,析出晶体的质量由大到小的顺序是________。
(7)当A中含有少量B时,提纯A,可采用________方法。
当B中含有少量A时,提纯B,可采用________方法。
1.如图是固体A、B、C的溶解度曲线,回答问题:
t1℃时,A、C的溶解度相同
A>B>C
升高
30
A>B>C
降温结晶
蒸发结晶
总结:提纯谁,就让谁结晶,陡用降温,平用蒸发。
P
2.气体的溶解度:某气体的______为101kPa和___________时,在________里达到___________时所溶解的气体体积。
一定温度
饱和状态
1体积水
压强
影响气体溶解度的因素
①压强:压强增大,气体溶解度变____。
②温度:温度升高,气体溶解度变____。
大
小
二、溶解度
定义:在_________下,某固态物质在________里达到__________时所溶解的_____,叫做这种物质在这种溶剂里的溶解度。“S”表示。
影响因素: 内部:______和______的性质 外部:_____。
固体物质溶解度曲线(三条典型曲线)
陡升_______,缓升_______,下降_________。
一定温度
饱和状态
100g溶剂
质量
1.固态物质的溶解度
溶剂
溶质
温度
压强增大,S气体变____。
温度升高,S气体变____。
大
小
KNO3
NaCl
Ca(OH)2
2.影响气体溶解度的因素:
1.下列对“20℃时,硝酸钾溶解度为31.6g”的解释正确的是( )
A.20℃时,31.6g硝酸钾溶解在100g水里
B.20℃时,100g溶液中含31.6g硝酸钾
C.31.6g硝酸钾溶解在100g水中达到饱和状态
D.20℃时,31.6g硝酸钾溶解在100g水中恰好达到饱和状态
D
2.如图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
A.t2℃时,甲的溶液降温到t1℃,一定能得到甲的饱和溶液B.t2℃时,甲的溶解度为70
C.t2℃时,甲、乙两种物质的溶液分别降温到t1℃,析出晶体的质量甲一定大于乙
D.乙中含有少量的甲,可用蒸发溶剂的方法提纯乙
D
3.如图是甲、乙、丙三种物质的溶解度曲线,请按要求回答下列问题:
(1)t1℃时,甲、乙、丙三种物质的溶解度大小关系 。
(2)t3℃时,将30g丙物质投入50g水中,充分溶解,所得溶液质量为 。
(3)甲中混有少量的乙,提纯甲可以采用 结晶。
(4)t2℃时,将75g甲的饱和溶液降温到t1℃,析出的固体质量是 。
乙>甲=丙
60g
降温
15g
20
2022-2023学年九年级化学下册 (人教版)
第九单元 溶液 Solution
课题2 溶解度
本课件内嵌3个视频,即点即播,使用方便(此页可删除)。
说明:本课件使用WPS制作,使用WPS体验更佳效果。
视频1:氯化钠在水中的溶解
视频2:硝酸钾在水中的溶解
视频3:海水晒盐
- Learning objectives -
第
1
课
时
1.
了解饱和溶液、不饱和溶液的概念
2.
了解使饱和溶液结晶的方法
我们知道,蔗糖或食盐很容易溶解在水里形成溶液。但是,它们能不能无限制地溶解在一定量的水中呢?
视频:氯化钠在水中的溶解
步骤 现象
①向20mL水加入5克氯化钠,搅拌
②再加入5克氯化钠,搅拌
③再加入15ml水,搅拌
物质溶解受 的影响,同种溶质在一定量的溶剂中_____无限制溶解。 全部溶解形成无色溶液
溶剂质量
不能
未完全溶解
全部溶解形成无色溶液
搅拌
20mL水
搅拌
5g氯化钠
↓
搅拌
5g氯化钠
↓
15mL水
↓
视频:硝酸钾在水中的溶解
搅拌
步骤 现象
①向20mL水中加入5克硝酸钾,搅拌
②再加入5克硝酸钾,搅拌
③加热
④再加入5克硝酸钾,搅拌
⑤冷却
物质的溶解受 的影响:对于大多数固体来说,温度升高,同种溶质在一定量的溶剂中溶解的质量______。 固体完全溶解形成无色溶液
固体未完全溶解
剩余固体溶解形成无色溶液
形成无色溶液
固体从溶液中结晶出来
温度
增大
20mL水
加热
冷却
5g硝酸钾
↓
搅拌
搅拌
5g硝酸钾
↓
5g硝酸钾
↓
一、饱和溶液与不饱和溶液
1.定义:在 ,向 里加入某种溶质,当溶质_______________所得到的溶液叫做这种溶质的饱和溶液;还能继续溶解的溶液,叫做这种溶质的 溶液。
一定温度下
一定量溶剂
不饱和
(1)必须指明“一定温度”、“一定量的溶剂”;
(2)应明确“某溶质”的饱和溶液或不饱和溶液;
如:在一定条件下的NaCl的饱和溶液,不能再溶解NaCl,但是还能溶解蔗糖。对NaCl来说饱和,对蔗糖来说不饱和。
不能继续溶解时
2.饱和溶液与不饱和溶液的判断——“1看2加”
(1)观察溶液底部是否有_____________。
(2)若溶液底部没有未溶解的溶质,可以向该溶液中加入少量_________,若______________,则该溶液是饱和溶液。
未溶解的溶质
同种溶质
溶质不再溶解
一、饱和溶液与不饱和溶液
A
B
不饱和溶液
增加溶质、蒸发溶剂或降低温度
增加溶剂或升高温度
(1)大多数固体溶质:
一、饱和溶液与不饱和溶液
3.饱和溶液与不饱和溶液的相互转化
饱和溶液
(2)少数如:熟石灰Ca(OH)2的溶解度随温度升高而减小。
不饱和溶液
增加溶质、蒸发溶剂或升高温度
增加溶剂或降低温度
饱和溶液
析出晶体后的溶液叫做母液,母液是 (饱和/不饱和)溶液。
4.结晶:溶液中的溶质以_____的形式析出的过程叫做结晶。
饱和溶液 结晶
降温结晶
蒸发结晶
饱和
又称为冷却热饱和溶液
晶体
一、饱和溶液与不饱和溶液
饱和溶液、不饱和溶液与浓溶液、稀溶液
相同溶质、相同温度
相同溶质、不同温度
不同溶质、相同温度 饱和溶液一定比不饱和溶液浓
稀溶液不一定是不饱和溶液。
浓溶液不一定是饱和溶液;
20℃
20℃
A
B
饱和
不饱和
5gA
↓
20gB
↓
100mL水
20℃
20℃
A
A
饱和
不饱和
5gA
↓
4gA
↓
100mL水
20℃
40℃
A
A
饱和
不饱和
5gA
↓
10gA
↓
100mL水
视频:海水晒盐
海水
贮水池
蒸发池
结晶池
食盐
母液
氯化钠
多种化
工产品
海水晒盐属于______结晶
蒸发
1.饱和溶液与不饱和溶液
①“一定温度”;②“一定量溶剂”;③“某溶质”。
2.饱和溶液的判断:“1看2加”
3.转化:
不饱和溶液
增加溶质、蒸发溶剂或改变温度
增加溶剂或改变温度
饱和溶液
4.结晶:
饱和溶液 结晶
降温结晶
蒸发结晶
1.下列有关饱和溶液和不饱和溶液的说法中,不正确的是( )
A.在一定条件下,不能继续溶解该溶质的溶液即为该溶质的饱和溶液B.浓溶液一定是饱和溶液
C.析出晶体后的溶液还是当时条件下的饱和溶液
D.冷却或蒸发溶剂都有可能使不饱和氯化钾溶液达到饱和
B
2.在一定温度下,将一瓶接近饱和的硝酸钾溶液转变为饱和溶液可采取的方法有( )
①升高温度; ②降低温度; ③增加硝酸钾;
④减少硝酸钾; ⑤增加溶剂; ⑥减少溶剂。
A.①②③ B.②③④ C.③④⑤ D.②③⑥
D
- Learning objectives -
第
2课
时
1.
理解固体溶解度的含义和溶解度曲线
2.
了解气体溶解度概念及影响因素
1.固态物质的溶解度:在一定______下,某固态物质在_____溶剂里达到_____状态时所溶解的_____。用“S”表示。
条件 ——
标准 ——
状态 ——
单位 ——
温度
饱和
100g
质量
溶解度
四要素
易错
一定温度
100克溶剂(水)
饱和
g
二、溶解度
例:NaCl在20℃时的溶解度为36g。
1. 20℃时,在100g水中达到_____状态时所溶解的NaCl的质量为36g。
2. 20℃时,在100g水中最___(多/少)溶解36gNaCl。
3. 20℃时,完全溶解36gNaCl,最___(多/少)需要100g水。
对固体溶解度的理解
饱和
多
少
温度 溶质的质量 溶剂的质量 饱和溶液的质量
20℃
36g
100g
136g
4.
一、判断下列说法是否正确,并指明错误原因。
1. 把20克某物质溶解在100克水里恰好制成饱和溶液,这种物质的溶解度就是20克。( )
2. 20℃时10克氯化钠溶解在水里制成饱和溶液,故20℃时氯化钠的溶解度是10克。( )
3. 20℃时10克氯化钠可溶解在100克水里,故20℃时氯化钠的溶解度是10克。( )
4. 20℃时36克食盐溶解在100克水中恰好饱和,故20℃时食盐的溶解度是36。( )
一定温度
标准:100g溶剂
状态:饱和
单位:g
溶解度与溶质、溶剂的质量无关
(1)20℃,100g水中最多溶解20gA达到饱和,A的溶解度=________。
(2)20℃,200g水中最多溶解40gA达到饱和,A的溶解度=________。
(3)20℃,50g水中最多溶解10gA达到饱和,A的溶解度=_________。
1.内部因素:______和_____的性质;
2.外部因素:_____
温度
溶剂
溶质
固体物质溶解度的影响因素
【练习】要使KNO3溶解度增大,采用的方法是( )
A.加水 B.增加KNO3 C.搅拌 D.升温
D
20g
20g
20g
搅拌/振荡只能加快溶解速率,不能增大溶解度
固体物质溶解度与溶解性的关系
溶解性 易溶 可溶 微溶 难溶
溶解度 (200c/g) >10 1~10 0.01~1 <0.01
.
.
.
0.01g
1g
10g
易溶
可溶
微溶
难(不)溶
上升 陡 物质溶解度受温度变化影响较 ,如 ,适于 结晶
平 物质溶解度受温度影响较 ,如 ,适于 结晶
下降 物质溶解度随温度升高而 ,如 。
2.固体溶解度曲线纵坐标表示_______,用横坐标表示_____。
意义:来表示固体物质的溶解度受_____变化影响。
溶解度
温度
温度
大
KNO3
小
NaCl
减小
Ca(OH)2
Ca(OH)2的溶解度曲线
降温
蒸发
二、溶解度
位置 溶液状态 意 义
在曲线上 表示该温度下该物质的__________
交点
曲线下方
该温度下两种物质的溶解度相同
溶解度
曲线上各点的意义
饱和
不饱和
P
N
(1)点P表示_________________________。
(2)t2℃时,A、B、C的溶解度由大到小为_______。
(3)要使接近饱和的C的溶液变为饱和,需要_____温度。
(4)t2℃时,向50g水中加入20gA,能否达到A的饱和溶液?加入30g?
(5)t2℃时,A物质的饱和溶液150g降温到t1℃析出A____g。
(6)t2℃时,将等质量A、B、C三种物质的饱和溶液降温到t1℃时,析出晶体的质量由大到小的顺序是________。
(7)当A中含有少量B时,提纯A,可采用________方法。
当B中含有少量A时,提纯B,可采用________方法。
1.如图是固体A、B、C的溶解度曲线,回答问题:
t1℃时,A、C的溶解度相同
A>B>C
升高
30
A>B>C
降温结晶
蒸发结晶
总结:提纯谁,就让谁结晶,陡用降温,平用蒸发。
P
2.气体的溶解度:某气体的______为101kPa和___________时,在________里达到___________时所溶解的气体体积。
一定温度
饱和状态
1体积水
压强
影响气体溶解度的因素
①压强:压强增大,气体溶解度变____。
②温度:温度升高,气体溶解度变____。
大
小
二、溶解度
定义:在_________下,某固态物质在________里达到__________时所溶解的_____,叫做这种物质在这种溶剂里的溶解度。“S”表示。
影响因素: 内部:______和______的性质 外部:_____。
固体物质溶解度曲线(三条典型曲线)
陡升_______,缓升_______,下降_________。
一定温度
饱和状态
100g溶剂
质量
1.固态物质的溶解度
溶剂
溶质
温度
压强增大,S气体变____。
温度升高,S气体变____。
大
小
KNO3
NaCl
Ca(OH)2
2.影响气体溶解度的因素:
1.下列对“20℃时,硝酸钾溶解度为31.6g”的解释正确的是( )
A.20℃时,31.6g硝酸钾溶解在100g水里
B.20℃时,100g溶液中含31.6g硝酸钾
C.31.6g硝酸钾溶解在100g水中达到饱和状态
D.20℃时,31.6g硝酸钾溶解在100g水中恰好达到饱和状态
D
2.如图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
A.t2℃时,甲的溶液降温到t1℃,一定能得到甲的饱和溶液B.t2℃时,甲的溶解度为70
C.t2℃时,甲、乙两种物质的溶液分别降温到t1℃,析出晶体的质量甲一定大于乙
D.乙中含有少量的甲,可用蒸发溶剂的方法提纯乙
D
3.如图是甲、乙、丙三种物质的溶解度曲线,请按要求回答下列问题:
(1)t1℃时,甲、乙、丙三种物质的溶解度大小关系 。
(2)t3℃时,将30g丙物质投入50g水中,充分溶解,所得溶液质量为 。
(3)甲中混有少量的乙,提纯甲可以采用 结晶。
(4)t2℃时,将75g甲的饱和溶液降温到t1℃,析出的固体质量是 。
乙>甲=丙
60g
降温
15g
20
同课章节目录
